基于FAERS数据库的司美格鲁肽不良事件信号挖掘研究
2022-11-15吴玥陈力何绪成四川大学华西第二医院药学部成都6004四川省彭州市第二人民医院药剂科四川彭州6934
吴玥,陈力,何绪成(.四川大学华西第二医院药学部,成都 6004;.四川省彭州市第二人民医院药剂科,四川彭州 6934)
胰高血糖素样肽-1(glucagon like peptide-1,GLP-1)是一种对血糖控制和体重调节具有重要作用的肠促胰岛激素[1],通过模拟天然GLP-1 激活GLP-1 受体,以葡萄糖浓度依赖的方式增强胰岛素的分泌,抑制胰高血糖素分泌,并能够延缓胃排空,通过中枢性的食欲抑制,减少进食量,从而达到降低血糖的作用[2]。因此,胰高血糖素样肽-1 受体激动剂(glucagon like peptide-1,GLP-1RA)成为了近年来的新型降糖药。司美格鲁肽(semaglutide)每周给药一次,可以提高患者的依从性和生活质量[3]。在2 型糖尿病的随机临床试验中,司美格鲁肽使普通患者的体重减轻量是其他GLP-1RA 的3 倍,肥胖患者的体重减轻量是其他GLP-1RA 的2 倍,接近15 kg。在小型随机对照临床试验中,司美格鲁肽在三餐中平均降低约25%的能量摄入,还可以降低糖尿病患者的心血管不良事件的风险[4],为全球第3 个上市的每周注射1 次的GLP-1RA[5]。
近日,国家医保局公布2021年国家医保目录调整的结果,司美格鲁肽正式纳入医保并将进行国家谈判,该药即将在临床使用中出现井喷式增长。作为一种新型药物,目前对其安全性研究较少,本文将通过挖掘美国FDA 不良事件报告系统(FDA adverse event reporting system,FAERS)对司美格鲁肽的不良反应进行研究,为临床用药提供参考。
1 资料与方法
1.1 数据来源
本研究提取美国FAERS 数据库中2019年第1 季度至2021年第3 季度共11 个季度的关于司美格鲁肽的不良反应报告,包括患者资料、药物使用信息、不良事件名称、结果、报告来源、日期和原发疾病等内容,将所得资料导入关系型数据库管理系统(MYSQL,版本5.7)中,再删除重复项,筛选出以司美格鲁肽为首要怀疑药物的不良事件报告共11 113 例。
1.2 数据标准化
药品不良事件(ADE)的分类和表达采用国际医学科学组织理事会《ICH 国际医学用语词典》(Medical Dictionary for Regulatory Activities,MedDRA)中药物不良反应术语集的首选系统器官分类(system organ class,SOC)和首选术语(preferred term,PT)。在MedDRA 官方网站,将需要汉化的SOC 和PT 英文名导入,系统自动输出中英文映射表。本文中SOC 和PT 的中英文表达均按照该映射表,提高了研究的可信度与准确度。
1.3 数据挖掘方法
本研究主要采用的数据挖掘方法为比例失衡法中的报告比值比法(reporting odds ratio,ROR)和比例报告比值法(proportional reporting ratio,PRR),具有较高的灵敏性和可信度[6]。该方法以比例失衡法四格表为基础,通过ROR 法与PRR法公式及阈值表格来计算ROR 和PRR 的数值[7],如果目标药物与不良事件之间的频次和信号强度均大于阈值,则称为失衡(disproportionality),此时提示生成1 个信号,计算得到的ROR 值和PRR值的数值越大表示信号越强,提示目标药物越可能与目标不良事件存在关联,但并不代表两者之间一定存在可疑因果关系[8]。
2 结果
2.1 不良事件报告病例基本特征
从美国FAERS 系统中得到以司美格鲁肽为目标药物的ADE 共7424 例,其中女性(4026,54.23%)多于男性(3244,43.70%)。在年龄分布上,平均年龄为62.2 岁,中位年龄为63 岁。报告者以消费者为主,共4339 例,占58.45%。美国报告数最多,有6467 例,占87.11%。具体报告情况见表1。
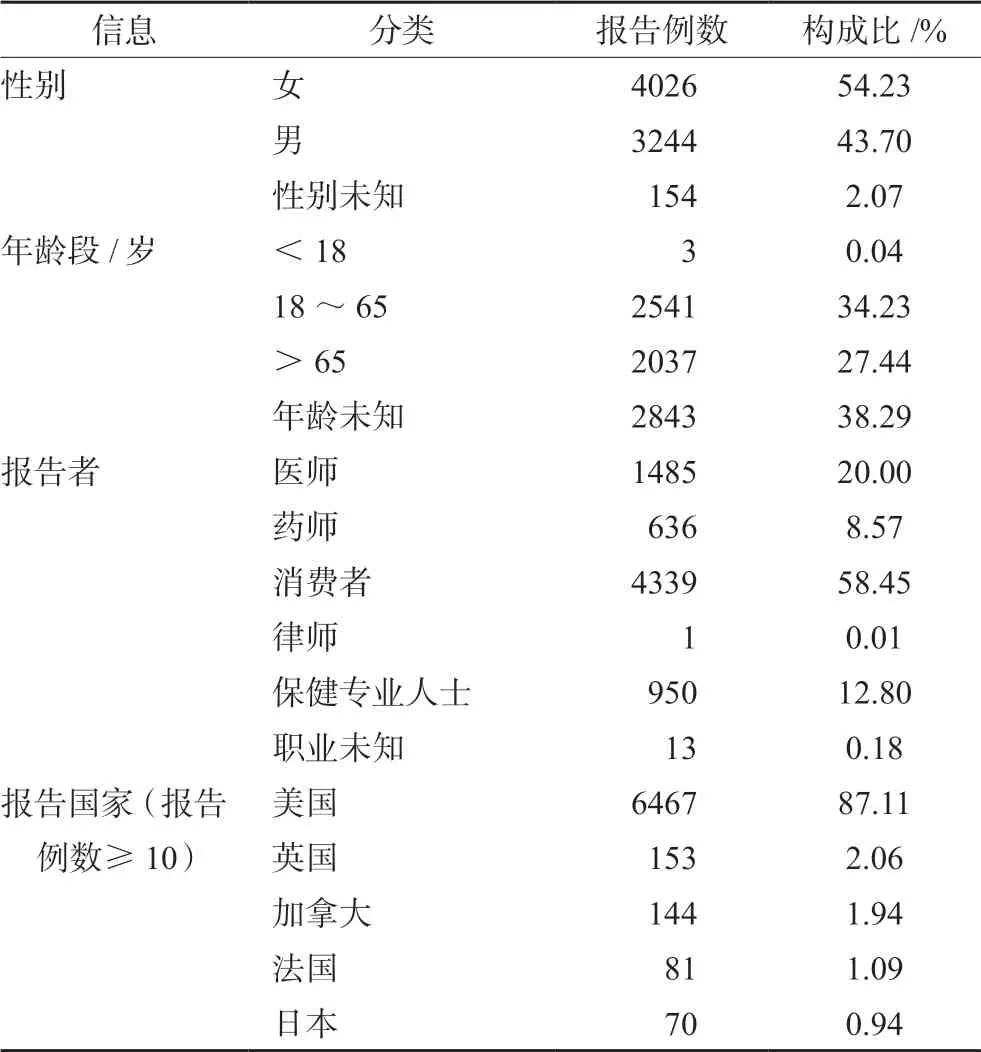
表1 2019—2021年司美格鲁肽相关不良事件报告基本信息Tab 1 Basic information of semaglutide related events from 2019 to 2021
2.2 ADE 累及器官
对提取到的以司美格鲁肽为目标药物的ADE,通过ROR 法和PRR 法进行筛选,最终得到有效信号192 个,涉及23 个SOC。其中报告数最多的为胃肠系统疾病,共计6480 例,占58.31%。此外,各类检查(1461 例,13.15%)、代谢及营养类疾病(1205 例,10.84%)也相对较多。具体见表2 及图1。
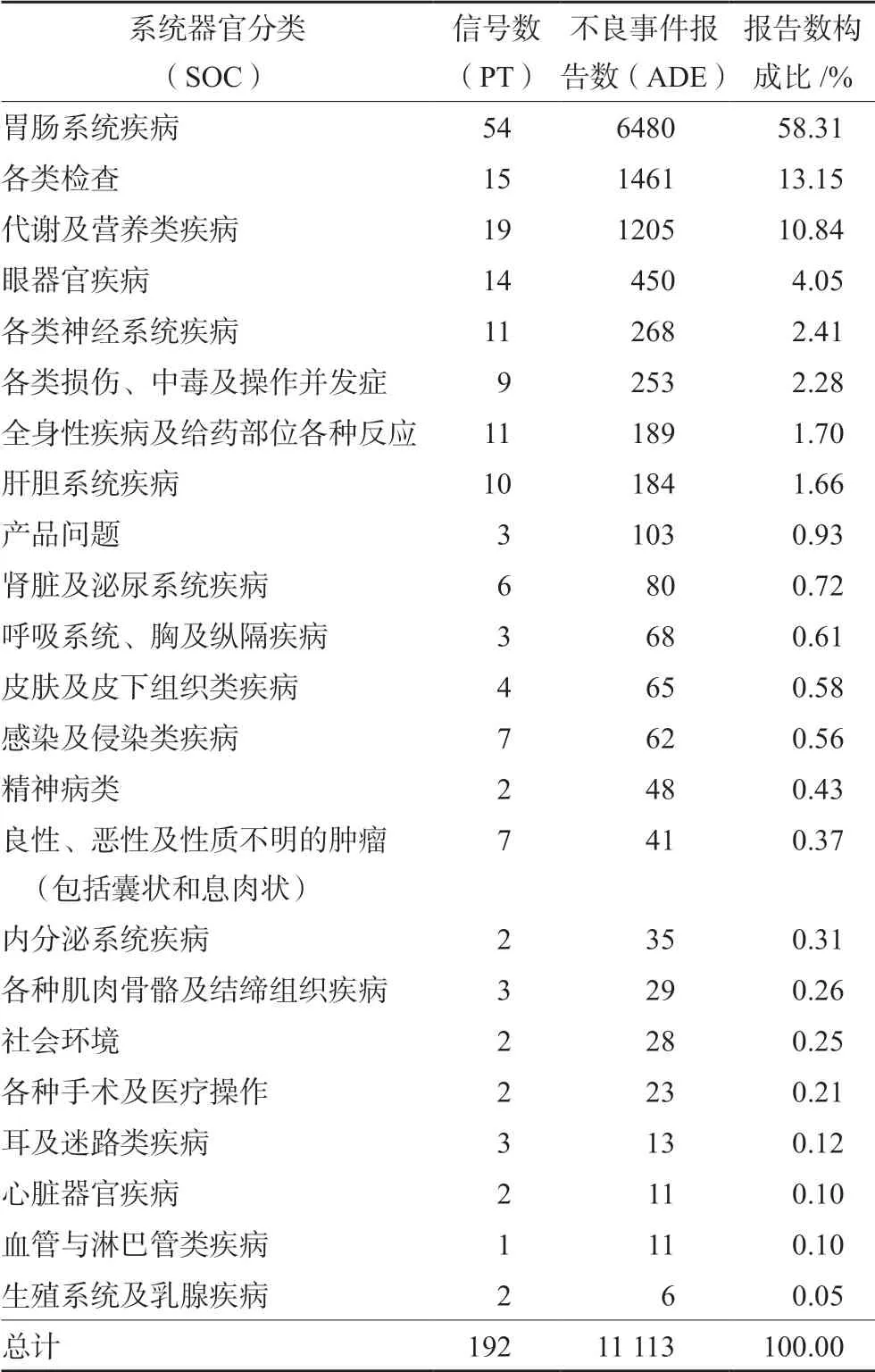
表2 SOC 项下司美格鲁肽ADE 信号检测Tab 2 ADE signals of semaglutide involved systems organs class
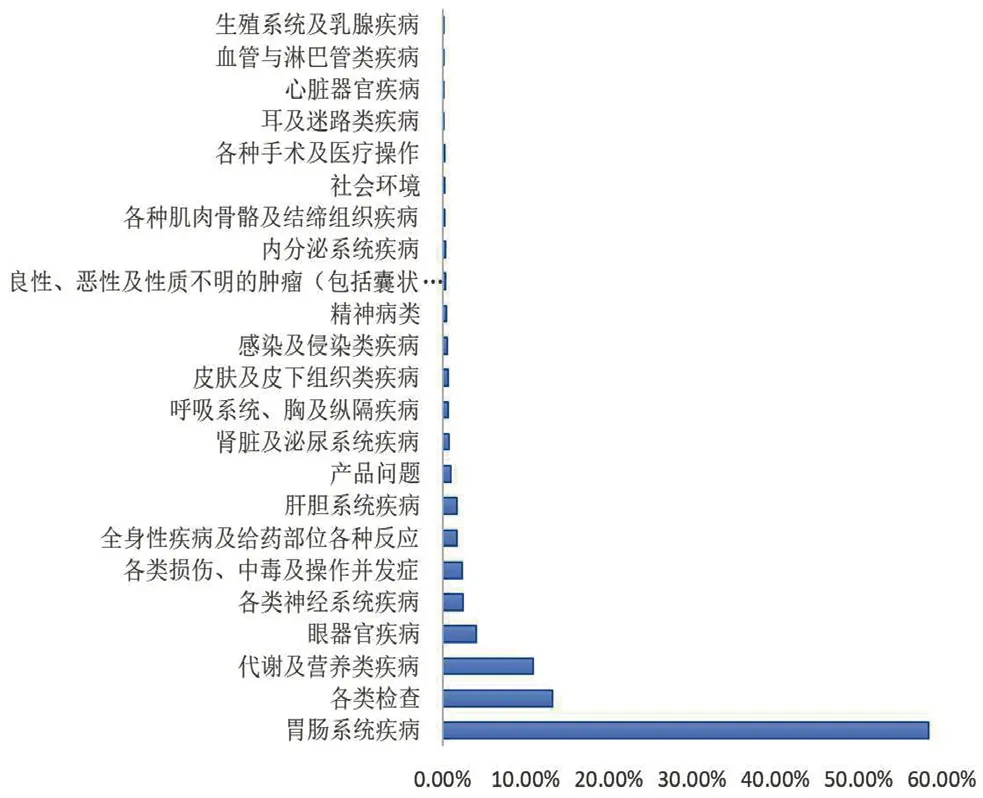
图1 各SOC 项下司美格鲁肽ADE 信号的报告例数构成比Fig 1 Proportion of reported cases of semaglutide ADE signal under each SOC
2.3 ADE 信号挖掘结果
对以司美格鲁肽为目标药物的ADE 进行筛除,通过ROR 法和PRR 法筛选后,最终得到司美格鲁肽信号数为193 个,PT 报告总数为11 113例。在有信号的PT 中,分别按相应ADE 发生频次(a 值)和信号强度(95%CI下限)的前20 位进行PT 排序(具体数据见表3、4)。其中较为常见的ADE 为恶心、呕吐、腹泻、食欲减退等;而相关性较高的ADE 为甲状腺髓样癌、嗳气、产品通信问题等。
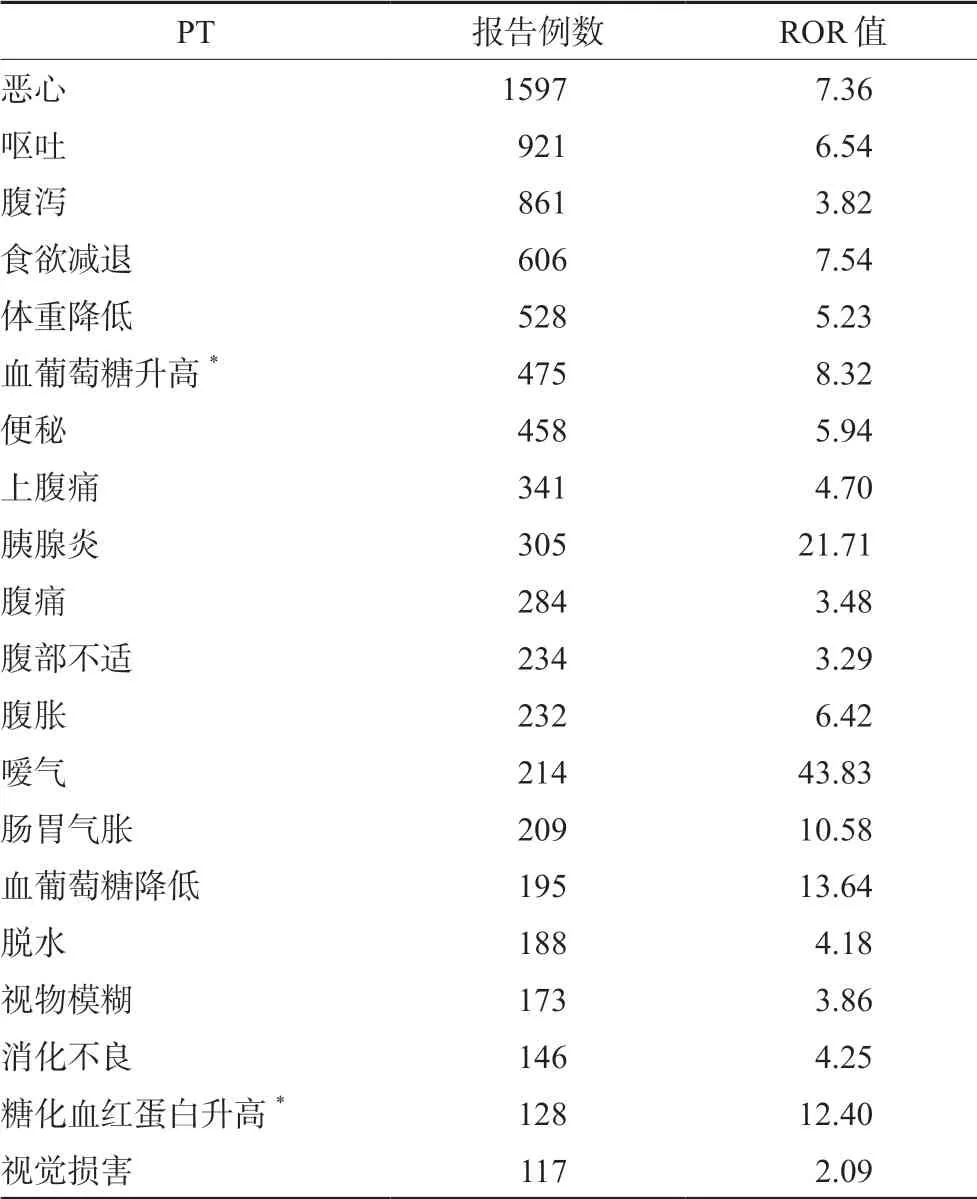
表3 司美格鲁肽报告数降序排列的前20 位ADE 信号Tab 3 Top 20 ADE signals of semaglutide signal strength and reports in descending order
3 讨论
本研究通过ROR 法与PRR 法得到的司美格鲁肽ADE 与已知的安全信息基本一致,证实了本研究方法的可靠性,主要的ADE 集中在胃肠系统、各类检查、代谢及营养类疾病等方面。
3.1 常见ADE 信号分析
3.1.1 胃肠道问题 司美格鲁肽的常见不良事件为恶心、呕吐、腹泻、便秘等,胃肠道反应为最常见的不良反应,多数为轻中度。有研究显示,司美格鲁肽的胃肠道不良反应会随着用药次数而减轻,患者的耐受性增强,作为一种长效制剂,司美格鲁肽在胃肠道耐受方面优于短效制剂,提示在临床用药选择上,若患者胃肠道反应大,可考虑使用本品,以降低患者发生胃肠道不良反应的风险[9]。
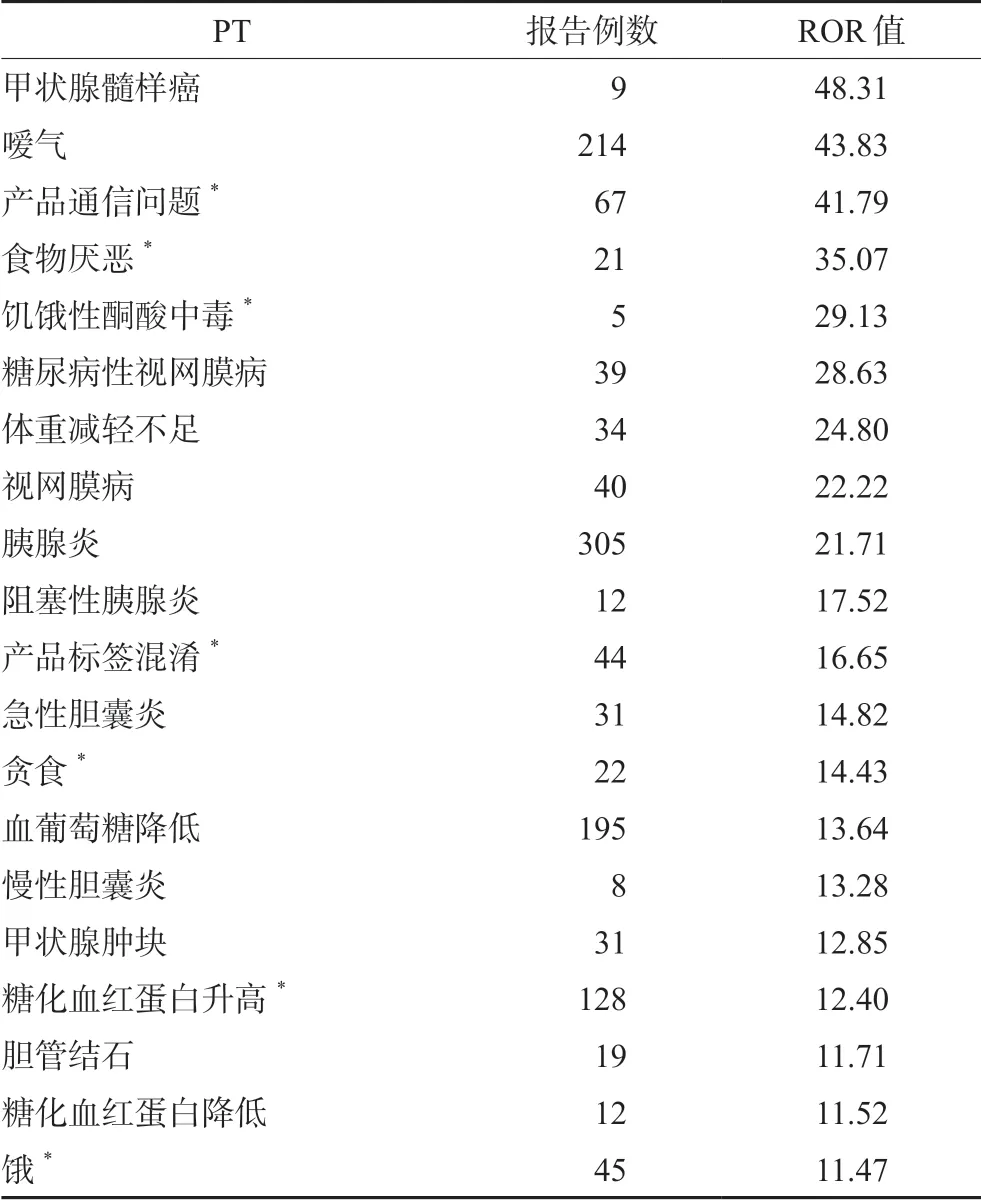
表4 司美格鲁肽信号强度前 20 位 ADE 信号Tab 4 Top 20 ADE signals of smeclutide signal intensity
3.1.2 产品问题 在产品问题方面,产品通信问题及标签混淆的信号强度高,导致产品配发错误较多,临床上常见的GLP-1RAs 包括艾塞那肽、度拉糖肽、利拉鲁肽和利司那肽,出现这些不良事件的原因可能是同类药品的通用名易混淆,如司美格鲁肽商品名为诺和泰,利拉鲁肽商品名为诺和力,医务人员在开药、取药等过程中易出现差错。医院药事管理中应加强易混淆药品管理。
3.1.3 胰腺的安全性 与健康人群相比,2 型糖尿病患者本身即存在胰腺炎发病率增高的风险,但仍存在少数接受GLP-1RAs 的患者发生胰腺炎的案例报道[10]。本研究也检测到司美格鲁肽具有胰腺炎及胰腺癌不良反应报告。一项关于利拉鲁肽的研究结果显示,胰腺炎的发生频数及信号强度均位于第二位[11],而本研究发现司美格鲁肽关于胰腺炎发生频数及信号强度位于第九位,提示司美格鲁肽的不良事件中胰腺炎构成比远低于利拉鲁肽。尽管目前对GLP-1RAs 引起的胰腺炎还有争议,但现在仍然将胰腺炎作为此类药物的风险,所以若有胰腺炎病史的患者应考虑其他治疗糖尿病的方法,若用药后疑似出现胰腺炎,应立即停药,并采取相应措施。
3.1.4 甲状腺的安全性 司美格鲁肽的两种制剂在美国都收到了关于甲状腺 C 细胞肿瘤的官方警告[12]。但这种ADE 仅在啮齿动物上有研究,机制研究显示,啮齿类动物甲状腺C 细胞中存在GLP-1 受体,GLP-1 受体激动剂可以特异性作用于GLP-1 受体激活甲状腺C 细胞,分泌降钙素,上调降钙素基因表达,从而诱导C 细胞增生和肿瘤形成[13]。但因临床数据有限,尚未明确啮齿动物中甲状腺C 细胞肿瘤是否与人类有相关性,所以人类使用本药后是否引发此种ADE 尚不明确。本研究显示,甲状腺髓样癌虽然报告数较少,但关联性是最大的,所以临床用药上需要特别注意此种ADE 的发生。
3.2 研究的局限性
首先,FAERS 数据来源大多数为美国、英国等欧洲国家,而亚洲国家报告的数据较少,不良反应的发生是否与国家、种族有关尚不明确,所以,研究结果可能与我国的情况有差异。其次,FAERS 数据库存在缺失、错误等情况,可能使结果出现误差。再次,本研究使用了比例失衡法中的ROR 法、PRR 法,可能存在假阳性信号的情况。最后,虽然本研究中检测出的 ADE 信号表示司美格鲁肽与该ADE 在统计学上具有相关性,但并不能代表它们在生物学上有因果联系,尚需进一步的临床试验进行探究[14]。在本研究中出现的说明书中未提及的不良反应,如血葡萄糖升高、糖化血红蛋白升高,这些可能是由于糖尿病的原发疾病而引起的;而神经紧张不安、注射恐惧,这些可能是糖尿病引起的病痛或者用药给患者造成心理上的痛苦所引起的。
4 结论
本研究基于美国FAERS 数据库,采用ROR 法和PRR 法对司美格鲁肽上市后的不良事件进行挖掘,结果与说明书基本一致。司美格鲁肽最常见的不良反应为恶心、呕吐、腹泻等,但大多为轻中度,且会随着用药次数而减轻。此外,对患有胰腺炎的患者应考虑使用其他抗糖尿病疗法。本研究对临床安全用药提供了一定的参考,丰富了司美格鲁肽的不良事件信息,有助于降低用药风险。
