临床药师参与1例血液透析患者经皮冠状动脉介入术后消化道出血的药学监护
2022-11-15何阳汤莹昕吴亮六安市中医院药剂科安徽六安237006
何阳,汤莹昕,吴亮(六安市中医院药剂科,安徽 六安 237006)
1 病例概况
患者,男性,91 岁,身高165 cm,体质量48 kg,2021年2月2日因“咳嗽喘闷1 d”结合心电图拟以急性冠脉综合征入院治疗。患者既往慢性肾脏病5 期10年,每周3 次规律血液透析治疗;脑梗死病史4年。入院诊断:急性冠脉综合征;慢性肾脏病5 期,肾性高血压;维持性血液透析;脑梗死后遗症期。
2 治疗经过
患者于入院当日行PCI 术,放入药物涂层支架1 枚,术后常规服用阿司匹林肠溶片100 mg po qd、替格瑞洛片90 mg po bid 抗血小板治疗;病程中患者因严重肾功能不全需血液透析,予依诺肝素钠注射液10 mg 血液净化用预防体外循环凝血;同时予抗感染、强心、调脂、平喘等药物治疗。入院血压140/75 mmHg(1 mmHg =0.133 kPa),查肾功能示:尿素13.56 mmol·L-1↑,血肌酐704.52 μmol·L-1↑;血常规示:血红蛋白(Hb)137.00 g·L-1,红细胞(RBC)6.15×1012·L-1,红细胞比容(HCT)43.10%,血小板计数(PLT)178×109·L-1(见图1);粪便隐血:阴性。2月9日患者大便色黑,腹痛明显,血常规示:Hb 105.00 g·L-1↓,RBC 4.62×1012·L-1,HCT 33.30%↓,PLT 186×109·L-1;粪便隐血阳性,提示上消化道出血。临床停用阿司匹林、替格瑞洛抗血小板药物,予质子泵抑制剂(PPI)注射用艾司奥美拉唑钠40 mg 静脉滴注q8h 和注射用生长抑素4.5 mg静脉泵入 q8h 护胃和止血治疗。在临床药师建议下,停用依诺肝素体外抗凝,予无肝素透析。2月19日由于患者出血进一步加重:血常规示Hb 81 g·L-1↓、RBC 3.52×1012·L-1、HCT 24.90%↓、PLT 86×109·L-1↓,考虑严重消化道出血,分别于2月19日、2月22日输注悬浮红细胞1.5 U、2.0 U。2月25日患者未再解黑便,电解质示血钙1.74 mmol·L-1,消化道出血相关症状、指标趋于稳定。同时患者体外通路出现血凝块,临床药师建议透析时恢复依诺肝素注射液血液净化,因患者透析器血凝块现象严重,依诺肝素剂量增加至20 mg 并于透析结束后予鱼精蛋白中和预防出血。2月27日患者右下肢静脉彩超提示右下肢静脉血栓形成,血常规示血红蛋白不再降低,已稳定3日,临床药师建议:① 暂不推荐全身抗凝治疗,可予地奥司明片0.45 g po bid 以及抬高患肢、弹力袜等物理治疗预防血栓进一步加重;② 推迟抗血小板治疗的重启,临床采纳。3月8日患者未再解黑便,出血相关指标稳定,同时心前区不适改善,透析器血凝块较前减少,病情好转予以出院。临床药师建议可恢复硫酸氢氯吡格雷片75 mg po qd 出院抗血小板治疗,临床采纳。
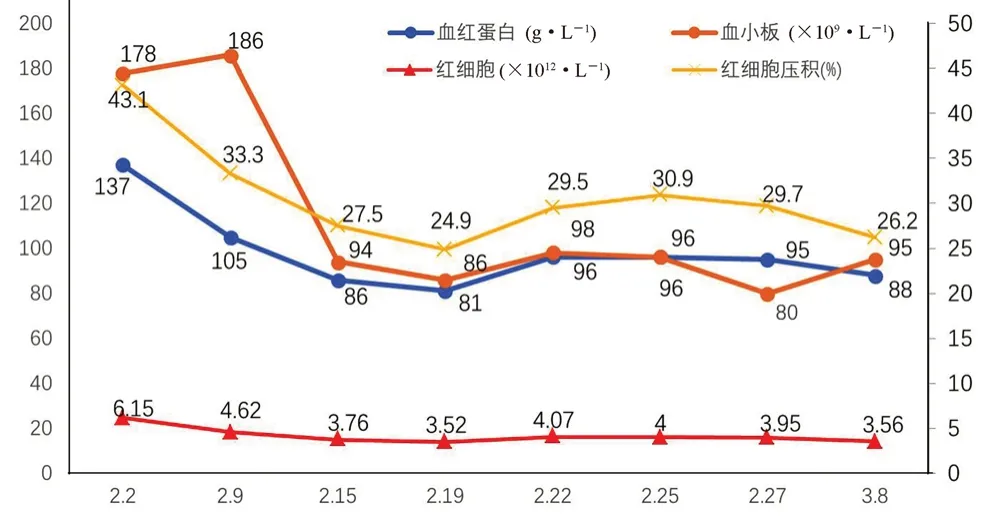
图1 患者住院期间血红蛋白、血小板、红细胞、红细胞比容变化趋势图
3 分析讨论
3.1 临床药师参与患者抗血小板治疗方案的调整
对PCI 术置入药物涂层支架的患者,若无禁忌证需要双联抗血小板治疗(DAPT)维持治疗至少12 个月,PCI 术后中断DAPT 会增加支架内血栓的风险。同时由于阿司匹林和氯吡格雷均通过肾脏清除,研究表明血液透析患者会对阿司匹林和氯吡格雷等药物治疗的抗血小板反应降低,且常表现出血小板高反应性(high on-treatment platelet reactivity,HPR),导致血小板活性抑制不足,血栓事件发生风险较高[1-2]。另一方面,在抗栓治疗过程中出现消化道出血亦会增加死亡风险,因此需要综合评估缺血和出血风险,制订个体化的临床治疗方案。
2月2日患者PCI 术后常规给予阿司匹林联合替格瑞洛双联抗血小板治疗,由于其出血风险较高且未考虑使用氯吡格雷换用替格瑞洛,2月9日患者出现消化道出血事件。根据相关指南建议,对于严重出血(BARC 出血分型≥3 型)的患者,应减少抗栓药物种类及剂量;当出血无法控制或可能威胁生命时,应立即停药并予输血等治疗。2月9日患者BARC 出血类型为3a 型,属于严重出血,应减少抗栓药物种类及剂量,临床停用抗血小板药物治疗。2月19日、2月22日患者出血情况进一步加重,临床予输血治疗。2月27日,患者控制出血稳定3日,能否恢复抗血小板治疗存在争议,临床药师认为虽然相关指南推荐控制出血后3 ~5日可恢复抗血小板治疗,但该患者肾功能严重不全,在CRUSADE、HAS-BLED 等出血风险评分中皆属于出血高危风险[2],根据其特殊病情临床药师建议推迟重启抗血小板治疗,临床采纳。3月8日,由于患者抗血小板药物已停用1 个月,需重点考虑支架血栓形成风险。支架血栓形成虽发生率较低(30 d 内发生率0.6%),但病死率高达45%,其中肾功能不全、停用DAPT等属于高危患者[3]。距PCI 术后7 d、1个月、3 ~6个月内支架血栓风险逐级上升,因此停用抗血小板治疗的时间不宜超过1 个月。该患者Hb 在不输血情况下已稳定12日,符合恢复抗血小板治疗指征,另外对于进行DAPT 的上消化道出血患者,相关指南建议优先恢复单一抗血小板治疗(SAPT)。相对于阿司匹林,P2Y12 抑制剂联合PPI 消化道出血的风险更低[3];同时新型P2Y12抑制剂替格瑞洛虽然相比氯吡格雷抗血小板疗效更优,但出血发生率也较高[4],因此临床药师建议先恢复氯吡格雷单一抗血小板治疗,临床采纳。
3.2 临床药师参与患者抗凝治疗方案的调整
患者入院时因慢性肾脏病5 期行血液透析治疗,《血液透析临床实践指南》建议抗凝治疗可防止在过滤装置和体外通路中形成血栓。低分子肝素因给药方便以及生物相容性较好,成为常用的抗凝药物,但是当患者出血风险增加时,应尽快停止或减少抗凝治疗[5]。因此2月9日患者发生消化道出血后,临床药师建议在停止DAPT 的同时应停用依诺肝素体外抗凝,予无肝素血液透析[6],临床采纳。2月9日至2月24日期间,由于长时间无肝素透析不能减轻血凝块的形成,在透析过程中血凝块一旦形成就会导致有效循环血量减少,透析器凝血检测和血液系统检测表现出低效率透析。透析过程中不使用抗凝剂是为尽量减少因抗凝造成的出血风险增加,但当出现管路凝血堵塞时造成凝血因子和血小板更多消耗,反而会增加出血风险[7],因此2月25日患者体外通路出现血凝块时需及时恢复体外抗凝。临床认为对于无肝衰竭的既往出血史患者,血液透析时使用枸橼酸盐局部抗凝,其抗凝效力几乎与肝素相当,且出血风险更低[8]。但由于患者血钙浓度较低(1.74 mmol·L-1),属于枸橼酸盐抗凝禁忌证,临床药师建议恢复依诺肝素体外抗凝。
2月27日患者右下肢静脉彩超提示右下肢深静脉血栓(deep venous thrombosis,DVT)形成,相关指南建议DVT 应积极开始抗凝治疗,但有出血并发症的患者应先稳定出血,需延迟或中止抗凝治疗。同时静脉活性药物治疗、物理治疗可一定程度改善DVT 症状,预防血栓进一步加重[9-10]。因此临床药师建议暂不全身抗凝,予地奥司明药物治疗及抬高患肢、弹力袜等物理治疗。
3.3 临床药师参与患者出院用药方案的制订
患者出院时服用氯吡格雷联合质子泵抑制剂(PPI)治疗,未予DAPT 及全身抗凝治疗。文献建议DAPT 期间因出血中断的患者,病情稳定后在确保安全的情况下应尽快恢复DAPT,且患者DAPT 评分大于25 分,仅需短期DAPT[11]。同时患者出血稳定后,下肢DVT 也需要短期抗凝治疗。《2016年急性冠状动脉综合征抗栓治疗合并出血防治多学科专家共识》提出,满足以下条件考虑出血已经得到控制:① 血流动力学稳定;②不输血情况下,Hb 稳定;③ 尿素氮不继续升高;④ 肠鸣音不活跃;⑤ 便潜血转阴。综上所述,临床药师建议患者出院后3 ~7日复查血压、血常规、肾功能、粪便隐血等指标,指标稳定后可进行抗栓治疗:① 应用阿司匹林联合氯吡格雷治疗3 个月,抗血小板治疗期间服用PPI 3 ~6 个月,之后考虑继续或间断服用PPI[12-13];② 短期使用低分子肝素全身抗凝3 个月,若仍有使用禁忌证可考虑植入下腔静脉滤器。
4 小结
PCI 术后由于伴随较高的支架血栓风险,需长期服用抗血小板药物,然而DAPT 引起的消化道出血使临床面临艰难抉择,若患者同时因血液透析需体外抗凝,将进一步提高抗栓治疗难度。本次案例临床药师在患者恢复抗血小板药物的时机及药物选择、体内外抗凝的停用及重启提供药物服务意见,为临床安全、有效地用药提供保障。
