卡维地洛预处理的人脐静脉内皮细胞低密度脂蛋白诱导损伤情况观察
2022-09-02徐红补娟闫凯欣周玲
徐红,补娟,闫凯欣,周玲
1 新疆维吾尔自治区人民医院老年医学中心,乌鲁木齐 830001;2 新疆维吾尔自治区人民医院基础医学教育中心
动脉粥样硬化(AS)是脂质成分持续在血管内膜累积,逐渐在血管内壁形成动脉粥样硬化斑块的疾病,是许多心脑血管疾病发生发展的重要病理生理基础[1]。当血管内皮细胞受到损伤时,其通透性在高脂、活性氧、促炎细胞因子等因素的刺激下会进一步增大,进而导致炎症细胞浸润和脂质成分累积于血管壁受损处,导致血管内壁增厚,管腔发生狭窄,促进AS 的发生[2]。在进行血管内皮细胞实验时,通常选用的细胞模型为人脐静脉内皮细胞(HUVECs)建立模型,其具有干细胞的潜能,能够多次进行传代[3]。氧化型低密度脂蛋白(ox-LDL)能引起内皮细胞发生损伤,从而使脂质成分、炎症细胞在损伤局部浸润,并促进AS的形成,在AS的发生过程中有着非常关键的作用[4]。他汀类药物常用于治疗AS,其能够降低血脂,缓解疾病的进展,但存在肌肉毒性反应、血糖升高和糖尿病、肝肾功能异常及脑卒中等不良反应。卡维地洛对钙离子通道有阻断作用,其通过α1受体阻断作用和非选择性的β受体阻断作用而引起两种毛细血管的扩张,减少外周阻力和降低血压。卡维地洛不仅能扩张冠状动脉及肾血管,降低外周血管阻力,还能降低体循环和肺循环阻力,在心力衰竭的基础研究[5]以及临床治疗急性心肌梗死[6]中具有抗炎和抗氧化作用。2020 年12 月—2021年5月,我们以HUVECs 为实验对象,给予不同浓度卡维地洛干预,后以ox-LDL 诱导细胞损伤,观察卡维地洛预处理的HUVECs ox-LDL 诱导损伤情况。
1 材料与方法
1.1 细胞、主要试剂及仪器 HUVECs 购买自凯基生物有限公司。DMEM(高糖)培养基和胰酶(0.25%Trypsin-EDTA)、青霉素—链霉素双抗(10 000 U)均为美国Gibco 公司产品,胎牛血清(FBS)购自Excell Bio 公司,PBS 磷酸盐缓冲液粉剂为北京中杉金桥生物产品,DMSO(细胞冻存液)购自Sigma 公司,CCK-8 细胞增殖/毒性检测试剂盒购自全式金生物公司,ox-LDL 购自广州奕元生物公司,卡维地洛购自北京巨能制药公司,LDH 检测试剂盒为欧易生物科技有限公司产品,油红O 染色试剂盒购自南京建成公司,15 mL 离心管、2 mL 冻存管、25 cm2培养瓶均购自Corning 公司。O2细胞培养箱(型号:Smart Cell HF-90)、生物安全柜及台式低速离心机(型号:DK-80)购自上海力康仪器有限公司,-20 ℃低温冰箱(型号:BCD-249LCK)、-80 ℃低温冰箱(型号:DW-HL388)来源于合肥美菱公司,手动单道移液器购自Eppendorf 公司(型号:Research plus),液氮罐购自成都金凤仪器厂(型号:YDS-50-125),荧光倒置显微镜来源于日本尼康公司(型号:Eclipse TS100-F),酶标仪采购自Bio-Rad 公司(型号:xMarkTM)。
1.2 HUVECs 培养 HUVECs 培养于DMEM(高糖)培养基+10%FBS+1%PS中,培养环境为37 ℃、5%CO2、饱和湿度。
1.3 HUVECs 分组、卡维地洛给予方法、ox-LDL 诱导及细胞活性检测 采用微板法。取生长状态良好汇合率达90%的HUVECs,按5×104个细胞/孔,接种于96孔板,置于37 ℃、饱和湿度、5%CO2细胞培养箱中培养24 h。将细胞分为5 组,A、B、C 组(测定组)分别加入5、10、20 µmol/L 卡维地洛预处理6 h,再加入100µg/mL 的ox-LDL 诱导培养24 h;D 组(对照组)加入100 µg/mL 的ox-LDL 诱导培养24 h;E 组(空白组)加入不含细胞的DMEM(高糖)培养基;每组3 个重复。对细胞进行离心处理10 min。每孔小心转移20µL 上清至96 孔板中。再加入25µL 反应混合液,室温孵育15 min,避光操作。用酶标仪在450 nm 处检测所有样本的OD 值。计算细胞活性,LDH 浓度(U/L)=(测定组OD 值-对照组OD值)/(对照组OD 值-空白组OD 值)/×标准品浓度(0.2 µmol/mL)×1 000。以LDH 浓 度 反 映 细 胞活性。
1.4 HUVECs 分组、卡维地洛给予方法、ox-LDL 诱导及细胞增殖率测算 采用CCK-8 法。取生长状态良好汇合率达90%的HUVECs,按5×104个细胞/孔,接种于96 孔板,置于37 ℃、饱和湿度、5%CO2细胞培养箱中培养24 h。分组及干预方法同“1.3”。待干预完成后,弃去培养基,各孔均加入100 µL 配置好的10%CCK-8 溶液,培养1 h 后放入酶标仪,测定450 nm 处的OD 值。计算细胞增殖率,细胞增殖率(%)=(实验组OD 值-空白组OD值)/空白组OD 值×100%。A、B、C、D 组是实验组,E 组为空白组。
1.5 HUVECs 分组、卡维地洛给予方法、ox-LDL 诱导及胞内脂滴形成情况观察 采用油红0 染色法。取生长状态良好汇合率达90%的HUVECs,按5×104个细胞/孔,接种于96 孔板,置于37 ℃、饱和湿度、5%CO2细胞培养箱中培养24 h。分组及干预方法同“1.3”,每组3 个重复,干预完毕后,丢弃培养基,用PBS进行2次冲洗;将细胞用4%的甲醛固定液500µL固定、冲洗,然后加入油红O染液对先前处理的细胞进行染色,染色时间设置为10 min。丢弃染液,PBS洗2 次,弃多余的染料,然后加入500µL 复染液,染色1 min,PBS洗2遍,用倒置显微镜观察胞内脂滴形成情况(反应卡维地洛对氧化低密度脂蛋白诱导的HUEVCs 损伤的保护作用,抑制脂滴形成,减轻动脉粥样硬化),并拍照。
1.6 统计学方法 采用SPSS21.0 统计软件。符合正态分布的计量资料以±s表示,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2 结果
2.1 各组LDH 活性比较 A、B、C、D、E 组LDH 活性 分 别 为(201.802 ± 27.738)、(226.126 ±12.483)、(253.521 ± 26.871)、(310.811 ±32.880)、(194.595±16.878)U/L,B、C、D 组分别与E组比较,A、B、C组分别与D组比较,P均<0.05。
2.2 各组细胞OD 值及增殖率比较 细胞OD 值及增殖率比较见表1。
表1 各组细胞OD值及增殖率比较(±s)
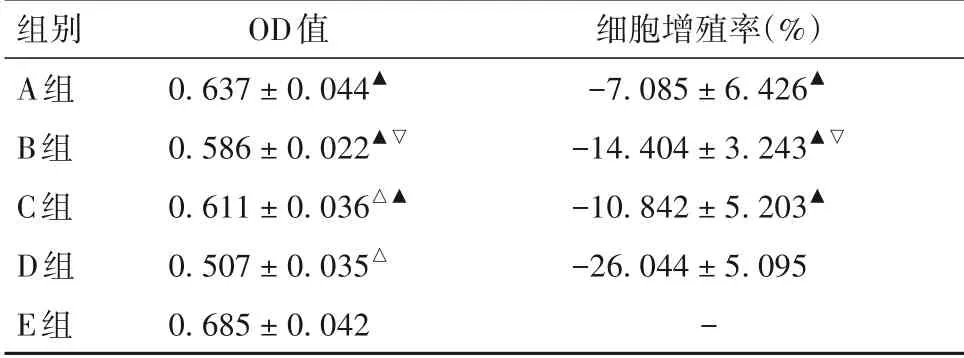
表1 各组细胞OD值及增殖率比较(±s)
注:与E 组比较,△P<0.05;与D 组比较,▲P<0.05;与A 组比较,▽P<0.05。
组别A组B组C组D组E组OD值0.637±0.044▲0.586±0.022▲▽0.611±0.036△▲0.507±0.035△0.685±0.042细胞增殖率(%)-7.085±6.426▲-14.404±3.243▲▽-10.842±5.203▲-26.044±5.095-
2.3 各组细胞胞内脂滴形成情况比较 与E 组比较,D 组细胞内红色脂滴积累显著增加;与D 组比较,A、B、C组细胞保内脂滴形成明显减少,其中以A组抑制脂滴积累效果最为明显(详见图1)。
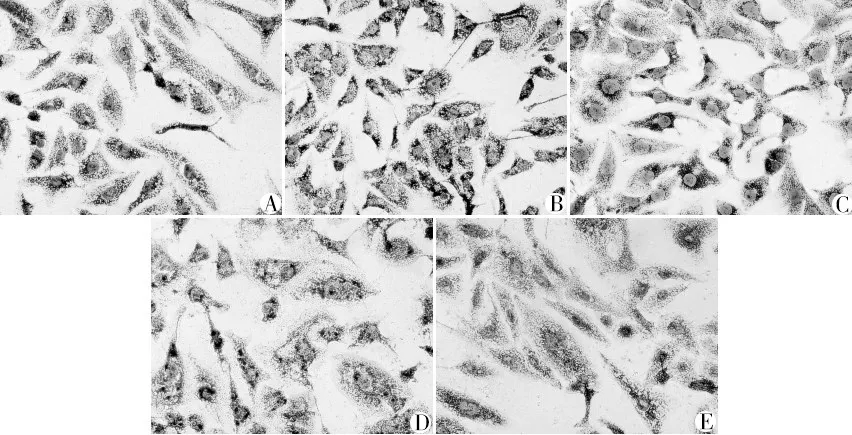
图1 各组胞内脂滴形成情况(油红0染色,×200)
3 讨论
AS 是一种临床常见的好发于大、中动脉的疾病,以动脉内膜脂质沉积、粥样斑块形成为特征,是冠状动脉疾病、脑梗塞和外周动脉硬化等疾病的重要病理基础。既往多用他汀类药物对AS 进行治疗,具有较理想的临床疗效,但仍偶有肝酶增高、肌肉酸痛等不良反应。故为更好提供药物治疗的理论依据,本实验选用HUVECs 来构建细胞模型进行研究。多项细胞实验均以ox-LDL 诱导内皮细胞损伤模型,作为研究AS 病理生理机制及防治手段的细胞模型[7-8]。本实验参考ZENG[9]等学者的研究结果,细胞模型的建立选用100 mg/L 的ox-LDL 培养HUVEC 细胞24 h,细胞活力均明显降低,表明ox-LDL 诱导HUVEC 损伤造模成功,后续将在该模型中研究内皮损伤的防治手段,进而为AS 的防治提供依据。
卡维地洛是临床常用的第三代β 受体阻滞剂,对于高血压及心肌梗死引起的心室重构具有改善作用[10-11]。在体外和体内研究中,均观察到了卡维地洛对于内皮细胞损伤的多种保护作用[12]。先前有临床研究[13]表明,卡维地洛对阿霉素引起的HUVECs损伤有一定的保护作用。同样有研究[14-15]证实,卡维地洛通过作用于HUVECs 线粒体,发挥对细胞的保护功能和心脏、外周血管疾病的改善作用。也有研究[16]发现,卡维地洛对AS 大鼠的动脉病理改变具有一定的改善作用。故本研究将ox-LDL 诱导的HUVECs 损伤来作为AS 的模型,以LDH 活性水平、细胞增殖情况、以及脂滴的形成程度作为观察指标,以卡维地洛作为药物干预措施,旨在研究卡维地洛对ox-LDL 诱导人脐静脉内皮细胞损伤的抑制作用。
正常情况下,LDH 不能透过细胞膜流出胞外,但当细胞受到损伤时,LDH 能够释放到细胞外,故LDH 水平的增高提示细胞活性的减低。本研究显示,与E 组比较,B、C、D 组LDH 活性增强;与D组比较,A、B、C 组LDH 活性减弱;与E 组比较,C、D 组OD 值减小;与D 组比较,A、B、C 组细胞OD 值及增殖率增加;与A 组比较,B 细胞OD 值及增殖率减小;与E 组比较,D 组细胞内红色脂滴积累显著增加;与D 组比较,A、B、C 组细胞保内脂滴形成明显减轻,其中以A 组抑制脂滴积累效果最为明显。提示卡维地洛能够抑制ox-LDL 诱导的HUVECs 细胞受损,促进细胞增殖,抑制胞内脂滴的形成,其中以A 组的作用效果最为显著,证实卡维地洛对ox-LDL 诱导的HUVECs 发生的AS 有保护作用。同样有研究[16]表明,适当浓度的卡维地洛对AS 的保护作用更加理想,与本研究实验结果吻合。由此我们认为,ox-LDL 能够对HUVECs 造成损伤,降低细胞活性,抑制细胞增殖,促进脂滴的形成,为AS 疾病的形成提供基础,而卡维地洛能对ox-LDL 诱导的HUVECs 的损伤发挥一定的保护作用。
本研究仅显示卡维地洛对ox-LDL 诱导的HUVECs 发生的AS 具有保护作用,但尚未探讨其具体机制。有文献[17]表明,卡维地洛也许是通过作用于NF-κB/COX-2/iNOS 途径来发挥其抗氧化和抗炎的作用。研究显示,卡维地洛能通过抑制乙二醇引起的组织学扰动和肾脏的NF-κB、p65等炎症因子表达,以及血清部分细胞因子水平的表达,来发挥其抗炎抗氧化作用[18]。相信随着研究的深入,特别是对其作用机制的系统探索,将为AS的临床治疗提供新的途径。
总之,卡维地洛预处理可以减弱ox-LDL 诱导HUVECs 损 伤,尤 以 浓 度 为5 µmol/L 时 效 果最佳。
