新型一氧化氮生物医学传感功能材料的制备及表征
2022-09-02陈道明郑霄刘晓军朱春楠刘超郑冬云
陈道明,郑霄,刘晓军,朱春楠,刘超,郑冬云
(中南民族大学 生物医学工程学院& 脑认知国家民委重点实验室&医学信息分析及肿瘤诊疗湖北省重点实验室,武汉430074)
金纳米颗粒(Au nanoparticles,AuNPs)作为一种典型的金属纳米粒子,因具有独特的光学、电学、较大的比表面积和良好的电催化活性,而在电化学传感领域应用广泛.已有研究将其用作电极修饰材料并应用于检测砷(III)[1]、酪氨酸[2]、多巴胺[3]等物质的高灵敏电化学传感.将AuNPs 及其复合物用作一氧化氮(nitric oxide,NO)敏感功能材料的工作也已见报道,但AuNPs通过化学合成法制备而成[4],合成过程中不可避免地使用了有毒化学试剂,这些试剂残留在AuNPs 中,会影响AuNPs 的生物兼容性;同时,实验废液最终会被释放进入环境,对环境和生物体的健康造成潜在威胁.因此,在所制备AuNPs的生物相容性以及AuNPs制备方法的环保性方面,尚有待改善.
有机染料导电聚合膜修饰电极具有稳定性好、催化性能高、选择性强等优点,已在电化学传感领域显示出良好的应用前景.例如,聚中性红、聚偶氮胭脂红、聚甲苯胺蓝、聚苋菜红、聚茜素红等有机染料聚合物薄膜已被应用于铬(VI)和镉(V)[5]、奥美拉唑和兰索拉唑[6]、过氧化氢[7]、色氨酸[8]等物质的电催化检测.灿烂甲酚蓝(brilliant cresyl blue,BCB),是一种氮杂苯类有机染料,常被用作活体染色剂、血液染色剂和氧化还原指示剂,其结构式如图1 所示.由图1可见:BCB 结构中有一个大的杂环共轭体系,且含有电子给体氨基.因此,可通过电化学聚合的方法将其聚合物薄膜修饰到电极表面,其电聚合过程与胺的电聚合类似,即具有自由基聚合的特点[9].为 书 写 方 便,通 常 将 聚 灿 烂 甲 酚 蓝 写 作PBCB[10]或PolyBCB[11]或Poly(BCB)[12].有关BCB 的电化学聚合[13]及其对多巴胺、维生素C[14]、甲醇[15]的电催化作用已见报道.作为一种氧化还原导电聚合物,PBCB 具有良好的电催化性能、快速的电荷转移能力以及离子传输能力[16].此外,PBCB 可在一定电位下氧化成相应的阳离子自由基[17],该阳离子自由基对同为自由基的NO 具有较强的结合作用,这为PBCB 对NO 的良好电催化能力及选择性提供了理论基础.
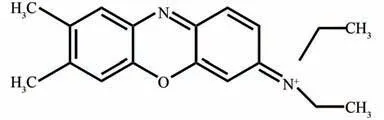
图1 灿烂甲酚蓝的结构式Fig.1 Structure formula of brilliant cresyl blue
一氧化氮(nitric oxide,NO)是人体天然产生的自由基,在机体免疫系统、血管稳态和神经系统中的信号转导中起着重要的作用.NO的分泌不足会导致高血压、动脉硬化等疾病,而过量的NO 会导致糖尿病、中风和感染性休克[18].神经系统疾病如帕金森氏病、阿尔茨海默病和多发性硬化都伴随着NO的过量产生.NO 在癌细胞中具有双重效应.它既能控制血管生成、细胞凋亡、细胞周期、细胞侵袭和血管扩张,也表现出杀瘤作用,揭示了NO 在体内作为潜在生物标志物的重要性.然而,由于NO 的自然状态、有限的水溶性、复杂的氧化性、化学性质和热学性质,在检测上产生了巨大的困难.电化学检测是一种简单易行的方法,具有便于微型化、可实现实时分析、灵敏度高、操作简单和成本低等特点[19].
为此,本文通过简单可控的电化学聚合法和绿色环保的电沉积法,制备出金纳米颗粒-聚灿烂甲酚蓝纳米复合膜,并实现纳米复合膜在玻碳电极表面的修饰固定,对纳米复合膜进行光谱学、形貌和电化学技术表征,并探讨纳米复合膜对NO 的电催化氧化,为新型高性能NO 生物医学传感器的研发提供基础.
1 实验部分
1.1 试剂与仪器
灿烂甲酚蓝、无水乙醇、甲醇、NaNO2、HNO3、H2SO4、NaOH、HCl、NaH2PO4、Na2HPO4、KCl、氯金酸、K2Fe(CN)6和K3Fe(CN)6均购自国药集团化学试剂有限公司;多巴胺(DA)、抗坏血酸(AA)和尿酸(UA)购自Sigma;高纯氮气(纯度99.999%)和高纯NO 气体(纯度99.999%)购自武汉纽瑞德特种气体有限公司,高纯氮气用于除去NO 检测底液中的氧气,高纯NO气体用于制备NO饱和溶液.
电化学实验均在CHI660D 电化学工作站上完成,采用传统的三电极系统:裸玻碳电极(glassy carbon electrode,GCE)或纳米复合膜修饰GCE 为工作电极,饱和甘汞电极(saturated calomel electrode,SCE)为参比电极,铂电极为对电极,CHI660D 电化学工作站、GCE、SCE 以及铂电极均购自上海辰华仪器有限公司;扫描电镜(scanning electron microscope,SEM)表征在场发射电镜-SU8010 上进行;疏水碳纸(10 cm×10 cm)购自高仕睿联(天津)光电科技有限公司,用作X 射线光电子能谱(XPS)表征时的基底;XPS 表征在X 射线光电子能谱仪(EscalabXi+,赛默飞)上进行;CL-200 型集热式恒温加热磁力搅拌(金坛市予仪器有限责任公司)用于溶液加热;pHS-3E 酸度计(上海佑科仪器仪表有限公司)用于调节溶液pH 值;KQ3200DB 超声仪(上海科导超声仪器有限公司)用于工作电极的清洗及溶液的混合;PGUV-10-AS 超纯水仪(武汉品冠仪器设备有限公司)用于实验用超纯水的制备.
不同pH 值磷酸盐缓冲溶液(phosphate buffered saline,PBS)的配制:先用超纯水制备磷酸 盐 缓 冲 溶 液(PBS),其 中 含 有137 mmol·L-1NaCl、2.7 mmol·L-1KCl、8.0 mmol·L-1Na2HPO4和1.5 mmol·L-1KH2PO4,再 根 据 实 验 需 要,用0.1 mmol·L-1NaOH 或0.1 mmol·L-1HCl 在pHS-3E 酸度计上对其pH 值进行调节.
1.2 不同电极的制备
纳米复合膜修饰GCE 的制备过程如下.
(1)裸GCE 的抛光处理:将直径为3 mm 的GCE 在含有抛光粉(直径为50 nm 的Al2O3)浆液的绒布上打圈研磨,抛光至镜面,再依次用体积比为1∶1 的硝酸水溶液、无水乙醇和超纯水对其进行超声清洗,并置于室温下自然晾干.
(2)裸GCE 的电化学预处理:将抛光处理好的GCE 置于0.5 mol·L-1的H2SO4溶液中,采用循环伏安法,在-0.5~1.5 V 的电位范围以60 mV·s-1的扫描速率扫描10 圈,以达到对裸GCE 表面进行活化处理的目的.
(3)聚BCB 修饰GCE 的制备:将电化学活化后的GCE 浸入聚合底液中,聚合底液由0.5 mmol·L-1BCB、0.2 mol·L-1NaNO3和0.1 mol·L-1PBS(pH=7.4)共同构成,借助于循环伏安法,首先在-0.8~1.8 V 这一引发电位范围内,以50 mV·s-1的扫描速率环扫15 圈,然后在-0.8~0.8 V 的聚合电位范围内以50 mV·s-1的扫描速率环扫15圈,制得PBCB/GCE.
(4)纳米复合膜修饰GCE 的制备:将PBCB/GCE 置于含有1.11×10-3mol·L-1氯金酸的0.1 mol·L-1PBS(pH=7.4)中,在-0.8~1.2 V 的电位范围内,以50 mV·s-1的扫描速率环扫10 圈,即可制得AuNPs/PBCB/GCE,其制备过程示意图如图2所示.
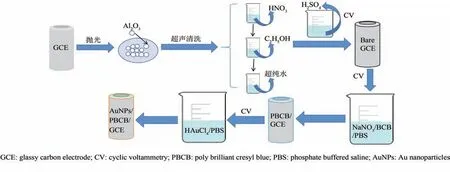
图2 AuNPs/PBCB/GCE 的制备过程示意图Fig.2 Schematic diagram of the preparation process of AuNPs/PBCB/GCE
为对比不同薄膜对NO 的电催化效果,本文还制备了其他几种薄膜修饰电极,其制备过程分述如下.
一步法PBCB/GCE 的制备:首先按照前述步骤(1)、(2)对裸GCE进行抛光清洗以及电化学预处理,然后将其置于由0.5 mmol·L-1BCB、0.2 mol·L-1NaNO3和0.1 mol·L-1PBS(pH=7.4)共同构成的聚合底液中,在-0.8~0.8 V的聚合电位范围内以50 mV·s-1的扫描速率环扫15圈,制得一步法PBCB(onestep)/GCE.
二步法PBCB/GCE 的制备:裸GCE 的抛光清洗以及电化学预处理过程依据前述步骤(1)、(2)进行,然后将其置于由0.5 mmol·L-1BCB、0.2 mol·L-1NaNO3和0.1 mol·L-1PBS(pH=7.4)共同构成的聚合底液中,首先在引发电位范围内(-0.8~1.8 V),以50 mV·s-1的扫描速率环扫15 圈,然后在聚合电位范围内(-0.8~0.8 V)以50 mV·s-1的扫描速率环扫15 圈,制得二步法PBCB(twosteps)/GCE.
AuNPs/GCE 的制备:预处理好的GCE 置于含有1.11×10-3mol·L-1氯金酸的0.1 mol·L-1PBS(pH=7.4)中,在-0.8~1.2 V 的电位范围内,以50 mV·s-1的扫描速率环扫10圈,即可制得AuNPs/GCE.
所有修饰电极在使用前,均在0.1 mol·L-1pH=7.4 的PBS 中,以100 mV·s-1的扫描速率在0.3~1.0 V范围内环扫10圈,以获得稳定的电化学背景信号.
2 结果与讨论
2.1 纳米复合膜制备及使用条件优化
2.1.1 PBCB制备方法优选
已见报道的聚灿烂甲酚蓝(PBCB)膜制备方法有两种,分别是一步法和二步法.MARIANA 等[20]通过一步电聚合法制备了PBCB 修饰玻碳电极,并将其应用于葡萄糖的生物传感.DING等[21]则采用二步电聚合法制备了PBCB 薄膜,并将其固定于石墨烯修饰玻碳电极表面,构建了一种肾上腺素电化学传感界面.一步法和二步法的主要区别在于:一步法是对BCB 进行直接电聚合;而二步法是先进行电引发过程,再进行电聚合.为保证所制备的AuNPs-PBCB 纳米复合膜对NO 具有较好的电催化效应,首先对PBCB的制备方法进行了优选.
分别采用一步法和二步法制得AuNPs/PBCB(onestep)/GCE 和AuNPs/PBCB(twosteps)/GCE,并 对比了其对NO 的电催化效果.二步法中,BCB 的电聚合过程如图3(a)所示,在图3(a)中可观察到一对明显的氧化还原峰,氧化峰电位约为-0.22 V,还原峰电位约为-0.34 V,表观电位约为-0.29 V,与单体BCB 氧化并随后还原为阳离子自由基有关[17].此外,氧化还原峰电流随着扫描圈数的增加而逐渐增大,表明PBCB 薄膜在GCE 表面逐渐形成.
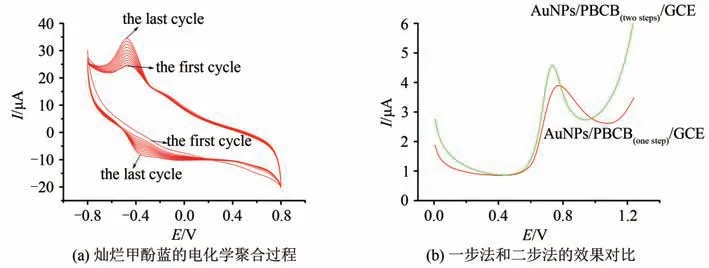
图3 灿烂甲酚蓝电化学聚合及不同聚合方式的效果对比图Fig.3 Brilliant cresyl blue electrochemical polymerization and comparison of the effects of different polymerization methods
图3(b)展示了相同浓度的NO 在AuNPs/PBCB(onestep)/GCE 和AuNPs/PBCB(twosteps)/GCE 上 的 电化学响应.在AuNPs/PBCB(onestep)/GCE 上,可以观察到一个峰形较钝的氧化峰,峰电位为0.76 V,峰电流为2.29 μA[图3(b)红线];而在AuNPs/PBCB(twosteps)/GCE 上,出现了一个峰形尖锐的氧化峰,峰电位为0.73 V,峰电流为2.83 μA[图3(b)绿线].显然,在二步法电聚合PBCB 的基础上所制备的AuNPs/PBCB(twosteps)纳米复合物薄膜对NO 的电化学氧化具有更显著的催化效应,这可能是因为二步法聚合前的电引发过程更有利于制备出结构及性能良好的聚合物膜.电引发过程具有产生阳离子自由基的作用,所产生的阳离子自由基之间以及自由基与BCB单体之间均可发生反应生成BCB 低聚物,BCB 低聚物可在更低的电位下氧化成相应的阳离子自由基,并进一步与BCB 单体或游离的阳离子自由基反应生成更大分子量的BCB 聚合物.因此聚合前的电引发过程有利于BCB 在较低的电位区间内进行电聚合,且有助于获得结构和性能良好的PBCB薄膜.
2.1.2 其他条件优化
为完善AuNPs/PBCB 纳米复合膜对NO 的高灵敏电催化性能,借助于电化学分析技术,对影响纳米复合膜性能的多种条件进行了实验优化,结果如图4 所示.根据图4 的结果,确定了本体系中AuNPs/PBCB 纳米复合膜的制备及使用条件,概况如下:(a)BCB 的最佳引发扫描圈数为15 圈;(b)BCB 的最佳电聚合圈数为15 圈;(c)AuNPs 的最佳电沉积圈数为10 圈;(d)检测底液的最佳pH 值为7.0,考虑到实际生物医学应用的需要,本文采用pH 值为7.4 的生理缓冲溶液;(e)最佳富集电位为-0.6 V;(f)最佳富集时间为10 s.
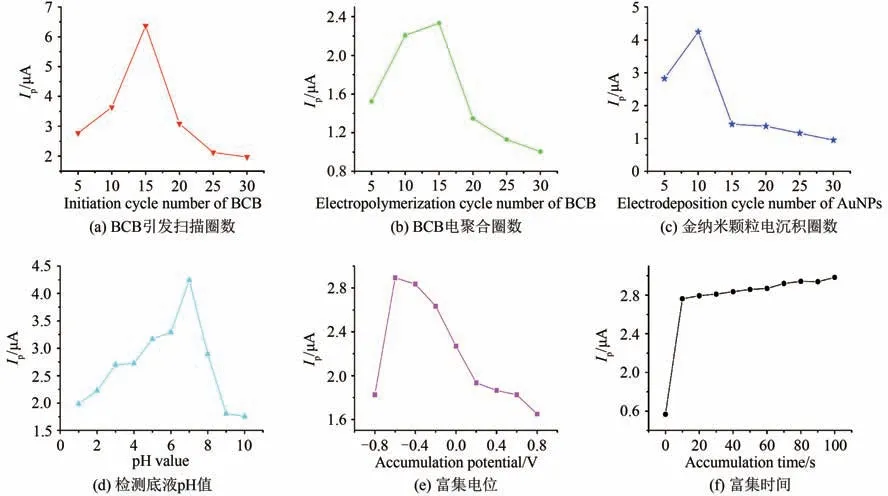
图4 条件优化图Fig.4 Diagram of condition optimization
2.2 纳米复合膜对NO的选择性电催化
为确认所制备的纳米复合膜对NO 的电催化能力,借助于差分脉冲伏安法,对2.25×10-5mol·L-1NO在不同电极上的电化学响应进行了对比分析,结果如图5 所示.由图5 可见:当底液中没有NO 存在时,观察不到明显的电化学响应信号;在裸GCE 上,仅在0.94 V 附近出现了一个很微弱的电化学信号,峰电流约为0.8 μA;在PBCB/GCE 上,NO 的电化学响应有所改善,峰电位负移至0.76 V,峰电流增大至1.15 μA,但峰形较钝;NO 在AuNPs/GCE 上的电化学响应改善更加明显,氧化峰电流增大至2.09 μA,但峰电位相较于PBCB/GCE 略微正移,为0.77 V;相较于其他电极,NO 在AuNPs/PBCB/GCE 的电化学响应最为灵敏,峰形尖锐,峰电位为0.75 V,峰电流为3.24 μA.结果表明:AuNPs/PBCB 纳米复合膜对NO的电化学氧化具有明显的电催化作用,这归功于AuNPs和PBCB 的协同作用.AuNPs具有较大的比表面积,有助于增大修饰电极的表面积,从而提高NO在电极表面的富集量;同时,AuNPs还具有良好的导电性,可有效促进NO 与电极之间的电子传递;而导电聚合物PBCB 则可作为电子媒介体在NO 的电化学氧化过程中发挥催化作用.

图5 不同电极的效果对比图Fig.5 Comparison of the effect of different electrodes
为满足生物医学应用需求,AuNPs-PBCB 纳米复合膜还应对NO 的检测具有良好选择性.借助于安培响应法,对该选择性进行了考察.将制备好的AuNPs/PBCB/GCE 置于5 mL 浓度为0.1 mol·L-1的无氧磷酸盐缓冲溶液(pH=7.4)中,设置工作电位为0.8 V,进行实验.在200 s 时,用微量进样器向底液中加入100 μL NO 饱和溶液(1.8×10-3mol·L-1),随后每隔50 s,依次向底液中加入5 倍浓度的多巴胺(DA)、抗坏血酸(AA)、尿酸(UA)、甲醇(MeOH)以及亚硝酸盐(NO2-),最后,于大概500 s时,再向底液中加入100 μL NO 饱和溶液,结果如图6 所示.由图6 可见:5 倍浓度的DA、AA、UA、MeOH 和NO2-均未对3.6×10-5mol·L-1NO 的测定产生明显干扰,表明AuNPs/PBCB 纳米复合膜对NO 具有良好的选择性,这归功于PBCB 中的阳离子自由基对NO 自由基的良好捕捉能力.
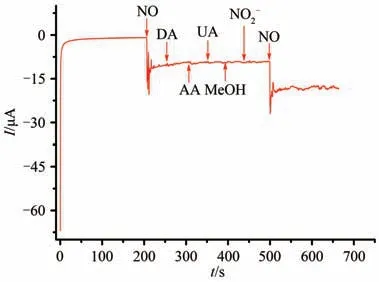
图6 抗干扰性能考察Fig.6 Investigation of anti-interference performance
2.3 纳米复合膜的表征
2.3.1 XPS表征
借助于X 射线光电子能谱(XPS)技术,对AuNPs/PBCB 纳米复合膜在电极表面的形成进行了进一步确认,结果如图7 所示.以AuNPs/PBCB 纳米复合膜修饰碳纸为基底,图7的XPS表征结果显示:电极表面存在的主要元素有C、Au、O 和N,其中,含量最高的是C 元素[图7(a)],这是因为XPS 表征是以碳纸为基底进行的,所以C 元素既来源于碳纸基底,也来源于PBCB,284.8 eV 的峰对应于碳纸表面或PBCB 结构里C—H 中的C,292.6 eV 的峰可能对应于纳米复合膜制备过程中在碳纸表面形成的C=O中的C,或PBCB 结 构 里C=O 和C=N 中的C[22];图7(b)是被分解为两个自旋轨道的Au 4f 的XPS 光谱图,Au 4f7/2和4f5/2的峰分别位于键合能(BE)84.5 eV 和88.2 eV 处,归于金属单质Au[23];图7(c)中532.7 eV 的峰对应于O2-、OH 和C=O 中的O[22];图7(d)中400.8 eV的峰对应于PBCB结构里C—N和C=N 中的N[24].以上结果表明,AuNPs/PBCB 纳米复合膜被成功制备并固定于基底电极表面.
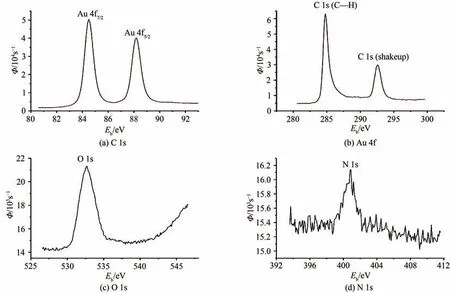
图7 AuNPs/PBCB纳米复合膜的XPS谱图Fig.7 XPS spectra of AuNPs/PBCB nanocomposite film
2.3.2 纳米复合膜的表面形貌表征
裸GCE、AuNPs/GCE 和AuNPs/PBCB/GCE 的扫描电镜图如图8 所示.由图8 可知:裸GCE 电极表面较光滑[图8(a)];电沉积AuNPs 在玻碳电极表面,可以观察到电极表面均匀分布着金纳米颗粒[图8(b)],这些小颗粒可以有效引导电子在电极和溶液之间传递,增加了电极的比表面积;AuNPs/PBCB/GCE 电极[图8(c)]整个表面呈现三维多孔结构,金纳米颗粒镶嵌在PBCB/GCE 电极表面.AuNPs/PBCB/GCE 复合膜具有较大的比表面积,提高了对NO 的电化学反应的催化性能.

图8 不同电极的扫描电镜图Fig.8 SEM images of different electrodes
2.3.3 电化学交流阻抗表征
电化学交流阻抗谱是研究修饰电极表面性质的有效工具,电子传递电阻是阻抗图中的半圆半径大小,它控制溶液与电极间氧化还原探针的界面电子传递速率,因此,电子传递电阻可用来描述电极的表面性质.本文中的电化学交流阻抗(EIS)测量是在底液为0.1 mol·L-1PBS 缓冲溶液(pH=7.4)中进行的,其中包含5.0 mmol·L-1Fe(CN)63-/4-,作为氧化还原探针,频率范围为1 Hz 到100 kHz.裸GCE、PBCB/GCE、AuNPs/PBCB/GCE 修饰电极的EIS图如图9所示.由图9 可见:裸GCE 的交流阻抗半径最大,PBCB/GCE 次之,AuNPs/PBCB/GCE 修饰电极的半径最小,这表明底液中溶解的氧化还原探针的电子转移电阻较低,加速了Fe(CN)63-/4-与AuNPs/PBCB/GCE修饰电极之间的电子转移.
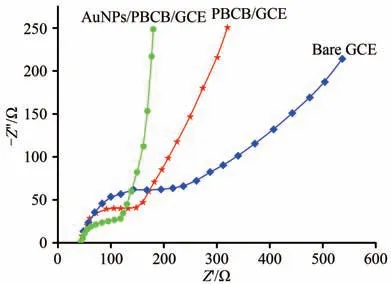
图9 不同电极的交流阻抗谱图Fig.9 Electrochemical impedance spectroscopy of different electrodes
3 结语
采用二步电聚合法及电化学沉积法制备了AuNPs-PBCB 纳米复合膜,对PBCB 的电聚合方法进行了优选,对纳米复合膜的制备条件及使用条件进行了优化,借助于X 射线光电子能谱(XPS)技术对纳米复合膜进行了成分分析,利用扫描电子显微镜技术对纳米复合膜的表面形貌进行了表征;使用电化学交流阻抗技术,对纳米复合膜的导电能力进行了评价;电化学技术表征表明AuNPs-PBCB 纳米复合膜对NO 的电化学氧化具有明显的电催化作用.以AuNPs-PBCB 纳米复合膜为敏感功能材料所制备的NO 生物医学传感器,其传感性能包括传感器的线性范围、灵敏度、检出限、响应时间、稳定性、重现性和特异性,以及传感器是否可用于实际生物医学样品中NO含量的监测,尚有待进一步研究.
