吲哚菁绿荧光技术在肝胆外科应用中的几个关键问题再认识
2022-08-22张中林刘符生袁玉峰
张中林,刘符生,袁玉峰
武汉大学中南医院肝胆胰外科 湖北省肝胆胰疾病微创诊治临床医学研究中心,湖北 武汉 430071
吲哚菁绿(indocyanine green,ICG)被发现并应用于临床已有近60年[1-2]。2008年Aoki等[3]首次应用荧光成像设备将ICG应用于肝胆外科手术的术中导航,开启了ICG荧光导航在肝胆外科应用的新时代。近年来,得益于新型荧光成像系统和荧光导航设备在临床中的广泛开发与应用,ICG荧光成像技术发展迅速,并在国内逐步普及。国内肝胆外科领域专家结合国内应用实践并结合国外数据,适时推出了多个ICG荧光技术应用的指南或专家共识[4-7],用以规范并指导临床ICG应用,笔者团队参加了这些“共识”的编写并提供了重要的参考数据[8-13]。然而,随着本中心临床应用经验的进一步积累,我们注意到,指南中所涉及的有关ICG临床应用的关键意见及建议在技术推广中面临一定的困难,相应的临床推荐方案在具体实践中亦存在少许问题,有必要对ICG荧光技术在肝胆外科应用中的若干关键问题进行重新认识。
一、ICG荧光技术在肝胆外科中的应用现状与面临的问题
近年来,ICG荧光技术在肝胆外科领域得到了前所未有的重视和推广,ICG在肝胆外科中的重要价值,如肿瘤荧光定位与导航、微小肿瘤病灶的识别与发现、精准断肝平面的引导以及肝外胆道识别等,已被充分肯定。然而,笔者所在团队在具体临床实践中也发现ICG荧光技术在应用推广中面临一些主要问题:一方面,国内外学者对于该技术的研究方兴未艾。国内肝胆外科领域近年来不断推出多个ICG荧光技术应用指南和专家共识,以促使其在临床应用中趋于标准化和规范化。国际学者对于该技术的专家共识及研究报道在很大程度为技术完善和更新提供了参考[14-18]。另一方面,由于荧光腹腔镜设备仍未充分普及、医疗资源分布差异等原因,不同级别医疗机构对该技术的认知存在一定偏差。常见认知有两种:其一,认为“ICG荧光技术形式大于实用”;其二,认为“该技术过于复杂,难以在基层医疗机构推广”。这两种认识在一定程度上反映了ICG荧光技术的应用现状,繁复的技术程序和较高的操作门槛阻碍了该技术进一步推广。因此,在准确适应证范围内探索更为直接普适的ICG应用方法成为必要。
本中心既往对ICG在肝胆外科的应用进行了深入的探索和研究。随着时间的推移和应用经验的积累,我们发现现有的文献中部分数据及推荐方法在具体操作实践中仍存在一定局限性,关于ICG荧光技术在肝胆外科应用中的若干关键问题,包括与手术方式相关的技术拓展、用药时机、剂量、浓度等要素,有必要进行深入探讨和再认识。通过对该技术在具体应用中的分析与归纳,结合笔者所在中心经验及数据,总结了本中心在针对不同染色方式时所使用的ICG剂量调整方法和技术验证。
二、ICG荧光使用中几个关键问题的再认识
1.肿瘤荧光定位术前注射ICG时机与剂量的再认识 用于术中肿瘤荧光定位的ICG注射常用方法是以足量(0.5 mg/kg)剂量、术前1~3 d经外周静脉注射,明显肝硬化病人需将时间延长至2~7 d。在临床中,用于肝储备功能评估的ICG 15 min滞留率(ICG R15)检测,在数天的等待期之后,通常能够刚好满足术中肿瘤荧光定位需求。然而,对于一部分仅用于术中肿瘤定位而不涉及ICG排泄试验的病人,为减少术前等待时间,减少ICG的给药量成为潜在可行的一个替代方案,以满足新时期医疗绩效考核需求。笔者观察到,对于轻、中度肝硬化病人,将ICG量减少至常用剂量的一半(12.5 mg),大概率可以取得成功(图1)。值得注意的是,对于严重肝硬化病人,即使按照标准流程注射ICG后经过长时间的术前等待,也常常由于广泛而严重的肝硬化结节而致ICG廓清困难,或者廓清几乎与肝肿瘤同步,从而导致失败,这些减低剂量、缩短时间的方法更难成功,因此对于该类病人需谨慎使用。
2.肝分段染色术中ICG使用剂量的再认识 通过ICG荧光正染或反染标记肝段或肝叶,引导断肝平面,配合其他技术手段实施精准肝切除手术,是近年来肝脏外科的重大进步之一。早期国内多数中心的经验以及相关“专家共识”或“指南”的推荐通常为:肝段正染约1.25 mg经目标肝段Glisson蒂门静脉注射的方法[5-6]。笔者早期就发现并指出,远低于该推荐剂量的ICG也能较好地达到染色效果并引导断肝,并能规避大剂量ICG所致的断肝平面浸染[9](图2)。随着使用经验的积累,这一观点被越来越多中心证实并接受。我们现在的做法是,无论是肝段正染或反染,均采取“1/1 000原药”(即0.025 mg/mL)的统一方案,根据目标肝段体积酌量取用。一般肝段正染取1~5 mL经目标肝蒂门静脉注射,肝叶反染先取10 mL经外周静脉注射,根据术中染色效果决定是否追加剂量,遵循“宁少勿多”的给药原则,达到手术平面的最佳荧光成像效果。
3.肝外胆管成像术中ICG使用时间、浓度和剂量的再认识 以肝外胆管显影成像为目的的ICG荧光应用分为两种情况,一种是经外周静脉注射、胆汁分泌的排泄性胆道显影,另一种是经肝胆管或胆囊管直接注射的胆道显影。前者易于操作,不易发生沾染、胆漏等问题,但偶尔受胆汁引流通畅度的影响;后者也是实现胆道快速显影的可靠方法,特别是在某些特殊情况下,如同时涉及胆管识别及胆漏检测等,尤为适用。我们观察了胆囊切除术中经外周静脉注射不同剂量(0.5~10 mg)ICG的肝外胆管显影时间和效果,发现手术开始前30 min以内0.5~1 mg剂量的ICG使用,均能达到较好的荧光成效,对手术的引导作用与大剂量(ICG>5 mg)使用无明显差异[9](图3)。近年来,国内有关厂商4K高清荧光腹腔镜系统能在0.025 mg(ICG)低剂量下呈现清晰胆管荧光(图4),满足手术需要。在某些急性胆囊炎或高体质量指数病例中,胆囊三角局部炎症水肿或脂肪堆积可能会导致肝外胆管不显影或显影效果不佳,但是通过分离、刮吸等操作打薄组织,并适度增大ICG剂量后,多数病例仍然能够呈现胆管荧光,对引导手术操作、避免胆管损伤很有帮助。胆管荧光成像,因为不存在肝分段染色中所顾忌的浸染问题,我们推荐适宜偏高的ICG剂量也许更有利于该技术推广和应用。经胆囊管或肝胆管直接注射ICG的胆管造影,推荐使用相同的浓度(1/1 000原药,即0.025 mg/mL),根据胆道扩张程度酌情确定ICG使用量,通常5~20 mL不等。事实上,胆管注射ICG并非浓度越高显影效果越好,过高浓度下ICG对近红外光的吸收能力会降低,适宜的低浓度ICG和血液中的白蛋白、脂蛋白等成分结合后,能够实现发光效率的显著提升[19]。因此,为获得胆管内注射ICG后胆管的清晰荧光图像,我们通常将ICG溶解并稀释到1/1 000原药,即0.025 mg/mL用于造影。
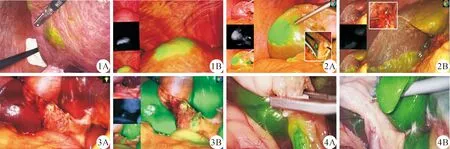
图1 吲哚菁绿(ICG)注射用于肿瘤显影:2例中等程度肝硬化病人,术前24 h经外周静脉注射半量(12.5 mg)ICG,术中显影效果 A.右后叶肝肿瘤;B.右前叶肝肿瘤 图2 低剂量ICG注射用于肝段显影 A.ICG荧光引导腹腔镜下肝右前叶切除术(正显影法);B.ICG荧光引导腹腔镜下肝右前叶切除术(负显影法) 图3 胆囊萎缩合并胆囊管结石病人,术前评估预测可能为复杂腹腔镜胆囊手术,术中证实胆囊颈管胆总管识别、分离困难,术中经外周静脉注射1 mg ICG后30 min显影效果 A.白光视野;B.荧光视野(荧光设备:加拿大Pinpoint Novadaq腹腔镜荧光成像系统) 图4 腹腔镜胆囊切除术病人,术中经外周静脉注射0.025 mg ICG后20 min显影效果 A.肝外胆道显影状态;B.肝脏显影状态(荧光设备:欧普曼迪4K荧光成像系统)
4.针对不同染色方式的ICG剂量调整方法 通过对ICG荧光技术在以上不同术式应用中的重新认识,我们总结了本中心在针对不同染色方式时所使用的ICG剂量调整方法。该方法基于1/10的标准浓度和1/1 000的工作浓度,简化了配药操作。简言之,取注射用ICG(25 mg/安瓿,卫材制药有限公司)1支以其自带10 mL灭菌注射用水溶解配制2.5 mg/mL的1/10标准浓度;再取1 mL(2.5 mg)上述1/10标准浓度的ICG溶液以生理盐水稀释至100 mL(或取2.5 mL标准浓度溶液稀释至250 mL),配制1/1 000的工作浓度溶液。根据不同术式取用相应的剂量,然后根据显影效果酌情加量调整(图5)。
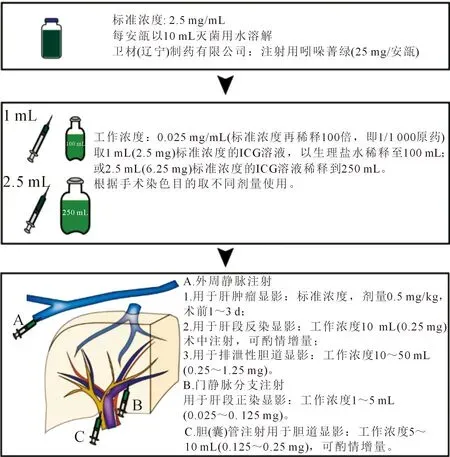
图5 湖北省肝胆胰疾病微创诊治临床医学研究中心在针对不同染色方式时所使用的吲哚菁绿(ICG)剂量调整方法
三、ICG荧光应用前景展望
1.ICG荧光技术的快速推广和下沉 目前国内外相关专家共识及指南对于ICG在肝胆外科中的推荐应用方式及操作细节已较为全面,在不同术式下的注射方式、时间及剂量均做出了较为明确的说明,有助于各级医疗机构在较为规范的情况下参考使用。随着技术扁平化和成本降低,ICG荧光将作为适宜技术在肝胆外科领域快速推广和下沉,带来更广泛的医疗机构应用和病人获益。
2.二区荧光的应用 当ICG特异性地分布于肝区域之后,向肝脏表面照射波长750~810 nm的外源激发光,即可激发肝脏内部分布的ICG探针产生780~900 nm波长的一区荧光和1 000~1 700 nm的二区荧光信号[20-21]。ICG在第二个红外窗口即荧光二区具有更好的成像质量,将有助于帮助发现深部肿瘤,利用荧光二区成像技术可以提高肝脏肿瘤监测的敏感度和肿瘤检出率[21]。因此,二区荧光在微小肿瘤发现、肝切缘肿瘤残留探查等方面,可能更具优势,二区荧光的应用或许是未来研究与实践的方向。
3.基于成纤维细胞激活蛋白抑制剂(FAPI)的术中ICG功能成像用于肝外肿瘤病变 ICG具有极强的亲肝特性——快速且特异地被成熟肝脏细胞摄取并经胆汁排泄。这一特性决定了其在原发性肝脏病变诊疗中的价值,同时也限制了其在肝外肿瘤病变中的应用,例如腹腔内肝外原发肿瘤或转移性肿瘤(包括腹腔淋巴结转移)无法利用ICG实现术中功能性成像。实体肿瘤微环境(TME)中FAPI被发现具有肿瘤特异性,其与放射性元素68Ga结合(68Ga-FAPI),被成功地应用于多种实体的肿瘤特异性核素扫描[22-23]。基于FAPI的ICG-FAPI偶联有可能应用肝外实体瘤术中功能成像,或许有助于扩大ICG荧光技术在腹腔内手术的应用范围。
四、小结
如前所述,笔者推荐的针对不同使用目的ICG 1/1 000普适性浓度和简单剂量微调方案,简化了目的相关的配药操作,消除了不同中心——特别是基层医疗机构,在使用ICG过程中最大的疑惑点,并用我们的数据验证了优化模式下的ICG荧光成像效果,这将非常有利于进一步技术推广和应用。目前,ICG荧光显影相关设备的国产化及更新迭代正在迅速降低应用成本,相关学术推广的深入正在加速技术扁平化,在可以预见的未来,使用成本的降低和技术的普及将使得ICG荧光作为适宜技术在肝胆外科领域快速推广、下沉,带来更广泛的医疗机构及病人获益。相关技术如二区荧光的应用,基于FAPI的ICG-FAPI偶联应用于肝外实体瘤的术中功能成像,以及荧光成像技术带来的肿瘤学获益等方面,有待进一步研究,以取得新的进展。
利益冲突所有作者均声明不存在利益冲突
