SpyGlass DS胆道镜系统在肝外胆管恶性肿瘤术前评估中的作用
2022-08-22黄泽坚吴祥陈亚进
黄泽坚,吴祥,陈亚进
1.中山大学孙逸仙纪念医院肝胆外科,广东 广州 510120;2.广州中医药大学第二附属医院胰胆外科,广东 广州 510120
肝门部胆管癌、胆总管癌是肝外胆管最常见的恶性肿瘤,疾病进展时常出现肝功能损害、胆道狭窄梗阻等相关症状,总体预后不佳,总体5年生存率不足5%[1-2]。提高肝外胆管恶性肿瘤预后的重要途径在于疾病的早期诊断和精准的定位、定性评估。常用的诊断肝外胆道恶性肿瘤的主要途径包括磁共振胰胆管造影(magnetic resonance cholangiopancreatography, MRCP),经内镜逆行胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP),超声内镜(endoscopic ultrasonography, EUS)等方式。
近年兴起的SpyGlass DS系统是一项操作相对简便且精准的内镜直视技术,为肝外胆管疾病的诊断治疗提供了新的途径。其是间接经口胆道镜的代表,可以通过普通十二指肠镜钳道内直接插入胆管或胰管,通过直视观察胰胆管内的病变,并且可以通过独立的活检通道进行活检、碎石、取异物等治疗操作,目前已在多种胆道、胰腺疾病的诊断治疗中取得良好效果[3-5]。然而,将SpyGlass DS系统应用于肝外胆管恶性肿瘤术前评估的研究较少,其有效性及安全性仍不明确。本研究旨在总结我中心采用第二代SpyGlass DS系统对于肝外胆管恶性肿瘤进行术前评估的经验,探讨其在肝外胆道恶性肿瘤术前诊断、肿瘤定位中的价值。
资料与方法
一、一般资料
选取中山大学孙逸仙纪念医院肝胆外科2021年6月至2022年5月期间经过CT或MRCP疑诊胆管恶性肿瘤,并且最终行SpyGlass DS完成直视下活检病理确诊胆管癌的病人。本研究最终入选9例病人,其中男性5例,女性4例,中位年龄65岁(54~73岁),术前中位黄疸指数191 μmol/L(15~512 μmol/L)。本研究已获得我院伦理委员会批准(批件号:SYSKY-2022-116-01),术前均获得病人的知情同意并签署相关知情同意书。
二、器械设备
FUJI ED-530XT4.2电子十二指肠镜,ERCP操作附件(包括十二指肠乳头括约肌切开刀,导丝,扩张球囊、胆道塑料支架、鼻胆引流管等),BostonScientific SpyGlass DS胆道镜及附件(SpyGlass DS成像导管和Spybite活检钳等),ERBE高频电外科系统VIO200D。
三、术前准备
操作前对病人情况进行详细评估,包括病史及体格检查、实验室检查、复习影像学资料等。术前应至少禁食禁饮6 h。术前签署知情同意书;围术期预防性使用抗生素。
操作前镇静方法:根据病人选择适当的镇静方式,例如中度镇静(咪达唑仑,哌替啶),深度镇静(丙泊酚)或全身麻醉。
四、手术方法
病人取左侧卧位,口腔、咽喉行利多卡因胶浆局部麻醉,戴好口圈后,给予静脉麻醉,麻醉成功后循口腔进镜,进镜顺利过贲门,到达胃腔后,找到幽门口后顺利过十二指肠球部并进入十二指肠降部,找到十二指肠主乳头后缩短镜身,寻找十二指肠乳头并进行插管,导丝置入胆总管后,造影显示肝内外胆道形态。随后将十二指肠乳头行小切开,并用扩张球囊扩张壶腹部括约肌(小扩张,扩张直径约6 mm),将 SpyGlass DS成像导管从十二指肠镜工作孔道插入胆管,进行直视下探查,获得清晰视野后,详细观察胆管病变位置、形态、大小、胆管肿瘤长度、表面血管情况等(图1),并且直视下探查肿瘤侵犯的上界(是否侵犯汇合部、左肝管和/或右肝管等,图2),接着用Spybite活检钳行直视下病变活检(图3)。观察活检部位无明显出血后,退出成像导管时,联合X线测量胆管肿瘤下端与壶腹部之间的距离(图4),以此来判断肿瘤下界的长度,并放置胆道支架或鼻胆引流管于肝总管,最后安全退镜,鼻胆引流管由鼻腔引出,标本送病理活检,病人清醒后返回病房。
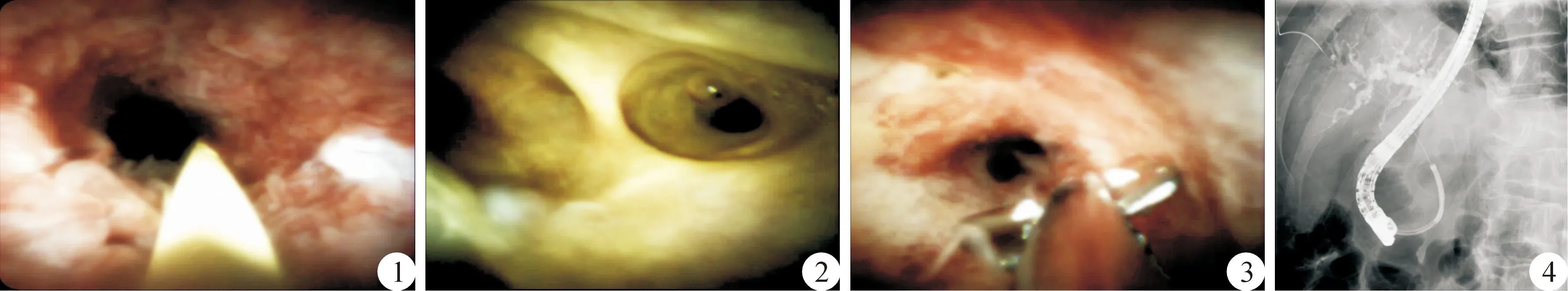
图1 肝总管肿瘤内镜下表现 图2 汇合部及左右肝管的内镜下表现 图3 Spybite活检钳行直视下肝总管肿瘤活检 图4 SpyGlass DS直视下联合X线定位测量胆管肿瘤下缘位置
结 果
一、病理结果
胆管恶性肿瘤内镜下表现为突入管腔内的结节或肿块,表面呈浸润性或溃疡性生长。最终9例病人均通过SpyGlass DS活检组织病理诊断为胆管细胞癌,其中中分化腺癌2例,低分化腺癌2例,另5例活检组织肿瘤细胞分化程度无法判断。
二、肿瘤位置及分型
根据SpyGalss DS探查结果,最终9例病人肿瘤分型为:胆总管中段癌1例;肝门部胆管癌8例,其中Bismuth Ⅰ型肝门部胆管癌2例,Bismuth Ⅱ型肝门部胆管癌1例,Bismuth Ⅲ型肝门部胆管癌4例(Ⅲa 2例,Ⅲb 2例),Bismuth Ⅳ型肝门部胆管癌1例。SpyGlass DS探查肿瘤的定性结论与术前CT及MRCP评估一致者共7例,另2例术前影像学考虑为胆管癌和胆管炎鉴别,炎性病变可能性大。SpyGlass DS探查肿瘤的定位分型结论与术前CT及MRCP评估一致者仅有1例(Ⅲa型肝门部胆管癌1例);另8例术前影像学分别在评估肿瘤侵犯左右肝管具体侵犯情况方面(6例)、肿瘤距离壶腹部的长度方面(2例)均不够准确。
三、并发症
8例病人术后经抗感染、补液及对症支持治疗后病情稳定,未发生术后并发症。
1例病人在术后第1天开始反复出现上腹部疼痛伴寒战高热,随后经CT检查见胆囊明显肿胀、大量造影剂蓄积,考虑胆道支架堵塞胆囊管引起急性胆囊出口梗阻、胆囊炎。遂立即予超声引导下胆囊穿刺引流,引流后病情逐渐稳定好转。
四、后续治疗
胆总管中段癌1例及Bismuth Ⅰ和Ⅱ型肝门部胆管癌3例病人最终行全肝外胆管根治性切除、局部淋巴结清扫、肝门区胆管整形、肝管空肠Roux-en-Y吻合术(其中腹腔镜2例,开腹2例)。Bismuth Ⅲa型肝门部胆管癌2例行开腹右肝(分别为右三肝及右半肝)切除联合左肝管空肠Roux-en-Y吻合术。Bismuth Ⅲb型肝门部胆管癌2例分别行左半肝加尾状叶切除联合肝管空肠Roux-en-Y吻合术、中肝叶切除联合肝管空肠Roux-en-Y吻合术。Bismuth Ⅳ型肝门部胆管癌1例最终因评估发现全身多发转移而未行手术治疗。
8例接受手术治疗的病人,术中探查胆道肿瘤浸润情况与SpyGlass DS探查情况一致,遂均按照术前规划手术方式行手术切除,并且术中均获取胆道切缘送冷冻病理,证实切缘阴性。最终术后病理结果回报均与术前SpyGlass DS探查活检结果一致。
讨 论
肝外胆管恶性肿瘤以胆囊管与肝总管汇合点为界,分为肝门部胆管癌和远端胆管癌,总体预后情况不佳,手术切除仍然是目前唯一可治愈该疾病的方法[6]。根据肿瘤病变位置的不同,肝外胆管癌的手术方式也多样,包括肝外胆管切除、联合肝脏切除、胰十二指肠切除等,术前准确的定位、定性是选择正确治疗方式最重要的因素。
相比于MRCP、ERCP、EUS等评估手段间接观察病变的情况,SpyGlass DS系统可以在直视下直接观察胆道内部形态,在进行常规刷检细胞学检查的同时,根据胆管形态决定是否直接活检,并且已有研究表明SpyGlass DS直视下活检提供的组织足以行病理诊断[7]。胆道内恶性肿瘤的内镜下表现通常为突入管腔内的结节或肿块,表面呈浸润性或溃疡性生长,并且肿瘤表面往往可以观察到不规则迂曲和扩张的肿瘤血管。Navaneethan等[8]的一项纳入了457例病人的系统回顾研究表明,SpyGlass DS联合Spybite活检对于诊断胆管恶性肿瘤具有良好的效果,其敏感性和特异性分别达到了66.2%和97.0%。本研究对影像学疑诊胆管癌的9例病人行SpyGlass DS胆道镜检查和直视下活检,最终活检标本均足够行病理学诊断,明确诊断为胆管细胞癌,检查的敏感度和特异度均达到100%。
肝外胆管癌手术方式的选择在于术前精准的手术定位与分型。对于肝门部胆管癌,肿瘤是否侵犯左右肝管出口对于是否需要进行大范围肝切除具有决定性意义;而肝外胆管癌向下侵犯的程度、肿瘤距离胰腺段胆管和壶腹部的长度则关系到是否需要行胰十二指肠切除术。精准的手术定位可以在达到根治性切除的同时,有效避免不必要的扩大切除手术。本研究中的9例病人,术前影像学对肿瘤的定位分型主要依赖于CT和MRCP的检查,然而影像学诊断的准确率尚无法令人满意,间接观察对于肿瘤实际的侵犯范围评估仍有一定偏差,最终影像学分型与SpyGlass DS检查评估一致者仅有1例。影像学检查的主要偏差在于肿瘤是否侵犯左右肝管及侵犯的深度、肿瘤远端距离壶腹部的长度的判断,这些对于手术策略制定均具有重大意义,直接关系到手术的可行性及具体的切除范围。
综上所述,SpyGlass DS系统一方面可以通过直视下活检,直接对病变行病理学确诊,敏感性和特异性均较高;另一方面可以精准评估肿瘤与左右肝管、十二指肠乳头的关系和距离,准确制定规划手术方案,其在肝外胆管癌的诊断和精准定位中均具有良好的运用价值。但是,本研究总体样本量较小,SpyGlass DS系统在胆管恶性肿瘤诊治中的安全性、有效性和在临床上的进一步推广应用仍需要更大样本临床研究进一步证实。
利益冲突所有作者均声明不存在利益冲突
