基于聚鸟氨酸修饰的玻碳电极用循环伏安法测定盐酸肾上腺素注射液中肾上腺素的含量
2022-06-23吕惠萍马心英陈美凤曾会青
吕惠萍,马心英,陈美凤,朱 琪,曾会青
(菏泽学院 化学化工学院,菏泽 274015)
肾上腺素(EP)是由肾上腺髓质分泌的一种激素[1-2],在医学上可作为拟肾上腺素药,用来缓解心跳微弱、血压下降、呼吸困难等症状,还可用于增加肾血流量、改善休克时重要器官的血液供应[3],是拯救濒死状态下人和动物的必备药品[4-5]。过量或过少使用EP 均会影响机体的多项生理功能,导致人或动物代谢紊乱,产生疾病,甚至危及生命[6]。因此,EP含量的测定在发展神经生理学、诊断和控制医学中具有重要作用[7]。
目前,常用的EP 测定方法有高效液相色谱法(HPLC)[8-11]、光化学法[12-13]、荧光法[14]等,但是这些方法需要昂贵的分析仪器、较长的检测时间和较多的样品。电化学法[15-16]具有检测成本低、灵敏度高、检出限低、方法稳定快速等特点,在药物分析中应用广泛[17-21]。EP 化学结构中含有酚羟基,具有一定的电化学活性。聚鸟氨酸(POrn)具有稳定性好和环境污染小的特点,以POrn修饰的电极具有较好的选择性、稳定性和灵敏度,但目前还未见该修饰电极在EP检测中的报道。
鉴于此,本工作制备了具有电催化活性的聚鸟氨酸修饰的玻碳电极(POrn/GCE),并用于盐酸肾上腺素注射液中EP 含量的测定,方法具有较高的灵敏度、选择性和重现性,可用于实际样品中EP含量的测定。
1 试验部分
1.1 仪器与试剂
CHI-660D 型电化学工作站;KQ-100型超声波清洗器;MT 型红外灯;78 HW-1型数显恒温磁力搅拌器;SYZ-550型石英亚沸高纯水蒸馏器。
磷酸盐缓冲溶液(PBS):pH 8.0,由适量0.1 mol·L-1磷酸氢二钠溶液和0.1 mol·L-1柠檬酸溶液混合配制而成。
EP标准储备溶液:取0.045 5 g EP标准品,用PBS稀释至50 mL,配置成5.0×10-3mol·L-1的标准储备溶液。
EP标准溶液系列:取一定量EP 标准储备溶液,用PBS逐级稀释,配制成2.0,3.0,4.0,5.0,10,20,30,40,50,100μmol·L-1的标准溶液系列。
鸟氨酸(Orn)纯度为98%;EP 标准品纯度为98%;盐酸肾上腺素注射液(1 mL∶1 mg)。
所用试剂均为分析纯;试验用水为二次蒸馏水。
1.2 仪器工作条件
以GCE 或POrn/GCE 为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极;电解液为PBS(pH 8.0);电化学方法为循环伏安法(CV);扫描电位为-0.4~1.0 V;扫描速率为0.08 V·s-1。
1.3 试验方法
1.3.1 POrn/GCE的制备
GCE经滴在麂皮上的三氧化二铝(粒径为35~45μm)悬浮液抛光后,依次用50%(体积分数)硝酸溶液、无水乙醇、水各超声清洗30 s,每次清洗后均用水冲洗干净,红外灯下干燥5 s。放入含1.0×10-4mol·L-1Orn的PBS(pH 8.0)中,用1.2节所述的三电极体系(工作电极为GCE),以10 m V·s-1扫描速率在-1.8~2.3 V 内循环扫描12段,取出电极,用水清洗,红外灯下干燥,即得POrn/GCE。
1.3.2 样品的测定
取盐酸肾上腺素注射液0.72 mL,用pH 8.0的PBS定容至50 mL 容量瓶中,分取10 mL 置于25 mL的小烧杯中,搅拌130 s,按照仪器工作条件测定。
2 结果与讨论
2.1 EP的电化学行为
按照仪器工作条件测定空白溶液(PBS)和5.0μmol·L-1EP标准溶液,其中曲线1和曲线3分别为空白溶液和EP 标准溶液在POrn/GCE 上的CV曲线,曲线2为EP标准溶液在GCE 上 的CV 曲线。
由图1可知:EP在GCE上氧化峰电流(以绝对值计,记为|ipa|)和还原峰电流(ipc)分别为15.3,1.66μA,氧化峰电位(Epa)和还原峰电位(Epc)分别为0.35,-0.07 V;EP 在POrn/GCE 上 的Epa、Epc和在GCE 上的基本一致,|ipa|、ipc分别为39.9,15.6μA,比在GCE上的均相对增大,说明修饰电极对EP 的测定具有一定的催化作用,而空白溶液在POrn/GCE上几乎无响应,说明空白溶液对EP 测定无干扰。
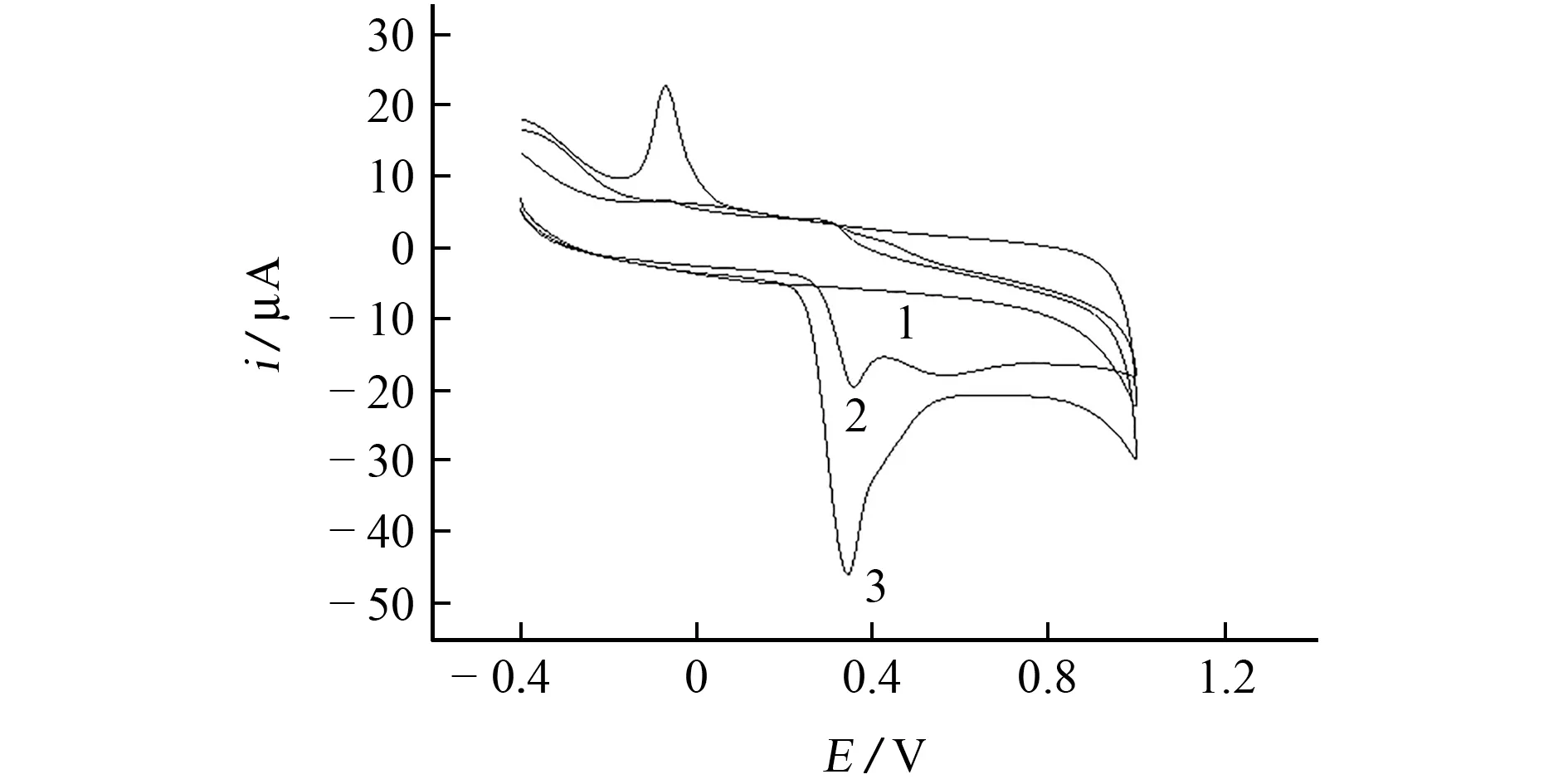
图1 空白溶液和EP标准溶液的CV 曲线Fig.1 CV curves of blank solution and EP standard solution
2.2 POrn/GCE制备条件的选择
电解液的酸度、扫描段数、扫描速率和扫描范围(低、高扫描电位)对电极性能均有影响。采用单一变量法,按照1.3.1节试验方法测定,分别考察了电解液酸度分别为pH 2.0,3.0,4.0,5.0,6.0,7.0,8.0,扫描段数分别为2,4,6,8,10,12,14,扫描速率分别为10,20,40,60,80,100,120 m V·s-1,低扫描电位分别为-2.0,-1.9,-1.8,-1.7,-1.6 V(固定高扫描电位为2.3 V),高扫描电位分别为1.9,2.1,2.3,2.4 V(固定低扫描电位为-1.8 V)时对EP 在POrn/GCE上|ipa|的影响,所得结果见图2。
由图2可知,在电解液的酸度不小于pH 8.0,扫描段数为10~12,扫描速率为10 m V·s-1,高、低扫描电位分别为2.3,-1.8 V 时,EP 在POrn/GCE上的|ipa|较大。为了使Orn尽可能地聚合在GCE上,试验选择的电解液酸度为pH 8.0,扫描段数为12,扫描速率为10 m V·s-1,扫描范围为-1.8~2.3 V。
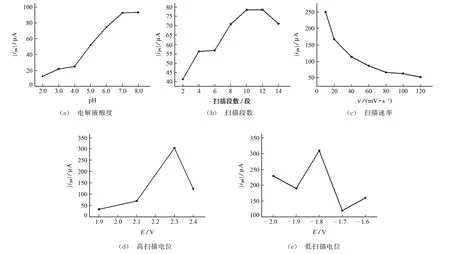
图2 电解液酸度、扫描段数、扫描速率、高扫描电位和低扫描电位对EP在POrn/GCE上的|ipa|的影响Fig.2 Effect of eletrolyte acidity,electropolymerization cycle,scanning rate,high scanning potential and low scanning potential on|ipa|of EP on POrn/GCE
在最优制备条件下,所得聚合CV 曲线见图3。
由图3 可知,在0.4 V 处出现氧化峰,-0.5,-0.7 V 处出现还原峰,说明电极表面发生了氧化还原反应。扫描12段后,取出电极,观察到其表面形成了深蓝色的膜层。
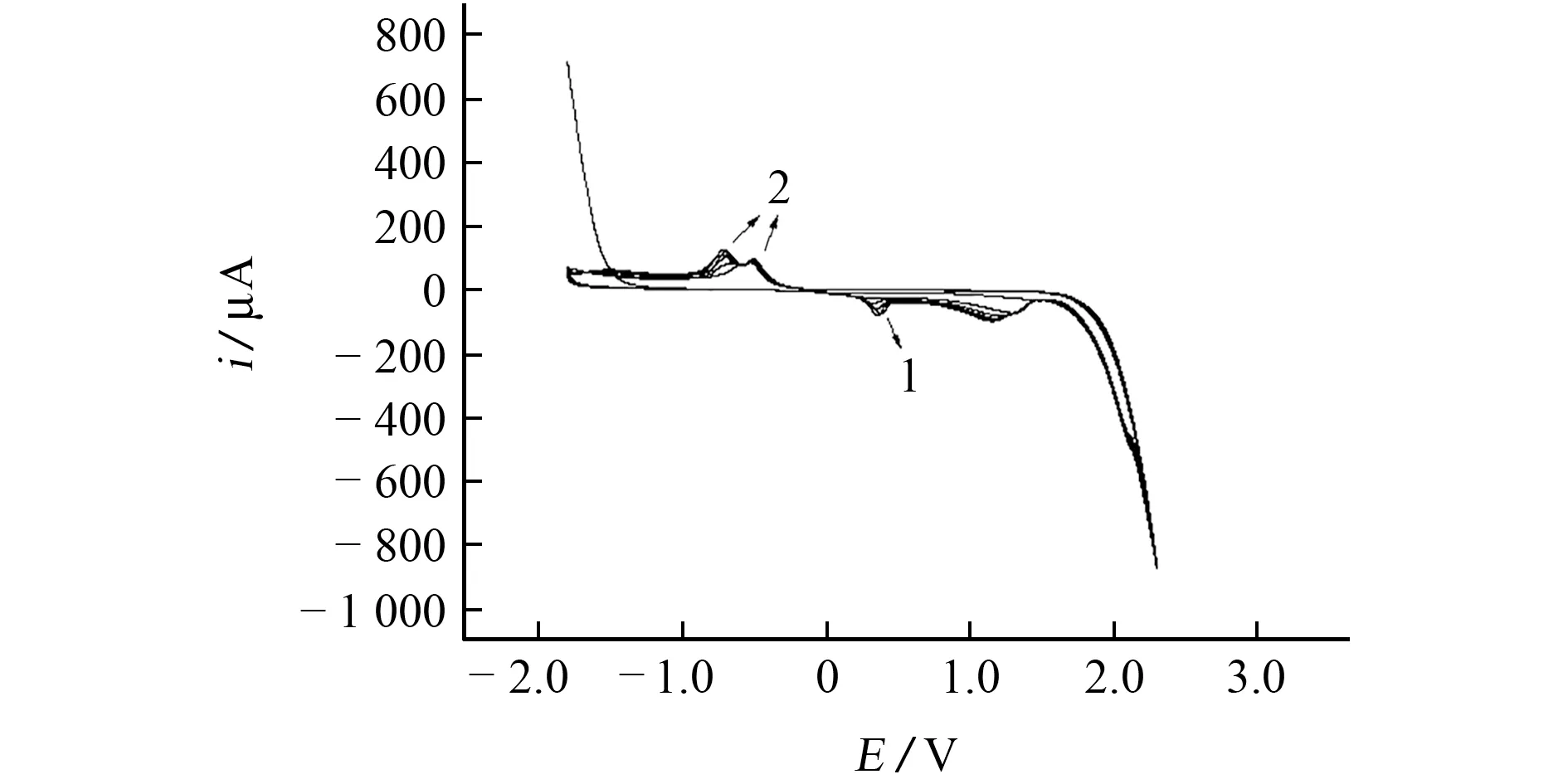
图3 聚合CV 曲线Fig.3 CV curves for polymerization
2.3 仪器工作条件的选择
2.3.1 酸 度
酸度对电极反应中EP峰电流及峰电位均有一定影响,因此试验考察了电解液酸度分别为pH 2.2,3.0,4.0,5.0,6.0,7.0,8.0 时 对EP 在POrn/GCE 上电化学响应的影响,所得CV 变化曲线见图4(a)(其中曲线1~7 对应酸度分别为pH 2.2,3.0,4.0,5.0,6.0,7.0,8.0)。以Epa为纵 坐标,酸度为横坐标进行线性拟合,所得结果见图4(b)。
由图4可知:在酸度为pH 8.0时,EP在POrn/GCE上的|ipa|较大,因此试验选择的酸度为p H8.0;Epa随着pH 的增加而降低,二者呈线性关系,线性回归方程为Epa=0.881 3-0.058 70 p H,相关系数为0.992 7,斜率的绝对值(0.058 7)接近0.059[22],表明EP氧化还原反应是一个有质子参与的过程,且参与反应的质子数和电子数相同。
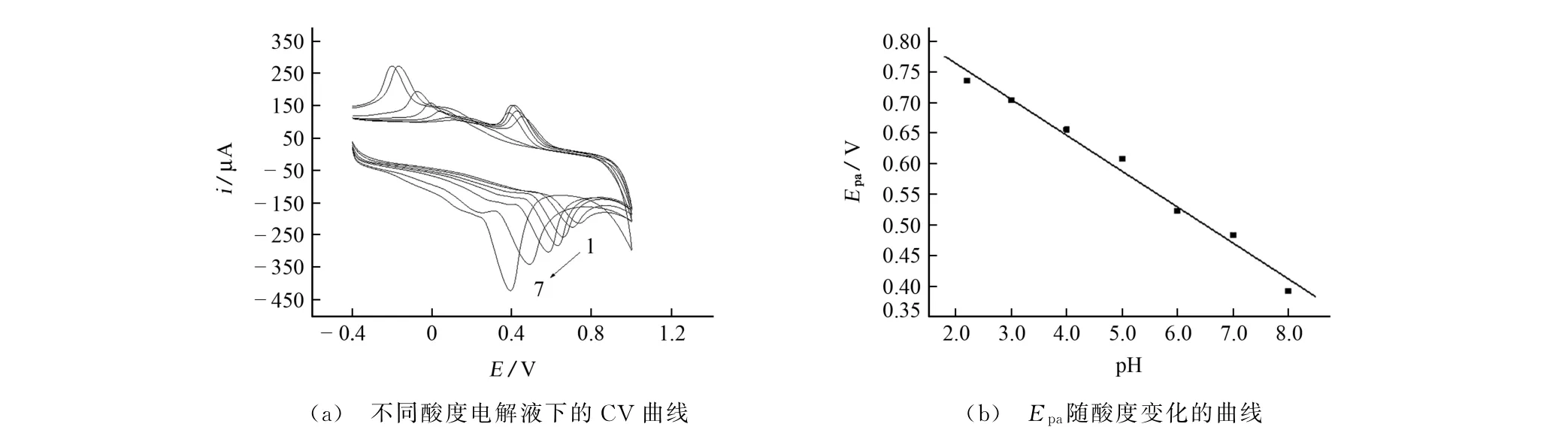
图4 不同酸度下CV 曲线和Epa随酸度变化的曲线Fig.4 CV curves with different acidities of eletrolyte and curve showing changes of Epa with acidity of eletrolyte
2.3.2 扫描速率
试验考察了扫描速率分别为0.02,0.04,0.06,0.08,0.10,0.12,0.14,0.16,0.18,0.20 V·s-1时 对EP在POrn/GCE 上电化学响应的影响,结果见图5(a)。以|ipa|为纵坐标,扫描速率为横坐标进行线性拟合,所得结果见图5(b)。
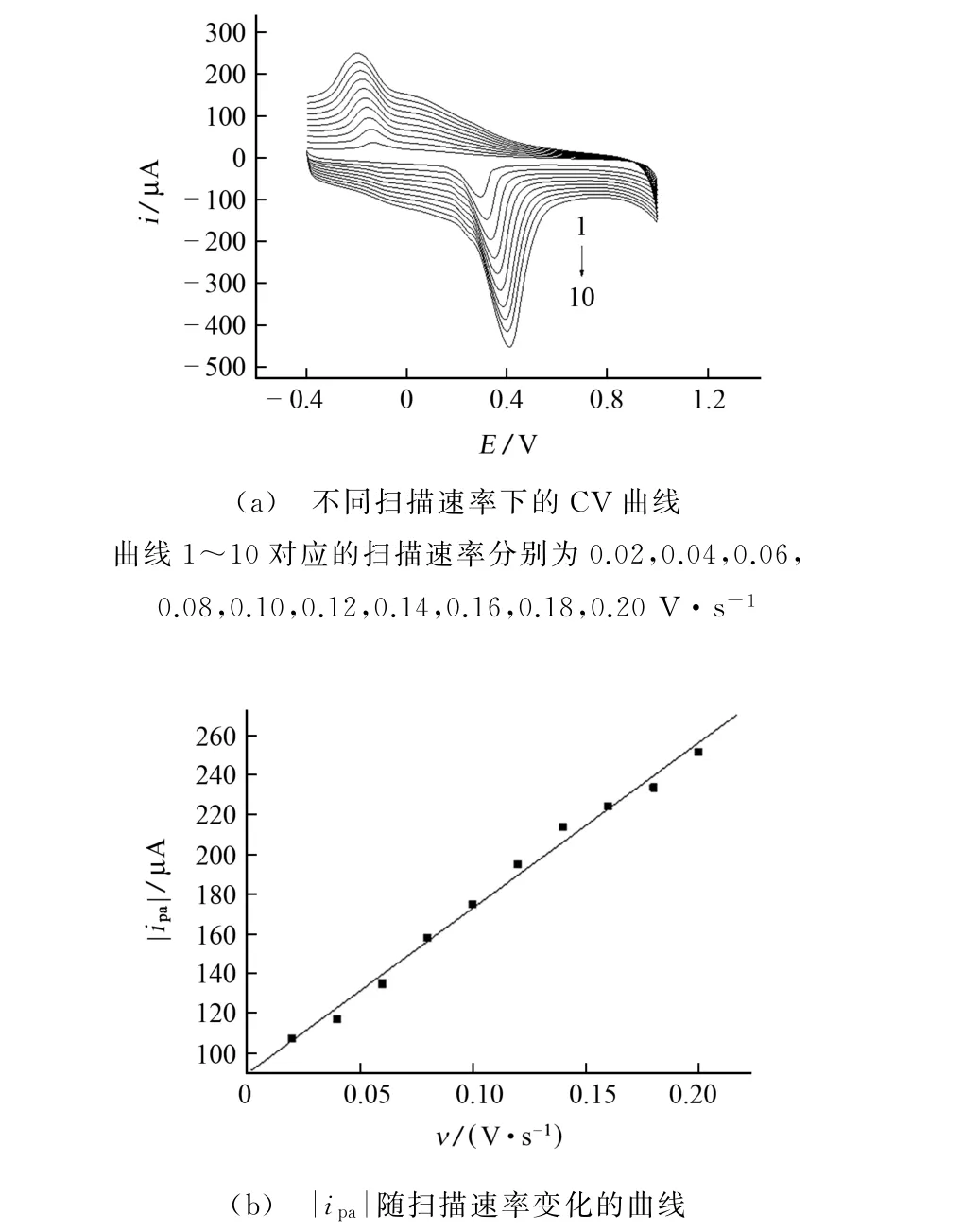
图5 不同扫描速率下的CV 曲线和|ipa|随扫描速率变化的曲线Fig.5 CV curves with different scanning rates and curve showing changes of|ipa|with scanning rate
由图5 可知:|ipa|随着扫描速率的增加而增加,考虑到电极灵敏度会随扫描速率的增加而下降,而扫描速率为0.08 V·s-1时的峰形较好,因此试验选择的扫描速率为0.08 V·s-1;|ipa|与扫描速率呈线性关系,线性回归方程为|ipa|=8.960×10-5+8.330×10-4v,相关系数为0.995 4,说明EP 在POrn/GCE上的反应为吸附控制过程。
2.3.3 高、低扫描电位和搅拌时间
高、低扫描电位以及搅拌时间对EP 在POrn/GCE上的|ipa|有一定影响。因此,试验考察了高扫描电位分别为0.6,0.8,1.0,1.2,1.4 V(固定低扫描电位为-0.4 V),低扫描电位分别为-0.8,-0.6,-0.4,-0.2,0 V(固定高扫描电位为1.0 V),搅拌时间分别为10,20,30,40,50,60,70,80,90,100,110,120,130,140,150 s时 对EP 在POrn/GCE 上|ipa|的影响。结果显示,当高、低扫描电位分别为1.0,-0.4 V,搅拌时间为130 s时,EP 在POrn/GCE上的|ipa|达到最大。因此,试验选择的电位扫描范围为-0.4~1.0 V,搅拌时间为130 s。
2.4 标准曲线和检出限
按照仪器工作条件分析EP 标准溶液系列,以EP的浓度为横坐标,其对应的|ipa|为纵坐标绘制标准曲线。结果显示,标准曲线的线性范围为2.0~100μmol·L-1,线性回归方程为y=2.190x+1.977×10-5,相关系数为0.991 5。
以出现可见|ipa|对应浓度作为检出限,结果为0.13μmol·L-1。
2.5 干扰试验
色氨酸、甘氨酸、赖氨酸、尿素以及Cd2+、Ca2+、Al3+、Fe3+可能共存于体液中,干扰测试结果。因此,试验在50μmol·L-1EP标准溶液中加入不同浓度的上述干扰物质,考察了这几种物质对EP 测定的干扰程度。结果显示,在相对误差的绝对值不大于5.0%时,100倍的尿素、色氨酸、甘氨酸和赖氨酸,50倍的Cd2+和Ca2+,10倍的Al3+和Fe3+都不干扰EP的测定。
2.6 重复性和稳定性试验
按照仪器工作条件重复测定5.0μmol·L-1EP标准溶液6 次,计算测定值的相对标准偏差(RSD),所得结果为3.9%,说明POrn/GCE 有良好的重复性。
将POrn/GCE 避光恒温保存7 d 后,再测量|ipa|,其较初始值减少了不到3.0%,说明修饰电极有较好的稳定性。
2.7 回收试验
按照1.3.2节试验方法对实际样品进行3个浓度水平的加标回收试验,计算回收率,所得结果见表1。
由表1可知:测定值与标签值基本相近,回收率为97.6%~102%,说明方法的准确度较好。

表1 回收试验结果Tab.1 Results of test for recovery
本工作制备了POrn/GCE,研究了EP 在该修饰电极上的电化学行为,电极的重复性和准确度均较好,可用于EP实际样品的测定,具有一定的应用前景。
