超声引导下单腔中心静脉导管置入术式在肾囊肿硬化治疗中的临床应用价值
2022-06-13伏钢冯军高远王新润
伏钢,冯军,高远,王新润
南京医科大学附属无锡市第二人民医院超声科,江苏无锡 214000
肾囊肿是一种良性病变, 也是肾脏疾病中最常见的一种疾病,多源于肾细胞的退行性改变[1-2]。肾囊肿一般生长缓慢,当其直径<4 cm 时,患者往往无任何临床症状,此时一般无需特殊处理,临床多建议定期复查即可。 但对于直径>5 cm 的肾囊肿,则容易出现腰痛症状,活动或劳累时症状加重,并且患者腰痛症状的严重程度随着肾囊肿大小的增加而变化。 当受到意外的外力挤压或继发感染后, 还可出现囊肿破裂出血, 进而引起高血压和肾功能损害等严重并发症。 传统的治疗方法不但创伤大、操作复杂,而且术中出血多、术后恢复也较慢,不易为患者接受,所以在临床应用中受到一定的限制[3]。 近年来,由于超声引导下的经皮穿刺肾囊肿硬化治疗具有安全、操作简便、创伤小、术中及术后并发症少等优点,逐渐成为单纯性肾囊肿患者的首选治疗方式。因此,选取该院 2019 年 1 月—2020 年 8 月收治的 36 例患者为研究对象,旨在探讨超声引导下联合DSA 的肾囊肿穿刺硬化治疗的临床效果,现报道如下。
1 资料与方法
1.1 一般资料
选取该院收治的72 例肾囊肿硬化患者为研究对象,按照治疗方式的不同,分为对照组和观察组,每组36 例。 观察组在超声引导下联合DSA 行单腔中心静脉导管置入术治疗, 对照组单纯在超声引导下行单腔中心静脉导管置入术治疗。 其中观察组男21 例,女 15 例;平均年龄(56.23±5.2)岁;32 例单侧治疗,4 例双侧治疗;囊肿直径 5~10 cm,平均(8.5±1.2)cm。 对照组男 22 例,女 14 例;平均年龄(58.56±7.2)岁;33 例单侧治疗,3 例双侧治疗;囊肿直径 5~10 cm,平均(8.5±1.5)cm。 患者及家属均知情并签署知情同意书,该研究通过医院伦理委员会的批准。
1.2 方法
对照组患者给予超声引导下行单腔中心静脉导管置入术治疗。具体操作:患者依据囊肿位置取健侧侧卧位或俯卧位,常规消毒铺巾,使用一次性无菌腔镜套包裹超声探头。超声观察进针线路,进针线路应避开肋骨、肠管、大血管、肾实质等重要脏器,在安全的前提下选用最短穿刺路线。单腔深静脉导管在距离顶端主孔约1~3 cm 处开2 个侧孔,侧孔直径约1 mm,两个侧孔在导管的侧面位置投影成90°角。 拉伸确认导管牢固,不易断裂。超声引导下用2%利多卡因5 mL 皮下及针道局部麻醉后,嘱患者屏住呼吸的同时, 用中心静脉导管包内自带穿刺针沿预设路线逐层穿入囊内。 确认穿刺针进入囊腔后, 退出穿刺针芯,沿穿刺针穿入导管包自带“J”形导丝,超声确认导丝进入囊腔后, 退出穿刺针后沿导丝穿入预先开孔的单腔中心静脉导管, 导管边旋转边逐层深入组织。 实时超声确认导管进入囊腔后,退出导丝,导管尾端连接三通开关,通道建立完成。之后将囊液吸尽并注入无水酒精反复冲洗, 直至抽出的无水酒精变清澈为止,最后将导管固定,保留 5 mL 无水酒精,包扎伤口。
观察组患者给予超声引导下联合DSA 行单腔中心静脉导管置入术治疗。具体操作:局部麻醉后,超声引导下联合DSA 取较佳穿刺点进行穿刺,用50 mL 注射器连接三通,全部抽出囊液并计量,用无菌生理盐水以1:50 比例稀释声诺维造影剂一支并注入囊腔,观察造影剂弥散情况,确认囊腔与集合系统不相通后。抽出造影剂溶液,注入抽出囊液量约1/3~1/4 的聚桂醇溶液,待10~15 min 后全部抽出。 随后缓慢拔出导管, 按压穿刺点3~5 min 后局部敷贴覆盖。 术后绝对卧床6 h 并进行心电监护,密切关注患者不适主诉及生命体征。
1.3 观察指标
比较两组治疗效果及不良反应发生情况。
临床治疗效果的判定[4]:痊愈:超声结果显示完全看不见囊肿;显效:超声结果显示囊肿大小显著缩小,且缩小体积在原来体积的一半以上;有效:超声结果显示囊肿大小有相应缩小, 但缩小体积未达到原来体积的一半;无效:超声结果显示囊肿大小未见任何缩小。总有效率=(痊愈例数+ 显效例数+ 有效例数)/ 总例数×100.00%。
1.4 统计方法
采用SPSS 21.0 统计学软件处理数据, 计数资料用[n(%)]表示,采用 χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者临床有效率比较
观察组临床总有效率明显优于对照组, 差异有统计学意义(P<0.05),见表 1。
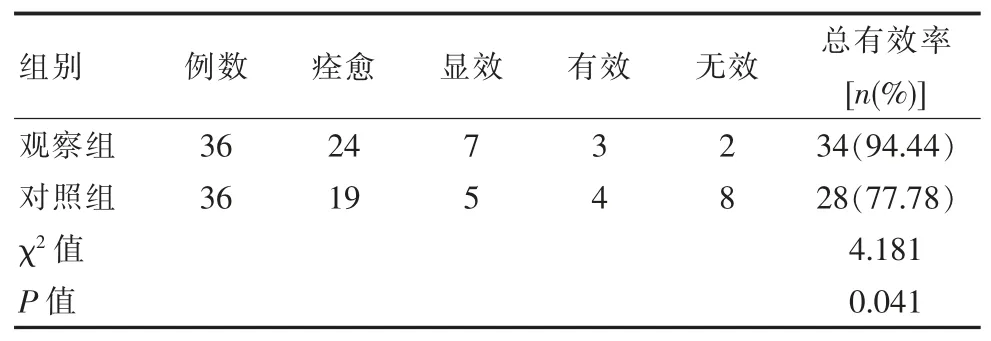
表1 两组患者临床有效率比较
2.2 两组患者不良反应发生情况比较
观察组不良反应发生率低于对照组, 差异有统计学意义(P<0.05),见表 2。
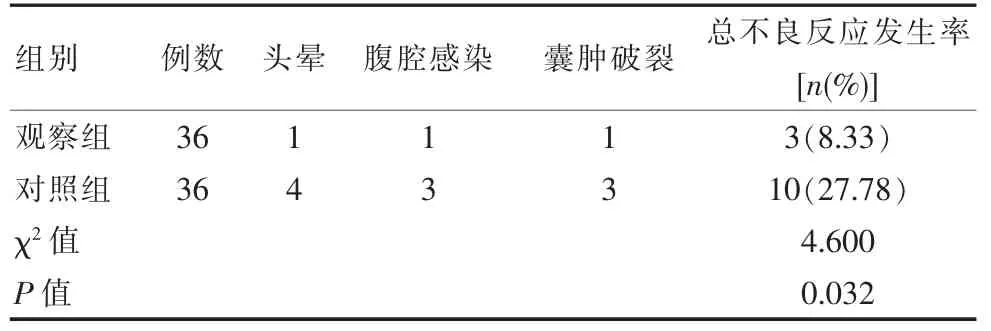
表2 两组患者不良反应发生情况比较
3 讨论
肾囊肿常起源于肾小管, 是单侧或双侧肾脏内出现的大小不等的与外界不相通的囊性肿块,基本都为良性,好发于中老年人。传统对肾囊肿的分类一般分为单纯性肾囊肿、 成人型多囊肾以及获得性肾囊肿[5]。 其中,成人型多囊肾还是一种染色体显性遗传性疾病。当肾囊肿出现囊壁局限性增厚、囊内多发分隔、囊壁钙化、囊内出血、感染等症状时则称为复杂性肾囊肿, 复杂性肾囊肿的恶性病变率大大增加[6-8]。不同患者的肾囊肿往往大小不一, 一般直径从0.5~10 cm 不等,对于直径<4 cm 且无集合系统压迫的单纯性肾囊肿患者, 一般无自觉症状, 也不需临床干预。 但当肾囊肿直径发展>5 cm 时往往可引起不同程度的临床症状,常表现为腹背部胀痛、腰部酸痛,对患者心理以及正常生活造成干扰。
随着影像学的进步, 超声引导以及CT 引导下的经皮穿刺肾囊肿硬化治疗逐渐兴起。 传统的超声引导下经皮穿刺肾囊肿硬化治疗多采用18~20 G 的PTC 针穿刺,针长15 cm 或20 cm,超声引导下穿刺针针尖进入囊腔后,一般使针尖位于囊肿的中后1/3处,拔出针芯,尾部接延长管,沿穿刺针及延长管完成抽液、冲洗及注入硬化剂硬化等操作[9-10]。 而超声以其可实时动态引导、 观察成为肾囊肿穿刺硬化治疗的首选影像学引导工具。 随着介入超声的不断发展, 超声引导下的经皮穿刺肾囊肿硬化治疗已经逐渐成为肾囊肿患者的首选治疗方式, 充分发挥了超声作为唯一的可动态观察的影像学技术的优势[11-14]。其中,行单腔中心静脉导管置入术式的优点如下:①对于内部没有分隔的囊肿, 囊腔内的囊液可以完全抽尽,不用担心稀释硬化剂,即使抽尽后超声无法观察到导管是否位于囊腔内, 仍可以通过注入生理盐水的方法使囊腔充盈,进一步确认导管位置。抽尽囊液的囊肿, 不需要通过反复置换提高囊内硬化剂的浓度。 ②导管置入囊腔内的长度较长, 可以适当盘曲,笔者的经验是参照穿刺时的深度,可以按照两倍的长度置入导管。这样即使患者剧烈咳嗽,导管也不会脱出囊腔导致手术失败[15]。 ③单腔深静脉导管为软管,所以不会刺伤囊壁引起出血,更不会刺伤临近大血管,治疗过程更安全。 ④囊肿内囊液抽尽后,即使有胃肠道气体干扰, 在通过注入生理盐水的方法使囊腔充盈再次确认位置后, 仍然可以按原计划继续治疗。 但单纯的超声引导穿刺仍缺乏有效的精准度,采用数字减影血管造影(DSA)和超声联合引导技术可以不受气体因素的干扰,对导丝、导管的走形判断更为准确。 因此可以有效提高穿刺精准度和手术安全性,改善肾囊肿治疗效果。 由该文结果可知,观察组治疗总有效率为94.44%, 明显优于对照组(P<0.05)。 观察组不良反应发生率低于对照组 (P<0.05)。这与田云飞等[15]学者在相关研究中得出,超声引导下行单腔中心静脉导管置入术联合DSA 治疗后,临床有效率为97.73%、不良反应发生率为6.82%,明显优于单一治疗,与该文所得结果相近。
在治疗的过程中,该研究发现,在置入单腔深静脉导管的过程中,囊肿周边会有部分囊液外渗,在囊壁的进针点周边形成新月样的积液。 这是由于囊肿内置入导丝后,穿刺针退出,部分囊液会沿着囊壁穿刺点外渗[16]。 而在沿着导丝置入导管的过程中,当导管头端接触囊壁时,会对囊肿造成一种推压,加速囊液的外渗。对于张力高的囊肿,外渗的囊液就更多一些。 单纯性肾囊肿的囊液成分与血清类似,无菌,无细胞成分。所以外渗的囊液不会对身体造成伤害,第2 天观察,外渗的囊液也会全部吸收。 但外渗的囊液会影响囊液抽出总量的计算, 从而对准确计算硬化剂的使用量产生影响。在后期术式的改进中,穿刺针穿入囊肿后,先通过穿刺针抽出一部分囊液减压,再置入单腔深静脉导管,这样囊液的外渗会大大减少。
综上所述,超声引导下联合DSA 行单腔中心静脉导管置入术治疗肾囊肿硬化, 可以提高临床治疗效果,降低不良反应发生率,值得临床推广。
