唑来膦酸对乳腺癌术后内分泌治疗患者骨折风险的影响
2022-06-09陈小英唐朝晖罗鹏飞丁思娟
陈小英,唐朝晖,罗鹏飞,吴 辰,丁思娟
永州市中心医院肿瘤内科, 湖南 永州 425000
乳腺癌是临床常见的高度异质性肿瘤,全球新发乳腺癌人数约为120万,占女性恶性肿瘤的20%~30%[1]。近年来,随着医学诊疗技术的发展,乳腺癌患者生存状况得到显著改善。当前综合疗法是治疗乳腺癌的主要方案,以手术、放化疗等为主,尤其是内分泌治疗方案的出现,使耐药性乳腺癌患者治疗方法及远期效果得到显著改善[2]。但内分泌治疗时间长,且有研究[3]报道,乳腺癌患者经内分泌维持治疗,骨量丢失明显增加,骨折风险提高。因此降低骨折风险,减少骨量丢失成为临床研究重点。唑来膦酸是一种氮双磷酸盐类药物,通过对破骨细胞引起骨重吸收过程的抑制,预防骨质疏松,常用于骨质疏松骨转移患者的标准治疗[4]。目前,关于唑来膦酸对乳腺癌患者内分泌治疗时骨折风险的影响,临床鲜有报道,为了更进一步分析唑来膦酸对乳腺癌患者内分泌治疗时骨折风险的影响,本研究回顾样本医院2016 年12 月—2018 年8 月收治的73例乳腺癌患者临床资料,分析医院乳腺癌内分泌治疗患者经唑来膦酸干预效果,现将结果报告如下。
1 资料与方法
1.1 临床资料
纳入标准:(1)在院行乳腺癌改良根治术。(2)雌激素受体或孕激素受体阳性。(3)治疗前未经双磷酸盐治疗。(4)未伴先天性骨疾病。(5)具有完整的临床资料。排除标准:(1)伴心、肝、肾等脏器障碍。(2)近期曾使用影响免疫机制的药物。(3)研究药物过敏史。回顾样本医院2016 年12 月—2018 年8 月收治的73 例乳腺癌患者,按不同治疗方法分为两组。对照组35 例,年龄40~68 岁,平均年龄(56.38±5.17)岁;分期:Ⅱb 期5 例,Ⅲa 期16例,Ⅲb 期14 例。观察组38 例,年龄40~68 岁,平均年龄(57.14±5.23)岁;分期:Ⅱb 期6 例,Ⅲa 期15 例,Ⅲb 期17 例。两组患者基线资料具有可比性(P>0.05)。本研究符合本院医学伦理委员会审批标准。
1.2 方法
对照组采用术后内分泌治疗,戈舍瑞林(AstraZeneca UK Limited,国药准字X19990231),3.6 mg/次,皮下注射,每4 周1 次;阿那曲唑(杭州中美华东制药有限公司,国药准字H20123048),1 mg/次,或来曲唑(江苏恒瑞医药股份有限公司,国药准字H19991001),2.5 mg/次,每天1次;维D钙咀嚼片[安士制药(中山)有限公司,国药准字J20100033],2 片/次,每天1 次。观察组术后内分泌治疗时结合唑来膦酸(正大天晴药业集团股份有限公司,国药准字H20041346),每次剂量4 mg+生理盐水100 mL,静脉滴注,每6个月1次。两组患者连续用药至今。
1.3 观察指标
(1)比较两组患者治疗前、治疗6 个月、12 个月、24个月股骨颈、腰椎骨密度量,采用双能X 线骨密度检测仪检测骨密度量。(2)对比两组患者骨折发生风险,即随访至2020 年9 月,统计骨质疏松性骨折发生例数。(3)比较两组患者肢体骨痛程度,采用视觉模拟法(VAS)进行评价,由我院制作的0~10 cm 标尺,由患者按照疼痛程度指出相应数字,并对应相应疼痛分值,无痛为0 分;轻微疼痛,未影响生活为1~3 分;中度疼痛,影响生活,要求使用镇痛药物为4~6 分;重度疼痛,必须要使用镇痛药物为7~10 分。(4)比较两组患者治疗前、治疗24 个月后免疫功能,即采集两组患者外周静脉血3 mL,用流式细胞仪测定T淋巴细胞亚群CD4+、CD8+及两者比值。(5)分析唑来膦酸应用期间的副作用。
1.4 统计学方法
采用SPSS 20.0 软件进行统计分析。计量资料以均数±标准差(±s)表示,组间比较采用t 检验。计数资料率以例数和百分比(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者不同时间点腰椎、股骨颈骨密度量情况
治疗前、治疗6 个月两组患者的腰椎、股骨颈骨密度量比较,差异无统计学意义(P>0.05);两组患者治疗12个月、24 个月股骨颈、腰椎骨密度量较治疗前有所下降,差异有统计学意义(P<0.05);观察组骨密度量高于对照组,差异有统计学意义(P<0.05),见表1。
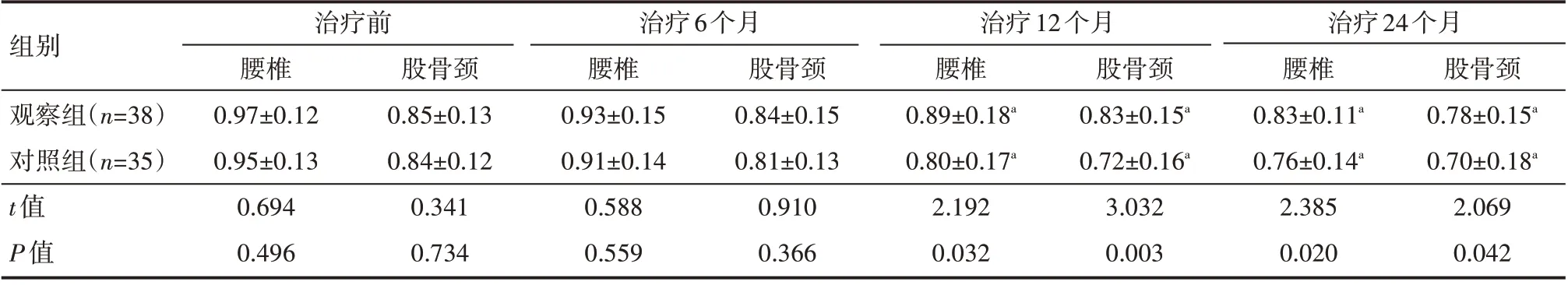
表1 两组患者不同时间点腰椎、股骨颈骨密度量情况 g/cm2
2.2 两组患者骨折发生情况
观察组骨质疏松骨折总发生率低于对照组,差异有统计学意义(P<0.05),见表2。
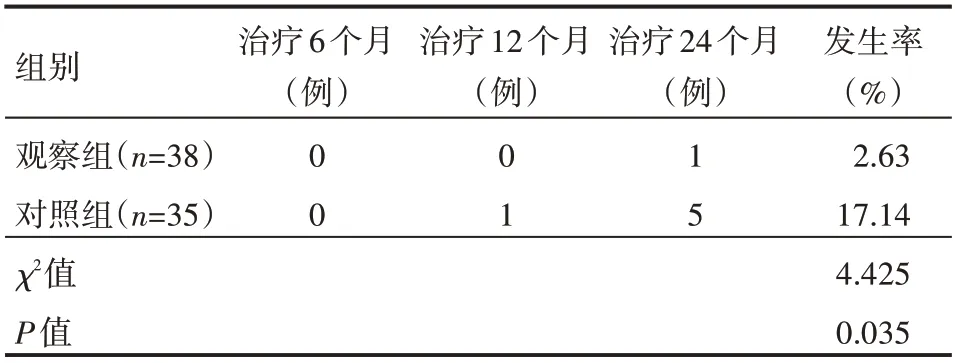
表2 两组患者骨折发生情况
2.3 两组患者肢体疼痛程度VAS评分情况
两组患者治疗前肢体疼痛程度比较,差异无统计学意义(P>0.05);两组患者治疗6 个月、12 个月、24 个月肢体疼痛程度高于治疗前,且观察组疼痛评分低于对照组,差异有统计学意义(P<0.05),见表3。
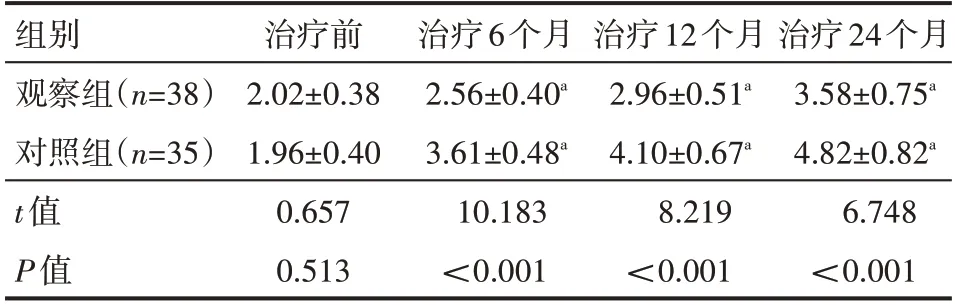
表3 两组患者肢体疼痛程度VAS评分情况 分
2.4 两组患者治疗前、治疗24个月后免疫功能情况
两组治疗前T 淋巴细胞亚群水平比较,差异无统计学意义(P>0.05);观察组治疗24 个月免疫功能高于对照组,差异有统计学意义(P<0.05),见表4。
表4 比较两组患者治疗前、治疗24个月后免疫功能情况(±s) %
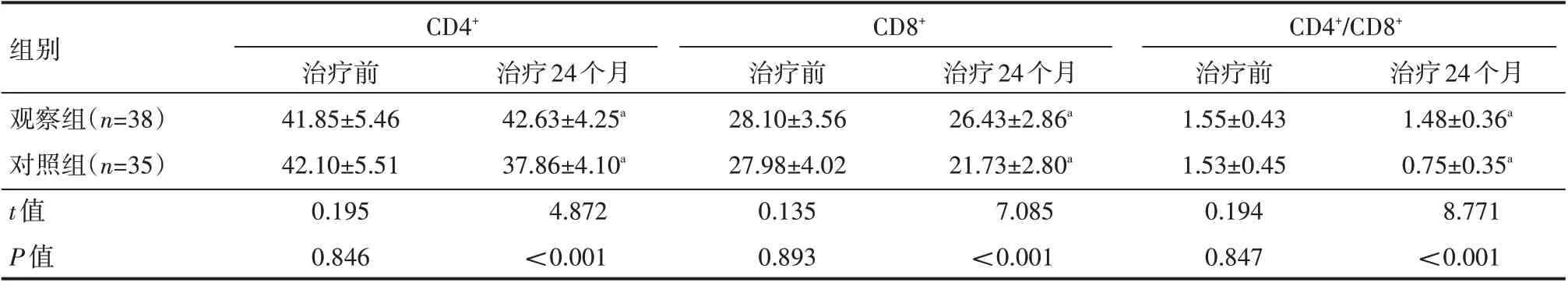
表4 比较两组患者治疗前、治疗24个月后免疫功能情况(±s) %
a表示与治疗前比较,P<0.05。
组别CD4+CD8+观察组(n=38)对照组(n=35)t值P值治疗前41.85±5.46 42.10±5.51 0.195 0.846治疗24个月42.63±4.25a 37.86±4.10a 4.872<0.001治疗前28.10±3.56 27.98±4.02 0.135 0.893治疗24个月26.43±2.86a 21.73±2.80a 7.085<0.001 CD4+/CD8+治疗前1.55±0.43 1.53±0.45 0.194 0.847治疗24个月1.48±0.36a 0.75±0.35a 8.771<0.001
2.5 两组患者不良反应发生情况
观察组患者经唑来膦酸首次治疗第2 天,有1 例患者出现骨骼疼痛,治疗第5 天出现2 例疲乏,1 例发热,8 例骨骼、肌肉疼痛情况,多数患者不良反应出现24h 内缓解,随访期间未出现血尿、肝肾异常。
3 讨论
内分泌是临床辅助治疗激素受体阳性乳腺癌患者的有效方法,并为乳腺癌治疗提供一条新的途径。戈舍瑞林、阿那曲唑或来曲唑的联合应用,成为治疗乳腺癌术后患者标准方案,尤其是对他莫昔芬耐药性患者更具效果。但内分泌治疗时,有资料[5]表明,内分泌治疗方案能降低体内雌激素含量,但会增加骨量丢失量,导致骨折发生。因此,重视患者治疗期间骨折发生风险,联合一种合理、有效的方法是研究重点。唑来膦酸是第三代双磷酸盐药物,常用于晚期乳腺癌伴骨转移患者,起到直接或间接性抗肿瘤作用;同时与其他抗肿瘤药物相应用,起到协同促使肿瘤细胞凋亡作用[6]。唑来膦酸具体抗肿瘤作用:(1)对肿瘤细胞增殖过程的抑制,阻滞肿瘤细胞周期,促使其凋亡,并能阻挡肿瘤细胞的黏附、入侵过程,促使肿瘤细胞凋亡;(2)阻滞肿瘤血管生成过程,减少肿瘤因子的释放,抑制肿瘤细胞活性;(3)通过调节机体免疫功能,阻断甲羟戊酸过程,具有间接性抑制肿瘤细胞作用[7]。而在保护骨结构方面,唑来膦酸通过对破骨细胞活性的抑制,促使破骨细胞凋亡,起到抗骨吸收的作用,并能减少溶骨性破坏,减少骨量的丢失[8]。
本研究中,两组患者治疗12 个月、24 个月股骨颈、腰椎骨密度量较治疗前有所下降;但观察组骨密度量高于对照组。观察组骨质疏松骨折总发生率低于对照组。周仕国等[9]报道,唑来膦酸的应用可显著增加老年骨质疏松椎体压缩性骨折术后骨密度量,改善骨代谢。吴阔等[10]研究表明,唑来膦酸联合同期放化疗治疗晚期乳腺癌骨转移,能够降低患者骨痛程度,降低血清钙和血管内皮生长因子水平。宋亚琪等[11]研究表明,早期唑来膦酸能预防内分泌治疗患者骨量丢失,对预防骨折发生起到积极促进意义。因此,多研究指出唑来膦酸可抵抗骨吸收,促使破骨细胞凋亡,减少骨量丢失。本研究结果表明,早期唑来膦酸能减轻内分泌治疗患者骨痛现象,分析原因是唑来膦酸通过抗骨吸收、减少骨量丢失,而能减缓骨痛程度。乳腺癌患者内分泌治疗时,在破坏肿瘤细胞时,也会损害周围的巨噬细胞、淋巴细胞等正常免疫活性细胞,导致患者免疫力下降。本研究结果表明,采用早期唑来膦酸能预防患者免疫功能下降。分析其原因为,采用早期唑来膦酸,具有直接及间接抗肿瘤活性,减少骨折风险事件的发生,并能识别多种肿瘤细胞表达的抗原,促使含磷抗原异戊烯焦膦酸大量聚集,进而提高机体免疫力[12]。在用药安全性方面,唑来膦酸治疗期间,患者出现不同程度的疲乏、发热与骨骼、肌肉疼痛等情况,多数患者在24 h内的不良反应有所缓解,随访期间未出现血尿、肝肾异常。因此,唑来膦酸的应用,有较高的用药安全性。但唑来膦酸治疗期间,容易出现骨骼、肌肉酸痛情况,或损害患者肾功能,故对肾功能障碍者,不宜采用唑来膦酸,而本研究患者未出现肾功能损害,可能是研究样本量少,其随访时间仍较短,需进一步延长患者随访时间,增加病例数,确定唑来膦酸的安全性。
综上所述,唑来膦酸用于乳腺癌术后内分泌治疗中,能减少骨量丢失,降低骨折发生风险,且无明显不良反应,临床意义高。但该研究尚有不足,研究样本量少、研究属回顾性研究,使其研究存在偏倚,故仍需后续研究开展大宗病例、设置前瞻性随机对照试验,以此明确唑来膦酸的应用效果。
