GC-NCI-MS衍生化法同时测定全血中的亚硝酸根和硝酸根
2022-05-21崔婉莹饶渝兰于忠山张云峰董林沛魏春明吴小军
崔婉莹,赵 鹏,饶渝兰,于忠山,张云峰*,董林沛,魏春明,吴小军
(1.中国人民公安大学 侦查学院,北京 100038;2.公安部物证鉴定中心,北京 100038;3.复旦大学基础医学院,上海 200032)
亚硝酸盐广泛存在于人们日常生活中,在工业中是常用的化工原料,在食品加工中常被用作防腐剂和发色剂。其外观与食盐相似,常因误食、自杀、投毒等原因引起亚硝酸盐中毒[1-4]。人体短时间摄入大量亚硝酸盐,会造成高铁血红蛋白血症,引起紫绀症、头痛、头晕、心律加快、恶心、呕吐、腹痛、腹泻等症状,严重者导致缺氧性死亡。食入亚硝酸盐的中毒量为0.3~0.5 g,致死量为3~5 g[5]。
亚硝酸盐中毒案件中,通常采用离子色谱-质谱法和食品中亚硝酸盐与硝酸盐的相关测定标准方法对胃内容物、呕吐物、剩饭剩菜等体外检材中的NO-2进行分析[4,6]。由于缺乏成熟的方法,通过对体内检材的分析检测来定性案件的案例鲜有报道,缺少体内检材的检测结果严重制约了中毒的鉴定和案件的侦破。NO-2和NO-3浓度的测定方法较多,包括比色法[7-8]、高效液相色谱法[9-10]、离子色谱法[11-12]、毛细管电泳法[13]和气相色谱-质谱法(GC-MS)[14-17]等,主要用于人体代谢监测、食品工业和环境监测等方面。通过保留时间和质谱图进行定性、定量的GC-MS 衍生化法因具有较高的准确性,被广泛用于血浆、血清、尿液、唾液等生物样品中亚硝酸盐和硝酸盐的同时定量研究[18-19],但很难测定全血中的NO-2和NO-3。血液是毒物分析的主要检材,具有易获取、不易被污染等优点,血液中的毒物浓度水平可用于解释中毒或死亡原因。在法医鉴定领域,由于普遍存在死后溶血现象,往往只能取到全血作为检材,而取不到血浆或血清。因此本文旨在建立一种灵敏度高、准确性好,可同时定量全血中NO-2和NO-3的GC-MS衍生化分析方法,解决以往亚硝酸盐中毒案件中全血作为检材检测困难的问题。
1 实验部分
1.1 仪器、材料与试剂
分析天平(梅特勒-托利多国际贸易(上海)有限公司);Milli-Q Direct 水纯化系统(德国Merck Millipore 公司);EYELA CM-1000 振荡器(日本东京理化公司);HeraeusTM FrescoTM 21 微量离心机(美国Thermo Fisher Scientific 公司);IKA MS 3 digital 数显型圆周振荡器(德国IKA 公司);全自动毒品毒物前处理W880 浓缩仪(北京吉艾姆科技有限公司);QP2010 气相色谱-质谱(日本Shimadzu 公司);2 mL离心管(赛谱锐思(北京)科技有限公司)。
亚 硝 酸 钠(NaNO2,99.999%)、亚 硝 酸 钠-15N(Na15NO2,≥98.5%)、硝 酸 钠-15N(Na15NO3,≥98.5%)、2,6-二叔丁基-4-甲基苯酚(BHT,>99.0%)、三苯基膦(TPP,>99.0%)、五氟苄基溴(PFB-Br,99%)购自上海阿拉丁生化科技股份有限公司;硝酸钠(≥99.0%)购自国药集团化学试剂有限公司;四辛基溴化铵(TOA-Br,98%)购自德国默克公司;乙醇、乙腈、丙酮、正己烷、甲醇、甲苯、乙酸乙酯、正己烷均为色谱纯,购自美国Fisher Scientific 公司;实验用水为电导率18.2 MΩ·cm-1的去离子水;空白血样购自北京复兴医院。
1.2 标准溶液与内标溶液的制备
精密称取NaNO2、NaNO3、Na15NO2和Na15NO3固体标样,用水分别配制NO-2质量浓度为1 mg/mL、NO-3为12 mg/mL、15NO-2为100 μg/mL、15NO-3为100 μg/mL的储备液,使用时按需用水逐级稀释。
1.3 样品前处理
取抗氧化剂混合溶液(1.5 mg/mL BHT、7.5 mg/mL TPP的乙醇溶液)200 μL于2 mL离心管,减压浓缩至干,以200 μL 全血样品复溶混匀。加入40 μg/mL 的15NO-2内标溶液、100 μg/mL 的15NO-3内标溶液各10 μL(即加入后全血中内标的质量浓度分别2、5 μg/mL),随后立即加入600 μL 乙腈涡旋振荡5 min。加入200 μL 相转移试剂(8 mmol/L 的TOA-Br 丙酮溶液),离心10 min,取上清液于2 mL 离心管中。加入100 μL 衍生化试剂(5%的PFB-Br 丙酮溶液)涡旋20 s,70 ℃减压浓缩40 min。取出加入150 μL异辛烷,振荡5 min,离心5 min,取上清液至GC-MS进样瓶待分析。
1.4 色谱与质谱条件
1.4.1 色谱条件色谱柱:J&W DB-5 MS 石英毛细管气相色谱柱(30 m×0.25 mm×0.25 μm);载气:氦气(纯度99.999%);压力:58.8 kPa;柱流速:1.00 mL/min;进样口温度:200 ℃;进样方式:分流进样,分流比1∶10,进样量1 μL;溶剂延迟时间:2.5 min。升温程序:初始温度60 ℃,保持5 min;以15 ℃/min升至200 ℃,保持1 min;再以30 ℃/min升至280 ℃,保持1 min。
1.4.2 质谱条件离子源温度:220 ℃;接口温度:220 ℃;离子化方式:负化学电离源(NCI);扫描方式:选择离子扫描(SIM)。目标物和内标衍生物的色谱保留时间及质谱特征离子见表1。
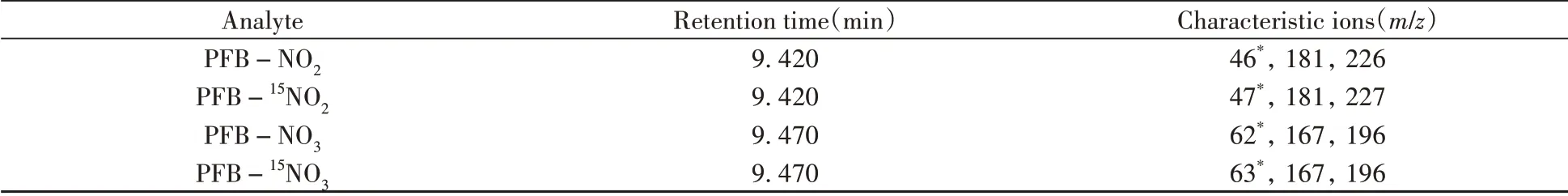
表1 全血中目标物和内标衍生物的色谱保留时间及质谱特征离子Table 1 Chromatographic retention times and mass spectral characteristic ions of target and internal standard derivatives in whole blood
2 结果与讨论
2.1 前处理条件的优化
由于NO-2不稳定、易氧化,通过添加抗氧化剂以减少NO-2在前处理过程中的氧化。结果表明,未添加抗氧化剂和添加抗氧化剂时的氧化比例分别为39.6%和2.4%,添加抗氧化剂可起到减弱氧化的作用。实验分别对目标物提取溶剂、衍生物提取溶剂、相转移试剂用量、衍生化方式、衍生化反应时间和温度进行了优化,优化条件时不添加内标物,通过比较NO-2和NO-3衍生物的平均峰面积选择最优条件。
2.1.1 目标物提取溶剂和衍生物提取溶剂的选择考察了分别以乙腈、丙酮、甲醇作为目标物提取溶剂时的效果,结果表明乙腈沉淀蛋白更完全,丙酮次之,甲醇的提取效果最差,因此选择乙腈作为目标物提取溶剂。对比了采用异辛烷、甲苯、乙酸乙酯、正己烷作为衍生物提取溶剂时的效果,结果表明异辛烷对于衍生化产物PFB-NO2的提取效果最好,甲苯对于衍生化产物PFB-NO3的提取效果最好,其它3种有机溶剂对PFB-NO3的提取效果相差不大。由于甲苯有毒,因此选择异辛烷作为衍生物提取溶剂。
2.1.2 相转移试剂用量的选择相转移试剂的使用可以增加反应产率和反应物的稳定性,考察了相转移试剂用量(50、100、150、200、250 μL)对衍生化反应的影响。结果显示,不同相转移试剂用量对PFB-NO3的生成无显著影响,PFB-NO2的生成量则随相转移试剂用量的增加而增加,并在200 μL 时达到最大,因此选择相转移试剂用量为200 μL。
2.1.3 衍生化方式的选择考察了水浴衍生后氮吹浓缩、水浴衍生后减压浓缩和直接减压浓缩3种衍生化方式对衍生效率的影响(见图1)。结果表明,氮吹浓缩后再复溶进样的衍生化效率较低且重现性较差(图1中未画出)。水浴衍生后减压浓缩方式虽小幅提升了NO-2的衍生化效率,但PFB-NO3的峰面积远小于直接减压浓缩衍生方式,且直接减压浓缩可以简化操作过程。因此选择直接减压浓缩的方式,将衍生化与浓缩过程一步进行。
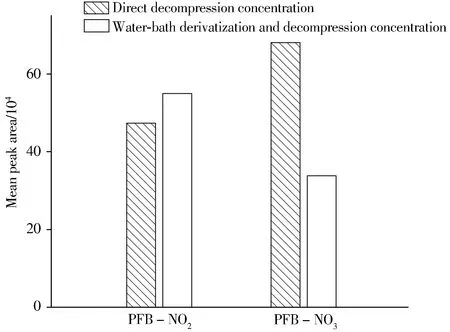
图1 不同衍生方式生成的PFB-NO2和PFB-NO3峰面积图Fig.1 Peak areas of PFB-NO2 and PFB-NO3 generated by different derivatization methods
2.1.4 衍生化温度与时间的选择分别对比了不同衍生化反应温度(40、50、60、70、80 ℃)条件下的衍生效率(见图2)。结果表明当温度低于70 ℃时,2个反应产物的峰面积随温度升高而增大,当超过70 ℃时峰面积下降,因此选择衍生化温度为70 ℃。在衍生化温度为70 ℃条件下,考察了衍生化反应时间(20、30、40、50、60 min)对衍生效率的影响(见图3)。结果显示2 种反应产物的峰面积随反应时间的增加而增大,在40 min 时峰面积达到最大,而后均呈下降趋势。为使反应物反应完全且不造成衍生产物损失,选择衍生化时间为40 min。
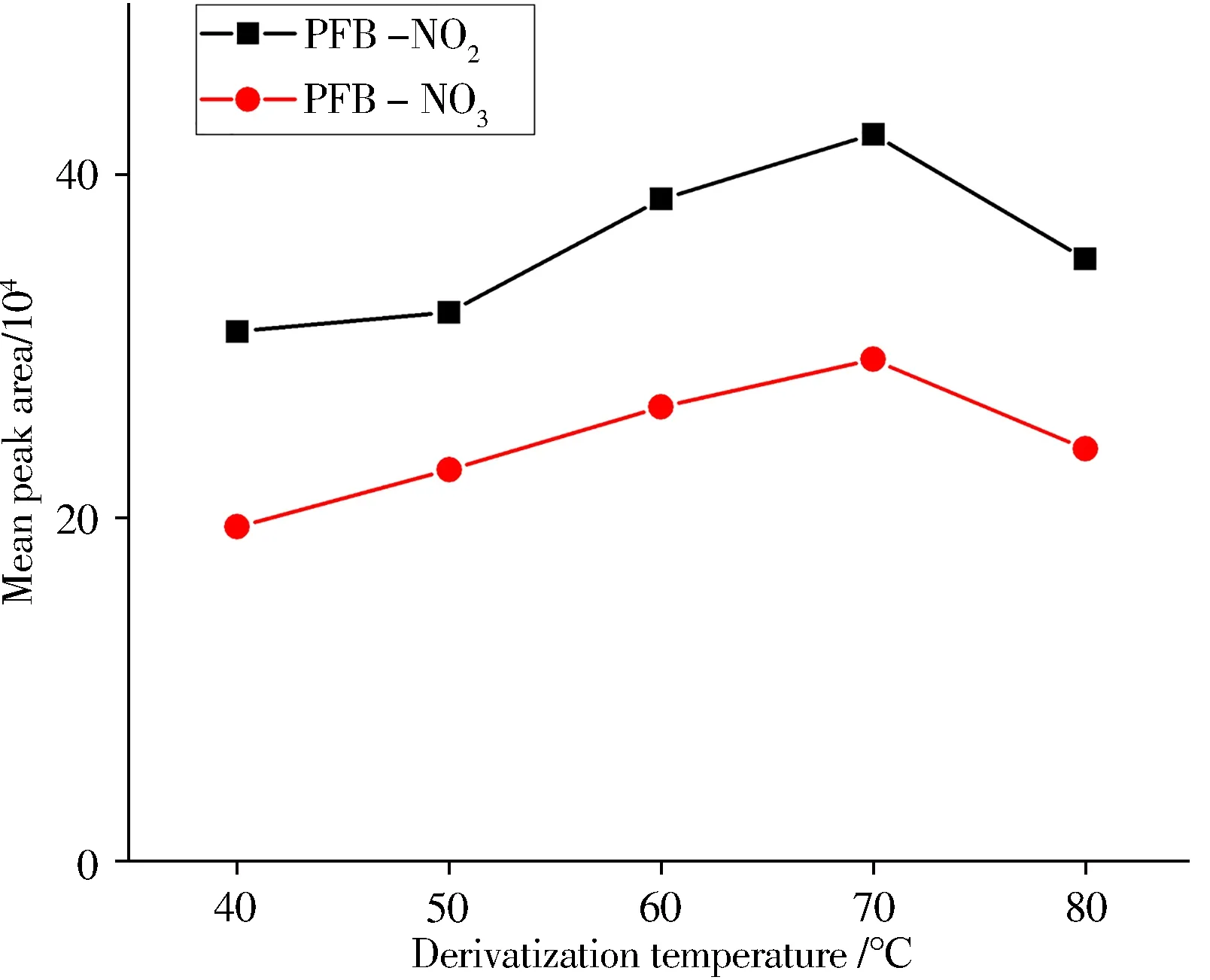
图2 衍生化温度的影响Fig.2 Effect of derivatization temperature
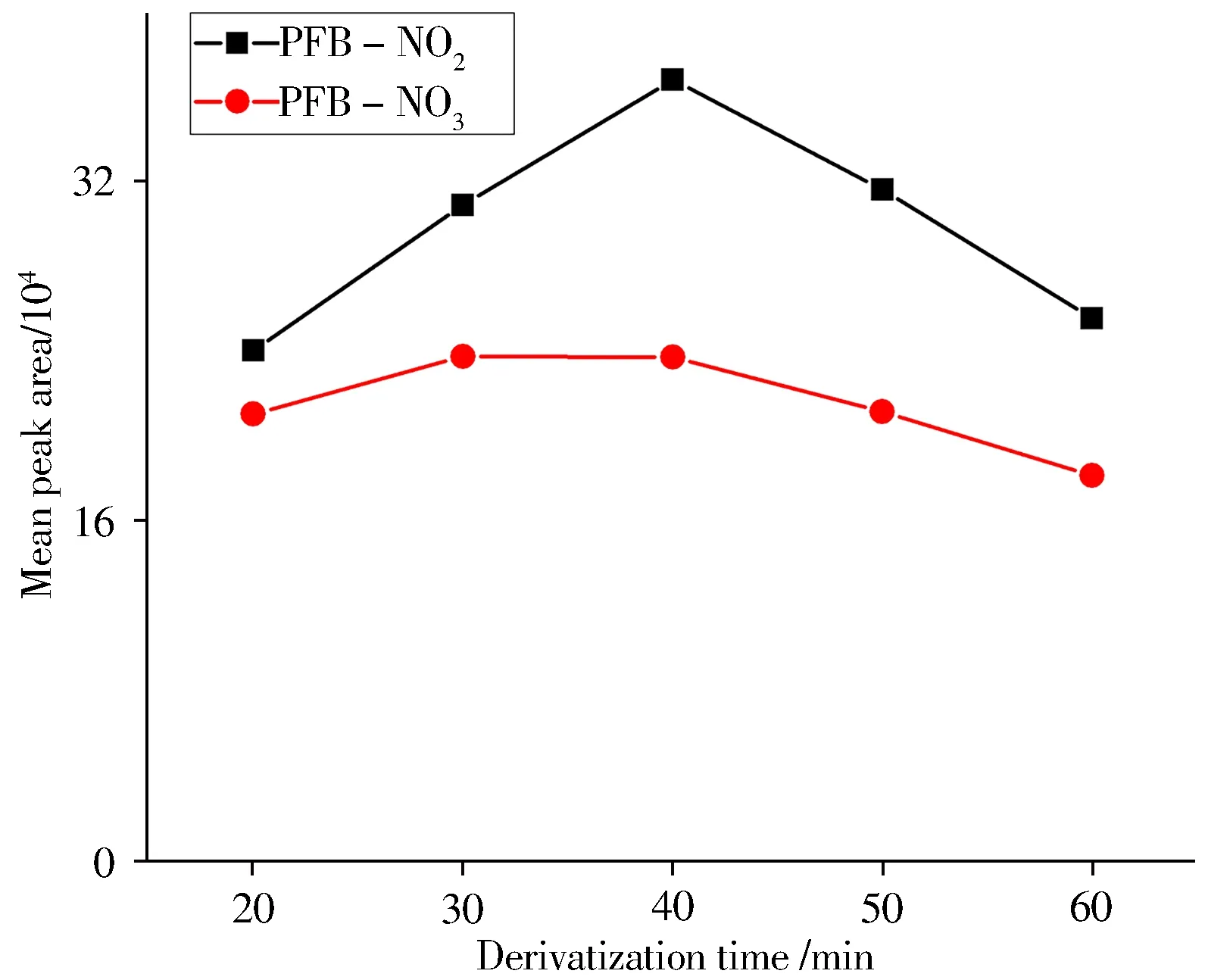
图3 衍生化时间的影响Fig.3 Effect of derivatization time
2.2 方法选择性
NO-2、15NO-2、NO-3和15NO-3的标准品溶液衍生后在全扫描模式下的质谱图如图4所示,全血中目标物与添加内标衍生后的SIM色谱图如图5所示。由图可知,衍生物PFB-NO2、PFB-15NO2的保留时间为9.370 min,PFB-NO3、PFB-15NO3的保留时间为9.420 min,通过离子碎片m/z46、47、62、63 结合保留时间和碎片离子可对目标物进行定性和定量。
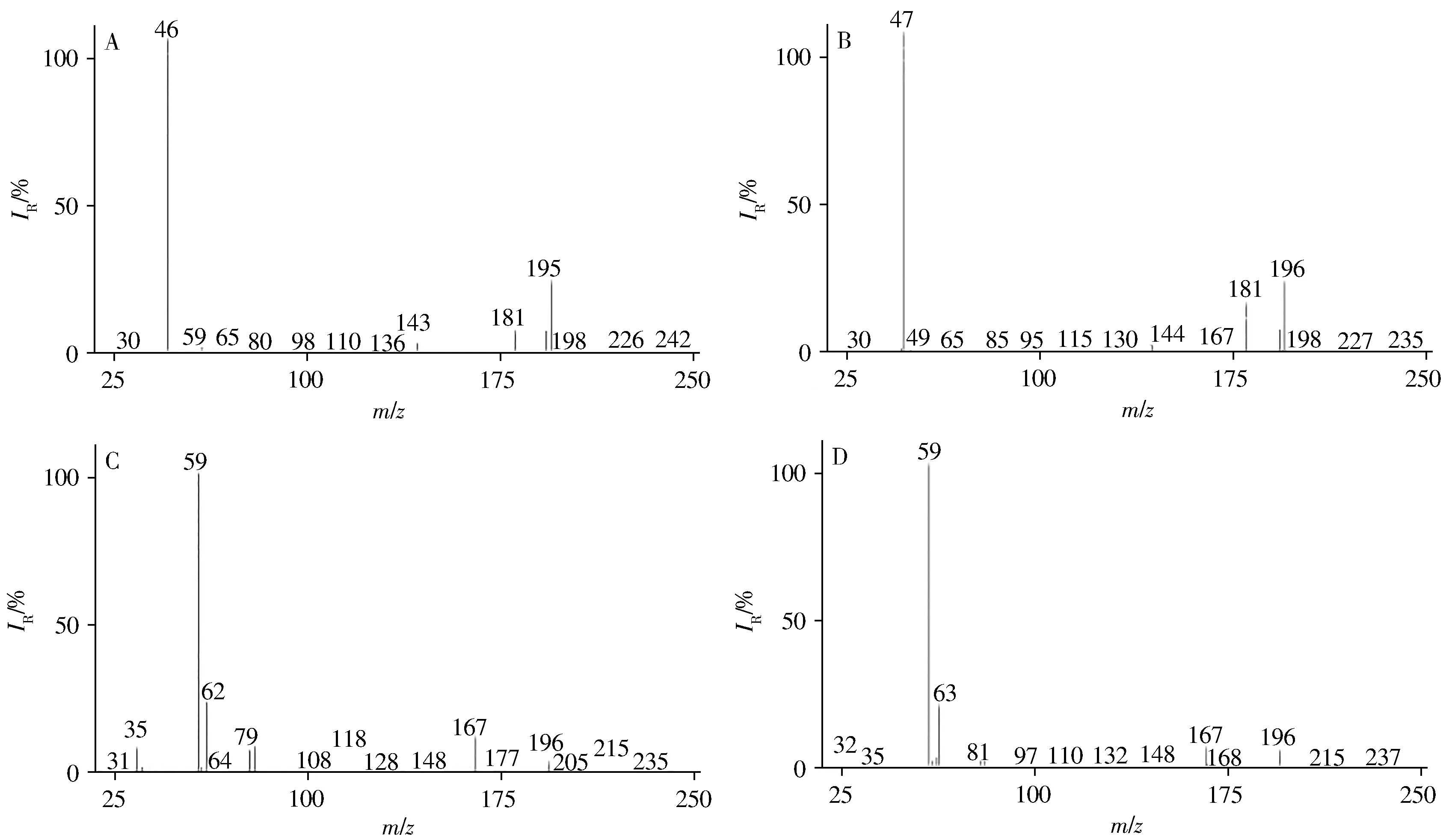
图4 衍生物PFB-NO2(A)、PFB-15NO2(B)、PFB-NO3(C)、PFB-15NO3(D)在全扫描模式下的质谱图Fig.4 Mass spectra of derivatives PFB-NO2(A),PFB-15NO2(B),PFB-NO3(C)and PFB-15NO3(D)in full scan mode
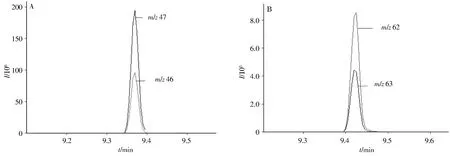
图5 全血中衍生物PFB-NO2、PFB-15NO2(A)和PFB-NO3、PFB-15NO3(B)的SIM色谱图Fig.5 SIM chromatograms of the derivatives PFB-NO2,PFB-15NO2(A)and PFB-NO3,PFB-15NO3(B)in whole blood
2.3 线性范围与检出限
按“1.3”步骤操作,加入不同质量浓度的NO-2和NO-3标准溶液,使全血中NO-2的质量浓度分别为0.05、0.2、0.5、1、2、5 μg/mL,NO-3的质量浓度分别为1、5、10、100、200、300 μg/mL。以加标后的血样中NO-2/15NO-2(或NO-3/15NO-3)峰面积比值减去空白血中NO-2/15NO(-2或NO-3/15NO-3)峰面积的比值为纵坐标,全血中NO-2和NO-3的质量浓度为横坐标,以1/X2为权重因子进行线性回归分析,绘制标准曲线。结果表明,全血中的NO-2和NO-3分别在0.05~5 μg/mL 和1~300 μg/mL范围内线性关系良好,相关系数(r2)分别为0.995和0.997,检出限(LOD,S/N= 3)分别为0.01 μg/mL 和0.2 μg/mL,定量下限(LOQ,S/N=10)分别为0.05 μg/mL和1 μg/mL(见表2)。

表2 全血中NO-2 和NO-3 的线性关系、检出限及定量下限Table 2 Linear relations,detection limits and quantitation limits of NO-2 and NO-3 in whole blood
2.4 提取回收率
提取回收率考察2种目标物质的低、中、高3个质控浓度,每个浓度考察5 个样品。NO-2质控浓度分别为0.15、1、4 μg/mL,NO-3质控浓度分别为3、30、250 μg/mL。取3 个质控浓度下的空白加标血样,按照“1.3”步骤操作后进样得到各待测物的峰面积,记录NO-2/15NO-(2或NO-3/15NO-3)的比值,减去同批空白血中NO-2/15NO(-2或NO-3/15NO-3)的比值后得到数值A1。同时取对应质量浓度下NO-2、NO-3的基质加标溶液,按“1.3”步骤操作,记录N-2/15NO(-2或NO-3/15NO-3)的比值,减去同批空白基质中NO-2/15NO(-2或NO-3/15NO-3)比值后得到数值A2,以A1/A2×100%计算提取回收率,结果如表3 所示。结果显示,全血中低、中、高3个浓度下NO-2的提取回收率分别为118%、109%和99.8%,NO-3的提取回收率分别为88.4%、80.3%和85.1%。
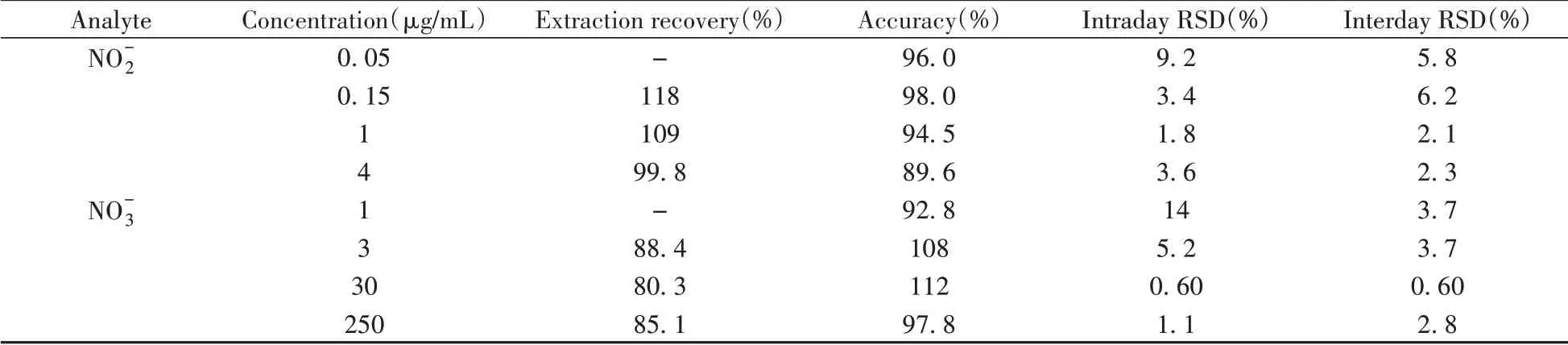
表3 全血中NO-2 和NO-3 的提取回收率、准确度及精密度Table 3 Extraction recoveries,accuracies and precisions of NO-2 and NO-3 in whole blood
2.5 准确度与精密度
选择定量下限(LOQ)、低、中、高浓度4个点作为质控浓度,每个浓度考察5个样品:NO-2的质控浓度分别为0.05、0.15、1、4 μg/mL,NO-3的质控浓度分别为1、3、30、250 μg/mL。加入不同质量浓度的NO-2和NO-3质控标液,按“1.3”步骤操作。GC-MS进样分析后,记录NO-2/15NO(-2或NO-3/15NO-3)比值,减去同批空白血样中NO-2/15NO(-2或NO-3/15NO-3)的比值后,代入线性回归方程反算其实测浓度,分别计算每个质控浓度的准确度、日内和日间精密度(n=3),精密度以相对标准偏差(RSD)表示。由表3可知,4 个质控浓度下NO-2的准确度为89.6%~98.0%,日内RSD 为1.8%~9.2%,日间RSD 为2.1%~6.2%;NO-3的准确度为92.8%~112%,日内RSD为0.60%~14%,日间RSD为0.60%~3.7%。结果表明,所建方法的准确性和重复性良好。
2.6 真实中毒案例应用
2020年9月,某女子被发现在树林中晕倒,经抢救无效死亡。现场勘查时,发现1袋打开的亚硝酸钠粉末和半瓶矿泉水。送检检材为该女子的血液样品,取200 μL血液按照本方法进行样品前处理和分析。测得该女子血液中NO-2和NO-3的质量浓度分别为0.29、224.11 μg/mL。取16份空白血样,按“1.3”步骤操作,记录NO-2/15NO-2或NO-3/15NO-3的比值,反算全血中内源性的NO-2和NO-3浓度。得到NO-2的质量浓度为0.05~0.10 μg/mL,NO-3的质量浓度为1.70~7.70 μg/mL。此案件中2种物质的浓度均远高于人体全血中内源性的浓度水平,可判定为亚硝酸盐中毒。结果表明,所建方法可满足实际案件的检验需求。
3 结 论
NO-2不稳定、易氧化,进入血液后大部分氧化为NO-3,全血中NO-2和NO-3的同时准确定量是案件定性的关键。本文建立了衍生化气相色谱-负化学电离源-质谱同时测定全血中NO-2和NO-3的方法,通过添加抗氧化剂的方式减少NO-2在前处理过程中的氧化。该方法特异性强、灵敏度高,结果准确、可靠,能够满足实际亚硝酸盐中毒案件的检验鉴定需求,可用于实际亚硝酸盐中毒案例分析。
