基于高效液相色谱一测多评法联合化学计量学的决明降脂片综合质量评价
2022-05-12陈薇娜陈丹丹李全清杭州师范大学附属萧山医院浙江萧山医院药学部浙江杭州浙江省食品药品检验研究院浙江杭州005浙江中医药大学药学院浙江杭州005
陈薇娜,冯 霞,陈丹丹,袁 强,李全清(.杭州师范大学附属萧山医院/浙江萧山医院药学部,浙江 杭州 0;.浙江省食品药品检验研究院,浙江 杭州 005;.浙江中医药大学药学院,浙江 杭州 005)
决明降脂片由茵陈、何首乌、决明子和桑寄生等加工而成,现代研究表明其具有显著的保肝、利胆、降血脂、降血压、抗动脉粥样硬化作用[1]。其质量标准[2]未对制剂所含任何成分进行定量分析,以往研究[3-4]仅对该制剂所含1 ~ 2种成分进行了定量分析,难以保证产品质量的均一性及有效性。多指标[5-6]的定量分析有利于较好地体现其整体性和系统性,本实验以2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷为内参物,运用高效液相色谱一测多评法对决明降脂片中滨蒿内酯、3,5-O-二咖啡酰奎宁酸、4,5-O-二咖啡酰奎宁酸、2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷、决明子苷B2、红镰霉素-6-O-β-龙胆二糖苷、决明子苷C、橙黄决明素和美决明子素进行同步检测,建立决明降脂片多指标质量评价模式,同时对3个厂家15批次决明降脂片进行化学计量学分析,以期为全面评价其内在质量提供参考。
1 仪器与试药
高效液相色谱仪(UltiMate 3000型,美国Thermo Fisher Scientific公司;Waters 2695型,美国Waters公司);SB3200DT型超声波清洗机(宁波新芝生物科技股份有限公司);XP205型电子天平(瑞士Mettler Toledo公司);Symmetry Shield C18柱、Welc Xtimate C18柱和Unitary C18柱(250 mm × 4.6 mm,5 μm)。
对照品滨蒿内酯、4,5-O-二咖啡酰奎宁酸、2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷和橙黄决明素(中国食品药品检定研究院,批号分别为111511-201704、111894-202104、110844-202116和111900-202006,含量依次为99.9%、95.1%、94.8%和99.0%);3,5-O-二咖啡酰奎宁酸和美决明子素(成都普瑞法科技开发有限公司,批号分别为PRF10031122和PRF8101721,含量依次为98.7%和99.6%);决明子苷B2、红镰霉素-6-O-β-龙胆二糖苷和决明子苷C(武汉天植生物技术有限公司,含量均为98.0%);决明降脂片(山西华元医药生物技术有限公司,批号200102、200103、201101、201103、210302、210802和210803,编号S1 ~ S7;吉林吉春制药股份有限公司,批号200102、210104、210304和200501,编号S8 ~ S11;长春人民药业集团有限公司,批号20201101、20210201、20210301和20210501,编号S12 ~ S15);乙腈和甲酸为色谱级别,其它试剂均为分析纯。
2 方法与结果
2.1 溶液制备
2.1.1 混合对照品溶液 精密称取对照品滨蒿内酯、3,5-O-二咖啡酰奎宁酸、4,5-O-二咖啡酰奎宁酸、2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷、决明子苷B2、红镰霉素-6-O-β-龙胆二糖苷、决明子苷C、橙黄决明素和美决明子素适量,用80%甲醇制成0.596、0.318、0.232、0.836、0.510、1.192、0.428、0.254和0.196 mg·mL-1的混合对照品贮备液。取上述贮备液用80%甲醇稀释20倍制得混合对照品溶液(9种成分质量浓度分别为29.8、15.9、11.6、41.8、25.5、59.6、21.4、12.7、9.8 μg·mL-1)。
2.1.2 供试品溶液 取决明降脂片,除去糖衣,研细,取细粉约0.5 g,精密称定,置于25 mL量瓶,加80%甲醇20 mL,超声处理60 min,放冷,80%甲醇定容,摇匀滤过,续滤液为决明降脂片样品溶液。取按决明降脂片质量标准制备的缺茵陈、缺何首乌、缺决明子的阴性样品,按上述方法制得相应的阴性样品溶液。
2.2 色谱条件
Symmetry Shield C18色谱柱(250 mm × 4.6 mm,5 μm),柱温30 ℃;检测波长为320 nm(0 ~ 25 min测定滨蒿内酯、3,5-O-二咖啡酰奎宁酸、4,5-O-二咖啡酰奎宁酸和2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷)[7-11]和284 nm(25 ~ 65 min测定决明子苷B2、红镰霉素-6-O-β-龙胆二糖苷、决明子苷C、橙黄决明素和美决明子素)[12-14];流动相为乙腈-0.1%甲酸,进行线性梯度洗脱(0 ~ 10 min,13.0%乙腈;10 ~ 19 min,13.0% → 26.0%乙腈;19 ~ 25 min,26.0% → 50.0%乙腈;25 ~ 55 min,50.0% → 61.0%乙腈;55 ~ 65 min,61.0% → 13.0%乙腈),流速1.0 mL·min-1,进样量10 μL。理论塔板数按内参物峰计≥5500。
2.3 专属性考察
取“2.1”项下混合对照品溶液及供试品溶液在“2.2”项下色谱条件下进样检测,记录色谱图(图1)。结果显示决明降脂片样品溶液中9种成分与相邻色谱峰的分离度均≥1.5;阴性样品不干扰各成分检测。
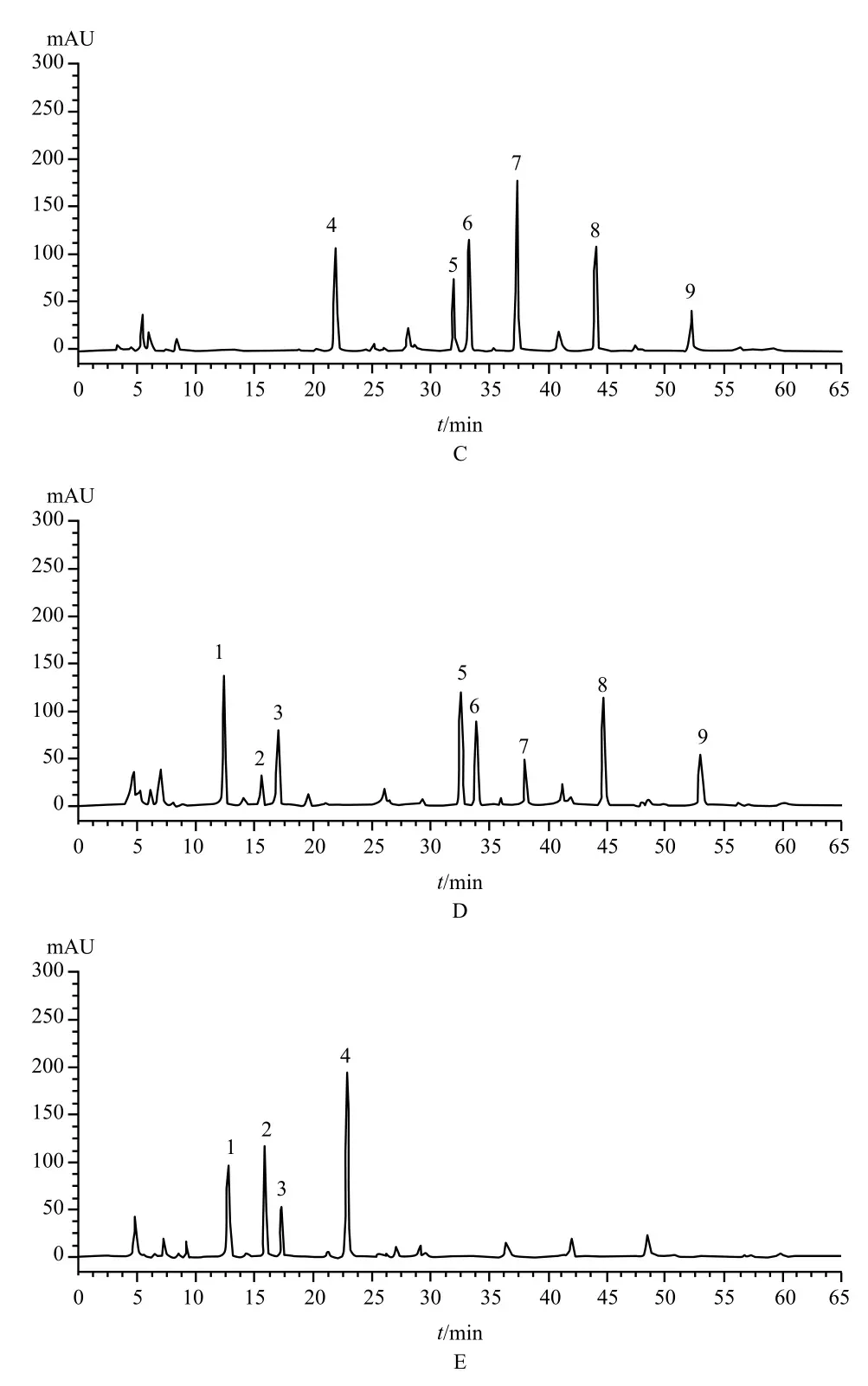
图1 HPLC色谱图Fig 1 HPLC chromatogram
2.4 方法学考察
2.4.1 线性关系 精密吸取“2.1”项下混合对照品贮备液,用80%甲醇分别稀释一定倍数制得6个混合对照品溶液,依法进样,以9种成分质量浓度和峰面积进行线性回归,计算得出9种成分的回归方程和线性范围,见表1。

表1 决明降脂片中9种成分的线性关系考察结果Tab 1 Linearity results of nine components in Jueming Jiangzhi tablets
2.4.2 精密度、重复性和稳定性 取决明降脂片(S1)溶液在“2.2”项下色谱条件连续进样6次,得9种成分峰面积的RSD依次为1.01%、1.34%、1.39%、0.77%、0.84%、0.58%、0.91%、1.26%、1.53%,表明仪器精密度良好。取决明降脂片(S1)适量,制备供试品溶液6份,在色谱条件下进样检测分析,并计算含量,得9种成分含量的RSD依次为1.47%、1.62%、1.70%、1.34%、1.46%、0.98%、1.56%、1.75%、1.92%,表明方法重复性良好。取上述进行重复性试验的任一份决明降脂片溶液,在色谱条件下于制备后0、2、4、8、15、24 h进样分析,得9种成分峰面积的RSD依次为0.98%、1.36%、1.44%、0.80%、0.79%、0.56%、0.93%、1.31%、1.49%,表明决明降脂片供试品溶液在24 h内稳定。
2.4.3 加样回收率 取已知待测成分含量并去除糖衣的决明降脂片(S1),研细,取细粉9份,每份0.25 g,精密称定后均分成3组,精密加入混合对照品溶液(9种成分质量浓度分别为0.461、0.239、0.155、0.659、0.397、0.914、0.332、0.199、0.103 mg·mL-1)0.8、1.0、1.2 mL,再依法制成加样样品溶液。依法检测,9种成分的平均加样回收率及RSD分别为99.55%(1.12%)、98.28%(1.35%)、97.82%(1.56%)、100.10%(0.79%)、98.67%(0.90%)、100.06%(0.58%)、97.33%(1.08%)、96.96%(1.32%)、97.86%(1.15%)。
2.4.4 相对校正因子(ƒ)的计算 依法进样“2.4.1”项下6个混合对照品溶液,用对照品质量浓度与峰面积之比计算各成分ƒ,即ƒk/s= ƒk/ƒs=(Wk/Ak)/(Ws/As)=(WkAs)/(WsAk)(其中W和A分别代表质量浓度和峰面积,k和s分别代表内参物和其他待测成分)。以2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷为内参物,分别计算其它8种成分与之的平均ƒ及RSD分别为0.781 2(0.56%)、1.247 9(1.89%)、2.124 2(1.60%)、0.841 6(1.46%)、0.721 3(0.96%)、0.898 1(0.78%)、1.685 9(1.37%)、2.883 7(0.44%)。
2.4.5 ƒ耐用性考察 取“2.1”项下混合对照品溶液进样检测,分别考察仪器(UltiMate 3000型和Waters 2695型高效液相色谱仪)和色谱柱(Symmetry Shield C18、Welc Xtimate C18和Unitary C18)、流速(1.0±0.2)mL·min-1、柱温(30±5)℃对ƒ的影响,结果显示不同仪器与色谱柱下平均ƒ及RSD分别为0.785 8(0.64%)、1.242 9(1.91%)、2.120 8(1.84%)、0.842 2(1.56%)、0.721 9(1.34%)、0.893 0(1.49%)、1.682 1(1.40%)、2.879 4(0.59%);不同流速时平均ƒ及RSD分别为0.775 4(1.18%)、1.242 6(1.90%)、2.122 7(1.74%)、0.845 3(1.58%)、0.715 9(1.25%)、0.895 6(0.82%)、1.686 6(1.66%)、2.881 0(0.68%);不同柱温下平均ƒ及RSD分别为0.783 6(0.69%)、1.241 6(1.93%)、2.129 5(1.45%)、0.847 6(1.40%)、0.726 2(1.10%)、0.903 0(1.06%)、1.685 8(1.48%)、2.885 7(0.63%)。
2.5 含量测定
取15批决明降脂片(S1 ~ S15),依法制备决明降脂片供试品溶液,再依法进样分析,分别运用外标法(external standard method,ESM)和一测多评法(quantitative analysis of multi-components by single marker method,QAMS)计算决明降脂片中各成分的含量,并比较两种方法检测结果的差异(表2)。结果显示两种方法无显著性差异(P> 0.05)。
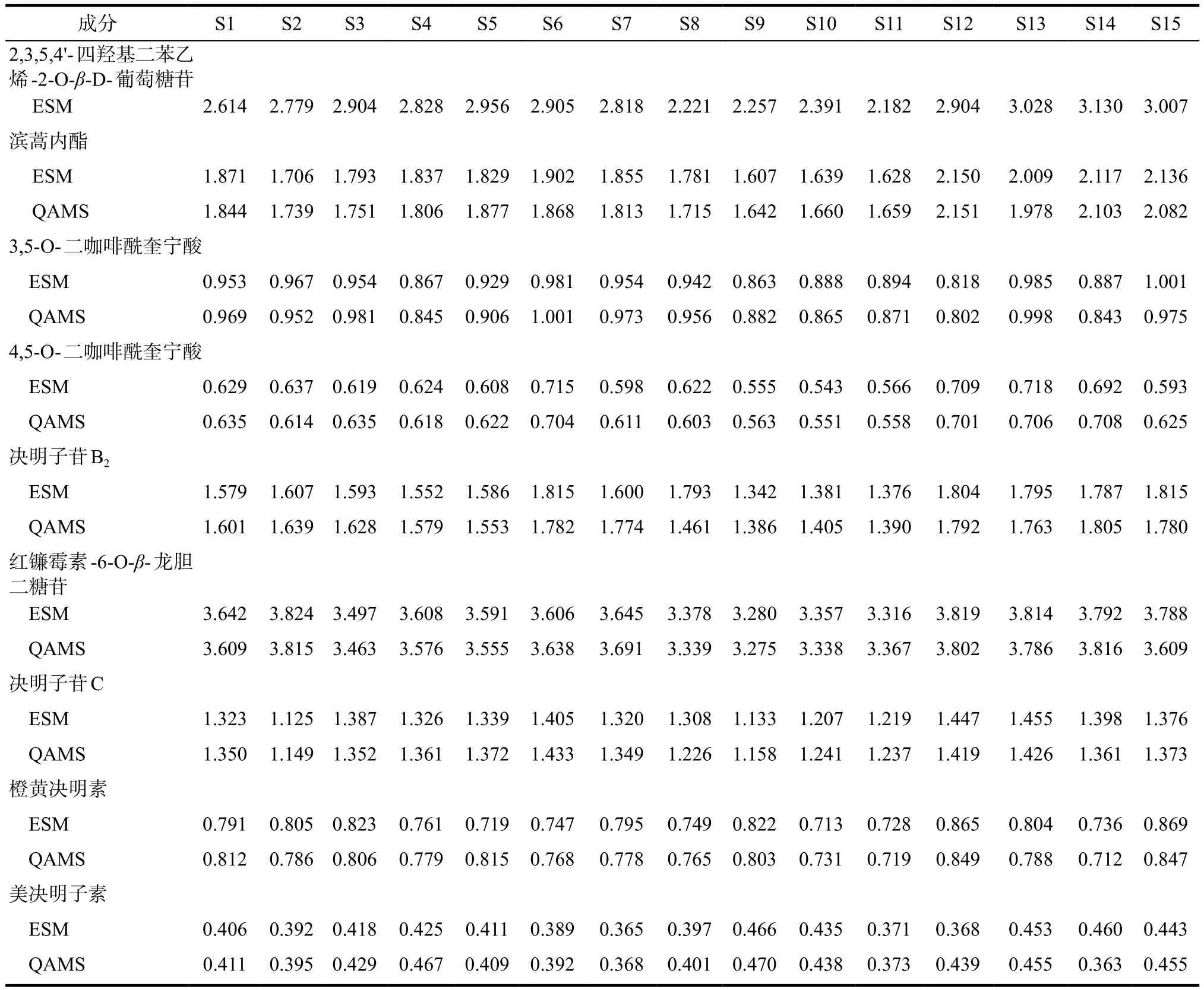
表2 含量测定结果. mg·g-1,n = 3Tab 2 Results of content determination. mg·g-1, n = 3
2.6 化学计量学质量分析
将表2中QAMS法数据导入SPSS 26.0统计软件中进行聚类分析和主成分分析。聚类分析结果显示15批决明降脂片聚为3类,同一厂家的产品聚为一类。主成分分析结果显示前3个主成分代表决明降脂片85.55%的质量信息。表明同一生产企业所生产的决明降脂片产品质量相对稳定,不同生产企业间决明降脂片产品质量有差异,中药复方制剂产品质量受原药材种属、产地、原药材内控标准以及各生产企业制剂生产所用设备、质控参数等影响。
3 讨论
3.1 指标成分及内参物的选择
决明降脂片由茵陈、何首乌、决明子和桑寄生等加工而成,方中茵陈清利湿热、利胆退黄,决明子清热明目、润肠通便,合为君药;何首乌解毒消痈、润肠通便,桑寄生补肝肾、强筋骨为臣药。本试验以茵陈、决明子、何首乌为研究对象,选择9种成分为指标,采用HPLC-QAMS法进行定量分析。选取质稳价廉、出峰时间适中且含量较高的2,3,5,4'-四羟基二苯乙烯-2-O-β-D-葡萄糖苷为内参物。
3.2 提取方式的选择
本试验在选择供试品提取方式时,首先以甲醇[9-11]和乙醇[13]为溶剂,超声提取后检测,结果以甲醇为溶剂时,9种成分的提取率较高,进而考察了超声[7-9]和加热回流[14],提取时间:50、60和70 min,同时摸索了甲醇溶液的浓度(50%[7]、80%[11]和100%[8-10]),结果显示80%甲醇为溶剂时,超声提取效果最好,提取60、70 min时,提取效果无显著差异,综合上述条件,选取80%甲醇超声提取60 min为供试品提取方式。
综上,本试验采用HPLC-QAMS法对决明降脂片中9种成分含量进行同时测定,建立了决明降脂片多指标成分质控模式,同时对3个厂家15批决明降脂片运用化学计量学进行分析,发掘复杂数据中潜在的规律。所建立的方法简单易行,准确可靠,为决明降脂片质量标准的提高提供了参考依据。
