基于治疗药物监测的老年患者替考拉宁血药浓度及疗效分析
2022-05-12周广青郭思维严建业湖南中医药大学科技创新中心湖南长沙41008长沙市第三医院药学部湖南长沙410015湖南中医药大学药学院湖南长沙41008
周广青,李 昕,郭思维,叶 超,严建业(1.湖南中医药大学科技创新中心,湖南 长沙 41008;.长沙市第三医院药学部,湖南 长沙 410015;3.湖南中医药大学药学院,湖南 长沙 41008)
替考拉宁为糖肽类抗生素,结构与万古霉素相似[1]。临床上主要用于治疗耐甲氧西林金黄色葡萄球菌、耐甲氧西林表皮葡萄球菌和肠球菌属等革兰阳性菌所致皮肤软组织、呼吸道、泌尿道和血液感染等。替考拉宁的消除半衰期较长,可达70 ~ 100 h,达到稳态浓度需要较长时间。由于老年患者生理功能的减退及病情变化的复杂性,药物在体内的代谢与年轻人间有较大的差异。国外研究[2]发现,老年患者替考拉宁个体间和个体内药代动力学参数也有较大的差异。目前国内有关替考拉宁相关研究所针对人群主要为成年重症感染患者,针对老年患者的研究不多。本文对老年感染患者替考拉宁治疗药物监测(therapeutic drug monitoring,TDM)结果进行回顾性分析,以期为老年患者合理使用替考拉宁提供参考。
1 资料与方法
1.1 研究对象
采用回顾性分析方法,收集我院82例使用注射用替考拉宁进行抗感染治疗的老年住院患者信息。纳入标准:①年龄≥65岁;②确诊或疑似革兰阳性菌感染,需要使用替考拉宁;③治疗期间能够监测替考拉宁血药浓度。排除标准:①疗程≤2 d;②局部给药;③治疗前后未监测实验室炎症指标;④进行血液透析治疗。本研究征得医院伦理委员会同意(批件号:CS3-KY-2021EC-026)。
1.2 TDM方法
采用二维高效液相色谱法[3]测定患者血浆中替考拉宁的浓度。实验所需的色谱柱及流动相如下:一维色谱柱为Aston SX3柱(4.6 mm×50 mm,5 μm),流动相为甲醇-60 mmol·L-1磷酸二氢铵(1∶4,v/v,pH =4.80),流速1.2 mL·min-1;二维色谱柱为Cholester waters柱(4.6 mm×250 mm,5 μm),流动相为甲醇-60 mmol·L-1磷酸二氢铵(2∶3,v/v),流速1.0 mL·min-1;中间柱为ASTON PLI柱 (4.6 mm×10 mm,3 μm)。检测波长282 nm,温度40 ℃。标准曲线范围为0.50 ~150.00 mg·L-1(r= 0.999 7),样品萃取回收率为78.0% ~88.0%,日内和日间精密度分别低于2.0%和6.0%。
1.3 给药及血样采集
临床医师根据药品说明书、患者的具体病情、给药前肾功能情况确定给药方案(负荷剂量6 mg·kg-1,q 12 h;维持剂量6 mg·kg-1,qd)。患者于第3、4天给药前30 min抽取静脉血2 ~ 3 mL测定谷浓度,采血管为肝素钠抗凝管,采血部位为给药对侧手臂。
1.4 疗效和不良反应评价
根据《抗菌药物临床试验技术指导原则》[4]对患者进行临床疗效评价:①有效:停药后患者症状、体征消失或完全恢复,实验室检查恢复正常;②无效:停药后患者症状、体征持续或不完全消失甚至恶化,或者出现了新的症状、体征和(或)使用了新的抗菌治疗措施。
不良反应关联性评价根据《药品不良反应报告和监测管理办法》,并采用万古霉素肾毒性定义对替考拉宁肾毒性进行判定[5-6],替考拉宁治疗期间血肌酐水平较用药前基线水平上升≥50%或肌酐清除率较用药前基线水平下降> 50%则为产生肾毒性。
1.5 统计学处理
数据应用SPSS 23.0软件处理,计量资料以中位数和四分位数间距表示,计数资料用“%”表示;治疗前后炎症指标比较采用配对样本秩和检验,组间差异采用χ2检验,相关性采用双变量相关分析。
2 结果
2.1 患者一般情况
共82例老年患者使用替考拉宁并接受了TDM,患者年龄83(80,87)岁,体重60(50,60)kg。血药谷浓度2.04 ~ 26.88 mg·L-1,中位数为9.34(6.88,12.39)mg·L-1。其中38例患者谷浓度≥10 mg·L-1,达标率46.34%。所有患者进行了病原学检测,送检标本包括血液、痰液、尿液、分泌物、导管尖;32例(39.02%)患者检测结果提示革兰阳性菌感染,行目标针对性治疗,其余行经验性治疗。患者一般情况见表1。

表1 患者一般情况Tab 1 General information of patients
2.2 血药浓度达标情况和影响因素
2.2.1 年龄 以10岁为年龄段间隔,分成三组,比较三组间血药浓度达标情况。结果显示65 ~ 74岁组血药浓度达标率为71.43%(5/7);75 ~ 84岁组血药浓度达标率为42.86%(18/42);≥85岁组血药浓度达标率为45.45%(15/33)。组间差异无统计学意义(χ2=1.920,P> 0.05)。
2.2.2 负荷给药方案 82例患者中有65例患者予负荷给药,其中33例(50.77%)谷浓度达标;17例患者没有进行负荷给药,仅5例(29.41%)谷浓度达标。但两组间血药浓度达标情况差异无统计学意义(χ2=2.472,P> 0.05)。
2.2.3 肾功能 将82例患者按照肌酐清除率(CrCl)不同进行分组,分别为CrCl > 60 mL·min-1,CrCl 30 ~60 mL·min-1,CrCl < 30 mL·min-1。结果显示CrCl >60 mL·min-1组血药浓度达标率为36.00%(9/25);CrCl 30 ~ 60 mL·min-1组血药浓度达标率为33.33%(9/27);CrCl < 30 mL·min-1组血药浓度达标率为66.67%(20/30)。经检验不同肾功能的患者之间,血药浓度达标率存在统计学差异(χ2= 7.897,P< 0.05)。重度肾功能不全组(CrCl < 30 mL·min-1)达标率较高。
2.2.4 浓度相关性分析 分别以血药谷浓度和性别、年龄、体重、首日剂量、次日剂量、CrCl以及血清白蛋白等进行双变量相关性分析,结果显示谷浓度与首日剂量、次日剂量及CrCl具有显著相关性(P< 0.05)。研究未发现谷浓度与性别、年龄、体重及血清白蛋白具有相关性(P> 0.05)。
2.3 临床疗效
2.3.1 有效率 谷浓度≥ 10 mg·L-1组,治疗有效23例(23/38,60.53%);谷浓度< 10 mg·L-1组,治疗有效21例(21/44,47.73%)。两组患者治疗有效率之间无显著性差异(χ2= 1.343,P> 0.05)。
2.3.2 治疗前后炎症指标比较 在替考拉宁治疗前后监测患者炎症指标,包括WBC、N%、PCT。结果显示谷浓度达标组患者治疗前后炎症指标变化差异有统计学意义(P< 0.05),见表2。谷浓度未达标组患者治疗前后指标WBC、PCT变化有统计学意义(P<0.05),指标N%变化无统计学意义(P> 0.05)。
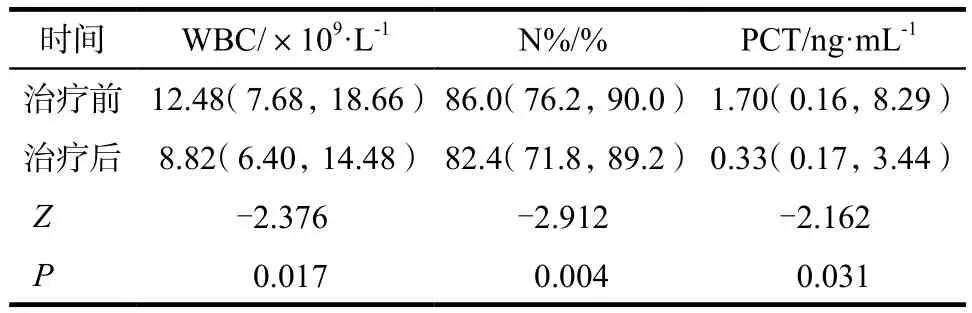
表2 浓度达标组替考拉宁治疗前后炎症指标情况Tab 2 Inflammatory indexes of the standard concentration group before and after teicoplanin treatment
2.4 不良反应
查阅所有患者病历记录以及我院不良反应上报系统,未见患者在治疗期间发生替考拉宁相关不良反应。逐一查阅治疗期间患者血肌酐水平,未见肾损害情况发生。
3 讨论
对于多数革兰阳性菌所致感染,指南推荐替考拉宁谷浓度≥10 mg·L-1即可[7-9]。本研究以谷浓度≥10 mg·L-1为目标,发现年龄65岁以上老年患者使用替考拉宁血药浓度达标率为46.34%,与以往研究[10]结果相近,该研究中113例老年患者替考拉宁血药浓度达标率为34.58%。一项针对儿童患者的研究[11]认为替考拉宁谷浓度可能与性别、年龄、体重和血肌酐有关。也有研究[12]认为,与常规剂量(负荷剂量400 mg,q 12 h,给药三次后采用维持剂量400 mg,qd)相比,高剂量组(负荷剂量800 mg,q 12 h,给药三次后采用维持剂量800 mg,qd)患者体重对药物谷浓度有显著影响。尽管研究条件各异,但有更多研究认为剂量和肌酐清除率对谷浓度存在影响,有研究[13]发现前3日平均给药剂量、尿素氮、肌酐清除率以及联用抗休克血管活性药物是影响替考拉宁谷浓度达标的重要因素;Wang等[14]研究认为替考拉宁谷浓度受剂量和肌酐清除率强烈影响,这与本研究结果相似。因此建议临床医生在替考拉宁实际应用中应特别注意给药剂量和患者肌酐清除率,在前2日给予足够的负荷剂量,之后制定个体化维持剂量,并尽可能进行TDM。另外,替考拉宁蛋白结合率较高,理论上其血药浓度应受血清白蛋白水平影响,但研究未发现谷浓度与血清白蛋白具有相关性,原因尚不明确,并且国内外文献也存在类似研究结果[15-16]。
本研究中血药浓度达标患者的临床有效率为60.53%,与以往文献[17]报道接近。但血药浓度达标与未达标的患者之间比较无明显差异,推测这与高龄老年患者人数偏多,患者营养和免疫状态较差,预后不好有关;或许谷浓度≥10 mg·L-1只能作为临床早期治疗反应指标,并不能完全反映最终临床结局。有少量关于耐甲氧西林金黄色葡萄球菌(methicillinresistantStaphylococcus aureus,MRSA)感染与替考拉宁药动学/药效学参数的体内外研究[17-19],研究结果认为药-时曲线/最小抑菌浓度下的面积指标可以有效评估抗MRSA疗效。但其是否能够替代谷浓度≥10 mg·L-1进一步评估替考拉宁临床抗菌疗效,需要更多研究去证实。
本研究中未见替考拉宁相关肾毒性的发生,可见替考拉宁临床应用相对安全。国外文献报道[20-21]替考拉宁中毒谷浓度上限为60 mg·L-1,本研究观察到患者最高谷浓度为26.88 mg·L-1,可能为实际临床用药较安全的原因之一。
综上所述,替考拉宁临床用药应特别注意在给药的前2日给予足够的负荷剂量,以尽快达到有效谷浓度;注意肌酐清除率对浓度的影响,以适当调整剂量使谷浓度维持在有效安全范围。通过TDM的有效手段,可为具有特殊生理病理状态的老年患者抗菌药物个体化用药提供服务和保障,为抗菌药物临床研究提供参考。
