基于系统药理学探讨莪术醇调控铁死亡和细胞自噬的作用机制
2022-05-12王佳慧何文星黄茹君何佳禧黎小清
王佳慧,何文星,黄茹君,何佳禧,黎小清,郑 洋,汪 磊
莪术是姜科植物蓬莪术(CurcumaphaeocaulisVal),广西莪术(C.kwangsiensisS.G.Leeet.C.F.Liang)的干燥根茎,具有行气破血、消积止痛之功,对胁痛等有效果[1]。莪术醇是莪术的主要活性成分,具有抑制肿瘤细胞增殖、抗炎等作用[2]。目前对莪术醇的研究主要集中在癌症以及慢性肝病领域。铁超载和脂质过氧化被认为是铁死亡的中心环节[3]。有研究[4]表明,诱导肝星状细胞发生铁死亡,可以有效阻止肝纤维化的发展。细胞自噬是通过溶酶体降解自身组分以维持稳态的过程。细胞自噬对肝纤维化的调控是双向的[5]。细胞自噬通过调节肝星状细胞的脂质代谢促进肝纤维化的发展;另一方面,细胞自噬通过调控肝细胞在肝脏炎症和肝脏代谢稳态等细胞功能抑制肝纤维化的发展[6]。铁死亡和细胞自噬在肝纤维化的发展中均发挥了重要作用,为了探究莪术醇和铁死亡与细胞自噬之间的关系。该研究使用系统药理学的方法对莪术醇调控铁死亡和细胞自噬的分子机制进行探讨。
1 材料与方法
1.1 莪术醇化学成分靶点预测本研究使用中药系统药理学分析平台(TCMSP)(http:ibts.hkbu.edu.hk/LSP/tcmsp.php)收集莪术醇药效成分信息,保存为mol2格式文件,然后将其上传PharmMapper(http://www.lilab-ecust.cn/pharmmapper/)。基于反向药效团匹配法,选择药物的药效团模型, 设置最终产生300个蛋白构象,得到与化合物相关的靶点名称、基因名称、Uniprot ID等结果。借助Uniprot(https://www.uniprot.org/),对化合物预测产生的靶点进行筛检,只保留物种为“Homo sapiens”的靶点。
1.2 铁死亡和细胞自噬相关靶点的获取铁死亡相关靶点是在FerrDb数据库(http://www.zhounan.org/ferrdb)中获取的,细胞自噬相关靶点在HAMdb(http://hamdb.scbdd.com/)数据库中检索获取,从而构建相应数据库。
1.3 网络的构建采用Venny2.1对莪术醇作用靶点与铁死亡相关靶点;以及与细胞自噬相关靶点进行交互处理,同时采用Venny2.1对三者共同靶点进行交互处理,而后借助蛋白互作String数据库获取相关靶点互作信息,使用Cytoscape3.6.0将互作靶点进行可视化处理。
1.4 生物信息学分析使用基因本体论(GO)注释数据库网站(http://www.geneontology.org),京都基因与基因组百科全书(KEGG)路径富集分析(http://www.genome.jp/kegg/)对这些靶点进行可视化和生物信息学分析。
2 结果
2.1 莪术醇作用靶点以及铁死亡和细胞自噬相关靶点的确定使用Pubchem数据库确认了莪术醇的结构,通过PharmMapper数据库获得了莪术醇的作用靶点300个,借助Uniprot数据库,对化合物预测产生的靶点进行筛检与检查,剔除重复、非人源与不规范的靶点,最终只得到了152个靶点。在FerrDb数据库中选取抑制和促进铁死亡以及其标志物,去除三者重复的靶点,最终获得与铁死亡关系密切的靶点259个,在HAMdb数据库中获取了与细胞自噬关系密切的靶点796个。
2.2 关键靶点的网络构建与分析对莪术醇作用靶点和铁死亡靶点进行交互处理,得到14个共同靶点,分别是MAPK8、AKR1C2、ALB、MAPK1、MAPK14、DPP4、NOS2、AKR1C3、AKR1C1、PTGS2、SRC、HNF4A、NQO1、ALOX15;莪术醇与细胞自噬靶点交互处理得到21个靶点,分别是MAPK8、MAPK10、KDR、ALB、MAPK14、IGF1R、FKBP1A、MAPK1、HSP90AA1、PPARG、CTSB、CHEK1、PKM、NOS3、IRGM、PDPK1、GSK3B、NQO1、PRKCD、CAMKK2、NOS2;莪术醇与细胞自噬和铁死亡共同重复靶点6个,分别是MAPK8、ALB、MAPK14、MAPK1、NOS2、NQO1,如图1A所示。
莪术醇抗铁死亡的14个靶点,借助String数据库获取其相互作用数据,导入Cytoscape3.6.0进行可视化(如图1B所示),其中度值排名前5的分别是PTGS2、ALB、MAPK1、MAPK8、MAPK14,说明这些靶点是关键靶点在这个调控网络中发挥重要的作用,图中节点的大小反映了度值的大小。
莪术醇抗细胞自噬的21个靶点,借助String数据库获取其相互作用数据,只获得了19个靶点相互作用的数据,导入Cytoscape3.6.0进行可视化(如图1C所示),其中度值排名前5的分别是HSP90AA1、MAPK1、MAPK8、ALB、NOS3,说明这些靶点是关键靶点在这个调控网络中发挥重要的作用,图中节点的大小反映了度值的大小。
莪术醇与铁死亡和细胞自噬重复靶点6个,借助String数据库获取其相互作用数据,导入Cytoscape3.6.0进行可视化(如图1D所示),其中度值排名前3的分别是MAPK1、MAPK8、ALB,说明这些靶点是莪术醇调控铁死亡以及细胞自噬的关键靶点,也反映了铁死亡和细胞自噬之间的关系密切,图中节点的大小反映了度值的大小。
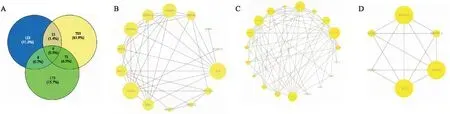
图1 莪术醇调控铁死亡和细胞自噬相关靶点A:莪术醇作用靶点与铁死亡以及细胞自噬相关靶点交互;B:莪术醇调控铁死亡靶点互作网络;C:莪术醇调控细胞自噬相关靶点互作网络;D:莪术醇与铁死亡和细胞自噬重复靶点互作网络
2.3 关键靶点途径和功能的富集分析从莪术醇作用的152个靶点中收集到14个调控铁死亡的靶点,为了确定相关的途径和功能,对这些可能的靶点按照P<0.01进行了通路富集和GO功能分析。这些靶点的生物过程、分子功能以及细胞组分分别是对刺激的反应、代谢过程、生物调节过程;细胞因子活力、抗氧化的能力、转录调节活力;主要位于细胞器和细胞膜上,富集途径主要包括血管内皮生长因子(vascular endothelial growth factor,VEGF)信号通路、花生四烯酸代谢通路、白细胞介素17(interleukin 17, IL-17)信号通路、肿瘤坏死因子(tumor necrosis factor,TNF)信号通路等,具体见图2。
从莪术醇作用的152个靶点中收集到21个调控细胞自噬的靶点,为了确定相关的途径和功能,对这些可能的靶点按照P<0.01进行了通路富集和GO功能分析。这些靶点的生物过程、分子功能以及细胞组分分别是细胞增殖、生长、免疫过程;结合、抗氧化的能力、转录调节活力;主要位于细胞器和细胞外,富集途径主要包括NOD样受体信号通路、自噬通路、FoxO信号通路、PI3K-Akt信号通路等,具体见图3。
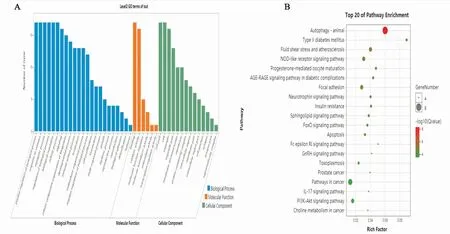
图3 莪术醇调控细胞自噬相关靶点功能富集分析A:莪术醇调控细胞自噬靶点的GO分析;B:莪术醇调控细胞自噬靶点通路分析
从莪术醇作用的152个靶点中收集到了6个与细胞自噬和铁死亡重复的靶点,为了确定相关的途径和功能,笔者对这些可能的靶点按照P<0.01进行了通路富集和GO功能分析。这些靶点的生物过程、分子功能以及细胞组分分别是生物过程的负调控、抗氧化的能力、主要位于细胞器,富集途径主要包括ErbB信号通路、GnRH信号通路、HIF-1信号通路等,具体见图4。
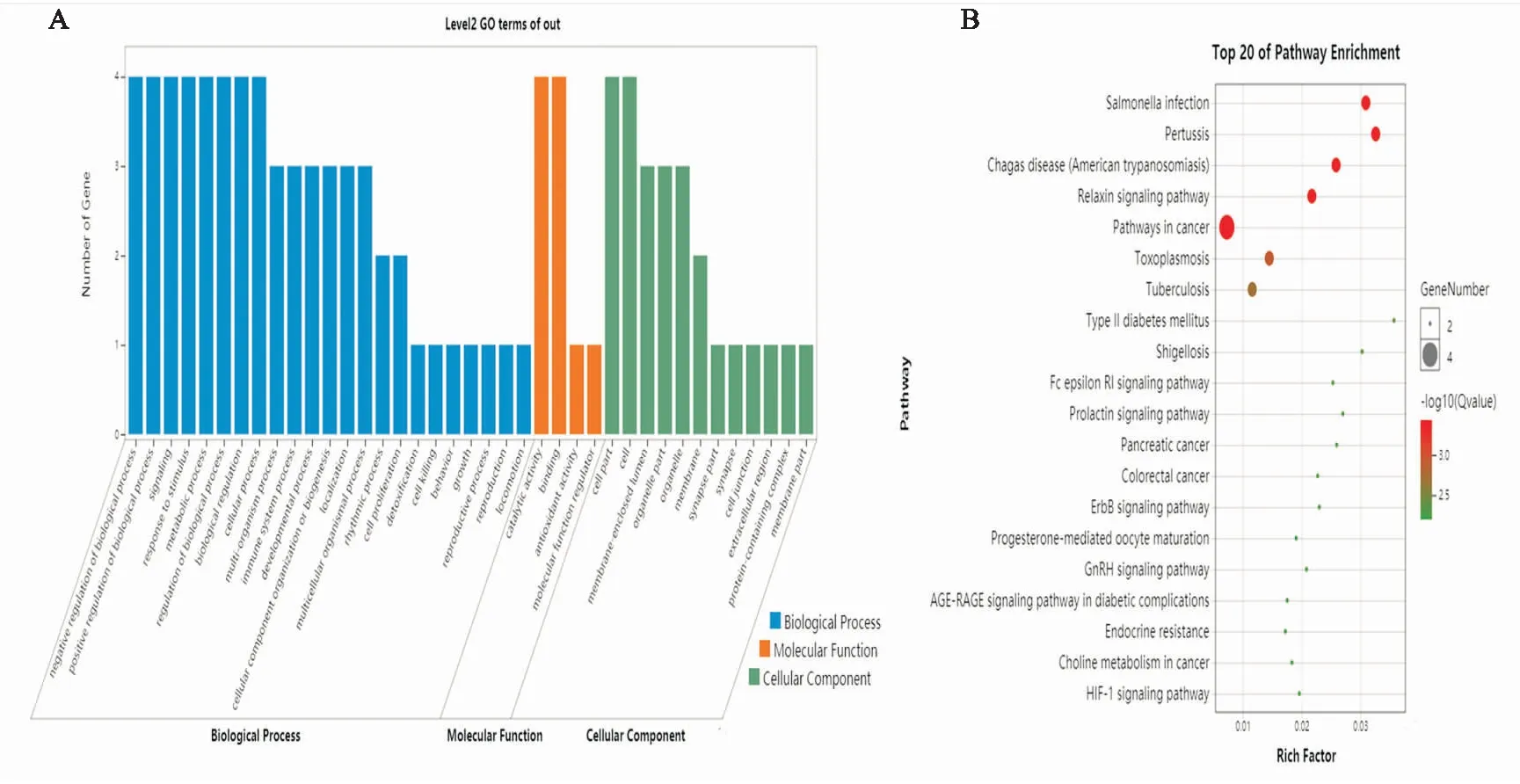
图4 莪术醇与铁死亡和细胞自噬重复靶点功能富集分析A:莪术醇与铁死亡和细胞自噬重复靶点的GO分析;B:莪术醇与铁死亡和细胞自噬重复靶点的通路分析
3 讨论
铁死亡是谷胱甘肽过氧化物酶4的含量下降,导致细胞氧化还原平衡被打破,引起脂质过氧化物积累,从而诱发细胞死亡的一种类型。细胞自噬主要由双层膜结构包裹衰老或受损的细胞器、蛋白质、病原微生物等形成自噬溶酶体,然后利用溶酶体中的各种水解酶降解所包裹的内容物,为细胞提供物质与能量来源,是细胞针对内外环境变化的重要调节机制[7]。近年来细胞自噬与铁死亡之间的调控关系受到广大科研工作者的关注,对两者之间的关系目前主要有三种观点:相互促进,双氢青蒿素通过促进铁蛋白自噬,增加ROS活性氧积累,诱导急性髓细胞性白血病细胞铁死亡,同时抑制自噬可以抑制细胞铁死亡的发生[8];相互独立,有研究显示西拉米辛和拉帕替尼联用既可以诱导乳腺癌细胞发生铁死亡,也可诱导细胞发生自噬性死亡,但两种死亡方式发生顺序不同,提示铁死亡过程与自噬过程独立发生作用[9];相互拮抗,抑制胶质母细胞瘤干细胞自噬活性可以诱导铁死亡发生,并且增加了其对替莫唑胺的敏感性,提示自噬和铁死亡之间存在拮抗关系[10]。
本研究通过系统药理学的研究方法,对莪术醇调控两种生理过程的可能机制进行了探究。结果表明,莪术醇可以通过PTGS2、ALB、MAPK1、MAPK8、MAPK14等靶点发挥调控铁死亡的作用,这些靶点的功能主要集中在调控细胞增殖、抗氧化活性、转录活性,靶点的途径主要集中在VEGF信号通路、TNF信号通路、缺氧诱导因子-1(hypoxia-inducible factor-1,HIF-1)信号通路,这些结果表明莪术醇很有可能是调控炎症反应以及血管新生等过程影响铁死亡的发生发展。莪术醇可以通过HSP90AA1、MAPK1、MAPK8、ALB、NOS3等靶点发挥调控细胞自噬的作用,这些靶点的功能主要集中在调控细胞增殖、抗氧化活性、转录活性,靶点的途径主要集中NOD样受体信号通路、FoxO信号通路、PI3K-Akt信号通路,PI3K-Akt以及FoxO信号通路都是调控细胞增殖、凋亡、生长的上游信号[11]。莪术醇可以通过ALB、MAPK1、MAPK8等靶点发挥调控铁死亡和细胞自噬的作用,这些靶点的功能主要集中在调控细胞增殖、抗氧化活性,靶点的途径主要集中在HIF-1信号通路,莪术醇调控铁死亡和细胞自噬与HIF-1、VEGF信号通路以及HSP90AA1、NOS3等靶点关系密切,而这些靶点和通路与血管新生关系密切。说明铁死亡和细胞自噬是可以调控血管新生的过程,本研究将为莪术醇在慢性肝病的研究领域开拓新的视角,进一步推动广西道地药材莪术的开发与利用。铁死亡和细胞自噬之间关系密切,但是具体的调控机制需要基础实验进一步验证。
综上,本研究显示莪术醇通过PTGS2、ALB、MAPK1等靶点发挥调控铁死亡的作用,也可以通过HSP90AA1、MAPK1、MAPK8等靶点发挥调控细胞自噬的作用,表明莪术醇可能通过调控铁死亡和细胞自噬发挥药理作用。
