还原敏感接枝型两亲性聚氨酯的合成及其胶束性能研究*
2022-05-11陶旺旺刘静怡陈红祥赵祖伊
陶旺旺 周 瑜 刘静怡 陈红祥 赵祖伊
(武汉科技大学化学与化工学院煤转化与新型炭材料湖北省重点实验室 湖北武汉 430081)
两亲性聚氨酯具有良好的生物相容性、生物降解性和结构易裁剪性,在水中还可自组装形成纳米胶束,因此在药物载体领域得到广泛研究[1-3]。目前用作药物载体的两亲性聚氨酯以线型结构居多,其自组装时主要通过各疏水链段的物理相互作用聚集成核形成胶束,作用力有限,故注射到血液后其胶束结构易遭破坏,从而出现所载药物的早释[4]。研究表明,胶束结构的稳定性与聚合物的拓扑结构密切相关[5-6]。接枝型两亲性聚合物中亲水和疏水链段相对集中,因此形成胶束的内核较紧密,使得其在剪切和稀释作用下比线型聚合物更稳定[7-8]。如Bláhová等[9]研究发现接枝型两亲性聚合物胶束具有良好的储存稳定性,且无早释现象。
除在血液中应具有良好的稳定性外,载药体系在病灶部位能及时释放药物也是衡量其性能的一个重要指标。本研究利用肿瘤细胞内谷胱甘肽(GSH)浓度较高和双硫键可在GSH作用下被还原的特点[10],将双硫键引入聚合物,合成了一种具有还原敏感性的接枝型两亲性聚氨酯(PUSS-g-mPEG),并对其性能进行了研究。
1 实验部分
1.1 原料和试剂
聚己内酯二醇(PCL,Mn=2 000)、聚乙二醇单甲醚(mPEG,Mn=1 000)、六亚甲基二异氰酸酯(HDI)、3-巯基丙酸、二苯甲酮(BP)、二环己基碳二亚胺(DCC)、4-二甲氨基吡啶(DMAP)、2,2-二硫二乙醇、谷胱甘肽(GSH)、1,4-丁烯二醇,分析纯,上海阿拉丁生化科技股份有限公司,其中PCL使用前需除水;盐酸阿霉素(DOX·HCl),分析纯,武汉市澳康达生物科技有限公司;三乙胺(TEA)、N,N-二甲基乙酰胺(DMAc)、四氢呋喃(THF),分析纯,国药集团化学试剂有限公司,其中DMAc和THF使用前需除水;牛血清白蛋白(BSA),生物试剂,上海金穗生物科技有限公司。
1.2 测试与表征
核磁共振氢谱(1H-NMR):采用安捷伦科技(中国)有限公司的DD2-600MHz型核磁共振仪,溶剂为氘代氯仿,四甲基硅烷为内标。
荧光光谱:采用珀金埃尔默仪器(上海)有限公司的LS55型荧光光谱仪。芘做荧光探针时,激发波长为300~350 nm,发射波长为394 nm,激发与发射狭缝宽度分别为5 nm;测量DOX时,发射波长为500~800 nm,激发波长为478 nm,激发与发射狭缝宽度分别为10 nm。
凝胶渗透色谱(GPC):采用安捷伦科技(中国)有限公司PL-GPC50型凝胶色谱仪,温度30℃,流速1 mL/min,溶剂为THF,标样为单分散聚苯乙烯。
胶束粒径及其电位:采用美国 Particle Sizing Systems(PSS)粒度仪公司的Nicomp 380 ZLS型动态光散射仪(DLS),散射角为90°。
1.3 PUSS-g-mPEG的合成
以 PCL、1,4-丁烯二醇、2,2-二硫二乙醇和 HDI为原料,通过预聚法合成主链含有碳碳双键和二硫键的聚氨酯 (PUSS-ene)。将PUSS-ene与3-巯基丙酸发生巯基-烯反应得到含羧酸侧基的聚氨酯(PUSS-COOH)后,再与mPEG发生酯化反应,合成具有还原敏感性的接枝型聚氨酯PUSS-g-mPEG。
1.3.1 PUSS-ene的合成
12.00 g PCL溶于5 mL DMAc后,加入4.27 g HDI,80 ℃下反应2 h。 再加入0.24 g 2,2-二硫二乙醇反应1 h后,继续加入1.59 g 1,4-丁烯二醇,反应11 h。结束后,经透析、干燥得到白色蜡状产物,即为PUSS-ene(产率为81.4%)。
1.3.2 PUSS-COOH的合成
将4.36 g PUSS-ene和2.77 g 3-巯基丙酸溶于DMAc后,再加入0.10 g二苯甲酮。在常温搅拌条件下,使用紫外灯(波长为365 nm)照射6 h。结束后,经透析、干燥得到浅黄色蜡状物,即为 PUSSCOOH(产率为86.2%)。
1.3.3 PUSS-g-mPEG的合成
将3.10 g PUSS-COOH、5.24 g mPEG 和1.13 g DCC溶于60 mL DMAc后,再加入1.26 g DMAP,在氮气条件下,于40℃搅拌反应30 h。反应结束后,经透析、真空干燥得到浅黄色蜡状物,即为PUSS-gmPEG(产率为82.6%)。
1.4 PUSS-g-mPEG的胶束化行为研究
将10 mg PUSS-g-mPEG溶于3 mL THF后,在搅拌条件下逐滴加入20 mL芘分散液中,待THF完全挥发后,再用芘分散液稀释得到含芘的一系列聚合物浓度溶液,避光静置2 d后测其荧光。
1.5 PUSS-g-mPEG胶束的制备及稳定性研究
30 mg PUSS-g-mPEG溶于5 mL THF后,搅拌滴加到60 mL pH=7.4的磷酸盐缓冲液(PBS)中,待THF完全挥发后,得到胶束溶液,测其粒径和电位。
储存稳定性:取10 mL胶束溶液,放置于4℃冰箱中冷藏7 d后,测其粒径。抗稀释稳定性:取1 mL胶束溶液,稀释至500 mL,静置1 h后,测其粒径。血清稳定性:取7 mL胶束溶液,加入2 mL BSA溶液,37℃下振荡2 h后,测其粒径。
1.6 PUSS-g-mPEG胶束的还原敏感性研究
取上述胶束溶液,分别加入GSH使其浓度为0(正常血液环境)、10 μmol/L(细胞外环境)和10 mmol/L(细胞内环境),于37℃下振荡24 h后测其粒径。
1.7 PUSS-g-mPEG胶束的载药及释药性能研究
取6.4 mg DOX·HCl,加入15 mL DMF 和1 滴三乙胺溶解后,再加30 mg PUSS-g-mPEG使其溶解。在搅拌条件下逐滴加到45 mL pH=7.4 PBS中,再转移至透析袋(MWCO6000)内,用pH=7.4的PBS透析48 h,得载药胶束PUSS-g-mPEG/DOX。
PUSS-g-mPEG/DOX胶束溶液冻干后,用DMF溶解,测其荧光,再根据标准曲线计算其载药量和包封率。向PUSS-g-mPEG/DOX胶束溶液中分别加入GSH使其浓度分别为 0、10 μmol/L和 10 mmol/L,转入透析袋(MWCO6000),并置于37℃、30 mL相应GSH浓度的PBS中。每隔一定时间从透析袋外取5 mL样品用于荧光检测,并补充相同体积的新鲜缓冲液。根据DOX的标准曲线,计算出不同时间段内载药胶束对DOX的累计释放量。
2 结果与讨论
2.1 聚合物的合成及表征
所得聚合物结构用1H-NMR表征,结果见图1。

图1 所得聚合物的1H-NMR谱图
从图1可以观察到PUSS-ene中各个链段上氢质子的化学位移。另外,采用GPC测试得到其Mn为13 500,分子量分布指数为1.65。结果表明已成功合成PUSS-ene。
图1 PUSS-COOH中归属于碳碳双键的氢质子峰已消失,表明 3-巯基丙酸已接枝到聚氨酯。PUSS-g-mPEG的图中出现了mPEG链段亚甲基的氢质子化学位移,说明已成功合成PUSS-g-mPEG;另外根据1H-NMR图中各质子的峰面积以及PUSS-ene的分子量,可计算出PUSS-g-mPEG中PCL和mPEG 链段摩尔比为 1∶2.44,Mn为 25 200。
2.2 PUSS-g-mPEG的胶束化行为
以芘为荧光探针,得到了含芘的一系列不同浓度聚合物溶液的荧光图谱,再由图中332 nm与335 nm处的荧光强度之比(I335/I332)对 PUSS-gmPEG浓度的对数(lgc)作图,结果见图2。

图2 芘在聚合物溶液中的荧光图谱(a)及I335/I332-lgc图(b)
从图2(a)可以看到,随PUSS-g-mPEG溶液浓度增加,芘的荧光强度逐渐增强,且其荧光最大激发峰的位置从332 nm逐渐红移至335 nm。说明随着聚合物溶液浓度的增加,芘逐渐从亲水环境转移到了疏水环境中,表明在水中PUSS-g-mPEG达到一定浓度时可自组装形成胶束。
由图2(b)可见,经拟合得到其临界胶束浓度(CMC)为7.74×10-4mg/mL。 PUSS-g-mPEG 具有较低的CMC,表明其在水溶液中易形成胶束,且在血液循环中可具有良好的抗稀释稳定性。
2.3 PUSS-g-mPEG胶束及其稳定性研究
利用DLS仪对PUSS-g-mPEG胶束粒径及其电位进行了测试。测得胶束粒径约为186 nm,分散指数约为0.18,粒径分布较均一。说明PUSS-g-mPEG可自组装形成纳米胶束,有利于其在血液循环中通过高渗透长滞留效应聚集到肿瘤部位,以减少药物在正常组织的聚集而产生毒副作用。且PUSS-gmPEG胶束在pH=7.4 PBS中的电位为-0.94 mV,其微弱的负电荷可与带负电荷的细胞膜以及血清成分产生静电排斥作用,有助其在血液中长效循环。
为了进一步表征PUSS-g-mPEG胶束在生理条件下的稳定性,在体外分别进行抗稀释稳定性、储存稳定性和血清稳定性测试,结果见图3。

图3 PUSS-g-mPEG胶束的稳定性试验
由图3可知,胶束在4℃下放置7 d或加入BSA后,其粒径几乎没有变化;当胶束浓度稀释到1/500倍后,其粒径变化不大,分布仍然较集中。说明PUSS-g-mPEG胶束具有良好的稳定性,这可能与接枝型结构导致其胶束疏水内核缠结较紧密以及表面带微弱的负电荷有关。PUSS-g-mPEG胶束优异的稳定性可延长其在体液中的循环时间,有助于增加其在肿瘤部位的聚集,从而提高疗效。
2.4 PUSS-g-mPEG胶束的还原敏感性研究
在模拟正常血液(pH=7.4 PBS)和细胞内外GSH 浓度(0、10 μmol/L、10 mmol/L)条件下,采用DLS仪测试了PUSS-g-mPEG胶束的粒径及其分布,以此衡量其还原敏感性,结果见图4。
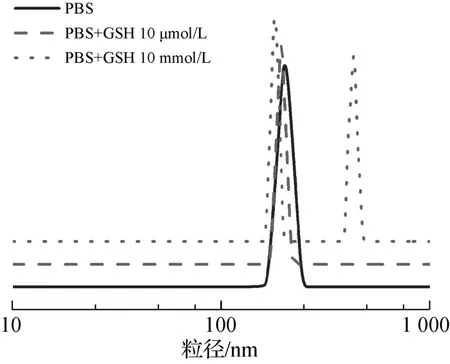
图4 PUSS-g-mPEG胶束在不同条件下的DLS图
当PBS中 GSH浓度为 0或 10 μmol/L时,PUSS-g-mPEG胶束的粒径基本一致;当PBS中GSH浓度增大为10 mmol/L时,胶束粒径分布呈现双峰,有较大粒子出现。说明在正常生理条件或细胞外GSH浓度较低时,PUSS-g-mPEG胶束具有良好稳定性;而在细胞内GSH浓度较高时,由于GSH的还原作用使聚合物中二硫键断裂,导致胶束解离,并重新聚集产生较大粒子,表明胶束有良好的还原敏感性。
2.5 PUSS-g-mPEG胶束的载药与释药性能研究
经计算得到PUSS-g-mPEG胶束对DOX的包封率和载药量分别为11%和1.9%。在37℃下PUSS-g-mPEG/DOX的体外释药结果见图5。

图5 PUSS-g-mPEG/DOX胶束的体外释药情况
在pH=7.4的PBS中,纯DOX在24 h内的累积释放量为84%,而载药胶束的累积药物释放量为23%,说明在正常生理条件下聚合物载药胶束无明显早释。当释药体系中GSH浓度分别为10 μmol/L和10 mmol/L时,60 h内载药胶束对DOX的累计释放量为41%和86%。可见,在GSH浓度为10 mmol/L时PUSS-g-mPEG载药胶束的释药速率明显增大,表现出良好的还原敏感释药性能,可实现对DOX的控制释放。
3 结论
通过预聚法、巯基-烯反应和酯化反应合成了具有还原敏感性的接枝型两亲性聚氨酯PUSS-gmPEG。PUSS-g-mPEG可自组装形成纳米胶束,在模拟生理条件下表现出良好的稳定性。该胶束对DOX具有一定的包载能力,相对于不含GSH或GSH浓度为10 μmol/L时,其载药胶束在GSH浓度为10 mmol/L时释药速率明显增大,表明 PUSS-gmPEG/DOX载药胶束具有良好的还原敏感释药性能。
