恩替卡韦治疗乙型病毒性肝炎失代偿性肝硬化的临床价值
2022-05-09刘胜
刘胜
(安远北方医院消化内科,江西 赣州 342108)
乙型病毒性肝炎简称乙肝,是一种由乙型肝炎病毒感染(Hepatitis B Virus,HBV)引起的传染性疾病。我国在世界上是乙肝大国,据权威数据调查显示,我国HBV 感染人数约9000 万,且在青年人群中HBsAg 阳性率占5%,其中有多数乙肝患者随着疾病发展最终导致失代偿性肝硬化,这也是乙肝患者的主要死亡原因[1]。目前临床上对该疾病的治疗有药物抗病毒治疗和手术肝移植治疗,由于我国手术费用较为昂贵且缺乏肝源,所以抗病毒治疗是首选的治疗方式[2]。在进行抗病毒治疗时,由于患者的病情需要,尽管不能治愈,但高效、安全用药可以抑制病毒复制,减轻肝脏损伤,延缓病情进一步恶化,故治疗中选择安全有效的抗病毒药物是控制延缓疾病发展的主要手段[3]。恩替卡韦作为一种具有强效和高基因屏障作用的抗病毒药物,可以帮助患者抑制机体的乙肝病毒复制,从而恢复部分甲状腺功能,具有一定安全性,但是对于该药物在患者失代偿性肝硬化中的应用报道较少[4]。基于此,本文主要研究恩替卡韦治疗对乙型病毒性肝炎失代偿性肝硬化患者的影响进行研究,旨在为该疾病的诊疗工作提供新思路。现将结果报道如下:
1 资料与方法
1.1 一般资料
选取2017 年2 月~2020 年1 月期间于我院治疗的66 例乙型病毒性肝炎失代偿性肝硬化患者进行研究。随机分为对照组(n=33,予以常规治疗)和研究组(n=33,在常规治疗的基础上予以恩替卡韦治疗)。其中研究组男19 例,女14 例;年龄28~62 岁,平均(43.58±7.24)岁;病程1~10年,平均(5.35±2.64)年;肝功能分级:Child-Pugh A 级10 例,Child-Pugh B 级15 例,Child-Pugh C级8 例。对照组男20 例,女13 例;年龄27~63岁,平均(44.01±7.82)岁;病程2~12 年,平均(5.61±2.54)年;肝功能分级:Child-Pugh A 级11例,Child-Pugh B 级13 例,Child-Pugh C 级9 例。两组基础资料对比不存在统计学意义(P>0.05),具有可比性。纳入标准:(1)患者皆满足《病毒性肝炎诊断标准》中关于乙型病毒性肝炎失代偿性肝硬化的诊断标准[5],并经病理检查确诊;(2)在我院治疗且病历资料完整无缺漏;(3)患者及其家属均知晓自愿参加研究,并签字。排除标准:(1)对本研究所使用药物过敏者;(2)存在精神疾病者或依从性差者;(3)合并其他肝脏疾病者;(4)存在心、肺、肾等功能异常者,合并恶性者肿瘤者;(5)处于特殊时期的女性,如:妊娠期、哺乳期。
1.2 方法
对照组予以保肝、抗感染、补充白蛋白、维持酸碱及水电解质平衡等常规治疗。研究组在对照组基础予以恩替卡韦治疗,使用方法如下:恩替卡韦片(生产厂家:北京百奥药业有限责任公司;批准文号:国药准字H20 193077;规格:0.5 mg*28 片)口服治疗,每次0.5 mg,一天1 次。两组患者均持续治疗1 年。
1.3 评价指标
1.3.1 甲状腺功能
抽取患者空腹静脉血3 mL,离心、抗凝处理(转速:3000 rpm,时间:10 min,半径:10 cm),吸取上层血清置于EP 管中,并保存在-80℃冰箱中待测,以酶联免疫吸附试验法检测患者的甲状旁腺激素水平。检测试剂盒均购自美国RD 公司。
1.3.2 疾病转归
以荧光探针法检测两组患者治疗前后病毒载量(Chronic hepatitis B Deoxyribonucleic acid;HBV DNA)水平及HBV DNA 转阴率。
1.3.3 肝功能
采用全自动生化分析仪检测肝功能相关指标,包括:丙氨酸氨基转移酶(Alanine aminotransferase;ALT)、天门冬氨酸氨基转移酶(Aspartate aminotransferase,AST)、白蛋白(Albumin,Alb)、总胆红素(Total Bilirubin,STB)。
1.3.4 不良反应
观察两组患者在治疗过程中有无头痛、疲劳、眩晕和恶心等不良反应发生。
1.4 统计方法
文中数据均以SPSS22.0 软件进行统计处理,甲状腺功能、HBV DNA 水平通过平均数±标准差()描述,t 检验;HBV DNA 转阴率、不良反应通过n(%)描述,χ2检验,以P<0.05 为差异具有统计学意义。
2 结果
2.1 甲状腺功能对比
表1:治疗前两组甲状旁腺激素水平对比,差异不具有统计学意义(P>0.05);治疗后两组甲状旁腺激素水平均较治疗下降,且以研究组下降最为明显,差异具有统计学意义(P<0.05)。
表1 比较两组治疗前后甲状旁腺激素水平(,n=33)

表1 比较两组治疗前后甲状旁腺激素水平(,n=33)
注:与对照组治疗后相比,#P<0.05。
2.2 疾病转归情况
表2:两组患者治疗前HBV DNA 水平比较,差异不具有统计学意义(P>0.05);治疗后两组患者HBV DNA 水平均较治疗前降低,且研究组低于对照组(P<0.05);研究组患者HBV DNA 转阴率为21.21%显著高于对照组患者HBV DNA 转阴率3.03%,差异具有统计学意义(P<0.05)。
表2 对比两组患者治疗前后HBV DNA 水平及HBV DNA 转阴率(,例(%),n=33)
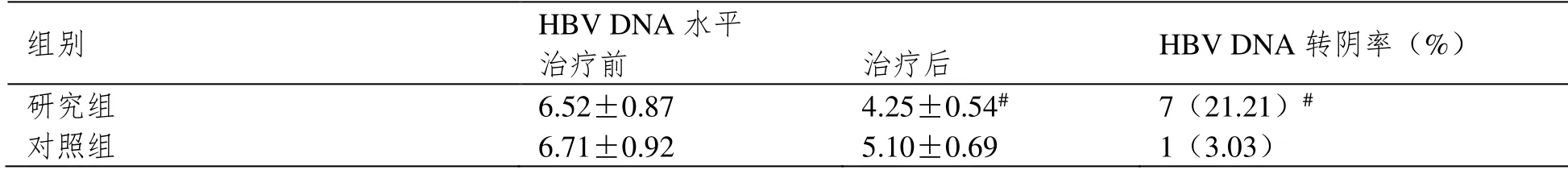
表2 对比两组患者治疗前后HBV DNA 水平及HBV DNA 转阴率(,例(%),n=33)
注:与对照组相比,#P<0.05。
2.3 肝功能
治疗前两组ALT、AST、Alb、STB 水平对比,差异不具有统计学意义(P>0.05);治疗后两组ALT、AST 及STB 水平均较治疗前降低,Alb 水平均较治疗前升高,其中以研究组变化最为明显,差异具有统计学意义(P<0.05),详见表3。
表3 对比两组治疗前后肝功能指标水平(,n=33)
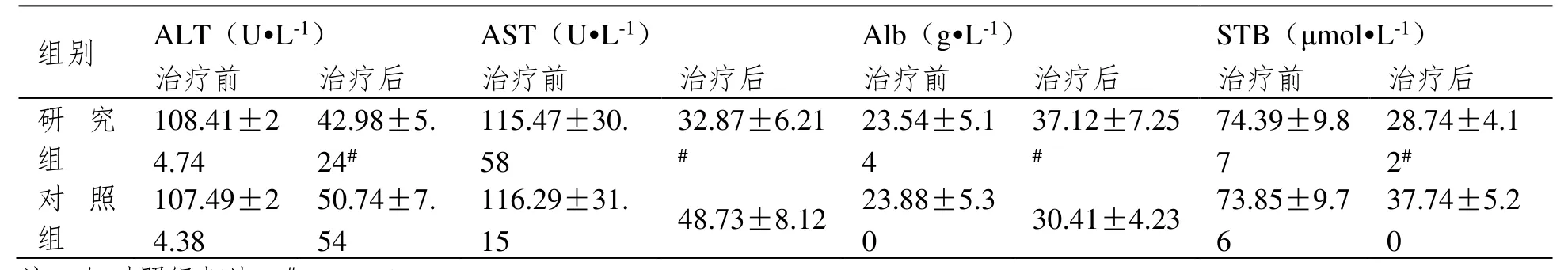
表3 对比两组治疗前后肝功能指标水平(,n=33)
注:与对照组相比,#P<0.05。
2.4 不良反应对比
研究组患者有3 例出现头痛,2 例出现疲劳,1 例出现眩晕,不良反应总发生率为18.18%;对照组患者有2 例出现头痛,2 例出现恶心,不良反应总发生率为12.12%。两组不良反应发生情况对比,差异不具有统计学意义(χ2=0.471,P>0.05)。
3 讨论
乙肝病毒感染是全球性的健康问题,由于病毒的长期不间断复制,肝炎持续发展,最终导致肝硬化,此时病毒活跃复制,患者进一步出现肝功能失代偿甚至发展为肝癌[6]。出现失代偿也就意味着患者预后变差,由此可见在治疗中对病毒复制进行抑制是关键措施[7]。受患者耐药性的影响,常规的治疗方式对乙肝病毒的复制控制效果欠佳,而恩替卡韦近年来在临床上被广泛应用,经过临床研究证实,其对病毒的控制效果明显,不易产生耐药性[8]。在既往文献中表示,相较常规抗病毒药物,恩替卡韦的抗病毒能力是其300 倍以上,对病毒具有强效的抑制作用,从而能够更为明显的减轻病毒对肝脏的损害[9]。因此,在本中选取了66 例乙型病毒性肝炎失代偿性肝硬化患者进行研究,划分为研究组和对照组,分别采取恩替卡韦治疗和常规治疗,通过研究结果可发现,研究组患者的甲状腺功能及肝功能改善幅度均优于对照组,且无不良反应增加,证实了恩替卡韦的疗效及安全性。乙型病毒性肝炎患者由于蛋白合成能力下降,导致患者营养状态欠佳,甲状腺功能异常,从文中可知两组患者治疗前甲状旁腺激素均处于异常升高状态,治疗后研究组恢复更为明显,说明恩替卡韦还具有改善患者甲状腺功能的作用,这与既往文献报道相一致[10]。同时本文结果显示,研究组治疗后的HBV DNA 水平低于对照组,HBV DNA 转阴率高于对照组,说明恩替卡韦对促进患者疾病转归的效果更为明确。
综上所述,乙型病毒性肝炎失代偿性肝硬化应用恩替卡韦治疗能够有效改善患者的甲状腺功能及肝功能,促进疾病转归,且无不良反应增加,具有一定安全性,值得推广应用。
