奥马珠单抗联合布地奈德治疗重度支气管哮喘患儿的效果
2022-05-07张小宁张向峰张志英
张小宁,张向峰,张志英
郑州大学附属儿童医院 河南省儿童医院 郑州儿童医院,呼吸科,郑州 450003
支气管哮喘是临床常见的呼吸系统慢性疾病,具有气道炎症、气道高反应性两大特征,发病机制较复杂[1]。临床采用吸入性糖皮质激素改善重度支气管哮喘患儿临床症状,但长时间使用会产生较多不良反应[2-3]。奥马珠单抗是用于哮喘治疗的首个靶向药物,是一种重组人源化抗免疫球蛋白E(IgE)单克隆抗体,主要结合游离的IgE,抑制Ig E 结合炎症细胞中的FcεRI等受体,促使辅助性T 细胞2(Th2)型免疫反应下降[4-5]。目前奥马珠单抗联合布地奈德雾化吸入治疗支气管哮喘患儿国内鲜有报道,因此本研究重点探究其对重度支气管哮喘患儿肺功能及外周血嗜酸性粒细胞(EOS)的影响。
1 资料与方法
1.1 一般资料
选取我院诊治的重度支气管哮喘患儿114 例。纳入标准:(1)符合儿童支气管哮喘诊断标准[6],重度哮喘为接受第四级或第五级治疗才能控制哮喘,或不能完全控制;(2)患儿年龄为12~17岁;(3)患儿经过敏原检测IgE呈阳性;(4)患儿经糖皮质激素雾化吸入治疗超过3个月及以上;(5)使用奥马珠单抗前血清IgE为75~1 500 IU·mL-1,(6)患儿家属签署知情同意书。排除标准:(1)患儿患有心、肝、肾等严重损伤;(2)患儿存在其他单克隆抗体治疗史;(3)患儿对奥马珠单抗存在禁忌证。采用随机数字表法分为观察组和对照组。观察组:55例,男36例,女19例,年龄为12~17岁,平均(14.23±1.22) 岁,病程为1~3年,平均(1.87±0.57) 年,血清总IgE为(433.94±109.32)IU·mL-1,体质量为(32.10±4.74)kg;对照组:59例,男39例,女20例,年龄为12~17岁,平均(14.45±1.27) 岁,病程为1~3年,平均(1.93±0.48) 年,血清总IgE为(430.78±107.94)IU·mL-1,体质量为(31.70±4.55)kg。2组患儿性别、年龄、病程比较,差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
对照组患儿给予由澳大利亚阿斯利康生产的布地奈德混悬液(规格:2 mL∶1 mg),吸入给药,每次1 mg,每日2次,早晚各1次,治疗6个月。观察组在对照组治疗的基础上联合奥马珠单抗联合治疗,给予患儿由Novartis Pharma Stein AG 生产的奥马珠单抗(规格:150 mg),给药剂量与频率按照患儿治疗前基线IgE水平和体质量决定,皮下注射,2周给药1次,每次150 mg。首次皮下注射需在医院观察2 h,后面注射需在医院观察30 min。16周后,观察患儿的总体改善情况,明显改善继续用药,反之停止用药。
1.3 观察指标
(1)临床疗效:参照《儿童支气管哮喘诊断与防治指南(2016年版)》[6]进行评估,显效:患儿临床症状、肺功能基本改善或消失;有效:患儿上述情况有所缓解;无效:患儿无变化,或加重。总有效率=(显效例数+有效例数)÷总例数×100%。(2)肺功能评估:治疗前后早上用AS-507型肺功能检测仪(上海伊沐医疗器械有限公司)检测第一秒用力呼气容积(FEV1)、用力呼气肺活量(FVC),计算FEV1/FVC。(3)EOS和IgE检测:治疗前后抽取患儿空腹静脉血2 mL,送至检验科分层,取血清置入微量离心管中。用RT-7200X 型全自动血液分析仪(武汉科尔达医疗科技有限公司)检测EOS;根据磁微粒化学发光免疫分析法,用BIOBASE2000型全自动酶免分析仪(章丘舜泽生物工程有限公司)检测Ig E 水平。(4)免疫功能评估:治疗前后,抽取患儿清晨空腹静脉血2 mL离心,取血清。采用MACSQuant 10型流式细胞仪(德国美天旎生物技术公司)检测Th2和辅助性T 细胞17(Th17),均严格按照试剂盒(德国美天旎生物技术公司)说明书进行操作。(5)哮喘控制评分、哮喘生活质量评分:治疗前后由2名护士在不知道具体分组的情况下采用哮喘控制评分评估哮喘控制情况,包括活动受限、心理情绪、哮喘症状等,总分为0~25分,得分越高表示哮喘控制情况越佳;哮喘生活质量评分包括活动受限,哮喘症状,对刺激原反应、心理情绪、自我健康的关心,共35项,总分为245分,得分越高,表示哮喘生活质量越好。(6)记录2组不良反应发生情况。
1.4 统计学方法
所有数据用SPSS22.0进行统计分析。肺功能、EOS、Ig E、T 细胞、哮喘控制评分、哮喘生活质量评分以()表示,组间比较采用t检验;临床疗效和不良反应以百分比表示,比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 2组临床疗效比较
观察组治疗后总有效率高于对照组(94.55%vs.81.36%),差异有统计学意义(P<0.05)。见表1。

表1 2组临床疗效比较Tab.1 Comparison of clinical efficacy between the 2 groups
2.2 2组肺功能指标比较
治疗前2组FEV1、FVC、FEV1/FVC比较,差异无统计学意义(P>0.05);治疗后,2组FEV1、FVC、FEV1/FVC均高于治疗前(P<0.05),且观察组FEV1、FVC、FEV1/FVC 均高于对照组,差异有统计学意义(P<0.05)。见表2。
表2 2组肺功能指标比较 ()Tab.2 Comparison of lung function indexes between the 2 groups ()
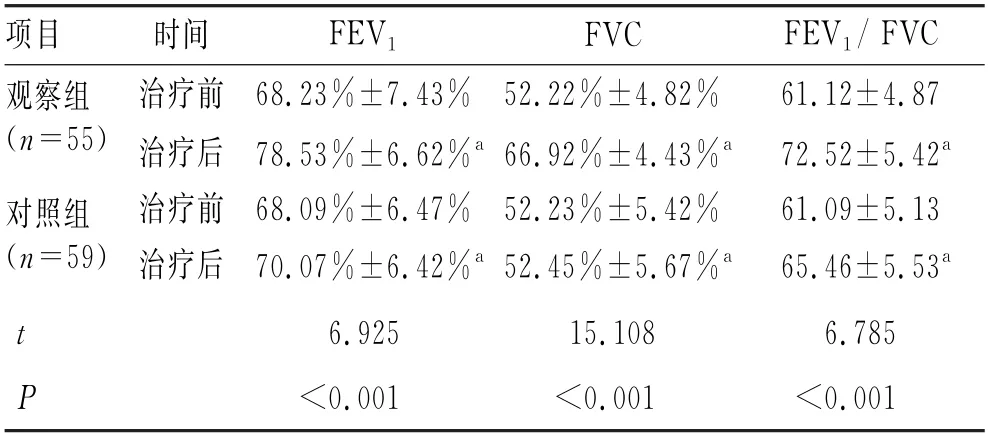
表2 2组肺功能指标比较 ()Tab.2 Comparison of lung function indexes between the 2 groups ()
注:与组内治疗前比较,a P<0.05。
2.3 2组EOS、IgE比较
治疗前2组EOS和IgE 比较,差异无统计学意义(P>0.05);治疗后,2组EOS和IgE 均低于治疗前(P<0.05),且观察组EOS和IgE 均低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 2组EOS和IgE比较 ()Tab.3 Comparison of EOS and IgE between the 2 groups()

表3 2组EOS和IgE比较 ()Tab.3 Comparison of EOS and IgE between the 2 groups()
注:与组内治疗前比较,a P<0.05。
2.4 2组Th2和Th17比较
治疗前2组Th2和Th17比较,差异无统计学意义(P>0.05);治疗后,2组Th2和Th17均低于治疗前(P<0.05),且观察组Th2 和Th17 均低于对照组,差异有统计学意义(P<0.05)。见表4。
表4 2组Th2和Th17比较 ()Tab.4 Comparison of Th2 and Th17 between the 2 groups()

表4 2组Th2和Th17比较 ()Tab.4 Comparison of Th2 and Th17 between the 2 groups()
注:与组内治疗前比较,a P<0.05。
2.5 2组哮喘控制评分、哮喘生活质量评分比较
治疗前2组哮喘控制评分和哮喘生活质量评分比较,差异无统计学意义(P>0.05);治疗后,2 组哮喘控制评分和哮喘生活质量评分均高于治疗前(P<0.05),且观察组哮喘控制评分和哮喘生活质量评分均高于对照组,差异有统计学意义(P<0.05)。见表5。
表5 2组哮喘控制评分、哮喘生活质量评分比较 ()Tab.5 Comparison of scores of asthma control and asthma quality of life between the 2 groups()

表5 2组哮喘控制评分、哮喘生活质量评分比较 ()Tab.5 Comparison of scores of asthma control and asthma quality of life between the 2 groups()
注:与组内治疗前比较,a P<0.05。
2.6 2组不良反应比较
2组均有恶心呕吐、乏力、嗜睡和双下肢水肿发生,均可自行消失,2组不良反应总发生率比较,差异无统计学意义(P>0.05),见表6。

表6 2组不良反应比较Tab.6 Comparison of adverse reactions between the 2 groups
3 讨论
临床治疗支气管哮喘主要以改善临床症状为主,包括糖皮质激素、白三烯抑制剂、抗胆碱药及β2 受体激动剂等,但对于部分重度支气管哮喘患儿来说,临床症状改善与哮喘控制效果均一般[7-8]。IgE 在支气管哮喘以及作为过敏反应媒介中发挥着重要作用,抗IgE单抗的使用证实了这一说法,奥马珠单抗主要用于确诊IgE为媒介的哮喘患者,能改善哮喘症状及减少口服激素量[9]。21世纪初,国外将奥马珠单抗用于重度变应性哮喘患者取得了较好的效果,为哮喘生物靶向治疗奠定了基础。
近年来,对于重度支气管哮喘患儿,临床主要采用对症治疗,包括平喘、抗感染、糖皮质激素等,其中糖皮质激素具有较好的抗炎作用,但长时间使用会导致不良反应发生率升高[10-12]。奥马珠单抗主要用于糖皮质激素雾化吸入等治疗后,能有效控制哮喘发作及有关过敏症状,还能降低糖皮质激素使用量[13]。有研究表明,奥马珠单抗治疗难治性支气管哮喘取得了一定成果,可减少支气管哮喘急性发作次数及糖皮质激素使用量等[14]。本研究结果表明,观察组治疗后总有效率高于对照组。提示奥马珠单抗联合糖皮质激素雾化吸入治疗重度支气管哮喘患儿效果较好,可改善支气管痉挛,抑制血管通透性,直接作用于支气管,与上述研究结果一致。重症支气管哮喘患儿在治疗中不仅要控制临床症状,还要确保肺功能正常运行。FEV1、FVC、和FEV1/FVC 是临床公认的用于评估阻塞性通气功能障碍的评估指标。有研究表明,将奥马珠单抗应用于中、重度支气管哮喘Ⅲ期患者中,可明显控制肺功能并升高FEV1水平[15]。本研究结果显示,观察组治疗后FEV1、FVC 和FEV1/FVC均高于对照组。说明奥马珠单抗联合布地奈德雾化吸入可保护重度支气管哮喘患儿的肺功能,其中糖皮质激素可改善气道高反应,降低呼吸道炎症,而奥马珠单抗可减少糖皮质激素使用量,减轻哮喘症状,两者发挥协同作用,进而保护肺功能。辅助性T 细胞释放白细胞介素-13(IL-13),嗜酸性粒细胞及肥大细胞也具有该作用,IL-13 参与气道炎症反应与气道重塑;气道炎症可表现IL-13激活嗜酸性粒细胞,缩短细胞死亡时间,激发IgE 抗体分泌和释放[16]。Th2细胞因子中IL-13 介导组织纤维化,IgE 水平与IL-13水平呈正相关,且不受年龄限制[17]。结果显示,观察组EOS和IgE低于对照组,说明奥马珠单抗联合布地奈德雾化吸入治疗重度支气管哮喘患儿可减轻炎症反应。有研究表明,Th2细胞可调控白细胞介素-4(IL-4)分泌,IL-4可对B细胞调控产生具有特异性的Ig E,同时IL-4、Ig E也会影响辅助性T 细胞0(Th0)发展成Th2[18]。相关研究表明,Th17细胞与其细胞因子白细胞介素-17(IL-17)可激活支气管上皮细胞、纤维母细胞及平滑肌细胞,增加白细胞介素-6(IL-6)、粒细胞集落刺激因子等表达,使气道内中性粒细胞快速浸润、增殖[19]。多项研究表明,Th17 细胞与其细胞因子IL-17能使变应性哮喘患者气道炎症及气道高反应加剧[20]。本研究结果表示,观察组治疗后Th2、Th17均低于治疗前和对照组,哮喘控制评分、哮喘生活质量评分均高于治疗前和对照组。说明奥马珠单抗联合布地奈德雾化吸入治疗重度支气管哮喘患儿可有效降低气道炎症及气道高反应。本研究结果显示,2组均有恶心呕吐、乏力、嗜睡和双下肢水肿发生,均可自行消失。说明两者联合应用安全性较高。
综上所述,奥马珠单抗联合布地奈德雾化吸入治疗重度支气管哮喘患儿,可明显改善患者的肺功能,降低EOS 和Ig E 水平,控制气道炎症,治疗效果较好。
