不同治疗方案对抗凝、抗血小板药物相关性脑出血患者预后的影响
2022-05-05郭颖翰王挺厅俞楷博俞晓波严锋水旭健杨施迪王成斌沈张锋王翊飞陈高
郭颖翰 王挺厅 俞楷博 俞晓波 严锋 水旭健 杨施迪 王成斌 沈张锋 王翊飞 陈高
脑出血是临床常见的高发病率、高致死率、高致残率的急性脑血管病,年发病率约为60~80/10万人,是我国居民死亡的主要原因之一[1]。随着人口老龄化与血管内治疗的广泛开展,抗血小板和抗凝药物的使用不断增加,在抗凝或抗血小板药物使用期间发生的脑实质内出血被称为抗凝、抗血小板药物相关性脑出血,约占全部脑出血的25.8%[2-3]。与单纯的自发性脑出血相比,抗凝、抗血小板药物相关性脑出血的血肿扩大发生率更高,功能预后更差,病死率更高[4]。笔者通过多中心回顾性分析抗凝、抗血小板药物相关性脑出血患者的临床资料,探讨不同治疗方案对此类患者预后的影响,现将结果报道如下。
1 对象和方法
1.1 对象 回顾浙江省6家医院神经外科2019年1月至2020年12月诊治的抗凝、抗血小板药物相关性脑出血患者872例(其中浙江大学医学院附属第二医院379例,金华市中心医院114例,宁波市医疗中心李惠利医院104例,诸暨市人民医院100例,萧山医院99例,嘉兴市第二医院76例),男485例,女387例,年龄 34~79(56.86±15.65)岁;口服抗凝、抗血小板药物时间1~11年,其中单用阿司匹林162例,单用华法林425例,联合阿司匹林及氯吡格雷285例。纳入标准:(1)通过 CT、CT 血管造影(CT angiography,CTA)等影像学检查,明确为自发性脑出血患者;(2)伴有剧烈头痛、恶心、呕吐、偏瘫、失语、意识障碍等症状;(3)正在服用抗血小板(如阿司匹林、氯吡格雷)药物或抗凝药物(如华法林)。排除标准:(1)经影像学检查明确的破裂动脉瘤、动静脉畸形、烟雾病、缺血性梗死出血转化、肿瘤卒中等引起的脑出血;(2)目前伴有严重疾病可能干预结局评估的患者。本研究经浙江大学医学院附属第二医院医学伦理委员会批准。
1.2 临床表现与检查 患者表现为突发剧烈头痛、恶心、呕吐、偏瘫、失语、意识障碍等症状,应用格拉斯哥评分(Glasgow coma scale,GCS)评价患者神经功能情况。依据入院首次CT检查估算的出血量,分为出血量<30 ml组、30~60 ml组、>60 ml组。收集患者入院时GCS评分、血压、Hb、PLT、凝血功能等临床指标。
1.3 治疗方法 入院后立即停用抗凝、抗血小板药物,强化降低颅内压治疗,密切监测凝血功能,应用维生素K、新鲜冰冻血浆等矫正凝血国际标准化比值(international normalized ratio,INR)。出血量<30 ml者均行保守药物治疗,出血量30~60 ml与>60 ml的患者中,部分在家属签字要求下予以药物保守治疗,其余患者应用开颅小骨窗内镜辅助下行血肿清除术或开颅血肿清除联合去骨瓣减压术。根据患者治疗方案分为药物保守治疗(保守组)、行开颅小骨窗内镜辅助下血肿清除术(微创组)及行开颅血肿清除联合去骨瓣减压术(开颅组)。
1.4 评价指标 出院后随访6个月,采用格拉斯哥预后评分(Glasgow outcome scale,GOS)评估预后情况,1~3分为预后不良,4~5分为预后良好。
1.5 统计学处理 采用SPSS 24.0统计软件。计量资料以±s表示,多组间比较采用单因素方差分析,两两比较采用LSD-t检验。计数资料以例数及百分比表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 分组情况 872例患者中出血量<30 ml组86例,30~60 ml组 535例,>60 ml组 251例。在 30~60 ml组中,保守组212例,微创组189例,开颅组134例;在>60 ml组中,保守组64例,微创组96例,开颅组91例。
2.2 30~60 ml组中不同治疗方案3组患者的临床指标及预后指标比较 3组患者GCS评分差异无统计学意义(P>0.05);微创组和开颅组患者年龄小于保守组,收缩压、GOS评分高于保守组,微创组GOS评分高于开颅组(均P<0.05);微创组Hb、INR均高于保守组和开颅组(均P<0.01);保守组病死率为16.0%(34/212),高于微创组的7.4%(14/189)、开颅组的11.2%(15/134),保守组与微创组病死率比较差异有统计学意义(P<0.05)。见表1。
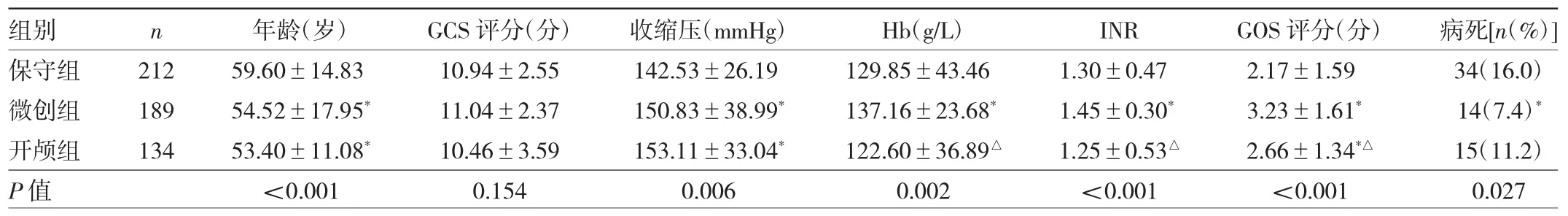
表1 30~60 ml组中不同治疗方案3组患者的临床指标及预后指标比较
2.3 >60 ml组中不同治疗方案3组患者的临床指标及预后指标比较 3组GCS评分、收缩压和GOS评分差异均无统计学意义(均P>0.05)。微创组和开颅组患者年龄小于保守组,开颅组的Hb低于微创组和保守组,微创组INR低于保守组,差异均有统计学意义(均P<0.05)。保守组病死率为37.5%(24/64),高于微创组的 19.8%(19/96)、开颅组的 24.1%(22/91),保守组与微创组病死率差异有统计学意义(P<0.05)。见表2。
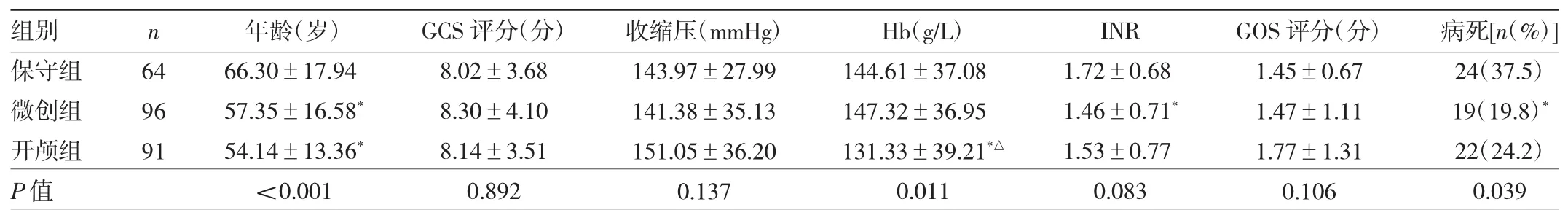
表2 >60 ml组中不同治疗方案3组患者的临床指标及预后指标比较
3 讨论
随着人口老龄化与抗凝、抗血小板药物不断发展与应用,相关脑出血发病率逐年升高[5],相较单纯脑出血患者,其病死率更高,预后更差,目前尚无统一的诊治共识,成为困扰临床医师的重要难题。
本研究发现,与指南公布的流行病学调查结果相比[6],抗凝、抗血小板药物相关性脑出血患者具有更高的致残率与病死率。在出血量30~60 ml患者中,相较于药物保守治疗,应用手术治疗可显著改善脑出血患者神经功能评分,降低病死率,其中应用微创手术方式比传统开颅血肿清除具有更好的治疗效果;在>60 ml组患者中,保守药物治疗的患者预后最差,病死率显著升高,应用手术治疗可小幅改善脑出血患者神经功能预后,微创手术治疗能显著降低患者病死率。
长期口服抗凝、抗血小板药物,使得血液保持在低凝状态,随着时间的延长,患者出血风险越来越高,同时长期服用口服抗凝、抗血小板药物,表明患者心脑血管基础条件差,一旦出现脑出血,往往导致比普通类型脑出血更加严重的神经功能损害,病死率极高[7]。微创血肿清除已经作为治疗脑出血的有效手段,微创治疗对局部脑组织及脑血管损伤小,操作简便,血肿清除过程中不干扰周围的可能出血责任区,不增加再出血的机会,同时在内镜辅助下对血肿周边出血责任区开展全方位探查,充分止血,显著降低术后再次出血风险[8]。
脑出血的手术治疗方式主要包括立体定向血肿穿刺引流、神经内镜辅助下微创血肿清除、开颅去骨瓣脑内血肿清除术等。手术方式的选择取决于脑出血的性状与患者凝血功能障碍程度,如血肿内有液平,可行立体定向穿刺引流[9];凝血功能障碍分级0~Ⅱ级的患者,可选择内镜辅助下微创血肿大部清除,充分降低颅内压,不必追求完全清除血肿[10];凝血功能障碍分级Ⅲ~Ⅳ级患者可行开颅去骨瓣减压术,围术期持续监测并矫正凝血功能,观察术区渗血状况,多次评估均为Ⅲ级的患者,建议根据患者血肿大小、部位和硬膜外止血情况决定是否清除脑内血肿[11]。抗凝、抗血小板药物相关性脑出血患者术后易再出血,术后放置血肿腔内引流管与皮下引流管有助于降低颅内压、减少再次手术的几率,有条件的医疗单位可放置颅内压探头持续监测颅内压[12]。
抗凝、抗血小板药物相关性脑出血手术中针对性术中止血策略的选择,取决于术中出血类型与术者的经验。动脉性出血多以小动脉为主,通常需确切的电凝止血,如果涉及重要的穿支动脉,压迫止血需要特别谨慎,患者凝血功能异常导致止血所需时间明显延长,形成血凝块的力学强度也有所下降,术后易再次出血,可选用相应止血材料加固出血点[13]。静脉型出血常可通过局部压迫加用止血材料予以止血,压迫力度应适中,避免静脉闭塞造成回流障碍。对于广泛的创面渗血,可应用温0.9%氯化钠溶液反复冲洗,识别出较大的出血点,用双极电凝止血,其余出血点可加用止血材料和明胶海绵压迫止血[14]。
综上所述,抗凝、抗血小板药物相关性脑出血患者具有出血量大、凝血功能障碍、预后差、病死率高等特点。在临床实践中,早期积极纠正凝血功能障碍,对患者全身情况开展综合评估,针对性选用诊疗方案,积极改善患者预后。
