基于增强CT特征的列线图模型在预测胃肠道间质瘤危险度分级中的价值
2022-05-05储海瑞张群峰郭东闯何剑郑屹峰吴晓
储海瑞 张群峰 郭东闯 何剑 郑屹峰 吴晓
胃肠道间质瘤(gastrointestinal stromal tumor,GIST)发病率及术后复发率均较高,有潜在恶性倾向,易向肝脏、腹腔内转移[1]。有研究表明,危险度较低的肿瘤可通过手术完整切除,而危险度高的肿瘤复发率和转移率明显增高,需要接受不同程度的伊马替尼辅助治疗[2-3]。因此,术前对GIST进行正确的诊断及危险度分级,对治疗方案的选择以及患者预后具有重要意义。增强CT检查操作简便易行,可在术前为肿瘤评估提供较全面的信息,且能避免活检取材造成的肿瘤破裂出血、腹腔种植等风险[4]。但常规CT检查的应用价值仅局限在定位、鉴别诊断及粗略评估,而列线图可进行个体化预测评分,并将预测结果直观、精准地呈现出来,在现代医疗决策中发挥重要作用[5]。本研究建立列线图模型,旨在探讨其在基于增强CT征象的术前预测评估GIST危险度分级中的应用价值,现报道如下。
1 对象和方法
1.1 对象 回顾2017年1月至2021年6月湖州市中心医院收治且符合以下标准的GIST患者135例。纳入标准:(1)病理检查证实为GIST患者,且有术前多期增强CT检查资料;(2)在增强CT检查前,目标病灶没有接受过任何治疗(包括手术、穿刺活检、放疗、化疗或激素治疗等);(3)CT图像质量佳,无伪影,病灶显示清晰。排除标准:(1)病理分级不明确;(2)肿瘤最大径<0.5 cm或>10 cm;(3)病灶破裂。根据美国国立卫生研究院(NIH)制订的病理分级标准及临床治疗策略[3],分为潜在恶性组和恶性组。其中潜在恶性组74例(极低危险度43例,低危险度31例),男31例,女43例,平均发病年龄(59±10)岁;恶性组61例(中危险度24例,高危险度37例),男29例,女32例,平均发病年龄(60±12)岁。两组患者性别、发病年龄的比较差异均无统计学意义(均P>0.05)。本研究经湖州市中心医院医学伦理委员会批准。
1.2 增强CT检查方法 采用日本东芝Aquilion One 320排CT仪进行腹部常规平扫及多期增强扫描,扫描参数:管电压120 kV,管电流150 mAs,扫描层厚0.5 mm,重建层厚5 mm,层间距2 mm;在肘静脉埋置18 G静脉留置针,采用双通道高压注射器,以2.5 ml/s速率注入非离子型对比剂碘佛醇,注射剂量为1.5 ml/kg。
1.3 图像分析与数据测量 由2位放射科高年资主治医师在不知病理检查结果的情况下独立阅片,对肿瘤的CT征象进行测量评估并记录,记录结果不一致时共同协商达成一致。纳入研究的分类影像特征包括肿瘤部位(胃、小肠)、生长方式(腔内、腔外、跨壁)、肿瘤内有无液化坏死、有无钙化、肿瘤边界是否清晰、肿瘤形态(类圆形或不规则)、强化方式(均匀或不均匀)、强化程度(以平扫期CT值为标准,静脉期强化程度<20 Hu为轻度强化,20~40 Hu为中度强化,>40 Hu为明显强化);计量影像特征包括肿瘤最大径、平扫期CT值、动脉期CT值、静脉期CT值,测量3次后取平均值。测量CT值时,绘制感兴趣区(region of interest,ROI)需避开肿瘤液化坏死及钙化区域。
1.4 统计学处理 采用SPSS 21.0和R 3.6.1统计软件。采用Shapiro-Wilk检验计量资料是否符合正态分布,正态分布的计量资料以±s表示,组间比较采用两独立样本t检验;非正态分布的计量资料以M(P25,P75)表示,组间比较采用Mann-Whitney U检验。计数资料组间比较采用χ2检验。采用多因素logistic回归分析预测GIST危险度分级的独立危险因素,并将差异有统计学有意义的指标导入R 3.6.1软件,采用“rms”包构建列线图预测模型。绘制ROC曲线评估预测模型的诊断效能,计算AUC,越接近1代表诊断效能越高。采用校准曲线比较预测概率和实际概率评估预测模型的拟合度,两者越接近,模型的拟合度越好。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者增强CT征象的比较 两组患者的肿瘤最大径、部位、生长方式、边界、形态、液化坏死、强化方式、静脉期CT值比较差异均有统计学意义(均 P<0.05),其余特征差异均无统计学意义(均P>0.05),见表1。典型病例见图1、2。
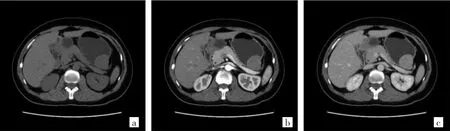
图1 52岁女性低危险度胃肠道间质瘤患者增强CT检查图像(a:平扫期见胃底部类圆形肿瘤,肿瘤最大径约4.1 cm,跨壁生长,无钙化及囊变;b:增强后动脉期肿瘤轻度强化;c:静脉期肿瘤明显均匀强化)
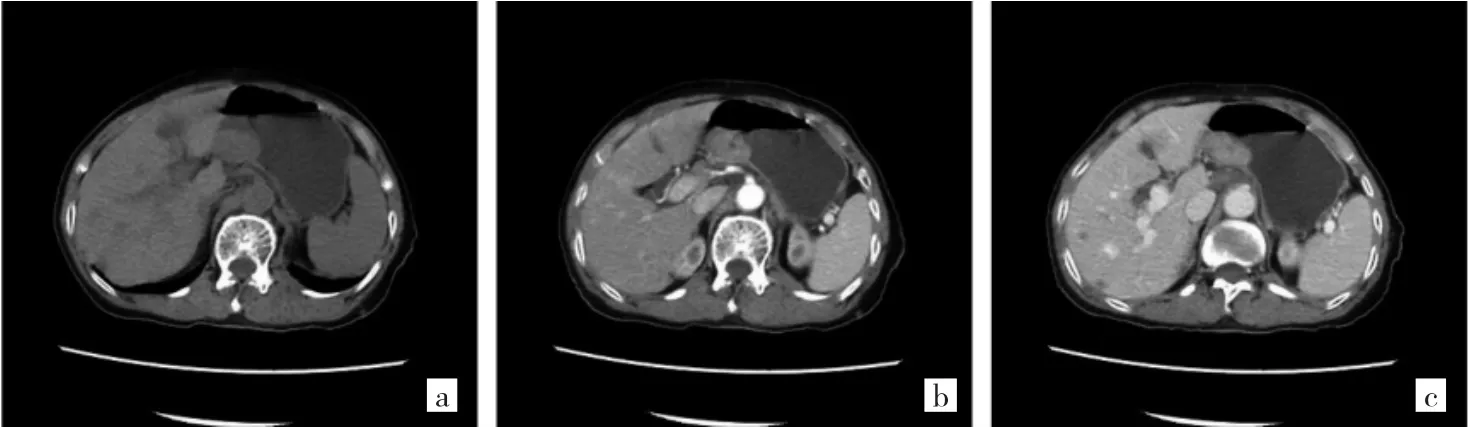
图2 61岁女性高危险度胃肠道间质瘤患者增强CT检查图像(a:平扫期见胃窦部类圆形肿瘤,肿瘤最大径约4.5 cm,跨壁生长,伴囊变,无钙化;b:增强后动脉期肿瘤轻度强化;c:静脉期肿瘤明显均匀强化)
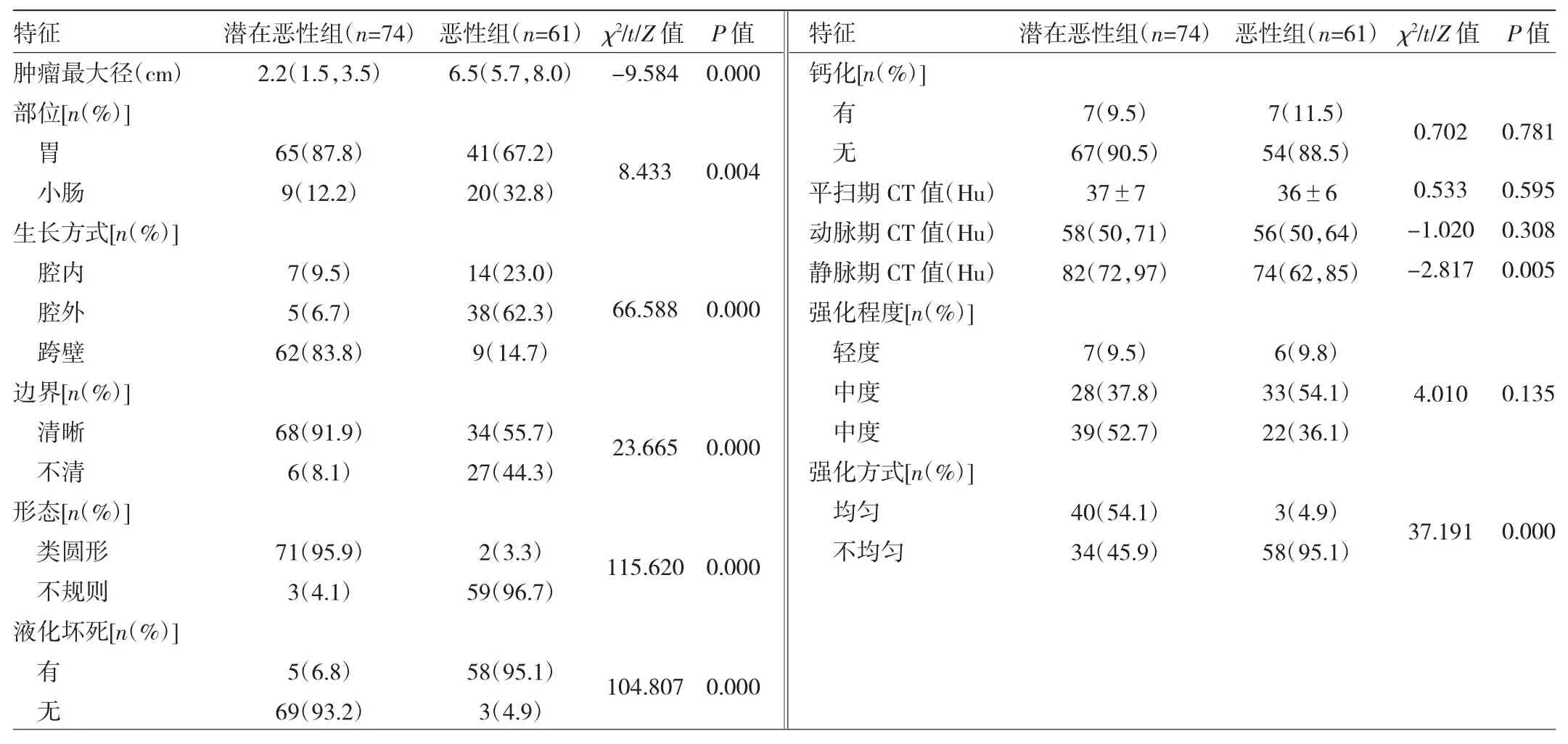
表1 两组患者增强CT征象的比较
2.2 多因素logistic回归分析结果及列线图模型的构建与评估 将差异有统计学意义的特征纳入多因素logistic回归分析,最终筛选出肿瘤最大径、形态及液化坏死是预测GIST危险度的独立危险因素,见表2。将3个特征构建列线图模型(图3),根据肿瘤最大径、形态及液化坏死情况对应图上方分数标尺上的位置获得评分,然后计算3个特征的评分和总分,总分所对应的下方预测风险值越接近0表示越倾向于潜在恶性,反之则表示越倾向于恶性。预测模型的校准曲线显示预测曲线与标准基本贴合(图4)。预测模型的AUC为0.952,灵敏度0.950,特异度0.833,说明预测模型具有良好的诊断效能(图5)。
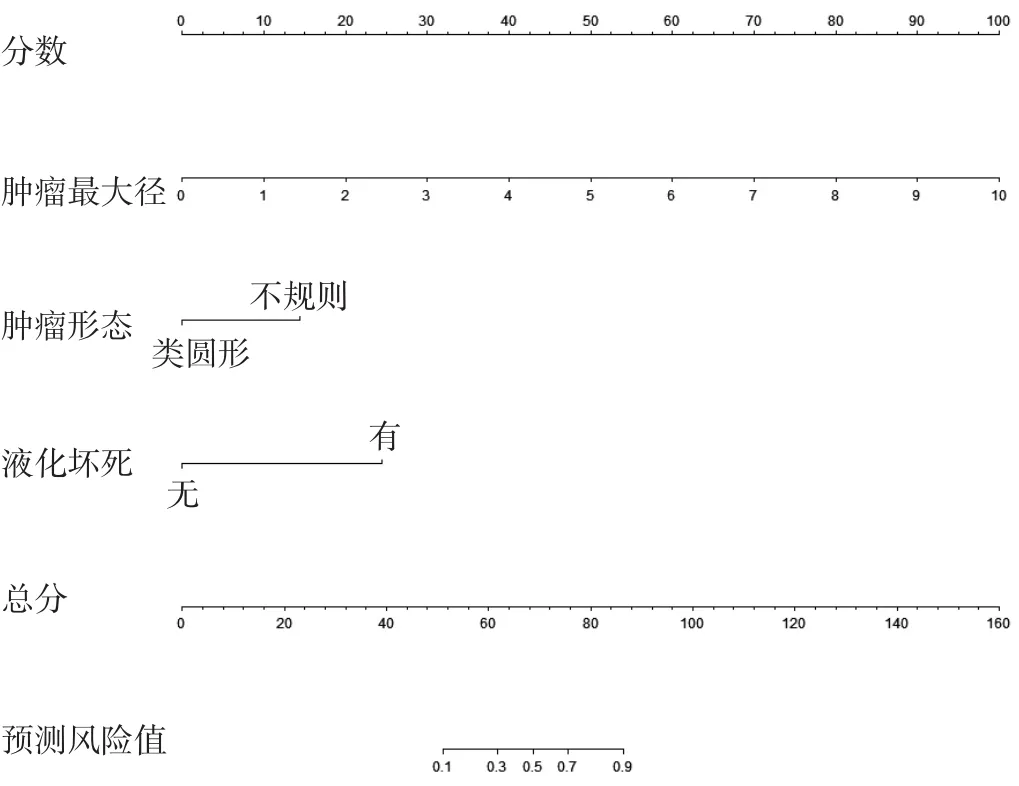
图3 用于预测胃肠道间质瘤危险度分级的列线图
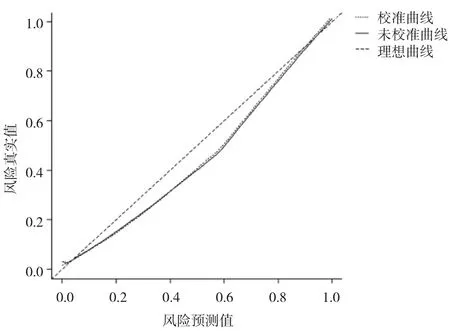
图4 列线图模型的校准图[校准曲线与理想曲线拟合度良好(Bootstrap自抽样,B=150)]
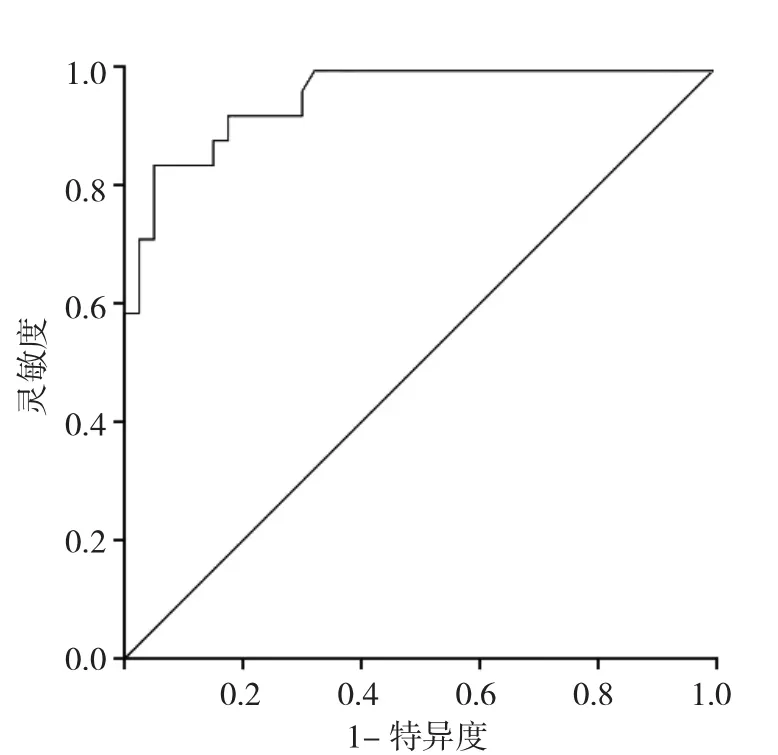
图5 预测模型诊断胃肠道间质瘤危险度分级的ROC曲线
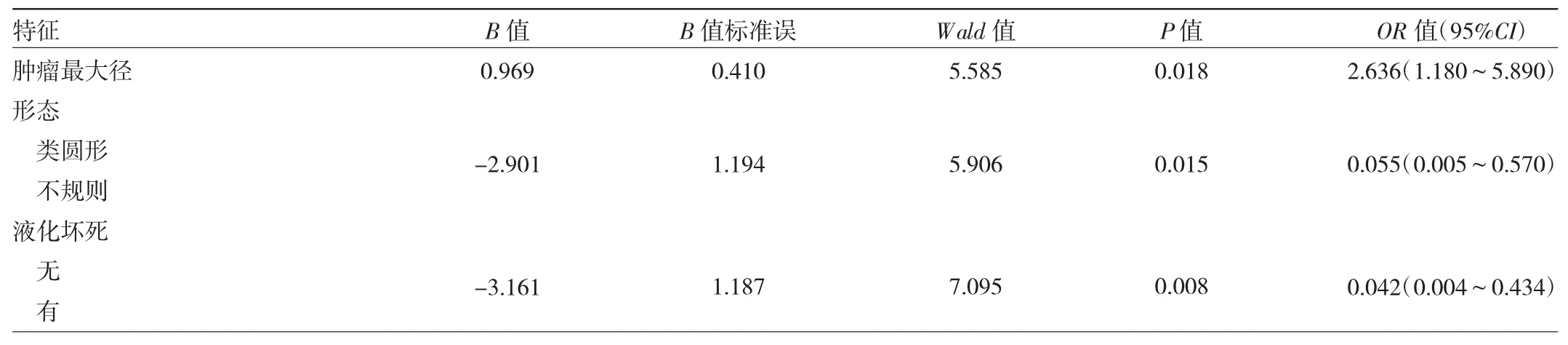
表2 两组患者的增强CT特征差异多因素logistic回归分析
3 讨论
GIST是消化道最常见的间叶组织来源的肿瘤,肿瘤不论大小均具有恶性潜向[6]。Nilsson等[7]及Tateishi等[8]研究结果显示,高、中危险度GIST患者的复发率及死亡率明显高于危险度较低的GIST患者。GIST主要以手术切除为主要治疗手段,对于极低危险度和低危险度GIST有机会选择创伤小、术后恢复快、并发症少的微创手术[9];雷程等[10]通过一项回顾性队列研究发现,对高危险度的GIST患者进行术前伊马替尼辅助治疗可降低肿瘤术中破裂出血的风险;还有研究表明患者在术前接受伊马替尼治疗且疗效最大化后可减小手术切除范围[11];另外高危险度GIST患者需在手术后接受不同程度的伊马替尼辅助治疗[12]。由此可见,术前对GIST进行正确的诊断及危险度分级对辅助临床制订治疗方案具有重要意义。然而部分研究及诊疗共识中提到,不适当的术前活检会造成肿瘤破溃、出血及肿瘤播散的风险[13-15]。
随着医学影像技术的日益发展,CT检查被越来越来越广泛地应用于胃肠道肿瘤的诊断。增强CT扫描操作简便、无创,能清晰显示GIST的发生部位、肿瘤最大径、形态、密度、生长方式、钙化、液化坏死、瘤内气体及迂曲血管、与邻近组织的关系等[16]。近年来多项研究表明,CT检查对GIST危险度分级具有重要的参考价值[17]。本研究结果显示潜在恶性组中肿瘤相对较小,多发生于胃,跨壁生长方式多见,肿瘤内发生液化坏死少见,多数呈类圆形,边界一般较清晰,增强后强化均匀且明显;恶性组中肿瘤一般较大,多数最大径>5 cm,小肠多见,多数向腔外生长,绝大部分肿瘤可发生液化坏死,肿瘤形态不规则,多呈扁平状或分叶状,部分肿瘤边界模糊不清,增强后由于肿瘤内部发生液化坏死,故强化不均,实性部分强化方式多样,以中至重度强化多见。由此可见,增强CT在GIST的术前诊断中发挥重要价值。
列线图作为一种个体化预测方法,能将结果可视化[18],已被广泛运用于多种疾病的鉴别诊断及预后预测[19-21]。在既往相关研究中,形态不规则被认为是由肿瘤向不同方向的增殖速率不同而引起的,并与恶性行为有关[22]。随着恶性程度增加,肿瘤分化和增殖速度加快,肿瘤体积快速增大,肿瘤内部供血不足,从而导致坏死的可能性增加[23]。上述研究表明肿瘤最大径、生长形态及内部液化坏死等特点能够反映肿瘤内部异质性,与肿瘤危险度密切相关。本研究发现,增强CT图像中显示的肿瘤最大径、形态及液化坏死是预测GIST危险度的独立危险因素。利用这3个特征构建的用于预测GIST危险度分级的列线图模型AUC值高达0.952,在校准曲线图中预测曲线与标准曲线拟合度良好,说明该预测模型具有良好的诊断效能且稳定可靠。
然而,本研究为回顾性研究,样本存在选择性偏倚,样本量不够大,且来自单中心,仅在两组间进行对比分析,缺乏外部验证。这些局限性有待今后进一步研究加以完善。
综上所述,GIST肿瘤越大、形态不规则、合并液化坏死则提示危险度高。根据肿瘤最大径、形态及液化坏死建立的列线图模型可通过简易评分对GIST危险度进行术前个体化精确预测,具有良好的预测效能。
