对1例使用克唑替尼进行治疗的MET突变型晚期肺腺癌病例的报道
2022-04-21杨雨佳蔡鑫翼廖天天祝朝富
赵 青,张 哲,杨雨佳,蔡鑫翼,廖天天,祝朝富★
(1. 成都中医药大学附属医院肿瘤内科,四川 成都 610075 ;2. 云南中医药大学,云南 昆明 650504)
肺癌是目前全球发病率最高的癌症。近年来,随着靶向治疗的广泛应用,肺腺癌的治疗效果得以显著提升。克唑替尼作为一种口服小分子TKI靶向药物,主要用于ALK 融合及ROS1 融合非小细胞肺癌的治疗。本文报道的病例是一位肺腺癌伴椎体转移MET 基因突变的患者,与患者及家属充分沟通后,对患者进行了6 个周期的单药培美曲塞二钠化疗( 静脉滴注,0.7 g/ 次,1 次/3 周)。但治疗后患者的病情加重,随后其自行购买克唑替尼进行靶向治疗,取得了较为理想的效果。
1 病例资料
患者女,60 岁,2018 年受外伤后常规行胸部、腰椎CT 发现左肺上叶占位及L2椎体压缩性骨折。住院后行L2椎体穿刺活检,病理查见异性细胞,考虑为恶性肿瘤细胞。结合临床CT 肺部占位特点考虑肺部来源的可能。为进一步明确诊断,患者于2018 年11 月行CT 引导下左肺占位穿刺活检术+ 微波消融术+ 腰椎骨水泥注入术,术后免疫组化检查提示:肿瘤细胞Ki67(+,约40%)、TTF-1(+++)、CK7(++)、P63(-)、P40(-)、PDL1(+)、CK20(-)、Pgp(++)、GSTπ(-)、TS(+)、TOPOII(+,2 级 )、MRP(+)、Syn(-)、Cga(-)、CD56(-)。结合患者的实际情况,建议其进行肺癌靶向基因检测[1-2],结果显示其存在MET 突变基因。反复与患者沟通后,其仍然拒绝一切系统治疗。2019 年3 月,患者出现不明原因的乏力,活动后加重,行PET/CT 检查提示:1)左肺上叶前段不规则软组织占位,代谢增高,倾向于肺癌;2)左肺门淋巴结增大,摄取增高,考虑为左肺门淋巴结转移;3)L2椎体骨质呈压缩性改变,内见高密度填充影,鉴于患者有腰椎骨折及骨水泥治疗史,具体应结合专科情况;4)双侧髂骨见高密度结节影,随访排除转移。沟通后,结合患者及家属意见,进行单药化疗,从2019 年3 月至2019 年7 月共进行了6 周期的培美曲塞二钠静脉单药化疗( 静脉滴注,0.7 g/ 次,1 次/3 周),化疗过程顺利,期间复查提示病情稳定。2019 年8 月复查胸部CT 提示局部病灶进展(见图1),建议患者换方案继续进行化疗或到外院进行局部放疗,患者拒绝继续化疗后出院。结合既往基因检测结果,患者2019 年8 月21 日于院外自行购买克唑替尼进行口服靶向治疗(250 mg/ 次,2 次/d)。2019年9 月复查CT 提示PR(见图2),之后2 ~3 个月复查一次,2020 年4 月复查提示SD(见图3)。患者继续院外口服克唑替尼进行靶向治疗。2020年10 月及2021 年1 月复查均提示SD(见图4、图5)。服药期间,患者未出现明显的不良反应。患者从2019 年8 月开始口服克唑替尼进行治疗至今。据统计,采用克唑替尼进行治疗的c-MET 突变晚期肺腺癌患者的中位无进展生存期约为7.4个月[3]。本例患者的无进展生存期已达17 个月,且目前仍在继续随访中。
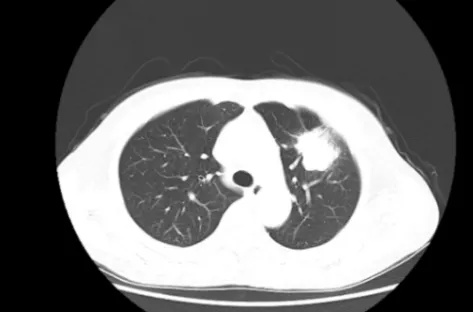
图1 2019 年8 月15 日患者的胸部CT 影像
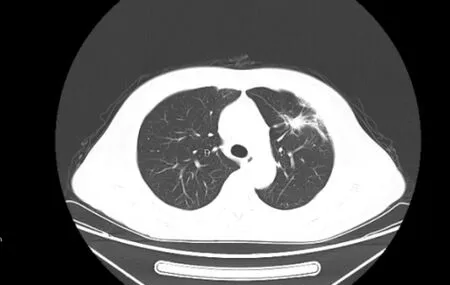
图2 2019 年9 月27 日患者的胸部CT 影像
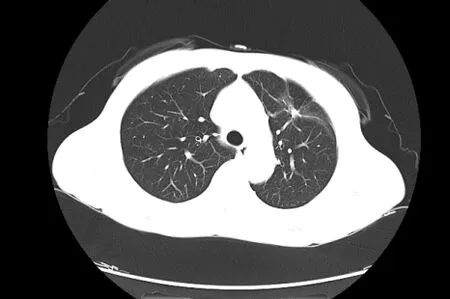
图3 2020 年4 月7 日患者的胸部CT 影像
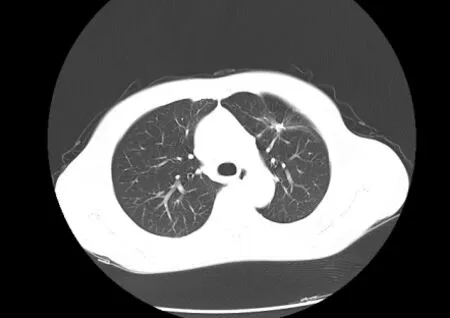
图4 2020 年10 月13 日患者的胸部CT 影像
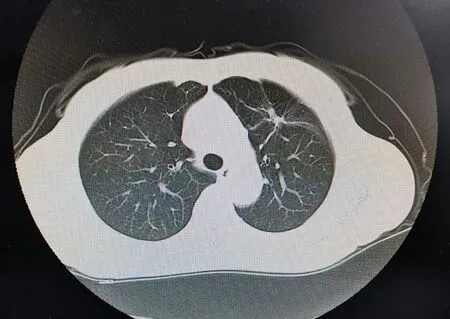
图5 2021 年1 月26 日患者的胸部CT 影像
2 讨论
目前,全世界范围内肺癌的发病率和致死率均居高位。2020 年,全球约有1930 万例新发癌症病例和近1000 万例癌症死亡病例,其中肺癌的发病率及肺癌患者的病死率分别为11.4%、18%[4]。近年来,随着分子靶向治疗学相关研究的不断深入,精准、个体化的靶向治疗在临床上得到了广泛的应用。MET 基因是非小细胞肺癌的肿瘤驱动基因之一。吴一龙[5]的研究发现,有0.9%的中国肺腺癌患者存在MET 14 外显子突变。MET 14 外显子编码的蛋白质c-Met 是肝细胞生长因子(hepatocyte growth factor,HGF)的酪氨酸激酶受体,它与肝细胞生长因子结合后可调控细胞的生长、增殖、迁移及对血管的侵袭[6-7]。在正常情况下,它能够促进正常组织的生长、修复,一旦发生突变,调节不受控制后,就可变成肿瘤细胞的驱动基因,从而促进肿瘤的增殖与转移。与MET 基因相关的基因异常状态主要包括MET 14 外显子跳跃突变、MET 基因扩增和蛋白过度表达三种情况。有研究显示,出现中、高度MET 基因扩增现象的晚期非小细胞肺癌患者其使用克唑替尼进行治疗的有效率为41.7%,其普遍能够耐受克唑替尼,且不良反应亦在可接受的范围内[8]。但上述研究结果尚缺乏大样本临床研究的支持。有研究表明,存在MET 14 外显子突变的晚期非小细胞肺癌患者使用克唑替尼进行治疗的效果较好,但目前尚无法确认MET 14 外显子突变是否是其取得显著疗效的主要原因[9]。根据作用位点的不同可将靶向治疗药物分为三大类,即抗HGF单克隆抗体药物、抗c-Met 单克隆抗体药物和小分子TKI 药物。其中小分子TKI 药物是目前临床上研究的重点,而克唑替尼属于多靶点的小分子TKI 药物,其主要作用于ALK、ROS1、MET 等[7]。此药于2013 年1 月由国家食品药品监督管理总局(CFDA) 批准用于对ALK 阳性的晚期非小细胞肺癌患者进行治疗[10]。目前,此药主要用于Ⅳ期ALK 融合非小细胞肺癌的治疗及Ⅳ期ROS1 融合非小细胞肺癌的治疗[11]。对于MET 突变是否能够成为下一个精准治疗的靶点,临床上还需要进一步探究。有研究指出,随着靶向治疗技术的发展,MET 基因突变将会成为非小细胞肺癌重要的治疗靶点。2020 世界肺癌大会线上会议中专门设置了“靶向治疗MET”专题,并发布了有关MET 基因异常流调、检测和治疗的最新数据。其中全球Ⅱ期临床研究GEOMETRY Mono-1(NCT02414139)的结果显示,用卡马替尼对亚裔MET Ex14 跳跃非小细胞肺癌患者进行治疗的效果确切,且安全性较高。Ⅱ期VISION 研究(NCT02864992)的结果显示,Tepotinib 可使脑转移患者的病灶缩小。目前,可作用于MET 的靶向药物有克唑替尼、卡博替尼、沃利替尼(赛沃替尼)、Tepotinib、Capmatinib、Glesatinib、Merestinib 等[12]。在 今年6 月22 日,赛沃替尼作为国内首个MET 抑制剂已经获批上市。最新的临床研究显示,用赛沃替尼进行治疗的70 例存在MET 外显子14 跳跃突变的晚期肺癌患者其治疗后病情的客观缓解率为42.9%,病情控制率为82.9%,中位病情缓解持续时间为8.3 个月,其中7 例患者(10%)的病情缓解持续时间至少达到了12 个月。治疗后,这些患者的中位无进展生存期为6.8 个月,其治疗后6 个月和治疗后12 个月的无进展生存率分别为52% 和31.9%,其中位总生存期(OS)为12.5 个月[13]。据统计,使用克唑替尼进行治疗的MET 突变型晚期肺腺癌患者其治疗后的中位无进展生存期为7.3 ~7.4 个月,其常见的不良反应包括视力障碍、转氨酶升高、腹泻、恶心等。相关的研究表明,用克唑替尼治疗MET 突变型晚期肺腺癌可取得较为理想的效果[3,14-15]。
综上所述,使用克唑替尼治疗MET 突变型晚期肺腺癌的效果较好,且安全性较高。
