基于GC-MS和LC-MS的人参冰酒成分分析
2022-03-16吴泳锡张美玉王一竹李方彤戴雨霖
吴泳锡,张美玉,王一竹,李方彤,刘 明,戴雨霖,郑 飞,越 皓
(长春中医药大学,吉林省人参科学研究院,吉林 长春 130117)
长白山道地药材人参(PanaxginsengC.A.Mey.)可作药食两用,具有机体免疫调节作用,近年来,人参功能性食品的多元化深加工产品成为研究热点。本实验室的人参冰酒以鲜人参、威代尔葡萄为原料,采用低温发酵技术,通过鲜人参和威代尔葡萄特定比例进行配伍,定向转化生成Rg2、Rf、Rg3、Rg5、CK等稀有皂苷,显著提高了生物利用度,并通过陶瓷膜过滤技术,使酒体晶莹剔透、入口细腻圆润、余味绵长,具有缓解疲劳、舒张血管、增强免疫力等作用。
Huang等[1]对中国和加拿大不同区域的冰酒进行感官分析,通过4种方法比较香气组分差异,发现中国产区略带坚果蜂蜜香气,加拿大产区略带玫瑰焦糖香气。乔梦丹等[2]通过超高效液相色谱-四极杆静电场轨道阱高分辨质谱法(UPLC-Q-Orbitrap-HRMS)比较人参发酵前后的皂苷类化合物成分,共检测出45种人参皂苷。Dimitrios等[3]通过核磁共振(NMR)、靶向及非靶向的LC-MS和GC-MS比较葡萄酒代谢组学特征,结果表明,NMR效果最差,而靶向GC-MS效果显著,具有足够的辨别代谢显著差异的能力。
人参冰酒的香气成分及非挥发性成分能够反映葡萄酒的质量及生产工艺等,利用LC-MS以及GC-MS研究人参冰酒的成分特点,对其质量控制和技术开发具有重要意义。基于此,本文拟采用气相色谱-三重四极杆质谱(GC-QQQ-MS/MS)和UPLC-Q-Orbitrap-HRMS技术分析人参冰酒的挥发性成分、酚类和人参皂苷类成分,旨为人参冰酒的质量标准提供技术支持,同时为进一步合理开发人参冰酒提供理论支撑。
1 实验部分
1.1 仪器与装置
TRACE 1310气相色谱仪、TSQ 8000三重四极杆质谱仪、Thermo Scientific Q-Exactive四极杆静电场轨道阱高分辨质谱仪、Dionex UltiMate 3000超高效液相色谱仪:美国Thermo Fisher公司产品;BT25S型分析天平:北京赛多利斯科学仪器有限公司产品。
1.2 材料与试剂
人参冰酒:长春方飞生物科技有限公司产品;甲醇、乙腈、甲酸:均为色谱纯,美国Tedia公司产品;超纯水:由德国Milli-Q超纯水系统制备;绿原酸、新绿原酸、隐绿原酸、没食子酸、龙胆酸、槲皮素、木樨草素、表没食子儿茶素、二氢槲皮素、人参皂苷(Re、Rf、Rd、Rb1、Rg1、F2、CK)标准品:纯度>98%,上海源叶生物科技有限公司产品。
1.3 样品制备
1.3.1GC-MS样品制备 取1 mL人参冰酒,过0.45 μm微孔滤膜,密封状态下,35 ℃水浴15 min,气相色谱直接进样。
1.3.2LC-MS样品制备 取50 mL人参冰酒,加入等量的水饱和正丁醇萃取4次,40 ℃水浴挥干溶剂,加入甲醇复溶,定容至10 mL,过0.45 μm微孔滤膜,得样品溶液。
1.4 实验条件
1.4.1挥发性成分的GC-MS测定 色谱条件:DB-Heavy WAX色谱柱(30 m×0.25 mm×0.25 μm);进样口温度250 ℃;载气为高纯氦气(He),纯度99.9%;流量1 mL/min;进样量1 μL;进样方式1∶20;程序升温:初始温度30 ℃,保持2 min,以4 ℃/min升至230 ℃,保持5 min。
质谱条件:三重四极杆串联质谱仪检测,电子轰击源(EI),离子源温度250 ℃,传输线温度250 ℃,质量扫描范围m/z50~550。
1.4.2非挥发性成分的LC-MS测定 色谱条件:Sigma HPLC Column C18色谱柱(500 mm×3.0 mm×2.7 μm);流动相A为0.1%甲酸水,B为乙腈;洗脱条件:0~10 min(5%B),10~15 min(10%B),15~18 min(15%B),18~20 min(20%B),20~21 min(25%B),21~22 min(30%B),22~25min(30%~35%B),25~30 min(35%B),30~35 min(40%~60%B),35~38 min(60%~80%B),38~40 min(80%~100%B),40~45 min(100%B),45~50 min(100%~5%B),50~60 min(5%B);流速0.2 mL/min;进样量5 μL;柱温30 ℃。
质谱条件:四极杆-静电场轨道阱高分辨质谱,电喷雾离子源(ESI)正、负离子模式检测,干燥气温度350 ℃,鞘气流速4×106Pa,辅助气流速1×106Pa,辅助气温度300 ℃,Full scan-ddMS2扫描模式,分辨率70 000 FWHM,质量扫描范围m/z150~2 000。
2 结果与讨论
2.1 GC-MS测定挥发性成分
根据美国国家标准技术研究所标准谱库中的保留指数和质谱信息分析挥发性成分。对已有标样的物质, 利用其对应的标准曲线定量;对没有标样的物质,利用化学结构、官能团相似、碳原子数相近的标样香气物质的标准曲线定量。按照峰面积归一化法,计算各组分的相对含量。
人参冰酒的GC-MS总离子流图示于图1,共检测出28种挥发性物质,包括8种酸类、4种酯类、6种醇类、3种醛类、7种其他类,列于表1。其中,酸类物质占挥发性总物质数量的28.6%,是人参冰酒含量最高的风味化合物;有15种成分的相对含量大于0.5%,为人参冰酒的主要香气贡献成分。
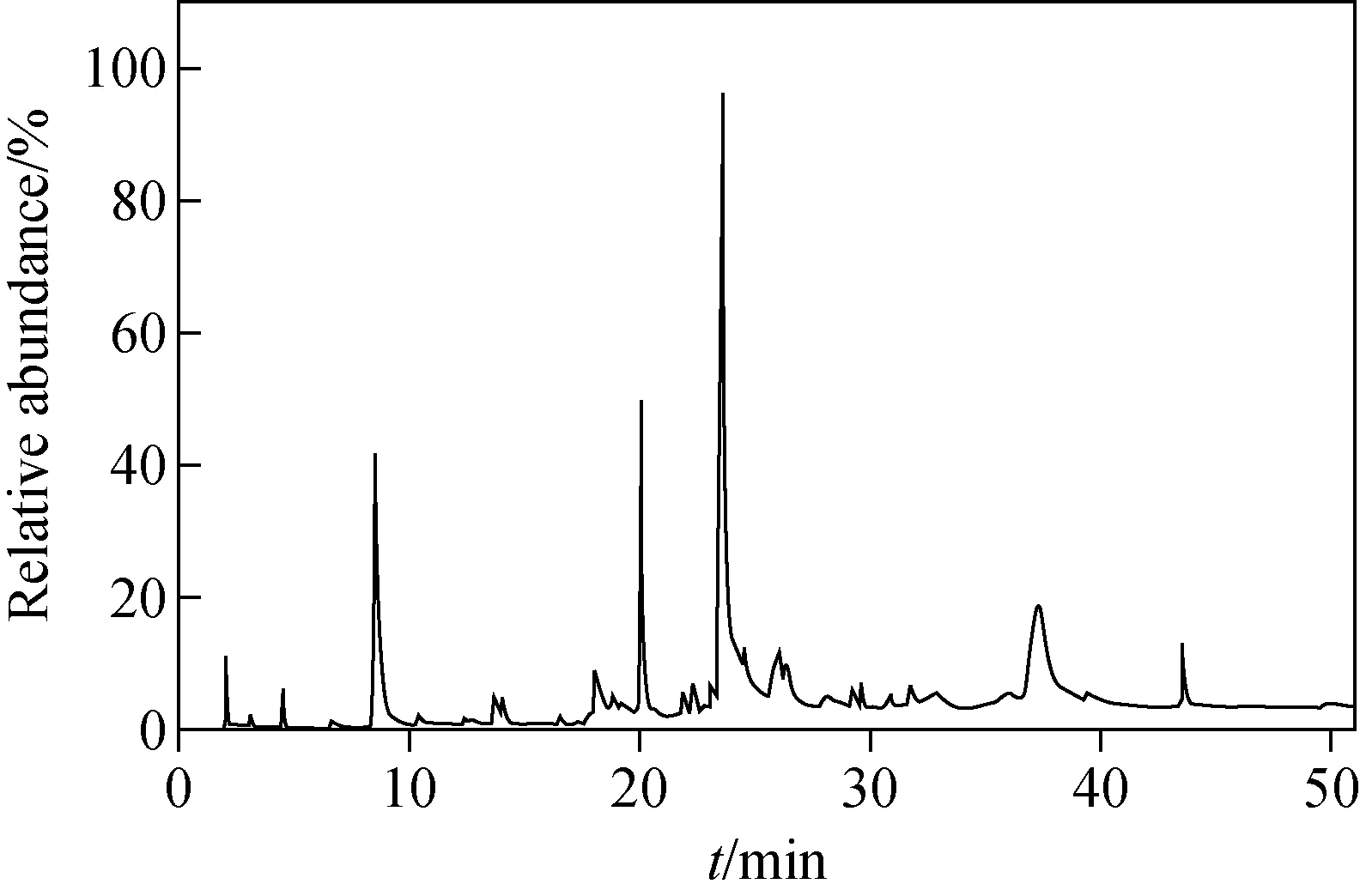
图1 人参冰酒GC-MS总离子流图Fig.1 Total ion chromatogram of ginseng ice wine by GC-MS

表1 28种挥发性化合物的GC-MS分析Table 1 Analytical parameters of GC-MS for 28 aromatics
人参冰酒产生的香气主要包括葡萄自身的香气、发酵过程产生的发酵香气和陈酿过程产生的香气及橡木香气[4]。香气成分不仅与葡萄品种有关,还与酿酒工艺[5]、陈酿时间[6]以及贮存条件有关。
2.1.1酸类物质分析 人参冰酒在发酵过程中,因醇的氧化或酵母代谢产生酸类物质。本实验共检测到8种酸类物质,分别为乙酸、辛酸、曲酸、4-甲基辛酸、间苯三酚甲酸、蓖麻油酸、棕榈酸和十五酸。乙酸具有酸味;辛酸具有奶酪、脂肪味;棕榈酸具有香料味。其中,4-甲基辛酸含量最高,相对含量为1.20%。少量酸类物质使香气成分更强,从而提高人参冰酒的品质。
2.1.2醇类物质分析 醇类是人参冰酒第二大类挥发性物质,主要由于酒精发酵与氨基酸转化,同时也可能受到葡萄自身含糖量及pH值等影响。本实验共检测到6种醇类物质,分别为正戊醇、2,3-丁二醇、3-呋喃甲醇、丙三醇、豆蔻醇和(Z)-十八-9-烯醇,占总香气的21.4%。其中,正戊醇具有醇香,(Z)-十八-9-烯醇的相对含量较高,为1.84%。
2.1.3酯类物质分析 酯类物质主要由于贮藏过程中的酯化反应、发酵过程中产生以及葡萄本身的酯类成分。本实验共检测出4种酯类物质,分别为乙酸乙酯、2-糠酸甲酯、十二烷二酸二甲酯和2-氯苯基硫代异氰酸酯,占总香气的14.3%。其中,乙酸乙酯具有果香、醋味;2-氯苯基硫代异氰酸酯的相对含量较高,为1.56%。
2.1.4醛类物质分析 醇的氧化或酸的还原生成醛类物质。在人参冰酒中共检测到3种醛类物质,分别为3-糠醛、苯丙醛和苯乙醛,占总香气的10.7%。其中,苯乙醛具有花香气味;3-糠醛的相对含量最高,为8.12%,具有特殊的香气。
2.1.5醚类及其他物质分析 在人参冰酒中只检测出三乙二醇单丁醚1种醚类物质,占总香气的3.6%,相对含量为1.42%。
2.1.6其他类成分 在人参冰酒中共检测到6种其他类成分,分别为氟乙酰胺、1,3,5-三甲基吡唑、对苯二酚、1-萘酚、间苯三酚和2-萘酚。间苯三酚含量最高,相对含量为41.31%。人参冰酒中芳香族物质相对含量较高,主要呈花果香,同时酚类物质对人参冰酒产生的苦味有影响[7]。
2.2 LC-MS测定非挥发性成分
在正、负离子模式下采集的人参冰酒总离子流图示于图2。在负离子模式下,共鉴定出19种多酚类和28种皂苷类成分,列于表2。其中,酚酸类成分包括有机酸类、类黄酮类和其他类成分。在正离子模式下,共鉴定出5种多酚类成分,列于表3。

图2 人参冰酒LC-MS正(a)、负(b)离子模式下的总离子流图Fig.2 Total ion chromatograms of ginseng ice wine in positive (a) and negative (b) ion modes of LC-MS
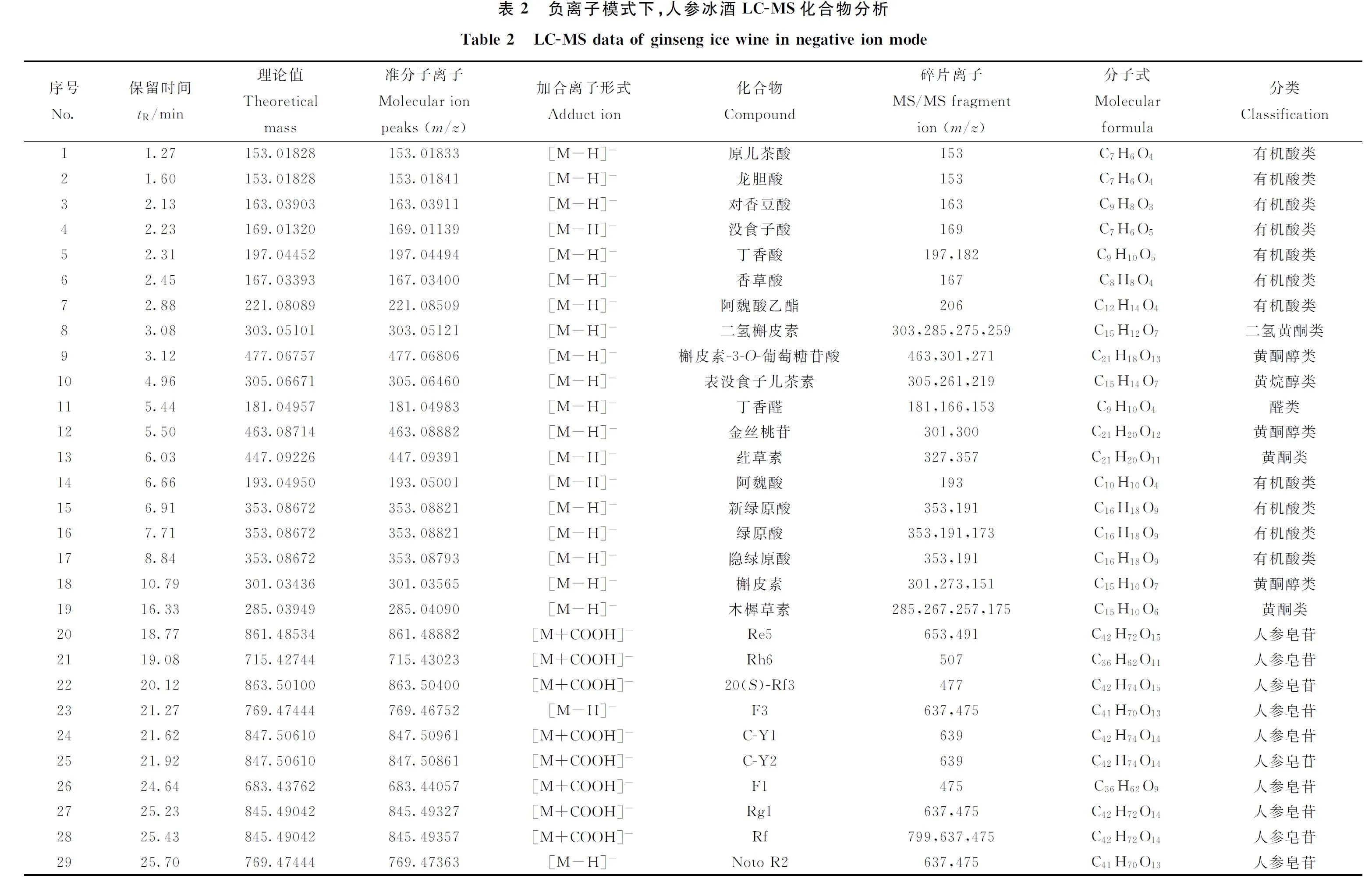

2.2.1多酚类物质分析 有机酸类物质分析:从人参冰酒中共鉴定出12种有机酸及其衍生物,在负离子模式下多以[M-H]-的形式存在。以化合物16为例,可检测到m/z353.100 9 [M-H]-准分子离子峰,碎片离子m/z191.466 5[M-H-H2O]-为脱去咖啡酰基生成,碎片离子m/z173.044 5为脱去1分子H2O生成。通过与标准品对比保留时间、碎片离子的种类和丰度,推断化合物16为绿原酸,裂解规律示于图3。同理,在负离子模式下鉴定出化合物1、2、3、4、5、6、7、14分别为原儿茶酸、龙胆酸、对香豆酸、没食子酸、丁香酸、香草酸、阿魏酸乙酯、阿魏酸;化合物15、17为化合物16的同分异构体,具有与其相同的裂解途径,通过与标准品比对,确定其分别为新绿原酸和隐绿原酸。在正离子模式下鉴定出化合物2为咖啡酰葡萄糖。

图3 绿原酸的裂解途径Fig.3 Fragmentation pathway of chlorogenic acid
黄酮苷元是多酚羟基化合物,具有微酸性,负离子模式下准分子离子[M-H]-丰度较高,一级质谱中碎片离子较少,有助于推断其分子质量。黄酮苷元在ESI-MS2谱中表现为丢失中性碎片CO(28 u)、H2O(18 u)、CO2(44 u),通过这些特征可判断其官能团取代情况,快速辨别同分异构体结构。当黄酮结构中羟基取代数目逐渐增多时,串联质谱中产生的碎片离子增多。黄酮醇苷元更易产生C环开环离子,而二氢黄酮苷元一般不丢失CO。同样,在黄酮类化合物中,3-O位与7-O位容易形成糖苷键,二级质谱中出现糖苷键均裂产物。
黄酮类物质分析:以化合物19为例,在负离子模式下其准分子离子峰为m/z285.040 9[M-H]-,通过与标准品比对,可知木樨草素的准分子离子为m/z285.039 4[M-H]-。碎片离子m/z267.072 7为木樨草素脱去1分子H2O形成;碎片离子m/z257.176 2为木樨草素脱去1分子羰基形成;碎片离子m/z175.958 8为木樨草素B环碎裂形成,其裂解规律示于图4。同理,可推断化合物13为荭草素。

图4 木樨草素的裂解途径Fig.4 Fragmentation pathway of luteolin
黄酮醇类物质分析:以化合物18为例,负离子模式下其准分子离子峰为m/z301.035 6[M-H]-,通过与标准品对比,可知槲皮素的准分子离子峰为m/z301.034 3[M-H]-。碎片离子m/z273.170 9为槲皮素脱去1分子羰基得到;碎片离子m/z151.039 0由黄酮类化合物最常见的RDA断裂形成。同理,可推断化合物9、12分别为槲皮素-3-O-葡萄糖苷酸和金丝桃苷。
黄烷醇类物质分析:以化合物10为例,负离子模式下其准分子离子峰为m/z305.064 6[M-H]-,通过与标准品对比,可知表没食子儿茶素的准分子离子峰为m/z305.066 7[M-H]-。碎片离子m/z261.134 6为表没食子儿茶素脱去1分子CO2得到;碎片离子m/z219.050 7为表没食子儿茶素裂解脱去C2H2O后得到。通过与标准品比对碎片离子信息和保留时间,可推断化合物10为表没食子儿茶素,其裂解规律示于图5。同理,在正离子模式下,推断化合物5为原花青素四聚体。

图5 表没食子儿茶素的裂解途径Fig.5 Fragmentation pathway of epigallocatechin
二氢黄酮类物质分析:以化合物8为例,负离子模式下其准分子离子峰为m/z303.051 2[M-H]-,通过与标准品进行对比,可知二氢槲皮素的准分子离子峰为m/z303.051 0[M-H]-。碎片离子m/z285.134 6[M-H-H2O]-为二氢槲皮素脱去1分子H2O产生;碎片离子m/z275.058 2[M-H-CO]-为二氢槲皮素脱去1分子CO产生;碎片离子m/z259.118 8[M-H-CO2]-为二氢槲皮素脱去1分子CO2产生。通过与标准品比对碎片离子信息并参考文献[8],可推断化合物8为二氢槲皮素。同理,在正离子模式下,可推断化合物4为二氢山奈酚-3-O-葡萄糖苷。
花色素类物质分析:在正离子模式下,花色素类成分通常较不稳定,易受光照或pH值改变而降解,通常以花色素C环上C3位羟基糖苷化的形式表现。结合保留时间及碎片离子信息并参考文献[9],推断正离子模式下化合物3为二甲花翠素-3-O-葡萄糖苷。
非黄酮类物质分析:在负离子模式下,通过查阅文献[10]发现,醛类化合物的基本裂解规律是以从醛基上脱去CO自由基为主,与羧酸类化合物的结构相近。以化合物11为例,负离子模式下其准分子离子峰为m/z181.049 83 [M-H]-,二级质谱下可检测到m/z166、153碎片离子,分别是由其母离子丢失中性碎片CH3、CO产生,因此,推测化合物11为丁香醛。在正离子模式下,化合物1的准分子离子峰为m/z229.068 5[M+H]+,二级质谱下可检测到m/z187碎片离子,是其母离子于苯环上2、3位和4、5位之间发生键断裂丢失中性碎片C2H2O产生;m/z145碎片离子为m/z187离子继续丢失1分子C2H2O得到。因此,推断化合物1为白藜芦醇。
人参冰酒的颜色受花色苷的B环取代基影响。在酸性条件下,当羟基增加时颜色变红,甲氧基增加时颜色变紫;咖啡酸对人参冰酒的颜色有一定影响[11];酚酸成分是人参冰酒非挥发性物质的重要组成成分,是调节香气的重要基础[12],对人参冰酒整体感官有很大的贡献。
已鉴定的多酚类物质中,白藜芦醇可以改善血管弹性[13],对骨损伤具有保护作用[14];木樨草素具有抗炎[15]、抗肿瘤[16];表没食子儿茶素对乳腺癌产生抑制作用[17-18];绿原酸可预防糖尿病[19-20]。多酚类化合物是人参冰酒潜在的活性物质基础,其活性机制需进一步研究。
2.2.2皂苷类物质分析 在人参冰酒中共检测出28种皂苷成分,负离子模式下皂苷主要以[M-H]-形式存在[21]。以化合物28为例,其碎片离子m/z845.493 5 [M+COOH]-为与流动相甲酸根结合而成;准分子离子m/z799.484 3[M-H]-、碎片离子m/z637.430 5和m/z475.376 6为位于C6位糖苷键相继裂解得到;碎片离子m/z391.898 2为三醇型皂苷母核脱去C20位烃基侧链而成。通过标准品的保留时间以及裂解规律可确定化合物28为人参皂苷Rf,其二级质谱图示于图6a,裂解途径示于图7。化合物27与人参皂苷Rf的一级质谱碎片离子m/z845.493 5 [M+COOH]-一致,在二级质谱下,两者均产生碎片离子m/z475和637。人参皂苷Rf在C6位裂解2个糖苷键,在25 eV轰击下,m/z475碎片离子丰度高于m/z637,证明人参皂苷Rf与C6位相连接的糖苷键较与葡萄糖相连接的糖苷键更容易碎裂;在50 eV轰击下,化合物27产生m/z475碎片离子,说明化合物27在C6位和C20位分别连接1个葡萄糖,推测为人参皂苷Rg1。经与对照品比对并结合保留时间,确认化合物27为人参皂苷Rg1。

图6 人参皂苷Rf(a),Rg3(b),Ro(c)的二级质谱图Fig.6 MS/MS spectra of ginsenoside Rf (a), Rg3 (b), Ro (c)

图7 人参皂苷Rf的裂解途径Fig.7 Fragmentation pathway of ginsenoside Rf
其他人参皂苷均有相似的裂解规律,通过参考文献[21],同时结合分子质量信息、中性碎片丢失和相对应的中性皂苷碎裂规律,得到化合物20~27、29~47分别为Re5、Rh6、20(S)-Rf3、F3、C-Y1、C-Y2、F1、Rg1、Noto R2、Rg2、Rh1、20(R)Rg2、20(R)Rh1、Ro、20(S)Rf2、Rc、Re、Rg7、F2、F4、Rh4/Rk3、Rg3、20(R)Rg3、Rk1、Rg5、Rh2、CK。人参皂苷Rg3、Ro的二级质谱图示于图6b,6c。人参皂苷Rg3对乳腺癌有抑制作用[22];Rh2具有抗炎、调节免疫作用[23-24];Re可缓解心脏衰竭[25];F2可调节酒精性肝损伤[26];CK可抑制骨肉瘤细胞的增殖[27]。
葡萄酒发酵过程为人参皂苷提供了酸性条件及糖类转化,进一步促进糖苷键断裂,使人参皂苷转化成稀有人参皂苷,同时部分稀有人参皂苷呈现出20(R),20(S)构型。稀有皂苷更利于人体吸收,提高生物利用度,同时具有较强的药理活性[28]。
3 结论
本研究利用UPLC-Q-Orbitrap-HRMS高分辨、定性准确的特点,鉴定了人参冰酒中24种多酚类物质和28种皂苷类成分,对人参冰酒中28种挥发性成分进行了鉴定及含量测定,并总结了化合物的裂解规律。该方法可为研究人参冰酒的化学成分提供快速、准确的方法,为人参冰酒的质量评价和进一步开发提供理论依据。
