PreCon-IRMS测定土壤游离氨基酸态氮稳定同位素丰度
2022-03-16袁红朝张丽萍耿梅梅许丽卫王久荣
贺 珍,袁红朝,张丽萍,耿梅梅,许丽卫,陈 闻,彭 灿,王久荣
(中国科学院亚热带农业生态过程重点实验室,湖南 长沙 410125)
土壤中有机氮通过微生物的矿化作用转化为铵态氮供给植物氮素营养需求,是土壤氮素循环和作物养分供给过程中重要的“库”和“源”[1-4]。作为土壤有机氮的代表性中间产物,氨基酸态氮在研究土壤肥力、循环机制和生物有效性等方面有着重要意义[5-6]。随着稳定同位素示踪技术在生态系统氮循环领域应用的不断拓宽和深入,氮稳定同位素示踪技术广泛应用于土壤氮循环研究[7-9]。土壤提取液中可溶性氮组分复杂,包括无机态氮,如铵态氮、硝态氮和亚硝态氮,以及可溶性有机氮,如氨基酸和少量氨基糖等[10-11]。因此,土壤游离氨基酸态氮同位素丰度的检测需要对样品进行前处理转化,其前处理方法的精确程度对质谱分析结果的准确度影响较大[12]。
目前,氨基酸类氮同位素测定方法主要有单个氨基酸的特定化合物同位素分析[13-14]和化学转化N2O产生法[15]。其中,单个氨基酸的特定化合物同位素分析涉及复杂的样品前处理过程,如气相色谱-燃烧-稳定同位素质谱(GC-C-IRMS)分析时涉及氨基酸的衍生化反应,而氨基酸类衍生化合物在室温下不稳定,且衍生物中碳氮比高,常引起色谱分析柱的过载和色谱峰共流出[14]。对于只针对土壤中游离氨基酸产生和消耗速率的研究,Noll等[15]发表了土壤游离氨基酸态氮化学转化为N2O测定氮同位素的方法,前处理方法为扩散法结合N2O产生法, 主要包括氨基酸的分离纯化和氨基酸态氮的化学转化两步骤。其原理为扩散法除去土壤提取液中的铵态氮后,氨基酸在Br-催化下由ClO-氧化生成NO2-[16],NO2-被NaN3还原生成N2O气体[17],用带自动预浓缩装置的稳定同位素质谱仪(PreCon-IRMS)测定N2O 中的15N 丰度。与单个氨基酸的氮同位素分析和间接法相比,该方法提高了样品通量,并在一定程度上简化了前处理步骤,但仍存在以下不足:1) 扩散法除去铵态氮需要2~3天,实验周期较长,且该过程存在氮同位素分馏,需要结果校正;2) 化学转化操作中使用NaN3还原NO2-生成N2O气体,涉及剧毒化学药品和反应中间产物,需要专用的仪器设备,操作过程相对复杂,易引入人为操作误差,导致测试结果不准确;3) NaN3还原NO2-生成N2O气体,从同位素分配角度看,形成N2O中的2个氮原子分别来自于亚硝酸盐(氨基酸态氮转化而来)和NaN3分子,因此,测得的N2O的15N丰度不是亚硝酸盐(氨基酸态氮)的15N丰度,需经公式换算,数据处理较繁琐。
针对以上问题,本研究拟在前期研究[15-22,24]基础上进行方法改进和测试条件优化,建立一种快速蒸馏法结合化学转化N2O的前处理方法,用带自动预浓缩装置的PreCon-IRMS测定土壤提取液中游离氨基酸15N丰度,并利用本实验室研制开发的自动化装置[23]替代原化学转化N2O中的部分人工操作,试验不同反应条件对氨基酸转化的N2O 产率的影响,明确最适宜的方法条件。以不同浓度和15N丰度的混合氨基酸标准溶液考察该方法对15N丰度测定的精密度和准确度,并通过加入混合氨基酸溶液到不同类型土壤中,验证该方法对实际土壤样品中游离氨基酸态氮稳定同位素丰度测定的适用性。
1 实验部分
1.1 方法原理
α-氨基酸态氮转化生成N2O:碱性条件下,次溴酸钠将氨基酸终端α-NH2裂解为NH4+,该反应被Br-催化,生成NH4+;真空条件下,NH4+继续与次溴酸钠反应,产生氮气和一部分N2O,该反应被Cu2+催化,并与pH值有关,可通过调节NaOH浓度改变反应体系的pH环境,提升次溴酸钠的氧化性能,从而提高N2O产率。涉及的化学反应为:

(1)

(2)
1.2 主要仪器与装置
Precon痕量气体预浓缩装置:T1~T3冷阱,Combi PAL自动进样器,96位气体样品盘,顶空瓶(12 mL),化学阱(填充高氯酸镁和碱石灰),poraPlot Q色谱柱,载气(氦气,纯度>99.999%);MAT253稳定同位素比质谱仪:高灵敏度电子轰击离子源,10 kV加速电压,C/N法拉第杯;质谱仪主机与外部设置系统控制、数据采集和处理:均由Isodat 3.0软件自动完成。以上仪器均为美国Thermo Fisher Scientific公司产品。XS3DU天平(百万分之一):瑞士梅特勒-托利多公司产品;干式恒温器(加热盘为64位,与12 mL顶空瓶匹配,控温范围为室温~150 ℃,精度1 ℃):杭州瑞诚公司产品。
全自动微量氮转化-N2O发生装置[23]:实验室自制(专利号:2018114796378),配备自动进样器、120位气体样品盘(与12 mL顶空瓶匹配)、自动气体置换及注入系统和自动加液系统等。
1.3 主要材料与试剂
氯化钾溶液(浓度1 mol/L),氧化镁(纯度≥99.5%),碱性次溴酸钠溶液(次溴酸钠溶液(含2 mmol/L Cu2+和10 mol/L氢氧化钠)):国药集团化学试剂有限公司产品;甘氨酸:纯度≥99%,上海源叶生物科技有限公司产品;混合氨基酸标准品A(20种氨基酸混标,15N丰度0.362 atom%)、混合氨基酸标准品B(20种氨基酸混标,15N丰度98 atom%):纯度≥99.5%,美国CIL剑桥同位素实验室公司产品;混合氨基酸标准溶液:将2种15N丰度的氨基酸标准品均配制成10 mmol/L的标准溶液A1和B1,再用低丰度标准溶液A1作为稀释剂,取一定量的标准溶液B1制备成15N丰度约为1.0 atom%和3.5 atom%的标准溶液C1和C2。使用元素分析仪-稳定同位素质谱(EA-IRMS)[17]测定标准溶液C1和C2的15N丰度(每个样品重复测定6次)作为参考值,分别为(1.01±0.02) atom%和(3.35±0.05) atom%,并用于后续的方法验证。N2O标准气体(浓度分别为0.300、1.50、3.00 μmol/mol):委托中国计量科学研究院国家标准物质研究中心制备。
土壤样品:采集于长沙农业环境观测研究站不同土地利用方式的稻田和旱地土壤,其基本理化性质列于表1。

表1 供试土壤基本信息 Table 1 Basic properties of tested soil
土壤提取液的制备:称取5 g经研磨过2 mm筛的土壤样品(土壤含水量30%),置于50 mL离心管中,加入500 μL标记的10 mmol/L混合氨基酸(15N丰度为3.35 atom%),充分混匀,重复3次,同时做不添加对照。处理后的土壤立即以土液质量比1∶5加入25 mL 1 mol/L KCl溶液,在25 ℃下以180 r/min振荡0.5 h,过滤液用于氨基酸浓度(荧光 OPAME 法测定[25])及氮同位素丰度测定。
N2O 参比气体:委托南京土壤所稳定同位素实验室进行标定,标定值可溯源至日本SHOKO有限公司的N2O 标准气体,该N2O参比气体的δ15NAir‰值为(6.008±0.020)‰,用于带自动预浓缩装置的稳定同位素质谱仪进行氮同位素比值测定。
1.4 实验条件及优化
1.4.1氨基酸态氮转化生成N2O条件 由Zhang等[16]研究可知,Strecker降解反应具有一定的位置特异性,反应主要发生在α-氨基端,对侧链氨基也有一定作用。因此,本实验选择结构简单的甘氨酸进行反应条件的优化探索。吸取0.1 mL 10 mmol/L甘氨酸溶液,置于12 mL顶空反应瓶中,在干式恒温器上蒸干,取出反应瓶,冷却后盖上密封瓶盖,再转移至全自动微量氮转化-N2O发生装置抽真空,连接自动加液系统,向反应瓶中加入1 mL不同碱度和浓度的碱性次溴酸钠溶液,最后注入一定量的惰性氦气。每组样品重复3次,反应生成的N2O气体浓度和15N丰度直接用带自动预浓缩装置的稳定同位素质谱仪测定,以确定影响N2O产率的参数及最优反应条件。
1.4.2混合氨基酸标准溶液及土壤样品中氨基酸态氮-N2O转化 在确定最优转化反应体系的基础上,对不同丰度混合氨基酸标准溶液及土壤提取液进行前处理。吸取一定量的15N系列混合氨基酸标准溶液,置于12 mL顶空反应瓶中,反应瓶中氨基酸含量分别为0.1、0.5、1.0 μmol,每组样品重复5次。将蒸干的反应瓶冷却后盖上密封瓶盖,转移至全自动微量氮转化-N2O发生装置抽真空,向反应瓶中依次加入1 mL碱性次溴酸钠溶液,最后注入一定量的氦气。反应生成的N2O气体浓度和15N丰度直接用带自动预浓缩装置的同位素比值质谱仪测定。
依据土壤中氨基酸含量,取一定量的土壤浸提液(<3 mL),置于12 mL顶空反应瓶中,加入约10 mg MgO后,置于120 ℃干式恒温器中加热(去除NH4+-N),浓缩反应液至微干,每组样品重复3次,后续N2O转化反应条件和操作同标准溶液。
1.4.3PreCon-IRMS测定15N-N2O丰度的工作条件 预浓缩装置的氦气流速20 mL/min,冷阱T2、T3的浓缩时间分别为180、300 s,色谱柱温度50 ℃。待仪器稳定后,将气体样品置于Combi PAL自动进样器上,经化学阱除去大部分水汽及二氧化碳干扰气体后,依次通过T2/T3冷阱浓缩。浓缩后,含N2O的混合气通过气相色谱柱分离,依次进入稳定同位素质谱仪主机进行检测。根据N2O参比气体的标定值,Isodat 3.0软件自动将样品的测定值校正成δ15NAir‰值,并最终获得15N丰度(15N atom%)。
同时,取同体积不同浓度的N2O标准气体进行检测,参考Lachouani等[17]方法对标准气体的峰信号强度Area All值和对应的标准气体浓度进行线性分析(R>0.995),样品产生的N2O气体浓度可通过该线性方程由峰信号强度换算得到。
1.5 数据处理与绘图
使用Excel 2013和SPSS 19.0处理实验数据,OriginPro 8软件绘图。
2 结果与分析
2.1 影响氨基酸态氮化学转化过程中N2O产率的因素
氨基酸态氮化学转化产生N2O涉及2个关键反应:第1步是氨基酸的α-NH2在Br-催化下被次溴酸钠裂解为NH4+;第2步是反应生成的NH4+在真空条件下继续与次溴酸钠反应,并在Cu2+催化下产生一部分N2O。本研究的第1步解离过程主要基于Strecker反应原理,根据Zhang等[16]报道,此过程中氨基酸-NH2解离效率差异主要源于氨基酸的分子构型及位点,它对α-NH2具有较强的特异性,同时对侧链氨基也有一定作用;而本研究的第2步,解离的铵态氮转化生成N2O的反应原理主要基于Schonberg等[20-22]研究,该反应过程中,N2O产率主要受反应体系的影响,也是氨基酸态氮转化的限制步骤。Laughlin等[21]发现,该反应体系除保证催化剂Cu2+浓度不小于0.5 mmol/L外,N2O产率主要取决于NaOBr的碱度。本研究也发现,提高NaOH和次溴酸钠浓度,氨基酸态氮反应体系中N2O产率增加,且在不小于150 mmol/L NaOBr条件下,当NaOH浓度为10 mol/L时,N2O产率可达到25%左右,在此基础上继续提高体系中NaOH和次溴酸钠浓度,N2O产率没有明显变化,示于图1。

图1 次溴酸钠浓度和碱度对甘氨酸化学转化成N2O产率的影响Fig.1 Effects of sodium hypobromate concentration and alkalinity on the yield of glycine chemical conversion to N2O
2.2 测定氨基酸态氮中15N的精密度和准确度
不同氨基酸氮含量和15N丰度的标准溶液经前处理后,结合气体预浓缩装置与稳定同位素质谱仪联用系统测定其15N丰度,获得的检测结果示于图2。从精密度来看,所有自然丰度的实验样品5次重复测定均能获得较好的精密度(CV<0.5%);而对于高丰度的实验样品,除0.1 μmol氨基酸的测量精密度稍差,在3.6%~4.0%之间,其他含量标准溶液的精密度均小于1%。从准确度来看,针对不同15N丰度,氨基酸氮含量等于或者超过1 μmol样品的15N丰度5次重复测量平均值分别为0.361%、0.991%、3.31%,与参考值基本一致。此外,0.1 μmol实验样品15N丰度的准确度和精密度与另外2组氨基酸氮含量较高的样品差异显著(p<0.05),在保证理想的测试准确度和精密度条件下,推荐单次反应体系中氨基酸的最低含量为0.5 μmol。本研究采用快速蒸馏除铵和浓缩处理土壤浸提液,并通过全自动微量氮转化-N2O发生装置替代Noll等[15]原方法中扩散法手工操作过程,大大缩短了前处理时间,提高了分析测试效率,降低了测试精密度对人员操作熟练程度的依赖,且不存在同位素分馏。
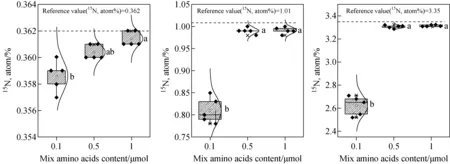
注:a,b表示不同氨基酸含量对丰度测定值的显著性影响(p<0.05)图2 化学转化N2O产生法测定不同15N丰度氨基酸态氮中15N的精密度和准确度Fig.2 Precision and accuracy of the determination of 15N abundance of amino acid-N by chemical conversion N2O method
2.3 土壤浸提液中游离氨基酸态氮的15N丰度
由于供试土壤中游离氨基酸含量较低,换算为干重含量仅为0.73~1.1 μmol/g,取10 mL土壤浸提液,先经冷冻浓缩后,再用于后续的氨基酸态氮转化前处理。
供试土壤样品中氨基酸含量及其15N丰度结果列于表2。可以看出,不同利用类型土壤游离氨基酸含量差异较大,土壤1的游离氨基酸含量约为土壤2的1.5倍,这可能是由于土壤1为稻田土壤,肥力较高,其全氮及有机碳含量均远高于旱地土壤,因此游离氨基酸含量也高于旱地土壤。此外,两种不同利用类型土壤添加的氨基酸回收率均较高(90%以上),这可能与土壤质地有关,两种土壤均为粉砂性,对氨基酸的吸附能力相对较弱,因此,添加后立即提取可获得较好的回收率。
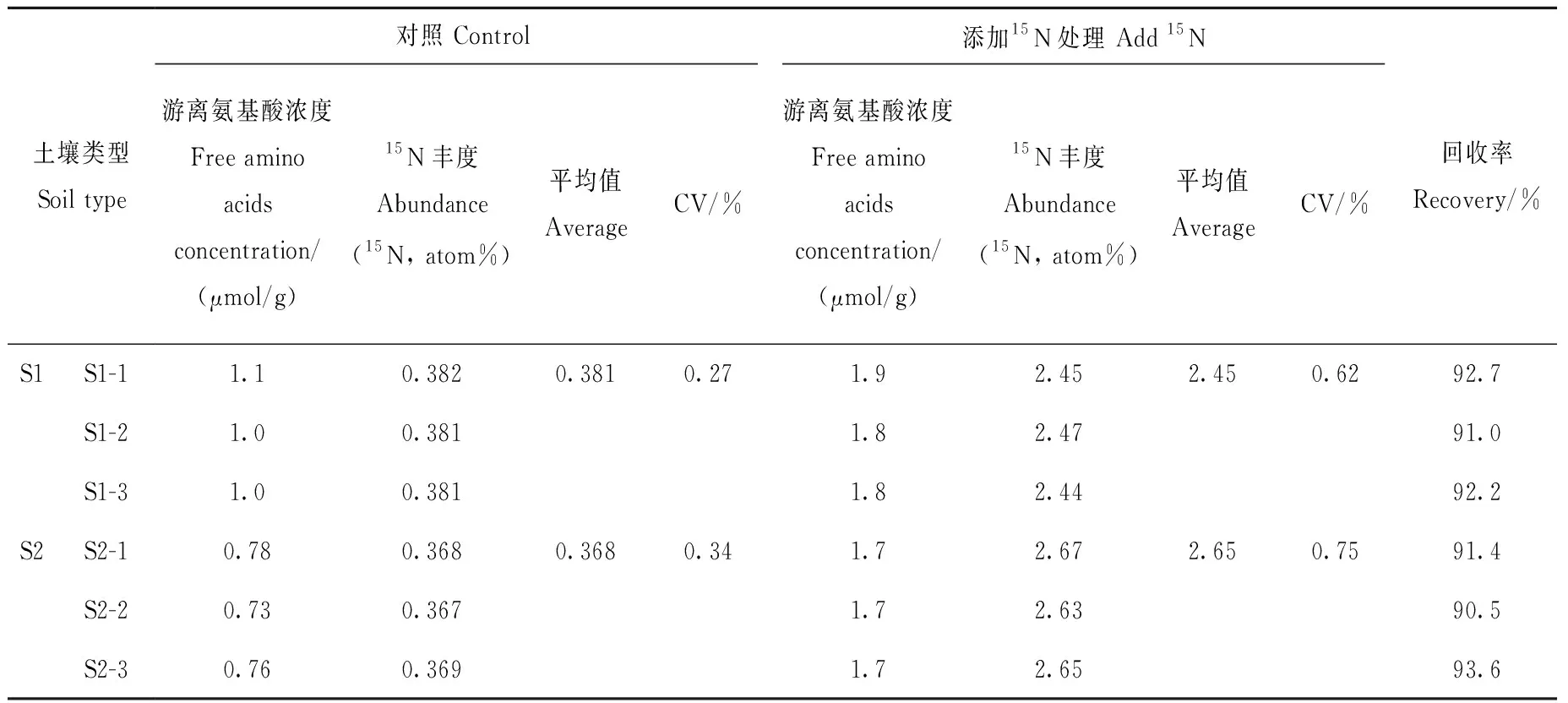
表2 供试土壤浸提液中游离氨基酸15N丰度Table 2 15N abundance of free amino acid in extractions of soils by chemical conversion N2O method
土壤15N丰度的测定结果显示,虽然2种不同类型土壤的15N丰度值差异较大,但是对照处理和15N富集处理的土壤15N丰度的重现性均较好(CV<1.0%),可满足相关科研工作的需求。
3 结论
本研究采用快速蒸馏法替代微扩散法,将批量样品前处理时间从原来的2~3天缩减至1 h内即可完成,且对氨基酸化学转化成N2O 的反应过程进行改进,避免使用剧毒化学品和外源氮导致的同位素分馏,同时结合全自动微量氮转化装置代替前处理过程中的部分手动操作,利用改进后的反应体系建立了一种简单、快速、准确且灵敏度高的土壤游离氨基酸前处理及上机测试分析方法,方法的最低检测限为0.5 μmol AA(1 mL反应体系)。采用本方法测定土壤游离氨基酸态氮的15N丰度,可以显著提高样品通量和检测效率,均能获得较理想的精密度,且无分馏现象发生。通过向不同类型土壤中加入混合氨基酸溶液,可实现nmol级氨基酸浓度土壤样品中游离氨基酸态氮稳定同位素丰度的测定。该方法的建立有助于推进土壤有机氮矿化、周转、氨基酸态氮的生物有效性及其影响机制等研究工作的开展。
