经导管主动脉瓣“瓣中瓣”植入1例
2022-01-21吴章民郭静文朱军李传伟曾春雨杨成明
吴章民,郭静文,朱军,李传伟,曾春雨,杨成明
主动脉瓣狭窄(AS),尤其是重度AS,既往主要依靠外科换瓣手术,而传统开胸术创面大,术后恢复慢,对于身体条件及心功能较差的老年患者而言风险高,甚至直接失去手术机会。近年来介入导管技术不断发展,经导管主动脉瓣植入术(TAVI)逐渐得到推广。本文报道1例重度AS患者症状反复发作,内科加强抗心力衰竭(心衰)治疗效果不佳,最终接受手术治疗,患者一般情况差、病情重,手术风险高,最终决定行TAVI,以主动脉瓣“瓣中瓣”解决了重度AS问题。
1 病例
患者,女性,68岁,因“反复活动后胸闷、气促1年,加重伴胸痛1月”于2020-8-25入院。近1月体力明显下降,走平路稍快即感胸闷、气促,伴夜间阵发性呼吸困难。入院查体:体温:36.3℃,脉搏76 次/min,呼吸19 次/min,血压99/62 mmHg(1 mmHg=0.133 kPa)。神志清,呼吸平稳,颈静脉无充盈,两肺呼吸音粗,未闻及干湿啰音。心前区无隆起,心尖搏动位于第5肋间左锁骨中线外0.5 cm,弥散不明显,心界向左下扩大,心率76 次/min,律齐,心尖部可闻及3/6级收缩期吹风样杂音,胸骨左缘、右缘第3肋间可闻及3/6级收缩期喷射样杂音,未闻及心包摩擦音,无双下肢凹陷性水肿。患者1年前于外院被确诊“心脏瓣膜病,主动脉瓣狭窄伴关闭不全,心功能Ⅲ级”,多次住院治疗后症状可好转,建议手术治疗,但患者拒绝,近1月症状明显加重入我院。辅助检查:肌酐80.1 μmol/L,N末端脑钠肽前体(NTproBNP)>30000 pg/ml;谷丙转氨酶43.5 U/L,谷草转氨酶48.3 U/L;肾小球滤过率评估80.98 ml/(min·L);血气、心肌损伤标记物、血常规、C反应蛋白、血脂、甲功等均无明显异常。胸片示风湿性心脏病二尖瓣病变(图1);超声心动图示:左房增大(41 mm),主动脉升部增宽,室间隔增厚(11.5 mm),左室后壁增厚(11.6 mm),主动脉瓣重度狭窄伴中度关闭不全(主动脉瓣口流速548 cm/s,压差120 mmHg,返流面积7 cm2),二尖瓣重度返流(面积直达心房顶部),三尖瓣中度返流,肺动脉高压形成(中度),左室射血分数47%。心电图示窦性心律,心率70 次/min,非特异性室内差异传导。
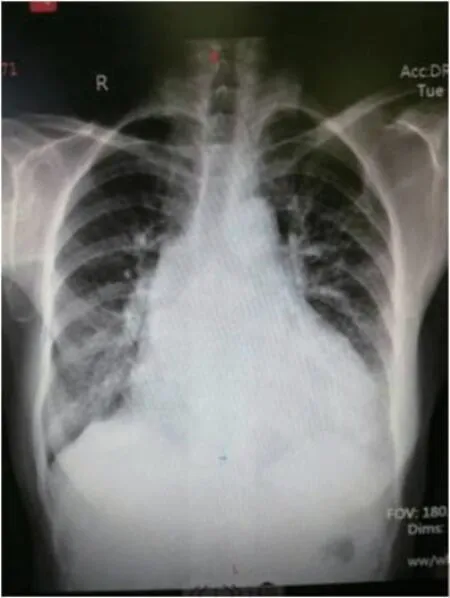
图1 患者胸片正位图像(注:心脏扩大,右心缘双弓影)
患者诊断明确,入院后予以强心、利尿、营养心肌等抗心衰治疗后症状缓解不明显。主动脉瓣重度狭窄伴中度关闭不全,二尖瓣重度返流,有换瓣指征,患者及家属趋向保守治疗,经专家商讨:老年患者,身体一般条件差,心衰指标高,美国胸外科医师学会评分5.7分,外科开胸手术风险高,建议行TAVI。患者及家属接受,完善胸腹部主动脉CTA、冠脉CTA检查后,于9-4全麻及临时起搏器保护下行经皮主动脉瓣置入术。完善术前准备后,经右侧股动脉以多功能造影管及JR4.0、JL4.0造影管行主动脉根部造影,主动脉瓣球囊扩张,经导管植入人工主动脉瓣生物瓣(MicroPort TAVI21),释放过程顺利,造影及超声评估生物瓣扩张不良,经右侧股动脉行球囊后扩张,再次造影及超声评估发现生物瓣仍存在扩张不良。鉴于人工主动脉瓣生物瓣下裙边张力最大,讨论后决定在上一枚瓣膜稍高一点位置植入另一枚人工主动脉瓣生物瓣,造影及超声评估植入效果好(图2)。立即测主动脉瓣压差从120 mmHg迅速降至20 mmHg,超声评估心功能明显改善。术中造影冠脉血流通畅,术后心电图未出现新的房室传导阻滞。术后第1 d复查NT-proBNP 5946 pg/ml,较前明显下降,术后12 h内患者出现发热,最高37.9℃。急查血常规:白细胞22×109/L,中性粒细胞比91.7%,血红蛋白92 g/L;C反应蛋白69.34 mg/L;留取血培养后予以抗感染治疗,体温2 d后降至正常,密切监测炎性指标显示逐渐下降(表1)。经进一步改善心功能、抗血小板、调脂、营养心肌等治疗后,病情较前明显好转,生命体征平稳,术后第8 d出院,继续抗心衰治疗,门诊随诊,患者心功能分级和生活质量明显改善。
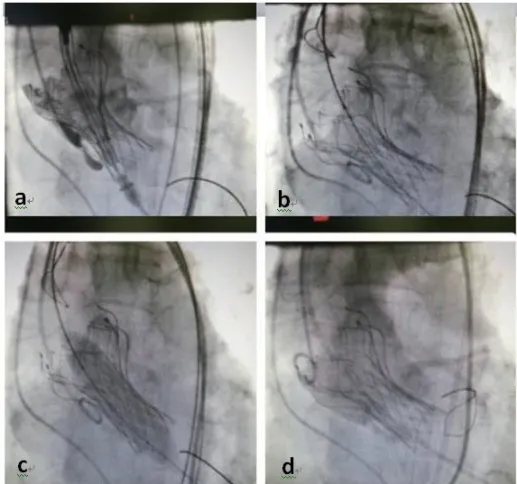
图2 患者第二个瓣膜植入图像(a:第二个瓣膜送入主动脉根部;b:第二个瓣膜完全展开;c:球囊扩张第二个瓣膜;d:第二个瓣膜植入术后造影)
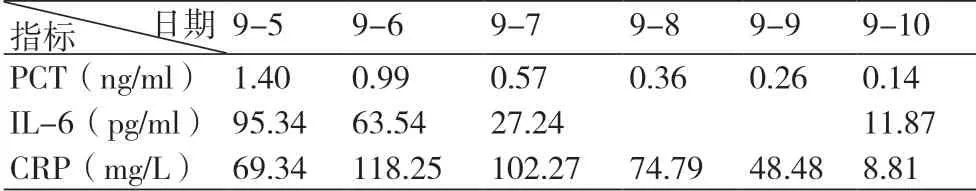
表1 患者术后炎性指标变化
2 讨论
AS是一种呈隐匿性进展的常见心血管疾病,在较长时间无任何症状,一旦出现胸痛、晕厥、心功能不全等症状,若不及时治疗或仅内科保守治疗不解除病因,重度AS患者2年无事件生存率仅30%~50%[1],预后极差。
TAVI问世前,外科主动脉瓣置换术(SAVR)是症状性重度AS的唯一根治办法。但是传统的SAVR需要体外循环、患者身体承受负担重,手术风险高,约33%重度AS患者因高龄、心功能差、合并严重并发症或体质虚弱等问题不能进行常规SAVR[2],又或者只是因为恐惧外科手术,趋向于选择保守治疗而放弃手术机会。在此环境下,经过临床医生与器械工程师们的不懈努力,TAVI顺势而生。
TAVI指经导管将组装好的主动脉瓣送到主动脉根部,瓣膜展开后固定在原主动脉瓣的位置,在功能上完成主动脉瓣的置换,故也称经导管主动脉瓣置换术(TAVR)[3],TAVI、TAVR两者并无本质区别。TAVI为上述无法耐受或者不接受SAVR的AS患者提供了新的治疗选择,其具有创伤小、无需体外循环、安全性高、术后恢复快等特点,受到医务人员和患者的青睐。自2002年TAVI首次成功应用于临床后,继欧美国家发布相关指南或专家共识后,2015年我国心血管病专家们结合中国实际情况发布了属于自己的专家共识[3],对我国AS患者的微创治疗起到了很好的指导作用。根据目前已有临床经验[4]来看,在疗效上,TAVI可迅速而显著的降低AS患者主动脉瓣跨瓣压,明显改善心功能,逆转左室重构,降低脑钠肽水平,改善患者的症状,提高生活质量和6 min步行试验。研究[5]显示TAVI术后患者1年生存率、超声心动图指标、生活质量等并不亚于甚至优于SAVR。国际上目前已将TAVI作为SAVR高危或有禁忌症AS患者的首选治疗方式[6],也是SAVR有效的替代治疗方案。
安全性方面,TAVI主要的并发症主要有心脏传导阻滞、瓣周漏、血管并发症、出血、冠脉阻塞和心肌梗死、脑卒中、急性肾脏损伤等,术前应做好严格评估,选择合适的瓣膜植入,术中操作轻柔,术后严密监测以减少并发症的发生。本案例中采用的“瓣中瓣”技术,于2007年首次应用临床,即在原有已置换过的瓣膜中再置入一个全新的瓣膜。在第一个瓣膜植入后出现明显返流或瓣周漏时,瓣中瓣可作为一种有效的补救措施。目前,瓣中瓣处理瓣膜返流或瓣周漏的效果是肯定的,且与TAVI非瓣中瓣患者相比,瓣中瓣患者的30 d死亡率和1年死亡率均无统计学差异[7]。
TAVI不仅为非外科手术的AS患者提供了一个相对安全的选择,且比传统内科标准治疗效果更好[8]。经临床实践,随着介入技术、器械工艺的不断精化,TAVI的适应症逐步向中危甚至低危的AS推进,其未来前景值得期待,也希望有更多AS患者从中获益。
