Ni/N-rGO催化苯酚选择性加氢制备环己酮性能
2022-01-13黄国强徐海升李善建郜鹏程
黄国强,徐海升,李善建,郜鹏程
(西安石油大学 化学化工学院,陕西 西安 710065)
随着化石能源储量的逐渐减少以及生态环境问题的日益凸显,寻找和开发新型环保能源已成为亟待解决的问题[1-2]。生物质经热解或液化得到的生物质油被认为是潜在的化石燃料替代品,但生物质油的氧含量较高,导致生物质油黏度高、热值低、化学稳定性差,这严重影响了其广泛应用[3-5]。加氢脱氧(HDO)或选择性加氢被认为是提高生物质油性能及获取高附加值产品的有效方法[6-7]。苯酚常作为生物质油模型化合物用于加氢反应探究[8]。
苯酚选择性加氢制备环己酮并及时分离,可实现间接脱氧的同时获取高附加值产品,具有较高的研究价值。苯酚选择性加氢制备环己酮的反应历程为苯酚首先加氢生成环己烯醇,环己烯醇经过烯醇式异构化得到环己酮,但环己酮不稳定会继续加氢生成环己醇[9]。因此,提高苯酚转化效率的同时提高环己酮选择性是该研究的主要目的。研究发现,苯酚在催化剂表面的吸附方式对催化产物选择性有显著影响[9-10]。在酸性位点,苯环和载体之间以共平面方式吸附,二者吸附作用较强,不利于环己酮脱附,所以更容易过度加氢生成环己醇;在碱性位点,苯环和载体之间以非共平面方式吸附,有利于环己酮脱附[11]。因此,笔者通过水热法合成了氮掺杂还原氧化石墨烯(N-rGO)载体,然后采用浸渍法制备了不同镍负载量的Ni/N-rGO催化剂,将其用于苯酚选择性加氢制备环己酮反应。考察了催化剂制备及加氢反应条件对催化剂活性和环己酮选择性的影响,并通过正交实验确定了最佳反应条件。
1 实验部分
1.1 原料和试剂
鳞片石墨,安徽安特生物化学有限公司产品;硝酸钠、过氧化氢(质量分数30%)、氢氧化钠、苯酚、环己酮,天津市科密欧化学试剂有限公司产品;2,4-二硝基苯肼,上海科丰实业有限公司产品;浓硫酸,四川西陇科学有限公司产品;浓盐酸,西安雁塔化学试剂厂产品;高锰酸钾,天津市北联精细化学品开发有限公司产品;Ni(NO3)2·6H2O,天津市华东试剂厂产品;尿素,天津永晟精细化工有限公司产品;无水乙醇,天津市大茂化学试剂厂产品。以上试剂均为分析纯。
1.2 实验仪器
DZF-6050AB型真空干燥箱,上海坤天实验仪器有限公司生产;SHZ-D(Ⅲ)型循环水真空泵,上海邦西仪器科技有限公司生产;L-500型离心机,上海利鑫坚离心机有限公司生产;KQ 5200B型超声波清洗器,昆山市超声仪器有限公司生产;FA 1004型分析电子天平,上海精科天平仪器厂生产;DF-101S型集热式恒温加热磁力搅拌器,上海棱标仪器有限公司生产;GW 300型变频高温滚子加热炉,青岛同春石油仪器有限公司生产;UV-2600型紫外可见分光光度计,日本岛津公司生产;100 mL间歇式高温高压反应釜,西安太康科技有限公司生产;ASAP 2020型N2吸附-脱附测定仪,美国麦克公司生产;D8 ADVANCE型X射线衍射仪,德国Bruker公司生产;Quanta 600 FEG型扫描电镜,美国FEI公司生产。
1.3 催化剂制备
通过一步水热法制备得到N-rGO载体。称取一定量采用改进Hummers法合成的氧化石墨烯(GO)加入去离子水[12-13],超声处理2 h,得到高度分散的1 mg/mL氧化石墨烯分散液,以尿素为氮源和还原剂,按照GO与尿素质量比为1∶30缓慢将尿素加入GO分散液中,室温继续超声搅拌0.5 h后倒入500 mL水热反应釜,在变频高温滚子加热炉中于180 ℃水热反应12 h,反应结束后,将反应釜中的悬浮液离心,抽滤离心管下层固体,并用去离子水和无水乙醇反复洗涤至中性,然后在真空干燥箱中充分干燥,得到N-rGO[14]。
采用浸渍法制备Ni/N-rGO催化剂。称取一定量的N-rGO作为载体,按比例加入0.1 mol/L的Ni(NO3)2水溶液,常温下磁力搅拌2 h,浸渍12 h后于70 ℃水浴中恒温搅拌蒸干浸渍液中的水分,将样品放置在烘箱中充分干燥;然后在氮气保护下于管式炉中400 ℃焙烧4 h,最后在氢气气氛中以5 ℃/min 的升温速率升至450 ℃还原2 h,得到镍基Ni/N-rGO催化剂。将镍负载量(质量分数,下同)为10%、20%、30%的催化剂分别记为10%Ni/N-rGO、20%Ni/N-rGO、30%Ni/N-rGO。
1.4 催化剂表征
采用美国Micromeritics公司生产的ASAP 2020型N2吸附-脱附仪测定Ni/N-rGO催化剂的比表面积(BET法)、平均孔径和孔体积(BJH法);采用德国Bruker公司生产的D8 ADVANCE型X射线衍射仪测定催化剂晶相结构,Cu靶辐射,管电压为40 kV,管电流为30 mA,扫描速率为5 °/min,扫描范围为10°~80°;采用美国FEI公司生产的Quanta 600 FEG型扫描电镜表征催化剂表面形貌和粒度分布情况。
1.5 催化剂性能评价
将制备的Ni/N-rGO催化剂和苯酚溶液装填到100 mL间歇式高温高压反应釜中,在给定实验条件下通入氢气进行苯酚催化加氢实验。实验结束后,准确称量反应结束后收集液的质量和体积,通过UV-2600型紫外可见分光光度计测定收集液中苯酚和环己酮的吸光度,然后根据苯酚和环己酮的标准曲线计算得到产物中苯酚和环己酮的质量[8],进一步由式(1)、式(2)计算苯酚转化率(x,%)和环己酮选择性(s,%)。
(1)
(2)
式(1)和式(2)中:mp表示反应的苯酚质量,g;mp0表示苯酚初始的质量,g;mc表示生成环己酮的质量,g。
2 结果与讨论
2.1 催化剂表征
2.1.1 N2吸附-脱附表征
表1列出了N-rGO载体及不同镍负载量催化剂样品的比表面积及孔结构性质。
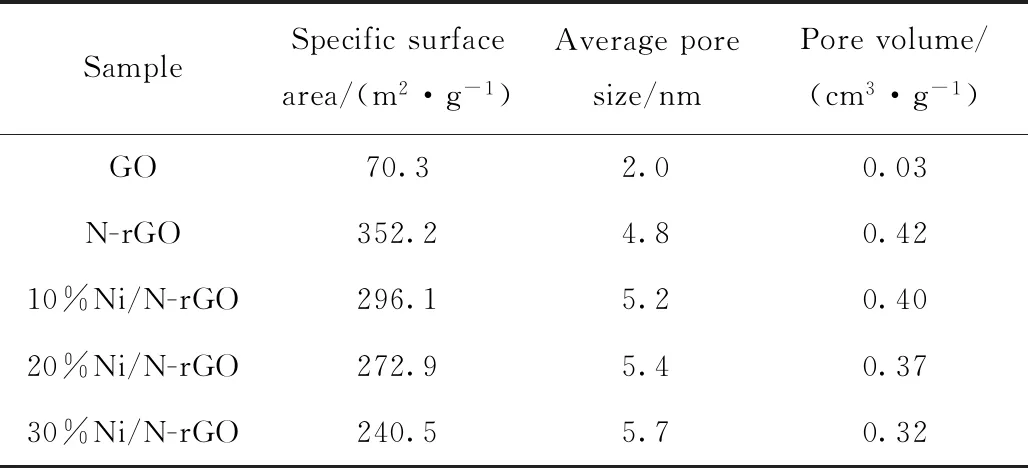
表1 载体及各催化剂样品的物理结构性质Table 1 Physical structural properties of each catalyst
由表1可知:N-rGO载体的比表面积、平均孔径、孔体积较GO明显增加,这可能是掺氮后GO片层间的大量含氧基团被去除,石墨片层间产生了空隙,因此N-rGO物性参数急剧增大;负载金属镍后,催化剂的比表面积和孔体积都有所下降但平均孔径有所提高,随着镍负载量增加这一现象更加明显。这可能是负载金属后,金属颗粒占据了载体的表面,导致催化剂比表面积下降;催化剂平均孔径增大可能是由于其表面的小孔优先被金属颗粒堵塞造成的。
2.1.2 XRD表征
图1为不同镍负载量催化剂样品的XRD谱图。

N-rGO—N-doped reduced graphene oxide图1 不同镍负载量催化剂样品的XRD谱图Fig.1 XRD patterns of catalysts with different nickel loadings
由图1可知:2θ在25.6°对应N-rGO的(002)晶面衍射峰,N-rGO的(002)晶面衍射峰宽而弥散,是非晶态碳材料的特征;2θ在44.5°、51.7°和76.3°对应Ni的(111)、(200)、(220)晶面衍射峰。随着镍负载量的增加,镍的晶面衍射峰越来越尖锐且强度越强,但N-rGO的(002)晶面衍射峰不断变小,可能是负载量较少时,金属镍分散均匀且金属尺寸较小;当镍负载量为30%时,可能是金属镍发生团聚金属颗粒变大覆盖了载体表面,导致N-rGO的(002)晶面衍射峰变小。
2.1.3 SEM表征
图2为载体N-rGO和20%Ni/N-rGO催化剂样品的SEM照片。由图2可知:N-rGO载体呈大片层状结构,表面有较多透明、无序薄纱状褶皱,说明氮掺杂引入了较多的缺陷位;负载金属镍后N-rGO载体表面变的粗糙,有较多颗粒状物质,说明金属镍负载成功且金属镍颗粒较小,分散相对均匀,局部有明显的大颗粒出现,为镍的团聚现象。

图2 载体N-rGO和20%Ni/N-rGO催化剂样品的SEM照片Fig.2 SEM images of carrier N-doped reduced graphene oxide (N-rGO)and 20%Ni/N-rGO catalysts(a)N-rGO;(b)Ni/N-rGO
2.2 Ni/N-rGO催化剂催化苯酚选择性加氢反应性能
2.2.1 镍负载量对催化剂反应性能的影响
在反应温度为150 ℃、反应压力为0.4 MPa、反应时间为2.0 h、Ni/N-rGO催化剂/苯酚质量比(简称剂/酚质量比)为0.35的条件下,考察镍负载量对苯酚选择性加氢制环己酮的影响,结果如图3所示。
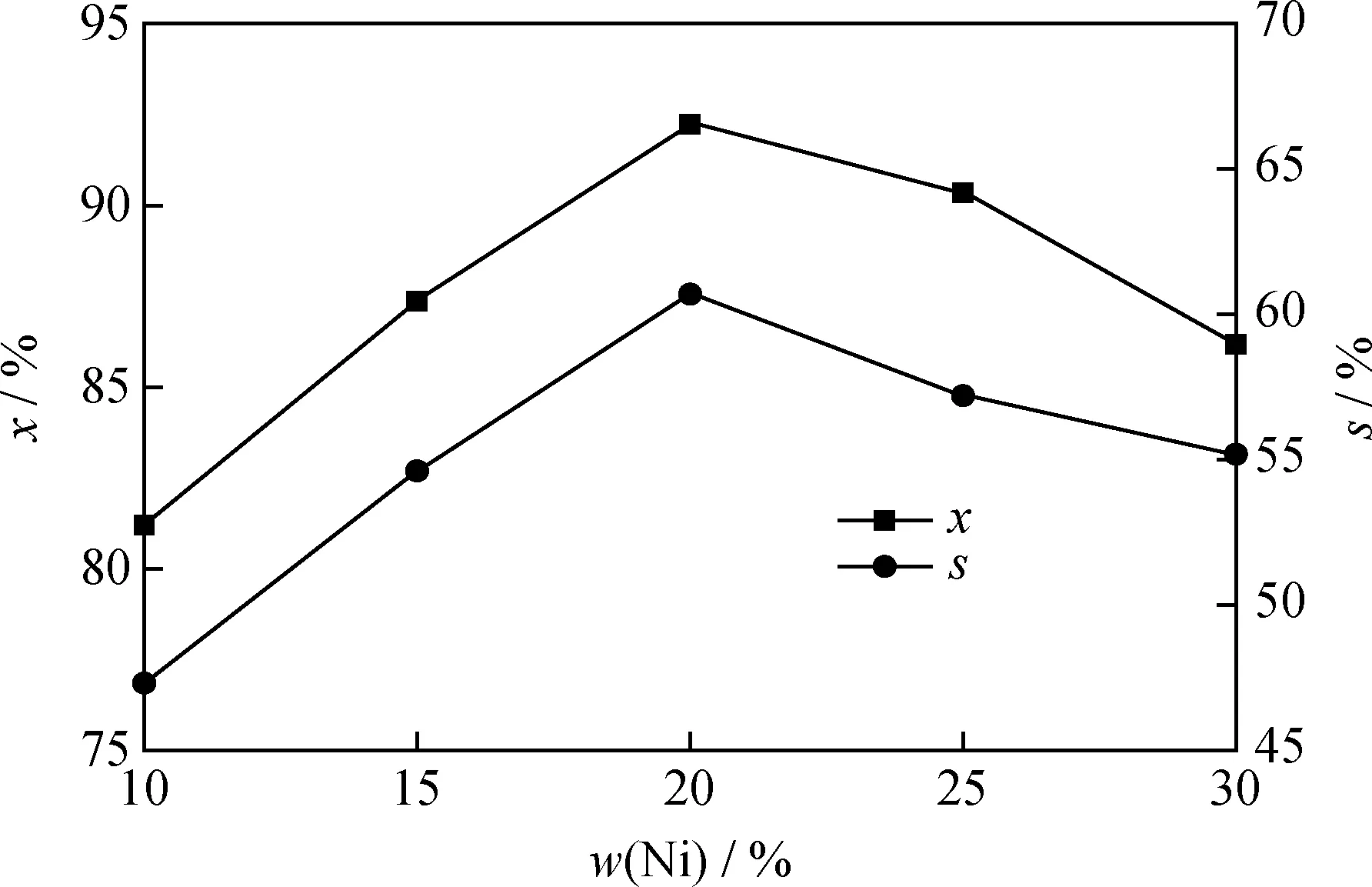
x—The conversion rate of phenol;s—The selectivity of cyclohexanone图3 镍负载量对Ni/N-rGO催化剂催化苯酚加氢制环己酮的影响Fig.3 Effect of nickel loading on hydrogenation of phenol to cyclohexanone catalyzed by Ni/N-rGO catalystReaction conditions:T=150 ℃;p=0.4 MPa;t=2.0 h;m(Ni/N-rGO)/m(Phenol)=0.35
由图3可见,随着镍负载量的增加,苯酚转化率、环己酮选择性均先增大后减小。当镍负载量为20%时,苯酚转化率达到92.23%,环己酮选择性最高为60.70%。这是因为当镍负载量较低时,催化剂表面活性中心较少,加氢反应不完全,致使苯酚转化率及环己酮选择性都较低;当镍负载量较高时,金属镍容易在催化剂表面团聚,堵塞催化剂孔道结构,致使催化活性和产物选择性降低。
2.2.2 尿素/GO质量比对催化剂反应性能的影响
在反应温度为150 ℃、反应压力为0.4 MPa、反应时间为2.0 h、剂/酚质量比为0.35的条件下,考察尿素/GO质量比对苯酚选择性加氢制环己酮的影响,结果如图4所示。

x—The conversion rate of phenol;s—The selectivity of cyclohexanone;GO—Graphite oxide图4 尿素/GO质量比对20%Ni/N-rGO催化剂催化苯酚加氢制环己酮的影响Fig.4 Effect of urea to GO mass ratio on hydrogenation of phenol to cyclohexanone catalyzed by 20%Ni/N-rGO catalystReaction conditions:T=150 ℃;p=0.4 MPa;t=2.0 h;m(Ni/N-rGO)/m(Phenol)=0.35
由图4可见,随着尿素添加量的增加,苯酚转化率逐渐提高,环己酮选择性呈先增大后减小的趋势。当尿素/GO质量比为30时,苯酚转化率为90.54%,环己酮选择性最高为62.19%。分析其原因可能是随着尿素含量增加,较多的氮原子掺杂到石墨烯中使得催化剂活性位增多;氮原子富电子特性能给活性金属Ni提供电子进而活化更多的氢,使得催化剂活性提高[15];且研究表明[16],适当的氮掺杂可形成OH—N或OH—π相互作用,致使苯酚以非共平面方式吸附在载体上,有利于环己酮从石墨烯表面快速脱附进而提高环己酮选择性。随着尿素添加量过高,金属Ni和载体之间相互作用进一步加强,部分未脱附的环己酮会继续加氢生成副产物,导致环己酮选择性下降。
2.2.3 H2还原温度对催化剂反应性能的影响
在反应温度为150 ℃、反应压力为0.4 MPa、反应时间为2.0 h、剂/酚质量比为0.35的条件下,考察H2还原温度对苯酚选择性加氢制环己酮的影响,结果如图5所示。
由图5可见,随着氢气还原温度的上升,苯酚转化率先快速升高后趋于下降,环己酮选择性呈先增大后减小的趋势。当还原温度为450 ℃时,苯酚转化率达到91.37%,环己酮选择性最高为61.03%。这是因为当还原温度较低时,只有少部分的NiO被还原,催化剂活性较低;随着还原温度升高,较多的NiO开始被还原,因此催化剂活性和环己酮选择性都快速提升[17];当温度达到500 ℃时,可能是还原温度过高导致部分还原态金属Ni发生了团聚,进而导致苯酚转化率和环己酮选择性都有所下降。
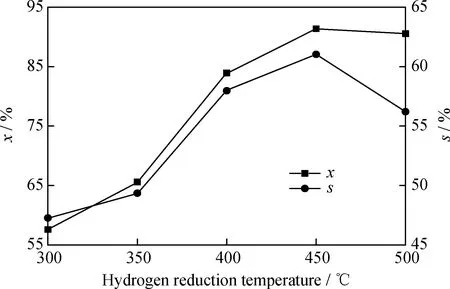
x—The conversion rate of phenol;s—The selectivity of cyclohexanone图5 氢气还原温度对20%Ni/N-rGO催化剂催化苯酚加氢制环己酮的影响Fig.5 Effect of hydrogen reduction temperature on hydrogenation of phenol to cyclohexanone catalyzed by 20%Ni/N-rGO catalystReaction conditions:T=150 ℃;p=0.4 MPa;t=2.0 h;m(Ni/N-rGO)/m(Phenol)=0.35
2.2.4 反应温度对催化剂反应性能的影响
在反应压力为0.4 MPa、反应时间为2.0 h、剂/酚质量比为0.35的条件下,考察反应温度对苯酚选择性加氢制环己酮的影响,结果如图6所示。
由图6可见,随着反应温度的升高,苯酚转化率持续提升,而环己酮选择性先升高后下降。当反应温度为150 ℃时,苯酚转化率为91.93%,环己酮选择性最高为61.75%。这是因为在实验条件范围内,升高温度会提高苯酚加氢反应速率,有利于苯酚转化。在150 ℃之后环己酮选择性开始减小,是由于苯酚加氢制备环己酮(ΔG=-145 kJ/mol)受热力学影响较大[18],较高温度并不利于环己酮生成。
2.2.5 反应压力对催化剂反应性能的影响
在反应温度为150 ℃、反应时间为2.0 h、剂/酚质量比为0.35的条件下,考察反应压力对苯酚选择性加氢制环己酮的影响,结果如图7所示。
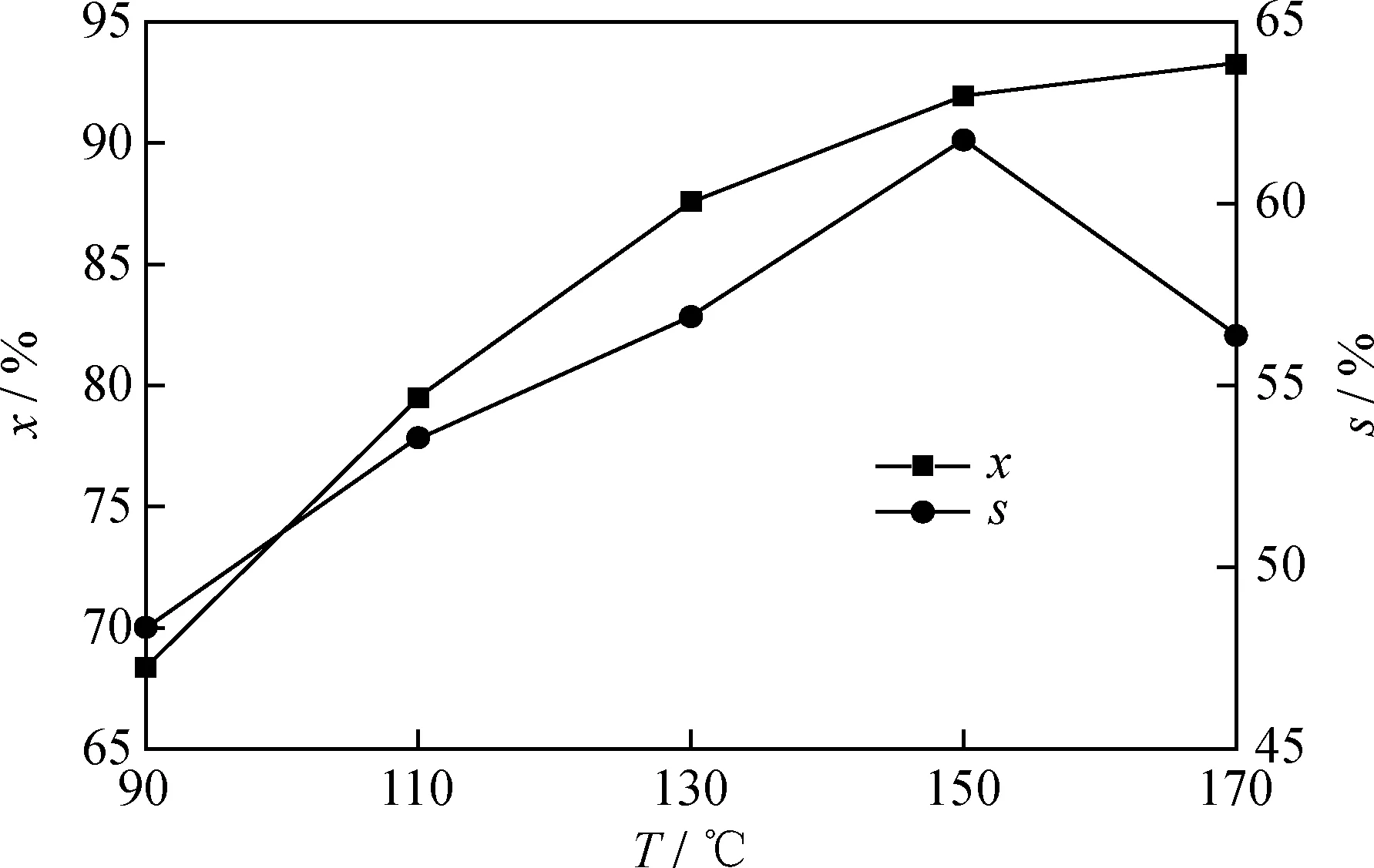
x—The conversion rate of phenol;s—The selectivity of cyclohexanone图6 反应温度对20%Ni/N-rGO催化剂催化苯酚加氢制环己酮的影响Fig.6 Effect of reaction temperature on hydrogenation of phenol to cyclohexanone catalyzed by 20%Ni/N-rGO catalystReaction conditions:p=0.4 MPa;t=2.0 h;m(Ni/N-rGO)/m(Phenol)=0.35
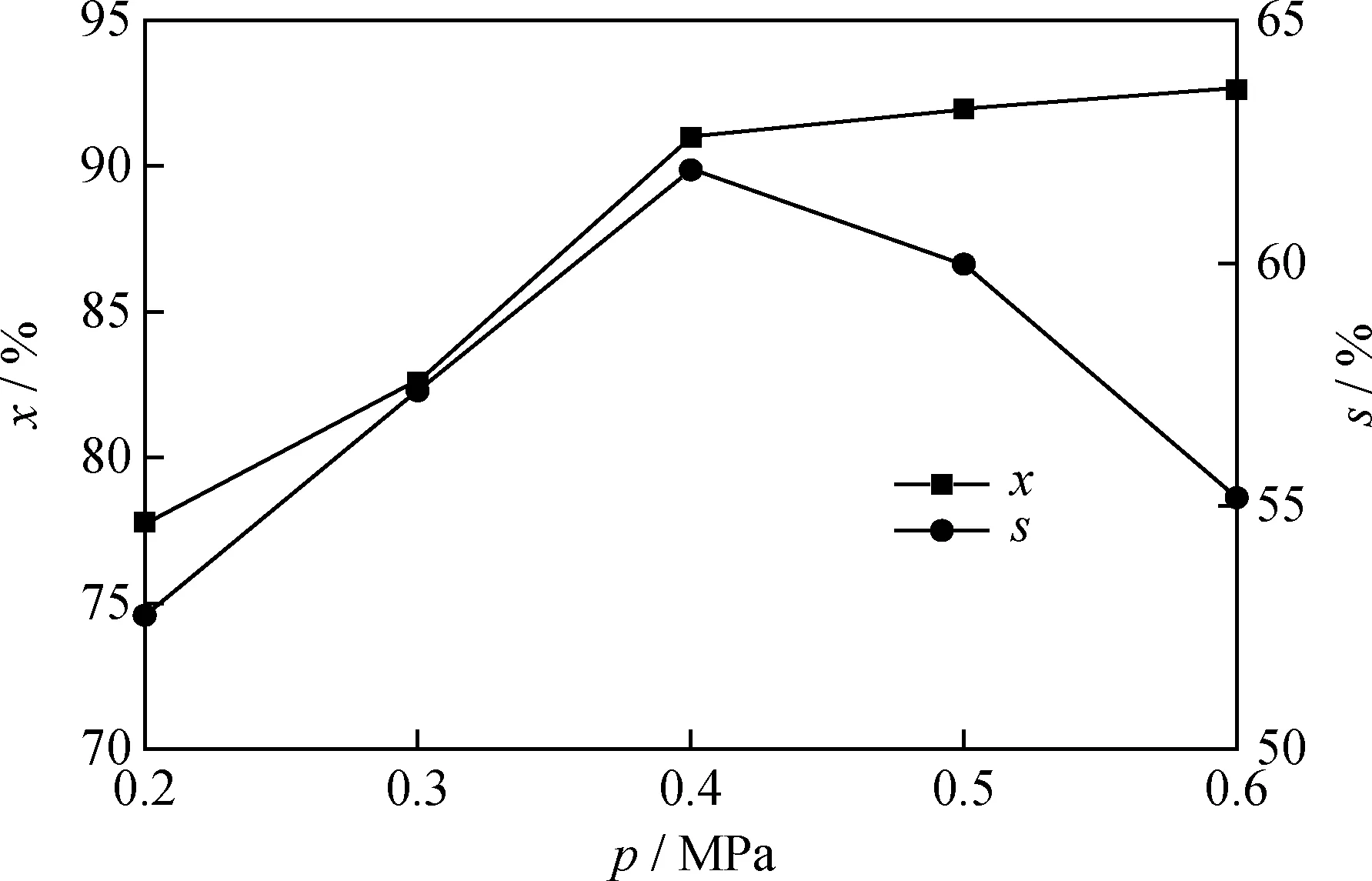
x—The conversion rate of phenol;s—The selectivity of cyclohexanone图7 反应压力对20%Ni/N-rGO催化剂催化苯酚加氢制环己酮的影响Fig.7 Effect of reaction pressure on hydrogenation of phenol to cyclohexanone catalyzed by 20%Ni/N-rGO catalystReaction conditions:T=150 ℃;t=2.0 h;m(Ni/N-rGO)/m(Phenol)=0.35
由图7可见,随着反应压力的增大,苯酚转化率先增大后趋于平缓,而环己酮选择性先增大后减小。当反应压力为0.4 MPa时,苯酚转化率为90.99%,环己酮选择性最高为61.92%。这是因为在实验条件范围内,适当增大反应压力可有效提高催化活性及环己酮选择性;环己酮是中间产物稳定性较差,随着反应压力继续增大,环己酮可能会继续加氢生成其他副产物,因而压力过高环己酮选择性会下降。
2.2.6 反应时间对催化剂反应性能的影响
在反应温度为150 ℃、反应压力为0.4 MPa、剂/酚质量比为0.35的条件下,考察反应时间对苯酚选择性加氢制环己酮的影响,结果如图8所示。

x—The conversion rate of phenol;s—The selectivity of cyclohexanone图8 反应时间对20%Ni/N-rGO催化剂催化苯酚加氢制环己酮的影响Fig.8 Effect of reaction time on hydrogenation of phenol to cyclohexanone catalyzed by 20%Ni/N-rGO catalystReaction conditions:T=150 ℃;p=0.4 MPa;m(Ni/N-rGO)/m(Phenol)=0.35
由图8可见,随着反应时间的延长,苯酚转化率呈上升趋势,而环己酮选择性先升高后下降。当反应时间为2.0 h时,苯酚转化率为90.01%,环己酮选择性最高为62.03%。这是因为随反应时间延长,较多活化的氢原子与苯酚充分接触,促进苯酚加氢生成环己酮;但随着反应时间过长,未及时脱附的环己酮会继续和氢气反应生成其他副产物,导致环己酮选择性下降。
2.2.7 20%Ni/N-rGO催化剂的稳定性
催化剂稳定性是评价催化剂性能指标的重要因素之一。将20%Ni/N-rGO催化剂重复利用,考察催化剂重复利用次数对苯酚选择性加氢制环己酮的影响,结果如图9所示。
由图9可见:20%Ni/N-rGO催化剂重复使用3次后,苯酚转化率和环己酮选择性略有下降;当20%Ni/N-rGO催化剂重复使用5次后,苯酚转化率和环己酮选择性下降比较明显,苯酚转化率下降约9百分点,环己酮选择性降至50.93%。这可能是随着循环使用次数的增加,催化剂活性不断流失及催化剂严重团聚造成的。
3 结 论
(1)通过N2吸附-脱附、XRD、SEM等表征手段对制备的载体N-rGO和不同镍负载量Ni/N-rGO催化剂进行表征,结果表明:载体N-rGO具有较大的比表面积和均匀的孔道结构;Ni/N-rGO催化剂中活性组分镍在N-rGO载体表面分散相对均匀,局部有团聚现象;适当氮原子的掺杂有利于提高催化剂的反应活性和选择性。

x—The conversion rate of phenol;s—The selectivity of cyclohexanone图9 20%Ni/N-rGO催化剂重复使用次数对催化苯酚加氢制环己酮的影响Fig.9 Effect of 20%Ni/N-rGO catalyst reuse times on hydrogenation of phenol to cyclohexanoneReaction conditions:T=150 ℃;p=0.4 MPa;t=2.0 h;m(Ni/N-rGO)/m(Phenol)=0.35
(2)通过考察催化剂的制备条件(活性金属负载量、尿素添加量及H2还原温度)和反应条件(温度、压力、时间)对Ni/N-rGO催化剂催化苯酚加氢制备环己酮的影响,得到Ni/N-rGO催化剂的最佳制备条件为:镍负载质量分数20%、尿素/GO质量比30、H2还原温度450 ℃;Ni/N-rGO催化剂催化苯酚加氢制备环己酮的最佳反应条件为:反应温度150 ℃、反应压力0.4 MPa、反应时间2.0 h;20%Ni/N-rGO催化剂在最佳反应条件下催化苯酚加氢制备环己酮,苯酚转化率可达91.93%,环己酮选择性可达61.75%。
(3)Ni/N-rGO催化剂制备工艺简单、成本低且具有较好的加氢性能,但其稳定性较差、高温易团聚,因此后续可以通过添加其他助剂或改进催化剂制备方法对Ni/N-rGO催化剂进一步改性优化。
