蛋壳制备羟基磷灰石及其对苯酚的吸附性能研究
2022-09-30毕鹏丽肖梓伊郭枫晚
毕鹏丽,曹 杰,张 锐,肖梓伊,李 玲*,郭枫晚,王 娟
(1.有机化工新材料湖北省协同创新中心 有机功能分子合成与应用教育部重点实验室 湖北大学化学化工学院,湖北 武汉430062;2.湖北兴发化工集团股份有限公司,湖北 宜昌 443000)
苯酚及其衍生物是造纸、焦化、炼油、塑料、纺织等工业废水中常见的剧毒有机污染物[1-3]。由于苯酚来源广泛、难降解、易富集,具有毒性和持久性,被列为优先污染物[4-5]。去除苯酚的方法有很多,其中吸附法应用最为广泛,最常用的吸附剂是活性炭[6-7],但活性炭成本较高。因此,开发高效去除苯酚的新材料具有重要意义。
羟基磷灰石(HAP)具有良好的吸附作用,可以去除废水中的金属离子[8]和某些有机物[9]。目前,制备HAP的方法较多,如溶胶-凝胶法[10]、化学沉淀法[11]、水热法[12]和微乳液法[13]等。
我国每年丢弃的鸡蛋壳(简称蛋壳)约40万t,大量废弃的蛋壳造成了严重的环境污染和资源浪费[14]。为了减少环境污染,提高蛋壳材料的利用价值,研究者[14-15]以蛋壳作为碳酸钙的替代来源制备HAP。在此,作者以蛋壳为原料,采用水热法制备HAP,并将其作为吸附剂吸附苯酚,研究初始苯酚浓度、HAP用量和pH值对HAP吸附苯酚性能的影响,拟为蛋壳的综合利用提供技术支持。
1 实验
1.1 材料、试剂与仪器
蛋壳,收集于学校厨房,洗净,干燥,粉碎。
NaOH、NH4H2PO4、苯酚,分析纯,国药集团化学试剂(上海)有限公司;实验用水为二次去离子水。
Bruker D8型X-射线粉末衍射仪,Bruker公司;傅立叶变换红外光谱仪,Perkin-Elmer公司;JSM6510LV型扫描电子显微镜,JEOL公司;Lambda 35型紫外可见分光光度计,美国PE公司。
1.2 HAP的制备及表征
将0.3 g蛋壳粉末分散于25 mL NH4H2PO4溶液(0.1 g·mL-1)中,并转移到四氟乙烯反应釜内,反应釜置于烘箱加热至200 ℃,24 h后冷却至室温;产物用蒸馏水和无水乙醇交替洗涤3次,60 ℃干燥24 h,即得HAP。
分别用X-射线粉末衍射仪、傅立叶变换红外光谱仪表征蛋壳、HAP的结构;用扫描电子显微镜观察HAP的形貌。
1.3 吸附实验
1.3.1 苯酚溶液的配制
将苯酚溶于二次去离子水,配制浓度为94.0 mg·L-1的苯酚溶液,并稀释至浓度(mg·L-1)分别为47.0、37.6、28.2、18.8、9.4、4.7;用0.1 mol·L-1盐酸或0.1 mol·L-1氢氧化钠溶液调节苯酚溶液的pH值分别为8、9、10、11、12、13。将配制好的苯酚溶液置于棕色玻璃瓶中,以防止光催化氧化。
1.3.2 吸附实验
取0.05 g制备的HAP置于装有不同浓度苯酚溶液的摇瓶中,一定转速下室温振荡60 min,将混合液置于离心管中,8 000 r·min-1离心8 min,取上清液,用紫外可见分光光度计测定其吸光度。按式(1)计算HAP对苯酚的平衡吸附量(Qe,mg·g-1),按式(2)计算HAP对苯酚的去除率(%):
(1)

(2)
式中:c0和ce分别为苯酚溶液的初始浓度和吸附平衡时的浓度,mg·L-1;m为HAP用量,g;V为苯酚溶液的体积,L。
2 结果与讨论
2.1 蛋壳和HAP的表征
蛋壳和HAP的XRD图谱、FTIR图谱如图1所示。

图1 蛋壳和HAP的XRD图谱(a)、FTIR图谱(b)

吸附苯酚前后HAP的SEM照片如图2所示。
由图2可知,吸附苯酚前,HAP的表面呈不均匀的块状(图2a、b);吸附苯酚后,HAP的表面出现了许多不均匀的块状固体(图2c、d)。因此,推断HAP对苯酚有一定的吸附作用。

图2 吸附苯酚前(a、b)后(c、d)HAP的SEM照片
2.2 HAP对苯酚吸附性能的影响因素
2.2.1 初始苯酚浓度的影响(图3)
由图3可知,随着初始苯酚浓度的增加,HAP对苯酚的去除率逐渐降低,而对苯酚的吸附量逐渐升高。

图3 初始苯酚浓度对苯酚去除率(a)和苯酚吸附量(b)的影响
2.2.2 HAP用量的影响(图4)
由图4可知,对于初始苯酚浓度相同的苯酚废水,随着HAP用量的增加,HAP对苯酚的去除率逐渐升高。因此,针对高浓度苯酚废水,增加HAP用量,有助于苯酚的去除。

图4 HAP用量对苯酚去除率的影响
2.2.3 pH值的影响
在室温、初始苯酚浓度为9.4 mg·L-1、HAP用量为0.10 g 的条件下,考察pH值对苯酚去除率的影响,结果如图5所示。
由图5可知,当pH值为10时,HAP对苯酚的吸附效果最佳。

图5 pH值对苯酚去除率的影响
2.3 吸附动力学
采用动力学方程对实验数据进行回归处理,探究HAP对苯酚的吸附动力学。准一级动力学方程和准二级动力学方程是研究吸附剂与吸附质之间作用机理较为常用的方法。
描述溶质在固体表面吸附的准一级动力学方程用式(3)表示:
ln(Qe-Qt)=lnQe-k1t
(3)
式中:k1为准一级吸附速率常数,min-1;Qe为苯酚的平衡吸附量,mg·g-1;Qt为t时刻苯酚的吸附量,mg·g-1。
以ln(Qe-Qt)对t作图,得到准一级动力学拟合曲线(图6)。拟合的准一级动力学方程为:y=1.18171-0.01567x,R2=0.9952。
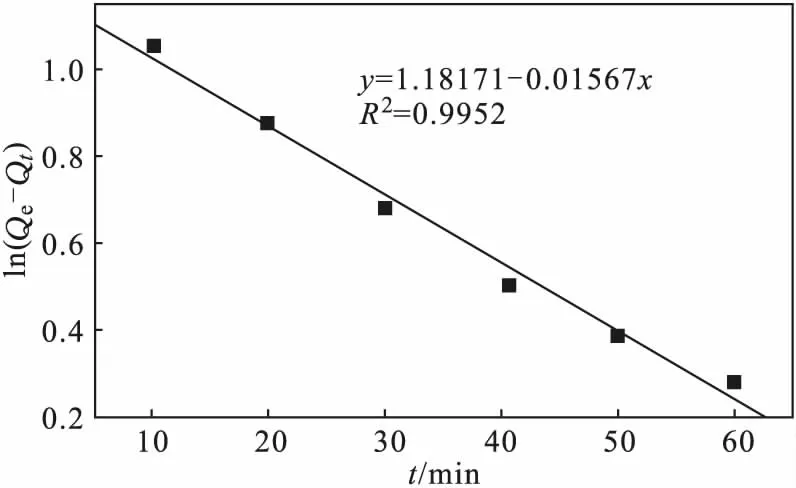
图6 HAP吸附苯酚的准一级动力学拟合曲线
描述溶质在固体表面吸附的准二级动力学方程用式(4)表示:
(4)
式中:k2为准二级吸附速率常数,g·mg-1·min-1。
以t/Qt对t作图,得到准二级动力学拟合曲线(图7)。拟合的准二级动力学方程为:y=-53.7243+43.97016x,R2=0.9596。

图7 HAP吸附苯酚的准二级动力学拟合曲线
准一级动力学方程的R2大于准二级动力学方程的,说明HAP对苯酚的吸附更符合准一级动力学方程。
2.4 等温吸附模型
为了更科学地描述HAP吸附苯酚的等温线,探究HAP的吸附类型及特点,选取Freundlich等温吸附模型和Langmuir等温吸附模型进行研究[16-17]。
(5)
式中:ce为吸附平衡时的苯酚浓度,mg·L-1;KF为Freundlich吸附常数,mg(1-1/n)·g-1·L1/n;n为常数。
以lnQe对lnce作图,得到Freundlich吸附等温线(图8a)。拟合的Freundlich等温吸附模型方程为:y=0.5018x+1.23912,R2=0.9908。
(6)
式中:Qm为理论上吸附剂最大吸附量,mg·g-1;KL为Langmuir吸附常数,L·mg-1。
以ce/Qe对ce作图,得到Langmuir吸附等温线(图8b)。拟合的Langmuir等温吸附模型方程为:y=0.0421x+0.49299,R2=0.9352。
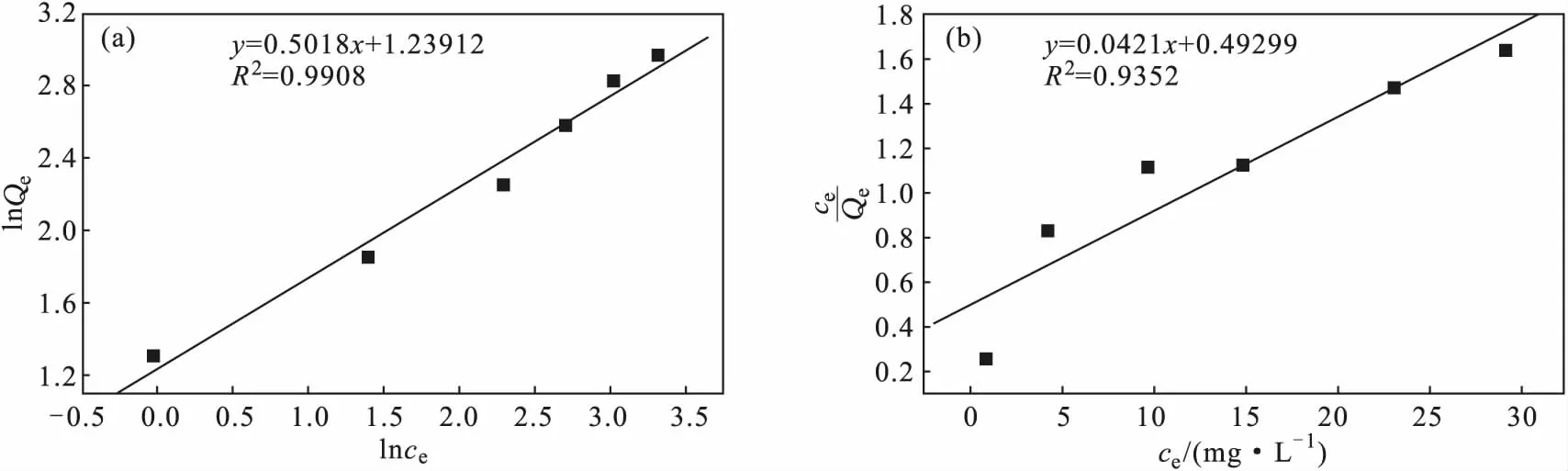
图8 HAP吸附苯酚的 Freundlich吸附等温线(a)和Langmuir吸附等温线(b)
对比图8a、b发现,HAP对苯酚的吸附更符合Freundlich等温吸附模型,说明HAP对苯酚的吸附是不均匀的单分子层物理吸附,且HAP具有很强的吸附能力。
3 结论
以蛋壳为原料,采用水热法制备HAP,研究了HAP对苯酚的吸附性能。结果表明,pH值为10时,HAP对苯酚的吸附效果最佳;HAP对苯酚的吸附过程符合准一级动力学方程和Freundlich等温吸附模型。该研究为蛋壳的综合利用提供了技术支持,但是HAP的重复回收利用是目前仍需解决的问题。
