基于动态共价键和非共价键相互作用的自愈合水凝胶研究进展
2021-12-30刘瑞雪陈纪超李迎博
刘瑞雪,陈纪超,李迎博
郑州轻工业大学 材料与化学工程学院,河南 郑州 450001
0 引言
水凝胶作为一种极其亲水的三维凝胶网络,能够在溶胀状态下吸收并保留大量水而不溶解,且其柔软的性能特点与人体软组织非常相似. 这种特殊的性能使得水凝胶材料广泛应用于生物医学、仿生材料等领域[1-3]. 然而,常规水凝胶被破坏或使用疲劳时,会使其失去原有性能,发生不可逆的损伤,这严重限制了水凝胶应用领域的扩展. 受生物系统内血管组织破裂的自修复、皮肤损伤后的自愈合等启发,在过去的一段时间内,许多研究人员对在损伤部位设计合成可自愈合的水凝胶产生了浓厚兴趣.
自我修复材料是指在损坏后能够自动将特性恢复到原始状态,从而延长使用寿命的材料. 自愈合水凝胶作为一种受损后可自我修复的功能性水凝胶,通过外部刺激(光、热量、pH值调节及自修复剂)或水凝胶内部官能团的相互作用(动态共价键、非共价键相互作用),可实现其自修复[4-7]. 但基于外部刺激的自愈合机制,通常会因外部刺激引起水凝胶发生相转变、性质不可逆变化或自愈合不能重复稳定发生而产生很大束缚,违背了自愈合设计的初衷. 因此,近年来,基于水凝胶自主式自愈合设计研究引起学者的广泛关注[8-10],一系列不同自愈合机制的功能性水凝胶应运而生,有效改善了水凝胶损坏后不能自主恢复的致命缺点,极大促进了水凝胶向多功能复合型水凝胶的发展,进一步拓宽了水凝胶在生物医用、人工智能、3D/4D生物打印等领域的应用. 本文基于水凝胶自主式自愈合机制,对近年来自愈合水凝胶的最新研究成果和应用现状进行梳理阐述,以期为未来设计开发性能更理想的自愈合水凝胶提供理论参考.
1 自愈合水凝胶概述
近期报道的关于水凝胶的自主式自愈合机制均基于其交联结构的可逆性,常常涉及动态共价键[11-12](如席夫碱键[13]、苯基硼酸酯络合物[14-15]、Diels-Alder 反应[16-19]和二硫键[20-21]等)及动态非共价键相互作用(如氢键相互作用[22-25]、离子相互作用(金属配位)[26-27]、主体与客体相互作用[28-30]、疏水性相互作用[31]等).众所周知,水凝胶的稳定性和自愈合能力及其机械性能与水凝胶合成过程中使用的化学键数量和强度(或类型)直接相关. 因此,了解水凝胶的自愈合机制对于设计不同自愈合效果的水凝胶至关重要.
1.1 基于动态共价键的自愈合水凝胶
传统化学法合成的共价键交联的水凝胶聚合物网络是不可逆的,且水凝胶往往呈现出较脆的性能,在使用过程中很容易疲劳或损坏. 而动态共价键作为一种可以在温和环境中可逆断裂-形成的化学键,因具有良好的动态可逆性,常被用于自愈合水凝胶的构建[32-35].
1.1.1 基于动态席夫碱键的自愈合水凝胶亚胺键是一种由伯胺和活性羰基(如醛基、酮基)通过可逆缩合反应生成的化学键,俗称席夫碱键.席夫碱键作为一类能动态可逆断裂重组的化学键,近年来被广泛引入水凝胶网络用于构筑自愈合水凝胶. 壳聚糖、聚乙烯亚胺等高分子聚合物可通过自身富含的氨基与含醛基、酮基的分子交联反应制备水凝胶,并可依靠亚胺键的动态可逆性获得独有的自愈合性能.


图1 基于动态席夫碱共价键的自愈合机理图[36]Fig.1 Self-healing mechanism based on dynamic covalent bond of Schiff Base[36]
1.1.2 基于硼酸酯键的自愈合水凝胶硼酸酯键作为一种能响应多种刺激(如温度、pH值等)的动态可逆共价键,同样被广泛应用于自愈合水凝胶的制备. 通常,以含有二醇结构的聚乙烯醇(PVA)或邻苯二酚结构的高分子为单体,与含有苯硼酸结构的高分子基于二醇-硼酸酯或邻苯二酚-硼酸酯络合形成硼酸酯键[39],用于自愈合水凝胶的分子设计.
G.F.Wu等[40]制备了PVA与改性海藻酸钠形成的自愈合水凝胶,合成机理如图2所示. PVA链上的羟基与改性海藻酸钠的苯硼酸基团形成动态重组的硼酸酯键,赋予水凝胶可以在几秒钟内完成的快速自愈合特性.而且,该水凝胶中甘油的存在增加了其耐寒性,在-25.1 ℃时仍表现出良好的抗冻性和弹性.
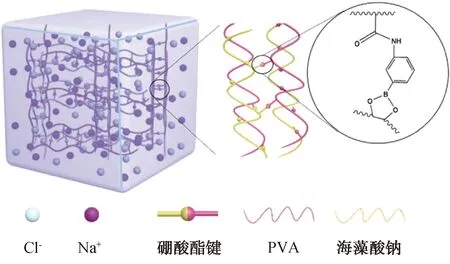
图2 PVA与改性海藻酸钠形成的自愈合水凝胶的形成机理及微观结构[40]Fig.2 Formation mechanism and microstructure of functionalized hydrogel composed of PVA and modified sodium alginate[40]
NaCl和其他无机盐还赋予该水凝胶良好的导电性,使其具有良好的类皮肤特性. F.Ji等[41]以甲基丙烯酸二甲氨基乙基酯(DMAEMA)为碱性单体,与1,4-苯二硼酸(BDBA)和N-羟甲基丙烯酰胺(NAM)自由基共聚合制备机械性能增强的室温自愈合水凝胶. 该凝胶表现出高达368 kPa的断裂应力、542%的断裂应变及良好的抗疲劳性能(在200%应变下进行拉伸循环实验后仅有轻微变形).由于BDBA与NAM间硼酸酯键的动态可逆性,所制备的水凝胶在室温下1 h内能成功恢复91%的断裂应力,并在24 h后实现100%的自愈合而无需外部刺激. 该水凝胶还具有pH响应性,酸性(pH=5)和中性(pH=7)条件下凝胶的机械性能恢复速率远小于碱性条件下的水凝胶. 这种简单有效的制备方法为基于硼酸酯键的自修复材料提供了一种新颖的思路,有望扩大自愈合凝胶在智能材料中的应用范围.R.W.Guo等[42]以双(苯基硼酸氨基甲酰基)胱胺(BPBAC)的硼酸基团为交联剂,与二醇或邻苯二酚发生络合反应,形成了含有多巴胺的甲基丙烯酰胺(DOPMA)水凝胶,其自愈合与响应机理如图3所示. 硼酸酯与邻苯二酚之间的动态平衡和键重排不仅可以赋予水凝胶多重响应性,而且还使其具有优异的自愈合能力. 切开的两片水凝胶无需外部处理就可以在约1 min内自动融合为一体,且大约5 min后,在自愈合区域观察不到明显的切割痕迹. 此外,愈合后的界面坚固到足以承受凝胶自身的重量. 大振幅重复扫描流变测试结果显示,该水凝胶的内部微结构重组修复可以瞬时完成. 这种无需外部干预即可快速自动愈合的过程,使得该自愈合水凝胶在智能药物输送系统、医用胶粘剂、密封胶等领域具有潜在的应用前景.

图3 BPBAC与二醇或含邻苯二酚的聚合物形成自愈合水凝胶及多重响应机理示意图[42]Fig.3 Schematic diagram of self-healing hydrogel formed by BPBAC and diol or catechol-containing polymer and its representative mechanism of multi-reactivity[42]
1.1.3 基于二硫键的自愈合水凝胶二硫键是动态可逆的共价键,普遍存在于生物体中,对维持蛋白质的三级结构和细胞内氧化还原电位起着重要的作用. 二硫键受pH值、氧化还原剂等外界环境的影响,可实现与硫醇的快速转变,被广泛应用于制备自愈合水凝胶.G.H.Deng等[43]开发了一种基于二硫键和酰基腙键的自愈合水凝胶. 在碱性环境下,该水凝胶通过二硫键-硫醇的转变反应实现了自愈合. 自愈合过程在室温下触发,无需外部刺激. 自愈合48 h的水凝胶的应力-应变测试曲线显示,断裂应力和应变可达到原始强度和伸长率的50%以上.酰基腙键的存在也使该凝胶在中性和酸性条件下具有自愈合能力. 二硫键和酰基腙键还可以响应化学试剂(例如二硫赤藓糖醇或H2O2)的刺激,使凝胶发生独特的溶胶-凝胶可逆转变. 因此,含二硫键和酰基腙键的自愈合水凝胶的多响应性将使其作为智能软材料,在器官修复或刺激响应性药物传递方面发挥巨大的作用.
1.1.4 基于Diels-Alder(DA)反应的自愈合水凝胶DA反应具有快速、高效、选择性高、无副产物等优点,被认为是交联水凝胶中最理想的共价键[44-46]. DA环加成反应具有可逆性,可用于自愈合水凝胶的制备[47-49].
C.Y.Shao等[50]开发了一种通过可逆的DA反应将呋喃基改性纤维素纳米晶体(CNC)与马来酰亚胺末端官能化的PEG交联,制备CNC-PEG纳米复合水凝胶简便有效的方法,合成路线与自愈合机理如图4所示. 该水凝胶表现出良好的机械性能、抗疲劳性和自愈合性,90 ℃条件下即可促进其自愈合,且机械性能恢复78%. CNC-PEG水凝胶良好的自愈合性能为设计高性能生物相容性水凝胶提供了新的思路.W.Zhao等[47]报道了以细胞相容性富烯改性的葡聚糖为主链,二氯马来酸改性的聚乙二醇为交联剂,生理条件下(pH=7.4、37 ℃)制备可逆的DA反应交联的葡聚糖基自愈水凝胶,该水凝胶在生理条件下表现出优异的自愈特性. 这项研究提供了一种制备多糖自修复水凝胶的简便方法,拓宽了自愈合水凝胶在细胞封装等生物医学领域的应用空间.

图4 自愈合CNC-PEG纳米复合水凝胶的合成路线与自愈合机理示意图[50]Fig.4 Schematic diagram of synthesis route of self-healing CNC-PEG nanocomposite hydrogel and self-healing mechanism[50]
动态共价键既拥有传统共价键优异的稳定性能,又具有断裂后自主缔合的特点,对水凝胶的自愈合有着重要的促进作用. 席夫碱、硼酸酯键、二硫键、DA反应共价键都是典型的动态共价键,基于这类化学键制备的自愈合水凝胶得到了很好的发展,极大延长了水凝胶基柔性材料的使用寿命. 但是,动态共价键的稳定性也存在对自修复环境(如pH值、温度等)要求较高的缺点.因此,构筑能在多种环境下发生自愈合行为的水凝胶是自愈合水凝胶研究的一个重要方向.
1.2 基于动态非共价键相互作用的自愈合水凝胶
动态非共价键相互作用是一种物理相互作用,具有天然的动态断裂重组可逆性和稳定性,是设计自愈合水凝胶的良好选择. 近年来,基于动态非共价键相互作用自愈机理制备自愈合水凝胶的研究受到了研究者青睐.
1.2.1 基于离子相互作用的自愈合水凝胶离子相互作用(金属配位)通常是指具有空轨道的过渡金属离子(Fe3+、Zn2+、Cu2+等)与含有孤对电子的基团(-COOH、-NH2、-OH等)的配位(螯合)作用,具有配体选择范围广、可快速响应、可调控的优点,在自愈合水凝胶合成中应用十分广泛[51].
T.T.Li等[52]通过预制、掺合和Al3+浸渍法,制备了聚丙烯酸-壳聚糖@单宁酸-铝离子(PAA-CS@TA-Al3+)双网水凝胶,合成示意图如图5所示. 交联的网络结构赋予凝胶优异的拉伸性(≈32 kPa)和断裂伸长率(≈1700%);Al3+与PAA的羧基、CS@TA的邻苯二酚的动态结合,赋予该水凝胶良好的自愈合性能,在60 min内自愈率约为92.2%;动态流变测试结果表明,自愈合后凝胶的储能模量(G′)可以恢复到96%,证实了其良好的自愈合能力. 此外,CS@TA使凝胶具有黏性,进一步加速了自愈合过程. W.Chen等[53]将羧甲基纤维素钠(CMC)引入PAA-Fe3+水凝胶,赋予了其高拉伸强度(4.42 MPa)、高韧性(耗散能达1.98 MJ/m3)和良好的自愈合性能.该水凝胶优异的自修复性能归因于PAA与CMC之间的金属离子配位键的动态重建.
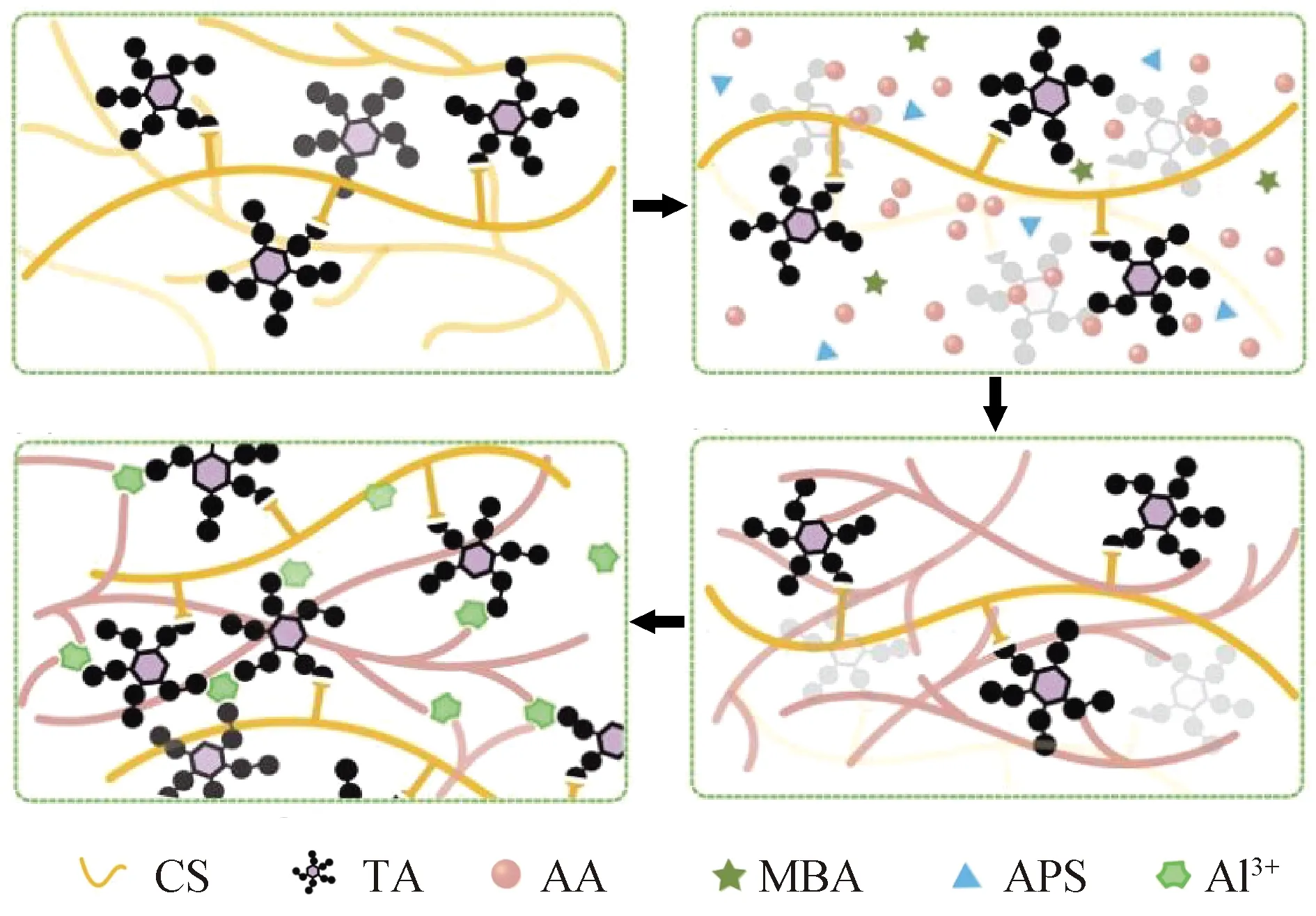
图5 PAA-CS@TA-Al3+双网络水凝胶的合成示意图[52]Fig.5 Schematic diagram of the synthesis of PAA-CS@TA-Al3+ double network hydrogel[52]
1.2.2 基于氢键相互作用的自愈合水凝胶
氢键是氢原子直接与高电负性原子(如氧原子、氮原子、氟原子)相互作用形成的,具有分子间易形成的优点,且随所处环境温度和pH值变化表现出不同的性质,即拥有可逆变化的能力. 当水凝胶受到外界破坏时,聚合物的分子链在氢键的作用下具有流动性,从而赋予其自愈合性[54].
X.X.Sun等[55]利用氢键相互作用制备了具有优异机械性能的自愈合PVA-琼脂水凝胶. 该水凝胶经冻融循环后,PVA分子间、PVA分子与琼脂分子间会形成氢键,使该水凝胶具有自愈合性能. 愈合后的水凝胶可以承受2.3 kg的重量、5.0 MPa的拉伸强度,断裂伸长率可达450%. J.S.Chen等[56]利用多重氢键的动态非共价键相互作用开发了一种具有良好可拉伸性、高电导率(13 s/m)和快速自愈合能力(30 s内完全的自愈合)的多功能聚苯胺/聚(4-苯乙烯磺酸盐)-2-脲基-4 [1H]-嘧啶酮水凝胶(PANI/PSS-UPy),其合成路线和非共价键相互作用机理如图6所示. UPy的多重氢键赋予了该水凝胶优异的自愈合能力,且该水凝胶能够准确、可靠地监测多种人体活动,包括手指和手腕弯曲的大运动,吞咽、说话、脉搏跳动等细微运动,因此该水凝胶在生物传感材料方面具有一定的应用潜力.

图6 PANI / PSS-UPy水凝胶的合成路线和非共价键相互作用机理示意图[56]Fig.6 Schematic diagram of the synthesis process and noncovalent interaction mechanism of PANI/PSS-UPy hydrogel[56]
1.2.3 基于疏水相互作用的自愈合水凝胶疏水相互作用[57]是疏水性聚合物链段在水溶液中相互聚集、缔合,形成动态的交联点[58],疏水缔合微区的可逆分解赋予水凝胶自愈合的能力,是开发自愈合水凝胶的常用方法之一. 改变疏水单体的化学结构、位置或含量可以调整疏水相互作用的强度,改善水凝胶的性能[59].
Q.F.Zheng等[60]利用海藻酸钠(SA)与Fe3+形成一个交联网络、十二烷基硫酸钠(SDS)胶束增溶的甲基丙烯酸十八烷基酯(SMA)和丙烯酰胺(AM)共聚后形成以胶束为物理交联点的另一个交联网络,设计合成了具有两个物理交联网络的互穿PAM/SA-Fe3+水凝胶,合成路线及交联机理如图7所示. 断切后,70 ℃条件下静置12 h后,该水凝胶可以完全自愈合.

图7 PAM/SA-Fe3+水凝胶的合成路线及交联机理示意图[60]Fig.7 Schematic diagram of the preparation of PAM/SA-Fe3+ hydrogel and its network structure[60]
L.Ye等[61]受完全物理交联的凝胶机理启发,选择以具有热凝化性能的多糖(Curdlan)为第一网络,以阴离子表面活性剂SDS、阳离子表面活性剂十六烷基三甲基溴化铵(CTAB)共同作用的胶束增溶SMA与AM共聚合,形成以胶束为物理交联点的第二网络,一锅法制备了具有良好机械性能、自恢复和自愈合性的双网络水凝胶,其在95 ℃条件下自愈合4 h后,各项性能恢复率约为50%.
1.2.4 基于主-客体相互作用的自愈合水凝胶主-客体相互作用一般发生在两个或多个化学物质通过非共价键相互作用时. 在超分子主-客体相互作用中,当一部分(客体)物理插入另一部分(宿主)时,两者之间会通过非共价键相互作用保持在一起,通过这种相互作用可逆性构造的聚合物网络表现出自愈合性质. 环糊精、金刚烷等主体大分子与客体分子间的相互作用被广泛用于自愈合水凝胶的制备.
Y.Zhou等[62]提出了一种基于“超分子交联剂”方法的分子设计,制备了具有超强可拉伸性、自愈合性、可注射性和理想的生物相容性的新型主、客体水凝胶,制备示意图如图8所示. 星形超分子交联剂HGP是由含有八个环糊精多面体的低聚倍半硅氧烷(OCDPOSS)和丙烯酰胺改性的金刚烷(Ad-AAm)之间经主-客体相互作用形成的. 刚性的OCDPOSS作为超分子交联剂的核心,赋予超分子水凝胶优异的机械性能;多价宿主与客体的相互作用改善了这些水凝胶的延展性,促进了凝胶网络内链的滑移和有效的客体识别功能,提供了HGP基水凝胶良好的机械行为和快速的自愈合特性.Z.X.Deng等[63]利用超分子主-客体相互作用制备了基于β-环糊精(β-CD)、N-异丙基丙烯酰胺(NIPAM)、多壁碳纳米管(CNT)和纳米结构聚吡咯(PPY)的自修复导电水凝胶.β-CD与NIPAM之间的超分子主-客体相互作用赋予了该水凝胶优异的稳定性和良好的自修复性能:连续应变测试显示,高应变扫描时(PNIPAM-co-β-CD)/CNT/PPY水凝胶的G′从380.0 Pa降至1.8 Pa;应变扫描恢复到1%,G′也能立即恢复.

图8 超分子交联剂HGP及其水凝胶的制备示意图Fig.8 Preparation of HGP supramolecular crosslinker and HGP hydrogel
基于离子、氢键、疏水缔合和主-客体等动态非共价键相互作用形成的自愈合水凝胶,快速的自愈合能力促进了其在生物医学、电子传感等方面的应用发展. 但由于动态非共价键的作用力较弱,水凝胶往往存在力学性能较差的缺点,这在一定程度上限制了自愈合水凝胶应用领域的扩展.
2 自愈合水凝胶的应用
自愈合水凝胶作为一种既拥有良好的自愈合性、耐疲劳性和可重复循环使用性,又兼具常规水凝胶的亲水性、对环境刺激的响应性等优点的新型功能性水凝胶,成为目前水凝胶研究的热点之一. 近年来,随着国内外专家学者对自愈合水凝胶的深入研究,自愈合水凝胶的应用领域得到了极大扩展,其在伤口敷料和药物输送、组织工程、仿生电子皮肤、可穿戴电子设备等领域显示出巨大的发展潜力.
2.1 伤口敷料和药物输送
自愈合水凝胶作为一类含水量很高的新型功能高分子材料,因其良好的吸水溶胀性、生物相容性、独特的自愈合性等优点,是生物医学理想的生物材料. 随着自愈合水凝胶制备策略的不断成熟,其应用领域也逐步扩大,特别是在伤口敷料、药物输送等方面的应用研究取得了较大进展.
Y.Zhu等[64]报道了一种基于多种次级键物理交联(包括氢键、疏水力和静电相互作用)的智能离子明胶/聚丙烯酰胺/纳米黏土水凝胶(GPNs).该水凝胶由于含有带负电荷的纳米黏土,表现出较高的电导率(10.87 mS·cm-1)、自愈率(在60 min内达到85%)和牢固的黏附力(最高达485 J·m-2),且具有多种响应性(如盐离子、pH值、应力响应性)、可观的压力传感线性响应性(施加压力高达2 kPa)及良好的生物相容性,为其在伤口敷料、药物输送领域的应用奠定了基础. M.Wu等[65]基于醛基化的聚合物和胺修饰的SiO2纳米颗粒之间的希夫碱反应,设计了一种易于制备的可注射、快速自愈合和超敏感的pH响应纳米复合水凝胶. 该水凝胶还具有良好的生物相容性、生理条件下极好的稳定性和弱酸诱导的急剧凝胶-溶胶转变性,使其有望作为局部给药的药物载体用于癌症治疗、伤口愈合、感染治疗等方面.
2.2 组织工程
水凝胶内部含有大量的水分,通常具有较好的亲水性和良好的黏弹性;其内部独特的三维网络结构使其具有与细胞外基质相似的结构,不仅具有良好的结构稳定性,还能够从外部转移营养,是组织工程支架的理想材料. 近年来,基于自愈合性水凝胶的组织工程应用报道日益增多.
X.Jing等[66]受贻贝黏性蛋白的启发,开发了壳聚糖/氧化石墨烯/聚多巴胺复合水凝胶,并将其用于组织工程材料,发现该水凝胶表现出优异的机械性能(50%压缩应变下,压缩强度从4 kPa到12 kPa,压缩恢复率为91%)、粘合性(粘合强度从0.15 MPa到0.95 MPa)、高稳定性(G′约250 Pa)、可注射性和快速自愈合性. 此外,该水凝胶还显示出对成纤细胞和心肌细胞的增殖作用(培养4 d后细胞存活率超过90%),且观察到了心肌细胞更快的自发搏动行为.这些优异的性能均表明该水凝胶在组织工程应用中的巨大潜力. M.Vahedi等[67]开发了一类基于席夫碱键的由明胶和支链淀粉多醛形成的可注射自愈合水凝胶. 经该水凝胶培养的人类骨髓源间充质干细胞(hBMSCs)5 d后存活率为85%~90%,14 d后可为骨细胞分化提供骨诱导支持,表明该水凝胶在细胞治疗、骨组织工程上具有很大的应用潜力.
2.3 仿生电子皮肤
随着人工智能领域的不断创新和发展,电子皮肤作为一种新型的仿生材料受到广大科研工作者的关注. 具有导电性能的自愈合水凝胶,因其柔软的机械性能、优异的自愈合性及外部刺激—电信号响应性,可以很好地满足电子皮肤应用的需求,使其成为电子皮肤的最佳材料之一.
R.Y.Yang等[68]通过便捷的预还原和一锅法制备了基于聚丙烯酸(PAA)和还原氧化石墨烯(rGO)的可伸缩、导电、自修复的PAA-rGO水凝胶. PAA与rGO之间构建的共价(酯键)和非共价(氢键)的分子间网络为PAA-rGO水凝胶提供了良好的机械、导电和自修复性能(室温下30 s内快速自愈,自愈率95%). 该水凝胶可直接连接到人体皮肤上作为应变传感器,监测外部运动,包括手指弯曲和腕部扭曲;且经自愈合的水凝胶仍能准确、可靠地检测外部应变,并稳定地显示出与断切之前相似的电流曲线. 这种愈合后仍能灵敏应变响应的特点表明该水凝胶在仿生电子皮肤中具有巨大的应用潜力.Y.J.Liu等[69]通过Fe3+和纤维素纳米晶体的动态离子配位,形成CNCs-Fe3+自愈合水凝胶.该水凝胶具有较高的拉伸性(断裂应变达1160%)、韧性((4.7±0.08) kJ·m-2)、弹性可恢复性(200%应变前的磁滞可忽略不计)和自愈合性(5 min内100%自愈),且该水凝胶在作为应变传感器使用时,能够准确、可靠地监测各种人类活动(包括手指弯曲、脉搏和呼吸检测),表明该凝胶在离子皮肤等方面具有应用潜力.
2.4 可穿戴电子设备
自愈合水凝胶作为一种无刺激性、损伤后可自主修复的柔性聚合物材料,在柔性可穿戴电子设备领域的应用潜力十分巨大. 随着柔性可穿戴传感器在健康监测和人机接口界面中应用要求的不断提高,为构建新型多功能自愈合水凝胶提供了新思路. 当前,科研人员在自愈合水凝胶作为传感器用于可穿戴电子设备监测人体运动方面的研究已取得了很大的进展.
J.F.Tie等[70]将Fe3+与聚乙烯醇乙酰乙酸酯(PVAA)/聚丙烯酰胺(PAM)共混制备了高度可拉伸/压缩的Fe3+/PVAA-PAM双网络自愈合水凝胶. 离子配位与物理交联的结合赋予了该水凝胶突出的可拉伸性(>700%)、高灵敏度、高愈合效率(24 h内80%)和良好的抗疲劳性. 此外,Fe3+的引入赋予了该水凝胶离子导电性,可用于可穿戴电子设备,在应变传感、压力传感、人体运动监测等方面显示出良好的应用潜力.J.Mao等[71]通过一步原位聚合法制备了基于离子配位交联与氢键相互作用的PAA-GO双网络自愈合性水凝胶. 该水凝胶表现出较高的自愈合效率(88.64%),并具有应变敏感性(在5%~50%的不同变形下表现出近似线性的响应,应变灵敏度为0.46)和可重复监测性(如对手指、腕部和肘部弯曲的身体运动的监测,在30%应变下循环500次,水凝胶相对电阻变化保持稳定).该水凝胶稳定、快速的响应行为和可重复监测性促进了其在可穿戴传感设备中的应用. L.L.Han等[72]受天然贻贝粘附机制的启发,通过原位聚合开发了一种基于PS-PAM(韧性层)/PDA-PAA(黏性层)的双层水凝胶. 该水凝胶具有优异的电导率(0.03 S·cm-1)、韧性(0.18 MPa)、附着力、自愈合性及稳定、灵敏的应变响应性. 作为应变传感器使用时,该水凝胶可直接粘附于人体皮肤监测人体动作与振动(电阻随肢体弯曲程度或振幅变化),且可多次重复. 此外,自愈合后的凝胶传感能力与原始水凝胶几乎相同.(PS-PAM)/(PDA-PAA)双层水凝胶优异的自愈合性、可粘附性、良好的信号检测灵敏度、稳定性和可重复性使其成为理想的柔性可穿戴应变传感器的候选材料,有望用于进一步的商业开发应用研究.
3 结语
本文以自愈合水凝胶的自愈合机理为出发点,分别对基于动态共价键(席夫碱键、硼酸酯键、二硫键及DA反应)和非共价键相互作用(氢键、离子相互作用、疏水相互作用及主-客体相互作用)的自愈合水凝胶的设计策略及自愈合水凝胶在伤口敷料、药物输送、组织工程、仿生电子皮肤、可穿戴电子设备等方面的应用进行了综述. 然而,目前对于自愈合水凝胶的认识依旧不够深入,单一的基于动态共价键或动态非共价键相互作用机制的自愈合水凝胶仍然存在力学性能弱、自愈条件苛刻、不能完全恢复等不足. 因此,如何在传统水凝胶优异性能的基础上赋予其独特的自愈合能力仍是未来需进一步思考和探索的方向.
本文对动态共价键和动态非共价键相互作用自愈机制的梳理与总结,为有效设计多重自愈网络机制的自愈合水凝胶,实现其优异的力学性能与多功能性(光响应、热响应等)相结合提供了理论参考;同时,也为进一步推动自愈合水凝胶作为智能软材料、生物材料迈向更高阶的应用提供了研究思路和方向.
