多发性骨髓瘤自体干细胞移植后中枢神经系统复发1例并文献复习
2021-12-20谢琼妮万程尧姚奕斌刘振芳
谢琼妮,万程尧,姚奕斌,周 莉,刘振芳
(广西医科大学第一附属医院血液内科,南宁 530021)
多发性骨髓瘤(multiple myeloma,MM)是以骨髓中克隆性浆细胞异常增生为特征的血液系统恶性肿瘤,以骨痛、贫血、肾功能损害、高钙血症为主要表现。MM累及中枢神经系统(CNS)是一种罕见的髓外病变(EMD),以浆细胞浸润中枢神经系统、脑膜或脑脊液(CSF)为特征,可在MM 初步诊断或疾病复发时出现。MM约占所有恶性肿瘤的1%,占血液恶性肿瘤的10%~15%[1]。大约7%的患者初步诊断时即伴有EMD,6%的患者在疾病复发时出现EMD[2]。多发性骨髓瘤中枢神经系统受累(CNSMM)较为罕见,约占所有MM 病例的1%,预后不良[3]。现报道广西医科大学第一附属医院MM自体干细胞移植后中枢神经系统复发1 例,并作文献复习。
1 临床资料
患者,女,50岁。因“后颈部不适2年,加重伴四肢乏力1 月”于2016 年3 月入院。既往史无特殊。查体:双侧颈肌紧张,C2~C5 两侧压痛,四肢肌力Ⅳ级,病理征阴性。查血常规:WBC 4.87×109/L,Hb 57.00 g/L,PLT 137.50×109/L。血清钙:3.061 mmol/L。免疫球蛋白3项:IgG 0.580 g/L,IgA 60.662 g/L,IgM 0.068 g/L。尿液β2-MG:0.278 µg/mL,血清β2-MG:4.12µg/mL。血清免疫固定电泳:IgA+κ型。尿液免疫固定电泳:κ型,lgGAM有反应性,κ 轻链有反应性,游离κ 轻链有反应性。骨髓形态学:MM骨髓象,骨髓增生活跃,G=25%,E=15%,粒系增生减低,红系增生活跃,浆细胞异常增生,占54%。活检:骨髓增生活跃,大量中等分化的浆细胞增生。颈椎及胸椎CT:颈椎、胸椎、肋骨、颅骨、颌面骨及下颌骨多发骨质破坏,并脊髓受压。诊断:MM IgA+κ 型DS Ⅲ期A 组ISS Ⅱ期R-ISS Ⅱ期高危组。在对症支持治疗基础上,于3月12日、4月30日予CyBorD方案(硼替佐米2 mg/d1、d4、d8、d11+CTX 300 mg/d1、d8+DXM 20 mg/d1~d4、d8、d11)化疗。
2016 年5 月14 日患者出现持续性四肢末端麻木,持物不稳,考虑硼替佐米药物不良反应,暂不化疗。2016年6月患者四肢麻木较前加重,手指僵硬,行走不稳,脚踩棉花感。查骨髓形态学:骨髓增生明显活跃,粒、红、巨三系均可,未见异常浆细胞。于2016 年8 月8 日、9 月23 日、11 月9 日、12 月21 日予CD 方案(CTX 300 mg/d1、d8+DXM 20 mg/d1~d4、d8~d11)化疗。2017年3月9日返院,查骨髓形态学:原诊MM,现骨髓增生活跃,粒、红、巨三系增生均可。活检:镜检见多量骨质及少许伴有挤压的有核细胞,中晚幼以后粒红细胞为主,数个巨核细胞。患者完全缓解(CR),于2017 年3 月21 日予大剂量CTX 方案化疗(CTX 2.8 g/m2d1~d2)、重组人粒细胞刺激因子(C-GSF)250µg q12 h动员外周血干细胞,4月12日、13日采集干细胞,4月14日回输自体外周血干细胞MNC 22.69×108/kg,CD34+细胞7.17×106/kg。2017 年9 月返院,查血尿免疫固定电泳阴性,血清蛋白电泳阴性,骨髓形态学:原诊MM,现骨髓增生活跃,粒、红、巨三系增生可,未见原幼浆细胞。患者CR,但存在t(4;14)染色体异常,建议继续巩固治疗,患者拒绝,选择来那度胺10 mg/d继续治疗。
2018 年9 月14 日返院,查血清免疫固定电泳:IgA+κ型。尿液免疫固定电泳:蛋白少,未见全部对应带。骨穿结果:浆细胞骨髓瘤治疗后(瘤细胞约占50%)。骨髓流式细胞术:髓系区域细胞约占有核细胞的72%,其中可见约17%异常细胞,主要表达CD38+、CD56-、CD138-、cKappa+细胞,考虑为免疫表型异常的残留浆细胞。头颅、颈、胸、腰椎及骶尾椎平片:头颅、颈、胸、腰椎各椎体及骨盆均有骨疏松,其内满布大小不等之穿凿样骨质破坏区,符合MM改变;颅内未见异常(图1)。患者CR 后复发,于2018 年9 月、11 月、12 月,2019 年3 月予VRD 方案(硼替佐米1.8 mg/d1、d4、d11、d18+地塞米松20 mg/d1、d4、d11、d18+来那度胺25 mg/d1-21) 化疗。2019年4月23日患者出现头痛,伴恶心,呕吐,呕吐物为胃内容物,非喷射性。查体:双侧瞳孔不等大,左侧直径3 mm,右侧直径2 mm,左侧肢体肌力Ⅴ级,右侧肢体肌力Ⅳ级,右侧巴氏征阳性。查头颅CT:左侧颞叶见一类圆形稍高密度肿块,大小约4.1 cm×2.6 cm(图2)。颅脑MRI+MRA:左侧颞部占位,大小约4.3 cm×5.8 cm×4.6 cm,左侧大脑中动脉及分支受压移位(图3)。于2019年4月30日行开颅左颞部肿物切除术,术后病理:镜下见肿瘤细胞形态大小较一致,弥漫性分布,浸润骨骼肌组织,可疑淋巴造血组织肿瘤。免疫组化:CD138(+),CD38(+),κ(+),λ(-),IgG(+),CD79α(+)灶性,Ki-67(+)约70%,考虑为中枢神经系统浆细胞瘤。术后予脱水降颅压、抗感染、营养神经及中医特色治疗,2019年6 月11 日复查骨髓形态学:原幼浆细胞占11.5%。活检:符合浆细胞骨髓瘤(瘤细胞约占85%)。骨髓流式:髓系区域细胞约占有核细胞的55%,其中异常细胞约占有核细胞的12.5%,主要表达CD38、CD56、cKappa,考虑为免疫表型异常的浆细胞。于2019 年6 月17 日予IRD 方案(伊沙佐米4 mg/d1,d8,d15+来那度胺25 mg/d1~d21+地塞米松20 mg/d1,d8,d15,d22)化疗。患者仍有轻微头痛、四肢麻木,四肢肌力Ⅴ级,2019 年6 月22 日出院,2019 年8 月上旬因头部术口处迅速长出一拇指头大小包块,轻微头痛,至当地医院急诊科就诊,予内科保守治疗,一周后呼吸、循环衰竭死亡,未行尸检。
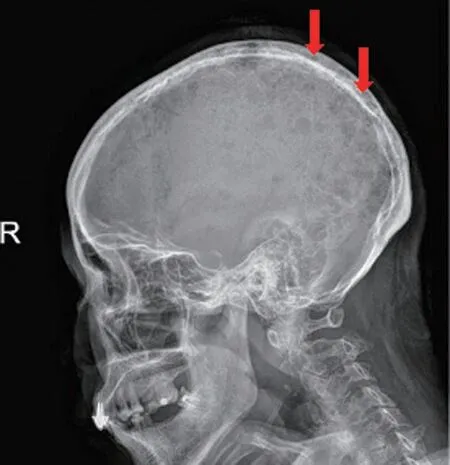
图1 头颅平片

图2 头颅CT
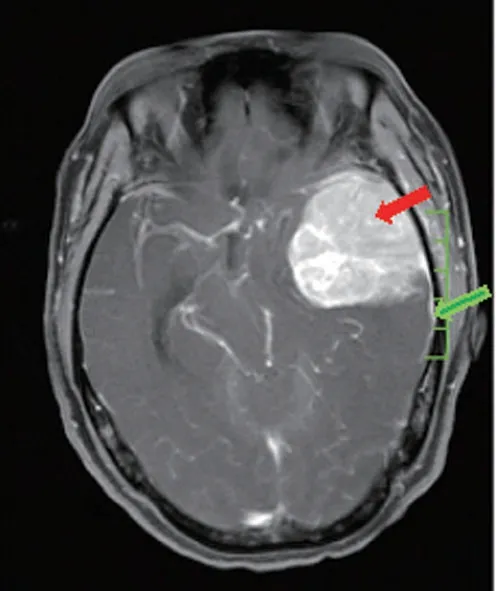
图3 颅脑MRI
2 讨论
MM 是浆细胞异常克隆增生性疾病,克隆性的浆细胞通常在骨髓内增殖,EMD 为MM 的表现之一。MM 患者出现中枢神经系统软组织肿瘤,为骨外髓外病变(EM-E)。CNS-MM是一种高度侵袭性的终末期疾病,与高β2-MG、乳酸脱氢酶(LDH)水平相关,β2-MG 提示MM 肿瘤负荷,与预后密切相关,高LDH 水平反映肿瘤高负荷及疾病的侵袭性[4]。常见的中枢系统受累症状主要包括头痛、肢体乏力、精神改变、认知功能障碍和脑神经麻痹等。多发性骨髓瘤自体干细胞移植后中枢神经系统累及的病例报道较少[5-10]。本例以骨痛为首发症状,为IgA+κ 型DS Ⅲ期A 组,具有预后不良因素t(4;14)染色体异常,行自体干细胞移植术(ASCT)24 月后,出现CNS 复发,颅脑病理活检确诊为中枢神经系统浆细胞瘤。在MM 疾病过程中任何阶段出现CNS受累均是独立的不良预后因素,总生存期小于6个月[11]。另有研究报道,CNS-MM预后极差,总体中位生存时间为2个月[12]。31例接受了全身化疗及鞘内注射治疗的MM患者,自确诊CNS-MM至死亡的中位生存期为4 个月[4]。在172 例CNS-MM的多中心回顾性分析中,整组中位生存期为7个月,未治疗和治疗的患者中位生存期分别为2 个月和8个月[13]。本例自自体干细胞移植至骨髓瘤临床和血液生化复发17个月,自骨髓瘤至CNS复发37个月,自自体移植至CNS复发24个月,总生存期44个月,自自体移植至死亡28个月,自CNS复发至死亡4个月。
CNS-MM的发病机制尚不明确,目前有以下几种假说:一种是恶性浆细胞通过血源性传播或浆细胞前体(淋巴细胞)脑脊膜传播;一种是颅骨溶骨性病变突破骨皮质直接侵犯;一种是克隆异质性,复发与耐药克隆群体的产生有关。MM进程可能与一系列基因事件相关,基因打击推动了克隆演化和亚型演变。抑癌基因TP53、癌基因RAS 突变可导致骨髓瘤细胞逃逸骨髓微环境,侵袭、浸润至髓外器官。EMD时浆细胞可以通过改变黏附分子的表达,使其能够归巢到其他器官,趋化因子受体表达减少(CCR1、CCR2 和CXCR4)及黏附分子表达下调(VLA-4、CD44 和CD56)被认为是关键因素[14]。本例患者骨髓CD56 阴性,未能检测髓外病灶中MM细胞CD56 的表达,这些机制是否与本例相关仍需进一步确定。
本例患者于2016 年3 月确诊MM,行自体干细胞移植术24 个月后出现头痛明显、四肢肌力减弱,影像学诊断考虑倾向于脑膜瘤。肿瘤切除后组织病理学提示IgG、kappa 轻链、CD38 阳性,诊断为中枢神经系统浆细胞瘤。患者行手术切除后,未行放疗,4 月后死亡,中枢神经系统浆细胞瘤是该例死因。文献指出,关于颅内浆细胞瘤最佳的治疗方法是完全手术切除,及时恢复颅内压、重建神经功能,术后接受放疗。与对照组相比,颅脑放疗可显著延长CNS-MM 患者的生存期[12]。少数患者可通过放疗、鞘内注射和应用免疫调节剂来实现长期生存,获得17.1个月的中位生存时间[11]。本例患者MM自体干细胞移植后,出现CNS 占位性病变,术后病理证实为浆细胞瘤,为及时挽救生命,患者接受开颅手术彻底清除病灶,但仍不能延缓疾病的进展、改善生活质量。这提示我们在MM的诊治过程中,由于大多数患者在确诊时年龄较大、基础疾病较多、药物不良反应等因素可能掩盖CNS受累的症状,需早期警惕和及时发现骨髓瘤CNS累及,并注意与脑膜瘤、转移癌、大细胞淋巴瘤及原发于神经系统的髓外浆细胞瘤相鉴别。MRI 增强检查比CT 更敏感,是检测CNS-MM 的首选方法,但存在一定的假阴性率。综合影像学、组织病理学、脑脊液检查、立体定向活检结果有助于明确诊断。该患者在疾病的诊疗及进展过程中,因颈椎、腰椎压缩性骨折及颅内压升高有形成脑疝的风险,未行腰椎穿刺术及鞘内注射。目前,CNS-MM 缓解率低、治疗手段有限、生存期短,临床诊治过程中常规脑脊液检查及鞘内预防性注射的疗效尚需进一步探讨。
髓外浆细胞瘤是MM 独立的不良预后因素,CNS-MM的预后因素尚未明确,细胞遗传学异常在EMD预后中具有重要价值,既往至少接受过一种抗骨髓瘤治疗、两种及以上细胞遗传学异常、高危遗传学异常、浆细胞标记指数被认为是重要的不良预后因素[13,15]。目前尚无可靠的早期预测MM 患者CNS 复发的分子标志物,且对于EMD 患者的最佳治疗选择尚未达成共识。CNS-MM 的系统治疗应包括能够通过血脑屏障控制中枢神经系统疾病和控制系统性骨髓瘤这两部分。对于MM 中枢神经系统侵犯,颅内出现占位性病变,外科手术切除病灶是否可以改善预后,尚需进一步对更多病例进行观察总结。联合新药、化疗、自体干细胞移植、外科手术、放疗及鞘内注射的治疗方案仍需个体化,CD38 单抗特异性免疫疗法、靶向BCMA 的CAR-T细胞疗法及临床试验有望使更多CNS-MM 患者获益。
