四种CTA后处理技术对颈脑动脉夹层的诊断价值比较
2021-11-30毛权良潘宇宁周佳丽
毛权良,潘宇宁,周佳丽
颈脑动脉夹层(CCAD)是导致脑卒中发生少见却重要的病因[1]。卒中早期病因诊断对于临床治疗方案的选择具有重要意义[2]。但CCAD的临床表现主要为头颈部疼痛、脑缺血及蛛网膜下腔出血,并不具特异性[2]。因此,临床上诊断CCAD主要依赖于影像学检查。数字减影血管造影术(DSA)被认为是诊断动脉夹层的“金标准”,但费用较高,并存在引起神经并发症的风险[3]。此外,DSA无法直接观察动脉管壁的缺点,在诊断动脉夹层时存在一定局限性[4]。CT血管造影(CTA)作为一种无创血管成像技术,可以观察动脉管壁变化,并且与各种后处理技术结合后,对于动脉夹层具有良好的诊断能力。本研究对CTA 4种后处理技术诊断CCAD情况进行分析,探讨其临床应用价值,报道如下。
1 资料与方法
1.1 一般资料 回顾性分析2010年1月至2020年1月在宁波市第一医院就诊的68例CCAD患者。均符合:(1)具有头或颈部疼痛、Horner综合征、蛛网膜下腔出血、脑神经麻痹、脑卒中等CCAD临床表现;(2)经DSA检查并确诊;(3)具有完整的CTA资料。排除:(1)CTA检查前已接受外科或介入治疗;(2)CTA图像存在严重伪影或其他因素干扰诊断。其中男41例,女27例;年龄19~76岁,平均(52.1±12.8)岁。高血压27例,血脂异常5例,糖尿病7例,有吸烟史17例。临床表现为头颈部疼痛34例,肢体麻木25例,头晕、视物模糊17例,蛛网膜下腔出血16例。急性期27例,亚急性期24例,慢性期17例。CTA-DSA检查间隔时间0.5~30d,中位时间3d。
1.2 检查方法 所有患者均在第二代日本东芝320排CT(AquilionONE)上完成。颅内动脉CTA扫描参数:管电压80 kV,管电流150 mAs,探测器宽度FOV 16 cm×22 cm,球管旋转速度为120 r/min,重建层厚0.5mm,扫描范围自颈2椎体水平到颅顶。使用美国Medrad公司双筒高压注射器注射对比剂,对比剂为德国拜耳公司370mgI/ml非离子型对比剂(优维显),注射剂量60ml,随后注射20ml 0.9%氯化钠注射液,注射流率为5.0ml/s。采用容积扫描方式,共分5个序列,第1序列延迟7 s扫第1圈;第2序列10.7 s开始,扫描3圈,每圈间隔2s;第3序列17 s开始,扫描6圈,每圈间隔2 s,每圈间隔2 s;第4序列29.4 s开始,扫描4圈,每圈间隔2 s;第5序列39.1 s开始,扫描5圈,每圈间隔5s。颈动脉CTA扫描参数:管电压120kV,管电流144mAs,探测器宽度FOV 16 cm×32 cm,球管单圈旋转时间0.5 s,重建层厚0.5 mm,扫描范围自主动脉弓到颅顶,注射参数与颅内动脉相同。采用对比剂示踪法,将监测层面定位于颈中部,ROI放置于解剖组织外,当颈动脉内出现对比剂时进行手动触发扫描。平扫与增强扫描参数相同。
1.3 影像学分析
1.3.1 CTA诊断标准 将CCAD的影像学征象分为敏感征象和特异征象。当观察存在至少一个敏感征象和一个特异征象时,则诊断为动脉夹层。其中敏感征象为动脉管腔瘤样扩张、狭窄或者闭塞;特异征象为壁内血肿、内膜瓣及双腔征。壁内血肿的定义为管壁增厚且血管外径较邻近同侧或对侧非夹层段血管增宽[5]。
1.3.2 CTA后处理评估方法 所有CTA影像资料均在后处理工作站上进行容积再现(VR)、最大密度投影(MIP)、曲面重建(CPR)及多平面重建(MPR)处理,并结合轴位图像进行评估。在血管水平对每一根血管进行评估,记录被评估血管的影像学征象。评估血管包括扫描范围内的颈内动脉、椎动脉、基底动脉、大脑前动脉A1A2段、大脑中动脉M1M2段以及大脑后动脉P1P2段。在患者水平,记录每种后处理技术完成1例患者评估所需时间,以每种后处理技术开始操作为起点,至完成所有目标血管评估为终点。所有影像学评估均由两名高年资神经影像医师独立审阅,对意见不同的结果通过引入第3位经验丰富的放射科医师讨论并取得一致意见。
1.4 统计方法 应用SPSS25.0统计软件进行分析。计量资料用均数±标准差表示,采用方差分析;计数资料比较采用2检验;诊断效能评估采用受试者操作特征(ROC)曲线<0.05为差异有统计学意义。
2 结果
2.1 夹层诊断结果 以DSA结果作为参照诊断,4例患者存在多发CCAD,共计72支血管被确诊为动脉夹层。其中椎动脉35支,基底动脉2支,颈内动脉20支,大脑中动脉8支,大脑前动脉3支,大脑后动脉4支。
2.2 CTA评估结果 因2例患者的CTA图像扫描范围未包含双侧大脑前动脉、大脑中动脉及大脑后动脉,最终共评估736支血管。4种后处理技术诊断CCAD的敏感性差异有统计学意义(2=134.01<0.05),CPR及MPR具有很高的诊断价值(表1)。在72支确诊的夹层动脉中,共71支(98.6%)夹层动脉在CTA图像上观察到了敏感征象,4种后处理技术的显示率差异无统计学意义;60支(83.3%)夹层动脉在CTA图像上观察到了特异征象,CPR及MPR对于内膜瓣、双腔征及壁内血肿的显示率高于VR及MIP(均<0.05),见表2。在患者水平,VR、MIP、CPR及MPR完成每例患者评估所需要的时间分别为(51.6±5.0)s、(53.0±4.9)s、(618.9±16.9)s、(284.2±12.3)s,4种后处理技术完成评估所需时间差异有统计学意义(=60771<0.05)。

表1 CTA 4种后处理技术的夹层诊断价值
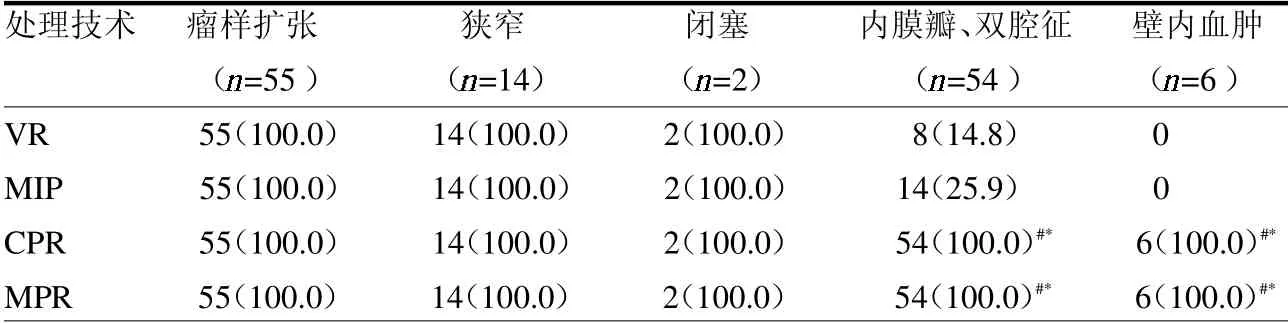
表2 夹层动脉CTA图像特征显示率 例(%)
3 讨论
CTA及其后处理技术作为一种无创血管成像技术,具有成像快、获取便捷、安全性高,且在诊断颈部动脉夹层方面比其他影像学方法更具优势[6]。以DSA结果为参考标准的研究显示,CTA在诊断颈部动脉夹层方面具有很好的敏感性及特异性[5,7-8]。本研究显示,CTA诊断CCAD的敏感性和特异性分别为83.3%、100%,诊断敏感性较上述研究稍低。这可能是因为本组病例亚急性期及慢性期患者占比较大[9];也可能与本研究包含有颅内动脉夹层有关,颅内动脉较颈部动脉更为纤细,而CTA的空间分辨率比DSA相对较低[6,10]。
VR、MIP、CPR和MPR是临床上诊断脑血管病变最常应用的CTA 4种后处理技术,不同后处理技术有着各自的应用优势。本研究显示,CPR及MPR对于CCAD具有很高的诊断价值,这是因为CPR、MPR对于壁内血肿、内膜瓣及双腔征的显示率高于VR、MIP(均<0.05)。壁内血肿、内膜瓣及双腔征是诊断CCAD的特异性征象[5]。本研究显示,VR及MIP不能显示壁内血肿。VR是经过减影后的血管重建技术,该技术减去了血管周围的骨质及软组织,可以直观、立体地显示血管的走形,但缺失了血管壁的信息。MIP则是在减影基础上利用投影成像原理,将三维数据朝着任意方向进行投影,有利于显示与正常血管存在密度差异的病变,但本研究显示CCAD的真假腔之间未能表现出良好地密度差异。CPR及MPR则能较好的显示壁内血肿、内膜瓣及双腔征,本组病例CTA影像均为各向同性扫描,MPR能够在保证良好空间分辨率的同时多平面、立体地观察病变;但在血管走形迂曲处显示病变的完整性欠佳。CPR则能够将走形迂曲的血管延展并显示在一个平面内,进一步完整地显示病变累及的范围。
CCAD通常会引起动脉管腔的变化,在本研究中被定义为敏感征象。在观察敏感征象时,4种后处理技术之间表现出了良好的一致性,而CTA显示动脉管腔改变与DSA具有很好的一致性[9]。这表明4种后处理技术对于夹层动脉管腔改变的评估都是可靠的。本研究在71支(98.6%)夹层动脉的CTA图像上观察到了动脉管腔的改变,仅有1支表现为正常管腔。这提示并不是所有的CCAD都会引起动脉管腔的明显改变,此时对于特异征象的观察是十分重要的[11]。
此外,每种后处理技术评估每例患者的目标血管所需时间是不同的。本研究显示,CPR完成评估所需时间最长,因为每一根目标血管都需要人为的去勾画;而VR需要的时间则是最短的。这一问题有望通过人工智能技术的发展及临床应用得以解决[12]。
本研究存在着一定的不足。首先,本研究为回顾性研究,病例均由DSA确诊入组,而DSA检查内膜瓣显示率仅约10%,且不能显示管壁情况,这使入组病例存在选择偏倚;其次,检查方法包含有颈动脉CTA及颅内动脉CTA,两种方法成像参数并不完全相同,这可能使成像结果存在一定差异;最后,本研究采用自身阴性血管作为对照组,缺乏与其他引起动脉管壁增厚的疾病对照研究。
