金毛狗脊指纹图谱前处理方法探索
2021-11-18陆燕萍徐佳兰彭小晶巩晓宇
陆燕萍,徐佳兰,彭小晶,何 嫣,巩晓宇*,赵 敏
(1.深圳市龙岗区人民医院,广东 深圳 518172;2.湖南网络工程职业学院,湖南 长沙 410018)
狗脊(Cibotii Rhizoma)为蚌壳蕨科植物金毛狗脊(Cibotiumbarometz(L.)J.Sm.)干燥根茎。作为国家二级保护植物金毛狗脊[1]生长于山脚阴湿缓坡或沟谷密林下阴湿的酸性土壤,主要分布于热带至亚热带地区。其资源分布广,福建、广西、贵州、云南、广东、江西、湖南、四川、重庆、浙江等地均有出产,其中以福建、广西、贵州、云南为多[2]。狗脊为《中国药典》收载的常用中药,功效为祛风湿、补肝肾、强腰膝等,临床用于治疗风湿痹痛、腰膝酸软、下肢无力[3]。其主要化学成分为水溶性酚酸类(以原儿茶酸为代表)、蕨素类、黄酮类、挥发油等活性成分[4],现代药理研究表明,具有抗骨质疏松、抑制血小板聚集、抗炎、抗风湿、保肝、抗氧化及抗癌等药理活性[5-10]。《中国药典》(2020年版)[3]以原儿茶酸为指标进行含量测定作为主要的质量控制方法,并不能完全反映狗脊多组分特征。本项目通过建立可反映中药狗脊多组分特征的HPLC色谱指纹图谱,用于狗脊种源鉴别、种植、加工、炮制、生产、检验和研究全过程的质量控制,为有效控制中药狗脊质量、提高狗脊质量标准提供依据。本文通过建立狗脊水溶性酚酸类多成分同时检测的基础上,运用正交实验设计及方差分析优化狗脊HPLC色谱指纹图谱样品前处理方法,为后期建立合理的狗脊HPLC色谱指纹图谱提供实验依据。
1 仪器与材料
仪器与试药:Agilent 1260高效液相色谱仪(Agilent OpenLAB 色谱工作站带四元泵、自动进样器、柱温箱、DAD检测器),FA2004型万分之一电子分析天平(上海天平仪器厂),VGT-01型超声波清洗器(深圳市威固特超声波科技开发有限公司),XK96-A快速混匀器(姜堰市新康医疗器械有限公司),甲醇、乙腈为色谱纯(德国MERCK公司);Milli Q 纯化水系统制备实验用水,其他试剂均为分析纯。
5-羟甲基糖醛(11626-202013,5-HMF)、原儿茶酸(110809-201906)、原儿茶醛(110810-201909)对照品均购置于中国食品药品检定研究院,纯度经HPLC检测大于99.9%。狗脊药材(产地广西玉林),购于深圳一致医药公司,经深圳市龙岗医院陆燕萍主任药师鉴定为蚌壳蕨科植物金毛狗脊的干燥根茎;样本存放于深圳市龙岗医院存样标本室。
2 方法与结果
2.1 检测方法的建立
2.1.1 色谱条件 色谱柱:Agilent Eclipse XDB-C18色谱柱(150 mm×4.6 mm,5μm)连接ZobaxC18(2.5 mm×4.6 mm,5μm)保护柱;以甲醇为流动相A,0.1%冰醋酸水溶液为流动相B,按梯度0.0~38.0 min,流动相A(%)5;38.0~48.0 min,流动相A(%)5~100洗脱;流速1.0 mL/min;进样量10μL;柱温30 ℃;检测波长260 nm。此色谱条件,各成分均达到基线分离,理论塔板数均大于2 000,典型色谱图具体见图1。
2.1.2 对照品溶液的制备 精密称取对照品5-HMF、原儿茶酸、原儿茶醛适量,加甲醇-1%冰醋酸(70∶30)溶液配制成浓度分别为630.0、450.0及760.0μg/mL的混合对照品储备液(母液)于4 ℃冰箱保存备用。上述储备液精密吸取5 mL于100 mL容量瓶中,加入甲醇-1%冰醋酸(70∶30)溶液稀释至刻度,边加边摇匀,即得含上述成分分别为31.50、22.50及38.00μg/mL的混合对照品工作溶液,待用。
2.1.3 供试品溶液的制备 狗脊药材粉碎后过三号筛,取粉末约0.4 g,精密称定,置10mL容量瓶中,精密加入甲醇-1%冰醋酸溶液(70∶30)至达到刻度线,称定质量,超声处理30 min,放冷,再次称定质量,用甲醇-1%冰醋酸溶液(70∶30)补足减失的质量,摇匀,滤过,取滤液即得。
2.1.4 标准曲线、线性范围及定量限(LOQ)/检测限(LOD) 上述混合对照品母液分别稀释5、10、20、50、100、200倍,按“2.1.1”项下色谱条件进样测定,分别记录其峰面积。横坐标为各成分的进样量对应峰面积为纵坐标,进行线性回归计算。取上述对照品工作溶液,依法测定其色谱峰信噪比(S/N),以S/N为10和3相应的浓度分别作为其LOQ与LOD。各成分线性范围及LOQ/LOD具体见表1。从所得结果看,在相应浓度范围内各成分线性关系良好,灵敏度表现良好。

表1 线性范围及定量限(LOQ)/检测限(LOD)结果
2.1.4 精密度试验 精密吸取上述混合对照品工作溶液,按“2.1.1”项下色谱条件连续进样6次,分别记录峰面积。5-HMF、原儿茶酸、原儿茶醛对照品峰面积相对标准偏差(RSD)值分别为1.53%、1.66%、1.22%,表明该方法精密度良好。
2.1.5 回收率实验 按“2.1.3”项下方法,称取同一批次狗脊细粉6份,每份1 g,加入等量各对照品溶液,平行制备样品,并按“2.1.1”项下色谱条件进行测定;回收率按公式(%)=(C-A)/B×100%(A:供试品所含被测成分量;B:加入对照品量;C:实测值)。5-HMF、原儿茶酸、原儿茶醛回收率分别为99.18%、100.17%、95.12%;RSD值分别为2.45%、1.89%、2.41%,表明该方法准确性良好。
2.1.6 稳定性实验 室温下取对照品工作溶液密封储存于进样瓶中,分别于0、2、6、10、16、24 h 按“2.1.1”项下色谱条件进样测定。结果显示5-HMF、原儿茶酸、原儿茶醛对照品峰面积RSD值分别为1.95%、1.84%、1.72%,表明在该溶液条件下,各成分24 h内稳定性良好。
2.1.6 重复性试验 按“2.1.3”项下方法,称取同一批次狗脊细粉6份,每份1 g,加入等量各对照品溶液,平行制备样品,并按“2.1.1”项下色谱条件进行测定。结果显示样品中5-HMF、原儿茶酸、原儿茶醛平均含量分别为0.305%(RSD2.73%)、0.039%(RSD3.51%)、0.021%(RSD3.24%),表明该方法重复性良好。
2.2 处理方法研究
2.2.1 单因素实验 其他条件不变,分别考察溶剂类型、溶剂比例、超声时间和次数对3个成分(5-HMF、原儿茶酸、原儿茶醛)总得率(Tc)的影响。
(1)溶剂类型:按“2.1.3”项下方法,准确称取0.40 g狗脊粉5份,分别加入甲醇、甲醇-1%冰醋酸(70∶30)、乙腈、乙腈-1%冰醋酸(70∶30)、含1%冰醋酸水溶液进行超声处理30 min。结果显示,添加30∶% 1%冰醋酸的混合溶剂处理时,Tc值最高,其次为含1%冰醋酸水溶液,纯有机溶剂最低。甲醇-1%冰醋酸与乙腈-1%冰醋酸无明显差异。
(2)溶剂比例:按“2.1.3”项下方法,准确称取0.40 g狗脊粉5份,按甲醇与含1%冰醋酸水溶液比例10∶90、30∶70、50∶50、70∶30、90∶10进行超声处理30 min。结果显示,甲醇与含1%冰醋酸水溶液比例70∶30时,Tc值最高。
(3)超声处理时间:按“2.1.3”项下方法,准确称取0.40 g狗脊粉5份,加甲醇-1%冰醋酸(70∶30)溶剂超声处理10、20、30、40、50 min。结果显示,超声处理时间为50 min时,Tc值最高。
(4)超声处理次数:按“2.1.3”项下方法,准确称取0.40 g狗脊粉3份,加甲醇-1%冰醋酸(70∶30)溶剂超声处理次数分别为1~3次,每次30 min 。结果显示,处理次数越多,Tc值越高。
2.2.2 正交设计及方差分析 在方法学考察和单因素实验的基础上,为优化处理方法的工艺条件,以溶剂比例、超声处理时间及次数3个因素为考察因子,Tc值为参考指标,具体实验按L9(34)正交实验表,见表2。正交实验结果及方差分析结果见表3和表4。
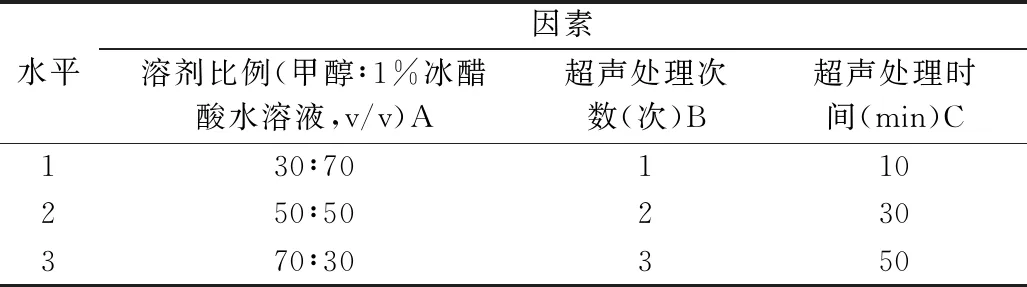
表2 正交实验因素水平
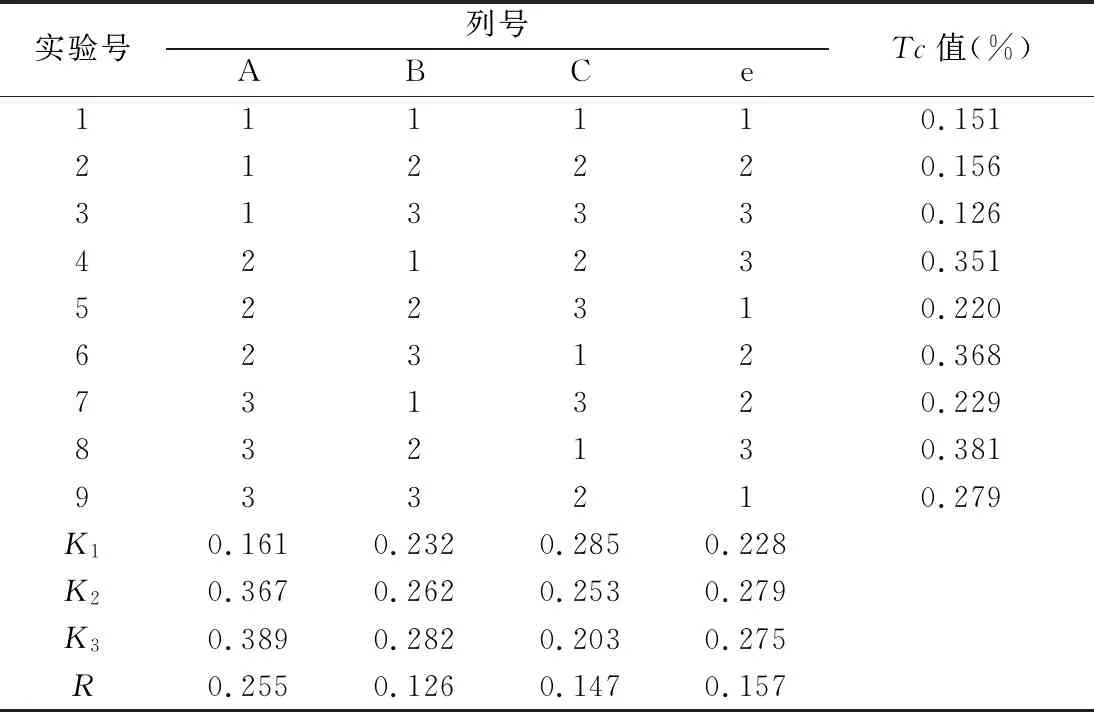
表3 正交实验结果
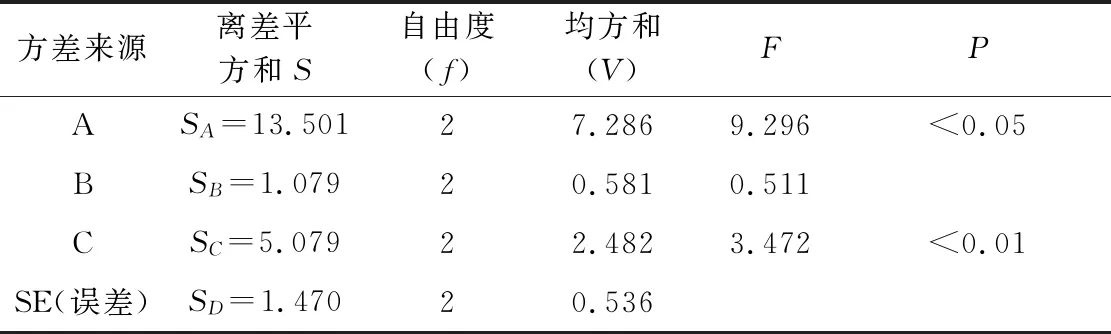
表4 方差分析
由表2、3可看出,前处理方法以Tc值作为考察指标,各因素对方法的影响大小依次为A>C>B,溶剂比例对方法影响最大,超声处理次数对方法影响最小。在实验范围内,最佳的条件为A3B1C2,即样品加入甲醇-1%冰醋酸溶液(70∶30)超声处理30 min,1次。
3 讨论
以“中药色谱指纹图谱方法”鉴别中药的真伪,控制其质量是较传统的方法,更能客观地反映中药物质基础的整体观,是更为科学、有效的质控方法。本方法已被国家正式推行[11]。狗脊化学成分为水溶性酚酸类、蕨素类、黄酮类、挥发油等多种活性成分[2-8],狗脊中抗炎、抗氧化的主要有效成分为原儿茶酸、原儿茶醛[12-14],现行《中国药典》采用原儿茶酸作为狗脊质量控制标准,但5-HMF也具有改善认知功能、抗氧化的活性[15],而且从药材含量上看,5-HMF含量要远远高于原儿茶酸、原儿茶醛,其色谱行为表现峰面积也远远大于原儿茶酸、原儿茶醛[1]。同时多种植物中都含有原儿茶酸,单以原儿茶酸作为质量控制指标专属性不强。因此,在进行狗脊的指纹图谱研究要综合考虑作为主要特征峰原儿茶酸、原儿茶醛及5-HMF的色谱行为。本文即在建立5-HMF、原儿茶酸及原儿茶醛的多成分定量测定的基础上,以3个成分总含量综合评价药材前处理方法,本方法专属性高,有利于狗脊指纹图谱质控方法的建立。
检测波长选择。5-HMF 的最大吸收波长为280 nm,但考虑在此波长下5-HMF灵敏度过高而影响其他2个成分的色谱行为,故选择5-HMF吸收相对较弱的260 nm 进行测定。
流动相选择。本实验系统地筛选了甲醇、乙腈及不同浓度各种有机酸、缓冲盐的配伍对各成分的影响,最终确定有机相为甲醇、水相为含0.1%冰醋酸水溶液时,各待测组分分离度高且色谱峰峰形最佳,且溶剂类型有药材处理方法一致,有利于操作。
