基于UPLC 指纹图谱及多指标定量分析的诃子药材质量研究*
2021-10-14陈九妹鞠成国
王 巍,张 强,陈九妹,鞠成国
(辽宁中医药大学 药学院,辽宁 大连 116600)
诃子原产于印度、缅甸等地,原名“诃黎勒”,在唐代随佛教传入我国,目前,收载于《中国药典》2020版一部,为使君子科植物诃子Terminalia chebula Retz.及绒毛诃子Terminalia chebula Retz. var. tomentella Kurt. 的干燥成熟果实[1],具有涩肠止泻、敛肺止咳、降火利咽之功效,多用于治疗“肠澼”。本课题组在研究过程中收集到的药材多为诃子,极少见绒毛诃子。其中部分云南和新疆所产诃子药材与广西、广东所产诃子药材在外观上存在较大差别。药典中对诃子的质量控制方法还仅限于显微鉴别和以对照药材为参照的薄层色谱鉴别,欠缺对主要成分的定性及定量分析。鉴于此情况,本研究在建立诃子高效液相指纹图谱的基础上,对共有峰进行主成分分析,并对可识别的主要成分进行含量测定,为诃子药材的质量评价提供依据,并为对其进行深入研究奠定基础。
1 实验部分
1.1 仪器、试剂与药材
1260 Infinity II 型超高效液相色谱仪(美国安捷伦科技有限公司);FA1004B 电子天平(上海精密科学仪器有限公司)。
没食子酸、鞣花酸购自成都曼思特生物科技有限公司(纯度≥98%,批号分别为MUST-13040103、MUST-14031010),柯里拉京、诃黎勒酸、五没食子酰基葡萄糖、诃子酸购自成都普瑞法科技开发有限公司(纯度≥98%,批号分别为PRF9101742、PRF8112 302、PRF9091704、PRF8071201);没食子酸乙酯为本实验室自制,经HPLC 鉴定纯度≥98%;甲醇、H3PO4为色谱纯;水为超纯水。17 批诃子药材经辽宁中医药大学张慧教授鉴定均为诃子Terminalia chebula Retz.的干燥成熟果实。
1.2 方法
1.2.1 供试品溶液制备 精密称取各批次诃子粉末(去核,粉碎,过60 目筛)0.1g,加入70%甲醇溶液50mL,精密称定重量,超声提取20min,放冷,再以70%甲醇溶液补足损失重量,摇匀,经0.22μm 微孔滤膜滤过,取续滤液,即得[2]。
1.2.2 对照品溶液制备 分别精密称取没食子酸、没食子酸乙酯、柯里拉京、诃黎勒酸、鞣花酸、五没食子酰基葡萄糖、诃子酸对照品适量,置于10mL 容量瓶,加入甲醇定容,分别制成浓度为0.22250、0.17400、0.68875、0.25250、0.17750、0.31625、0.49125mg·mL-1的对照品溶液。
1.2.3 色谱条件 Agilent Poroshell 120 EC-C18色谱柱(100mm×3.0mm,2.7μm);流动相0.3%磷酸水(A):甲醇(B),梯度洗脱,程序如下:0~3min,B 为3%;3~5min,B 为3%~5%;5~15min,B 为5%~8%;15~25min,B 为8%~14%;25~30min,B 为14%~18%;30~35min,B 为18%~20%;35~38min,B 为20%~25%;38 ~45min,B 为25%;45 ~55min,B 为25% ~30%;55 ~60min,B 为30% ~45%;60 ~65min,B 为45% ~60%;65 ~70min,B 为60% ~100%;70 ~78min,B 为100%;78~80min,B 为100%~3%;。进样量2μL,流速0.8mL·min-1,柱温30℃,检测波长270nm。
2 结果与讨论
2.1 指纹图谱方法学考察
2.1.1 精密度试验 取S1批次样品,按“1.2.1”项下方法制备供试品溶液,在“1.2.3”项条件下连续进样6 次,以诃黎勒酸计算各对照品相对保留时间RSD分别为0.82%、0.80%、0.67%、0.00%、0.95%、0.66%、0.78%,相对峰面积RSD 分别为1.30%、1.12%、1.35%、0.00%、1.19%、1.36%、1.22%,表明仪器精密度良好。
2.1.2 重复性试验 取S1批次样品,按“1.2.1”项下方法平行制备6 份供试品溶液,在“1.2.3”项条件下进样,以诃黎勒酸计算各对照品相对保留时间RSD分别为0.69%、0.68%、0.71%、0.79%、0.69%、0.68%、0.68%,相对峰面积RSD 分别为1.80%、1.92%、1.67%、1.77%、1.68%、1.82%、1.71%,表明该方法重复性良好。
2.1.3 稳定性试验 取S1批次样品,按“1.2.1”项下方法制备供试品溶液,在“1.2.3”项条件下,分别于制备后0、2、4、8、12、18、24、36、48h 进样,以诃黎勒酸计算各对照品相对保留时间RSD 分别为0.91%、0.87%、0.96%、0.00%、0.79%、0.90%、0.89%,相对峰面积RSD 分别为1.91%、1.87%、1.97%、0.00%、1.82%、1.80%、1.88%,表明供试品溶液在48h 内稳定性良好。
2.2 指纹图谱建立
取各批次诃子(共17 批),按“1.2.1”项下方法制备供试品溶液,在“1.2.3”项下色谱条件进样检测,将所得色谱数据导入“中药色谱指纹图谱相似度评价系统2012 版”,去除溶剂峰,剪切65min 之前的色谱峰,进行共有峰的匹配,中位数法生成对照图谱,以对照图谱计算各批次的相似度[3]。结果共识别26 个共有峰,与对照品对比鉴定,其中2 号为没食子酸,11 号为没食子酸乙酯,12 号为柯里拉京,19 号为诃黎勒酸,21 号为鞣花酸,22 号为五没食子酰基葡萄糖,23 号为诃子酸。各批次相似度在0.626~0.971 之间,其中S8为0.626、S5为0.895、S10为0.841、S16为0.856,其余均在0.9 以上。各批次诃子指纹图谱叠图见图1。

图1 各批样品UPLC 指纹图谱Fig.1 UPLC fingerprints of different batche samples
2.3 主成分分析
将17 批样品共有峰的峰面积作为原始数据,以SPSS 17.0 软件进行主成分分析,将数据标准化处理后计算相关矩阵的特征值及方差贡献率,结果见表1。

表1 UPLC 指纹图谱的主成分信息和方差贡献率Tab.1 Principal component information and variance contribution rate of UPLC fingerprint
由表1 可见,以特征值(VIP)>1 为提取标准[4],得到前7 个主成分的累计方差贡献率为91.182%(>80%),说明前7 个主成分反映了诃子26 个成分中91.182%的信息量,基本上可以代表诃子UPLC指纹图谱的特征。
对各主成分的权重比例与各共有峰对应的相关系数,结果见表2。

表2 主要因子载荷矩阵表Tab.2 Main factor load matrix table
由表2 可见,7 种已知成分和其他未知成分均作为主要信息参与了诃子的质量表达,其中第1 主成分主要反映了色谱峰6、8、9、10、16、17、19 (诃黎勒酸)、20、22(五没食子酰基葡萄糖)的信息,第2 主成分主要反映了色谱峰2(没食子酸)、11(没食子酸乙酯)、12(柯里拉京)、15、23(诃子酸)、24 的信息,第3 主成分主要反映了色谱峰26 的信息,第4 主成分主要反映了色谱峰3 的信息,第5 主成分主要反映了色谱峰25 的信息,第6 主成分主要反映了色谱峰14 的信息,第7 主成分主要反映了色谱峰21(鞣花酸)的信息。
2.4 含量测定方法学考察
本研究建立的指纹图谱分析方法,可同时对诃子中没食子酸、没食子酸乙酯、柯里拉京、诃黎勒酸、鞣花酸、五没食子酰基葡萄糖、诃子酸7 种主要成分进行含量测定。方法的精密度、重复性和稳定性试验参见“1.2.1”项下部分。
2.4.1 专属性试验 取S1批次样品,按“1.2.1”项下方法制备供试品溶液,取没食子酸、没食子酸乙酯、柯里拉京、诃黎勒酸、鞣花酸、五没食子酰基葡萄糖、诃子酸苷对照品,按“1.2.2”项下方法制备对照品溶液,并制备混合对照品溶液,分别在“1.2.3”项下条件进样。对照品溶液与供试品溶液色谱图中各对照品色谱峰与相邻峰分离良好。结果见图2。

图2 各成分UPLC 色谱图Fig.2 UPLC chromatograms of various constituents

2.4.2 线性关系考察 分别精密称取没食子酸、没食子酸乙酯、柯里拉京、诃黎勒酸、鞣花酸、五没食子酰基葡萄糖、诃子酸对照品,以甲醇溶解并逐级稀释。分别在“1.2.3”项条件下进样,以质量浓度为横坐标(X),峰面积为纵坐标(Y)进行线性回归,回归方程分别为:没食子酸y=8672.1x+4.0441(r=0.9999);没食子酸乙酯y=5746.9x+0.9143(r=0.9999);柯里拉京y=4699.9x-11.578(r=0.9999);诃黎勒酸y=3790.5x-1.0095 (r=0.9998); 鞣花酸y =6414.9x -1.445(r =0.9999);五没食子酰基葡萄糖y=5999x+0.8232(r=0.9999);诃子酸y=3979.1x-2.6536(r=0.9999)。结果表明:没食子酸在4.45~222.5μg·mL-1,没食子酸乙酯在3.48~174μg·mL-1,柯里拉京在13.78~688.75μg·mL-1,诃黎勒酸在5.05~252.5μg·mL-1,鞣花酸在3.55~177.5μg·mL-1,五没食子酰基葡萄糖在6.33 ~316.25μg·mL-1,诃子酸在9.83~491.25μg·mL-1与峰面积呈良好线性关系。
2.4.3 加样回收率试验 分别精密称取6 份已知含量S1批次样品0.1g,加入相当于样品中成分含量100%的7 种对照品,按“1.2.1”项下方法制备供试品溶液,在“1.2.3”项条件下进样,计算加样回收率及RSD,结果表明,没食子酸加样回收率为98.96%,RSD为1.60%;没食子酸乙酯加样回收率为99.00%,RSD为1.68%;柯里拉京加样回收率为99.03%,RSD 为0.95%;诃黎勒酸加样回收率为99.79%,RSD 为1.05%;鞣花酸加样回收率为98.41%,RSD 为1.19%;五没食子酰基葡萄糖加样回收率为100.39%,RSD 为1.22%;诃子酸加样回收率为100.22%,RSD 为0.94%,均符合要求。
2.5 样品含量测定
取17 批样品,按“1.2.1”项下方法制备供试品溶液,按“1.2.3”项下条件进行分析,根据外标一点法分别计算各成分含量,结果见表3。
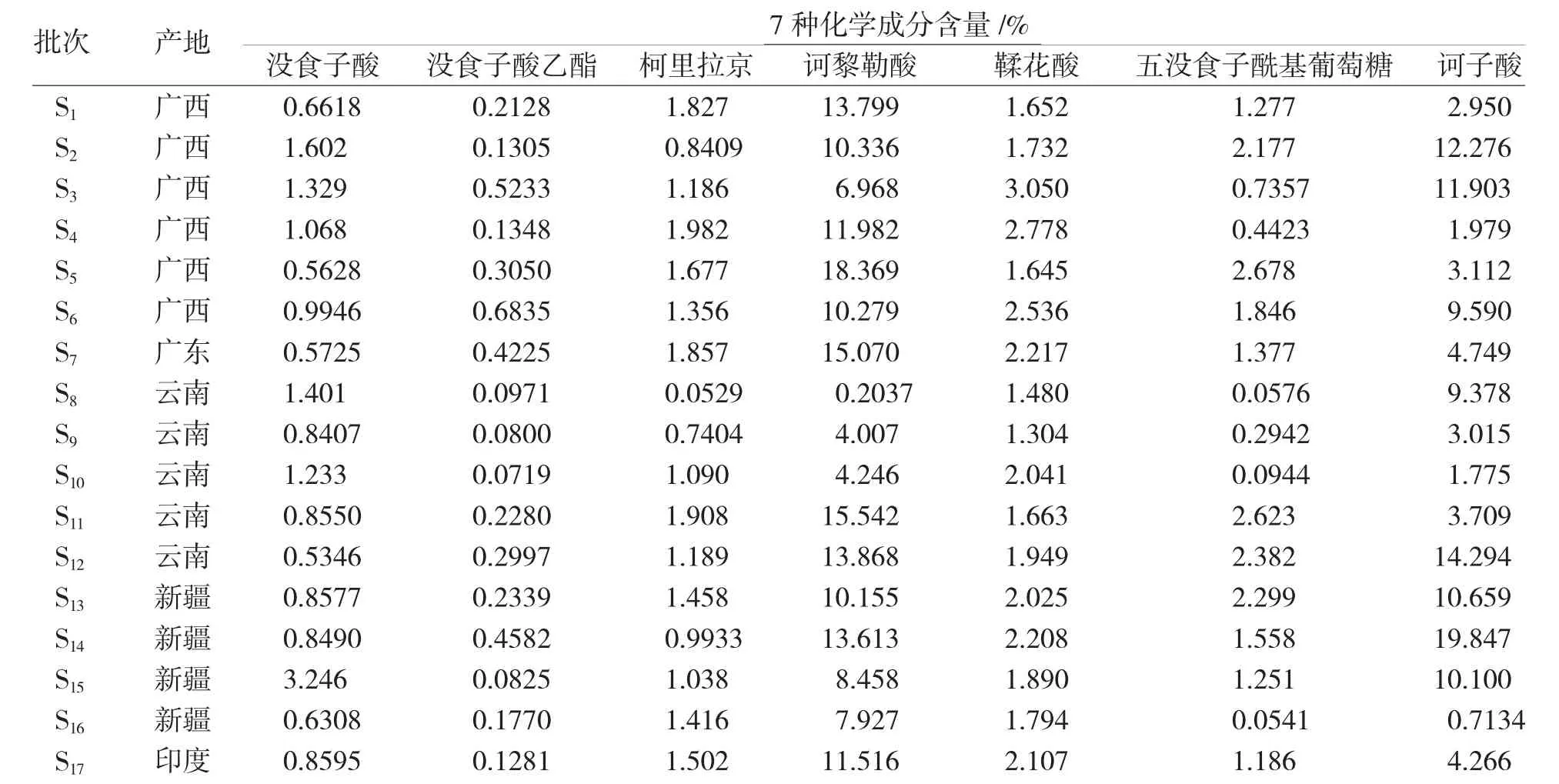
表3 各成分含量测定结果Tab.3 Results of content determination of various constituents
2.6 讨论
诃子在我国藏医、蒙医中应用极其广泛,地位相当于中医中的甘草。据文献报道,藏医、蒙医中超半数以上的复方含有诃子[4]。现代化学研究表明,鞣质是诃子的主要化学成分[5-7],其中没食子酸、没食子酸乙酯、柯里拉京、诃黎勒酸、鞣花酸和诃子酸是含量较高的几种鞣质,而五没食子酰基葡萄糖为一分子葡萄糖的1、2、3、4、6 位连接五分子没食子酸,这7 种化合物是诃子中的代表性化合物,也是诃子的潜在质量标志物。然而现行中国药典中并未对诃子中主要成分含量有所规定,在很大程度上限制了诃子质量评价系统的完善。本实验的指纹图谱相似度结果表明,各批次诃子相似度差别较大,质量不一,其中S8质量较差,相似度最低,从图谱中可以明显看出与其它批次具有显著差异。主成分分析结果显示,7 个指标成分均作为主要信息因子参与了诃子的质量表达,表明7 个指标成分的含量与药材质量高度相关,可直接影响药材质量。7 个指标成分的含量测定结果表明,各个批次成分含量差别较大,说明诃子各批次存在差异,验证了相似度的结果。
3 结论
本实验方法以指纹图谱相似度、主成分分析以及含量测定结果综合评价诃子药材质量,结果准确,可为诃子临床用药的安全有效提供依据及保障。本实验识别的7 种指标成分可反映诃子药材质量,可能为诃子的潜在质量标志物。本实验在药材收集时并未收集到绒毛诃子,后续对于诃子药材的质量评价还需更全面的深入研究。
