酸性磷酸酶在5′-肌苷酸生产中的研究进展
2021-09-27孔凡明王海雷
孔凡明,王海雷,吴 涛
(通辽梅花生物科技有限公司,内蒙古 通辽 028024)
5′-肌苷酸(Inosine-5′-monophosphate,简称IMP)因具有独特鲜味,通常与5′-鸟苷酸(Guanosine-5′-monophosphate,简称GMP)协同作为各种食品添加剂中的风味增强剂,其以质量分数5%~12%加入谷氨酸中呈味效果比单用谷氨酸钠高约8倍,有“强力味精”之称[1-2]。核苷酸的呈味机理和其独特的分子结构有很大关系,研究表明:只有5′-碳原子上连接磷酸基团才表现出鲜味,而2′-和3′-碳原子磷酸酯化无鲜味,且5′-碳原子的磷酸基团上的两个羟基解离才能产生鲜味,因此5′-肌苷酸鲜味剂通常以钠(或钾、钙)盐的形式存在[3-5]。
肌苷酸生产方法分为酶解法和发酵法,其中酶解法包括酶解核糖核酸法和酵母菌体自溶法,发酵法包括肌苷酸直接发酵法和肌苷发酵-转化法[6]。酶解核糖核酸法和酵母菌体自溶法原料来源丰富,成本低廉且一次可得到4种核苷酸的混合物,但提取高纯度产品难度大,提取工艺繁琐,导致生产周期长。直接发酵法生产肌苷酸不仅要考虑解除产物合成代谢过程反馈抑制,而且还要考虑改变细胞通透性使肌苷酸合成后能正常转运到胞外,由此带来发酵工艺复杂、发酵周期长、成本高和指标难以有效提升等一系列问题[7]。利用发酵法生产肌苷不存在直接发酵法存在的弊端,因此可通过发酵出肌苷后进一步磷酸化生产肌苷酸[8]。目前,较多生产厂家均采用化学磷酸化方法生产肌苷酸,其虽然有专一性强、副产物少和磷酸化产率高的优势,但过程所用到的原料成本较高,且对人体及环境有较大危害。近几年,随着环保观念的普及和人们绿色发展理念的不断提升,酶转化法生产核苷酸日益受到科技工作者的广泛关注[9]。
1 磷酸化过程酶的选择
酶转化法具有反应条件温和、不需要保护基团和专一性强等特点,因此具有化学转化法无法比拟的优越性。目前,通过核苷磷酸化生产核苷酸的酶主要有核苷激酶(Nucleoside kinase)和酸性磷酸酶[10],核苷激酶是能将三磷酸腺苷(ATP)的高能磷酸基团特异性地转移到核苷上的一类酶,其反应过程为
ATP+核苷→5′-核苷酸+ADP
激酶可用于催化合成多种核苷酸,Hove-jensen等[11-13]就尝试着利用肌苷/鸟苷激酶生产肌苷酸/鸟苷酸。此方法不足之处在于催化过程需要一直消耗ATP,所以必须同时培养能再生反应中消耗ATP的微生物,使核苷激酶在核苷酸生产应用中受到极大的限制[14]。
5′-肌苷酸二钠分子结构式为
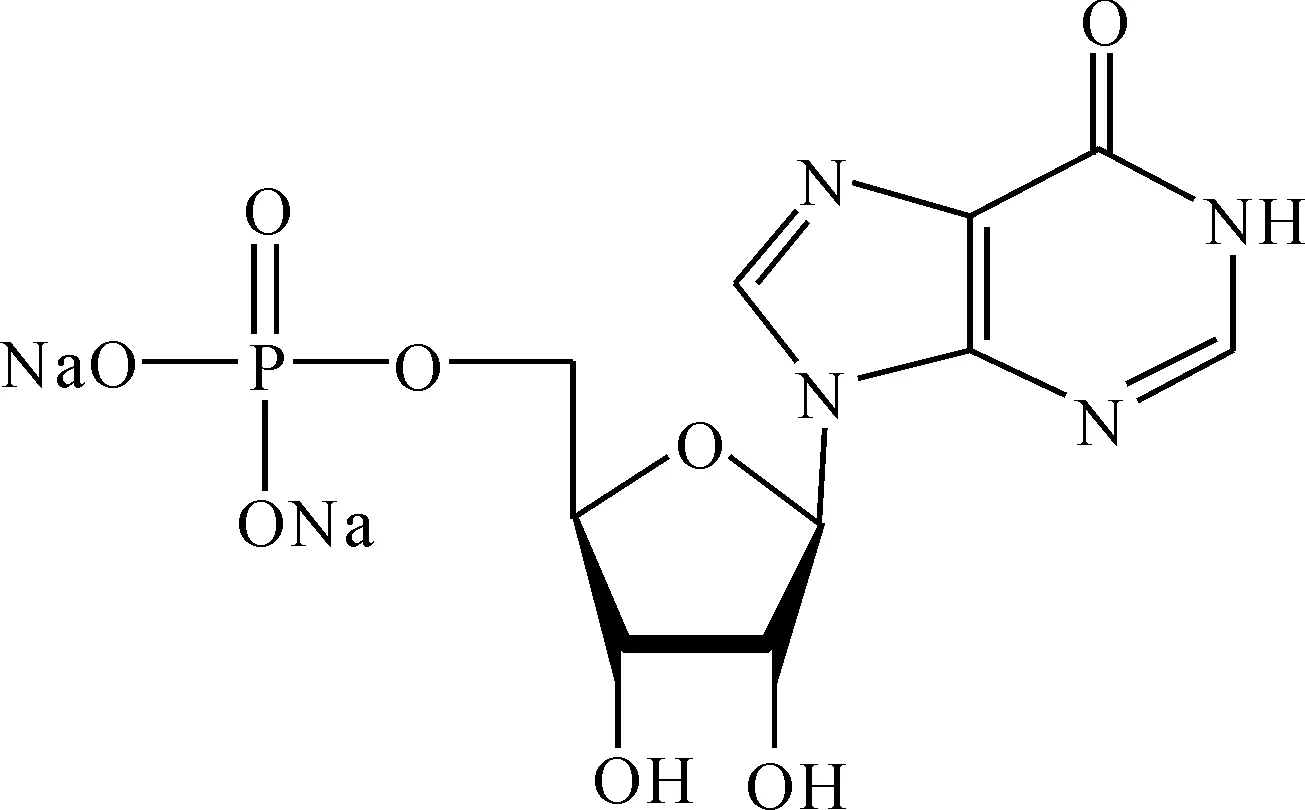
酸性磷酸酶(Acid phosphatase/phosphpotransferases,简称AP/PTases,EC3.1.3.2)广泛存在于植物、动物和微生物中。其在酸性条件下能以焦磷酸盐或聚磷酸盐等富能量物质为底物,特异性地催化核苷合成相应的核苷酸[15]。根据催化底物的不同,可将酸性磷酸酶分为非特异性酸性磷酸酶(NSAPs)和特异性酸性磷酸酶[16-17]。非特异性酸性磷酸酶不表现出明显的底物特异性,通常能够水解广泛的有机磷酸酯,比如核苷酸、葡萄糖-6-磷酸和磷酸二羟基丙酮等[16]。非特性性酸性磷酸酶的分类如表1所示。根据氨基酸序列同源性的不同,NSAPs可分为A,B,C 3个大类,进一步又可以将A类细分为A1~A33个亚类,其中研究较多的非特异性酸性磷酸酶为摩根氏菌属(PhoC-Mm)、鼠伤寒沙门氏菌(PhoN-St)和福氏志贺氏菌(Apy-Sf)[18-19]。由于酸性磷酸酶对多种磷酸化合物均具有脱磷酸活性且过程不需消耗ATP,因此为酶转化法生产肌苷酸提供一条新思路[20-21]。

表1 非特性性酸性磷酸酶的分类
酸性磷酸酶不仅具有特异的磷酸转移酶特性,而且还具有5′-核苷酸酶活性,5′-核苷酸酶会将生成的肌苷酸进行水解,在转化过程中会有逆反应发生,因此通过构建重组菌株提高过程转化率显得尤为重要。酸性磷酸酶以焦磷酸盐和肌苷为底物进行磷酸化和去磷酸化的反应,其反应过程如下:
1) 磷酸转移酶活性,肌苷磷酸化反应过程为
Pi inosine

2) 5′-核苷酸酶活性,肌苷酸去磷酸化反应过程为
inosine H2O

式中:E为酸性磷酸酶;PPi为焦磷酸盐;Pi为磷酸盐。
2 酸性磷酸酶重组菌株的构建
最早开展核苷生物法磷酸化研究的为日本学者Asano等[22],他发现摩氏摩根菌(M.morganii)中的磷酸化酶对肌苷和鸟苷具有催化作用,可生成相应的肌苷酸和鸟苷酸,且催化反应效率基本相同。之后Mihara等[23]发现菌株M.morganiiNCIMB10466发酵可产生具有选择性磷酸转移活性的酸性磷酸酶,经过提取相关磷酸转移酶基因并引入一系列突变后将其转入大肠杆菌中,成功获得一株高磷酸转移酶活性突变株。使用该突变株进行肌苷酶转化,肌苷酸的收率可达85%。为了进一步提高酶活,Mihara等[24]利用点饱和突变技术对蟑螂埃希氏菌(E.blattae)的酸性磷酸酶基因上活性位点进行一系列突变获得突变菌,该突变菌株酸性磷酸酶的活性得到明显提高。
国内学者在重组酸性磷酸酶菌株的构建方面成果丰硕。梁胜华[25]以产气肠杆菌为出发菌和以pBV220为表达载体构建高效表达温度诱导型的酸性磷酸酶基因工程菌。将温度提高到42 ℃诱导4 h即可诱导外源蛋白的大量表达。赵洪新等[26]以产气肠杆菌为出发菌,获得酸性磷酸酶基因序列PhoC,将其与不同的载体连接,分别克隆进大肠杆菌构建酸性磷酸酶基因工程菌。与野生型相比,工程菌合成肌苷酸活力提高,而水解肌苷酸的活力明显下降。Liu等[27]通过基因工程技术合成来源于E.blattaeJCM 1650的酸性磷酸酶基因,并将酸性磷酸酶基因定向克隆并构建成表达载体转入E.coliBL21(DE3)中,成功构建重组大肠杆菌重组菌,经工艺优化和IPTG诱导表达后,生物量达3.2 g/L,酶活达145.6 U/L,比优化前分别提高1.5倍和2.1倍。沈爱萍等[28]对重组E.coliBL21(DE3)/pET28b-AP/PT开展发酵工艺优化实验,确定最佳诱导剂为乳糖,诱导剂乳糖质量浓度为10 g/L,最佳诱导时机为OD600在7.0左右,最高酶活可达221.4 U/L。何菊华[15]以大肠杆菌重组菌为出发菌株,确定获得高酶活的细胞发酵工艺。其中诱导剂最适添加时机为对数前期,诱导OD600为2.0~2.5,持续诱导培养8 h,最高酶活可达1 980.07 U/L。
3 酸性磷酸酶在转化肌苷生产肌苷酸中的研究
酸性磷酸酶在转化生产肌苷酸中的研究报道主要集中在转化过程菌株选择与酶处理方式、酶转化条件优化和底物浓度优化等方面。
3.1 菌株选择与酶处理方式
不同微生物种属酸性磷酸酶活力相差较大,为了提高酶转化效率对于菌株选择显得尤为必要。Mihara等[29]将来自M.morganii,P.stuarrtii,E.aerogenes,E.blattae,K.planticola的AP/PTase基因分别克隆进E.coli,然后用于催化肌苷合成5′-IMP,并对它们催化效率进行比较。与其他菌株相比,发现M.morganii更适合用来催化肌苷磷酸化。
酶液状态对酶转化反应过程影响较大,酸性磷酸酶属于胞内酶,对于胞内酶一般需要经过细胞破碎将酶释放到胞外才能发挥更高的酶活性。Asano等[22]利用M.morganii游离细胞以焦磷酸钠和肌苷为底物催化合成肌苷酸,底物肌苷浓度37.3 mmol/L,反应9 h,得到肌苷酸浓度11.4 mmol/L,产率30.6%。Asano等[30]进一步利用从M.morganii中纯化出的酸性磷酸酶粗酶液催化肌苷磷酸化合成肌苷酸,肌苷浓度80 mmol/L,反应6 h,最终得到肌苷酸浓度32.6 mmol/L,收率41%,对比利用游离细胞指标有进一步提升。赵洪新等[31]以产气肠杆菌(E.aerogenes)AM 1183研究酶液状态对转化过程的影响,发现破碎细胞液在转化肌苷合成肌苷酸方面优于静息细胞。
3.2 酶转化工艺优化
在酶转化过程,转化温度和pH对酶转化过程影响较大。在适宜的转化条件下,酶转化效率能得到大幅提升[32]。综合前人研究酸性磷酸酶一般最佳转化温度为35 ℃,最佳转化pH为4.5。张玲[33]对构建重组大肠杆菌进行酶学性质研究,确定该酶的最适pH为5.0,最适反应温度为30 ℃。进一步考察静息细胞特异性磷酸化过程的影响,得到静息细胞最适反应温度为35 ℃。当底物浓度为37 mmol/L时,5′-肌苷酸的收率达到83.3%。永井秀忠等[34]利用三聚磷酸钠为底物制备呈味核苷酸二钠,在酶转化优化过程中确定最佳pH为4.5,最佳温度为35 ℃,并指出pH是影响酶解转化过程的关键因素。孙丽慧等[35]对游离细胞和固定化细胞反应条件对比发现,经过固定化后的酸性磷酸酶最适转化温度为35 ℃,稍高于游离细胞转化温度。二者最适反应pH均为5.0,但固定化后的酸性磷酸酶作用pH较游离细胞更宽泛。酸性磷酸酶经过固定化后操作稳定性较好,重复使用12批后相对酶活力仍在54.5%。
3.3 底物浓度优化
酸性磷酸酶在转化肌苷过程的磷酸供体主要为多聚磷酸及其盐,如焦磷酸、焦磷酸盐和三聚磷酸盐等。通过对肌苷和磷酸盐质量浓度的优化,在发酵成本控制、酶转化效率提升和成品提取精制等方面均有重要作用[36]。梁胜华[25]以产气肠杆菌(E.aerogenes)为出发菌株构建的温度诱导性酸性磷酸酶基因工程菌进行肌苷酶转化实验。当底物质量浓度为50 g/L肌苷+300 g/L焦磷酸钠时,反应2 h可得到肌苷酸质量浓度为90.6 g/L,收率为92%。当底物质量浓度提高到100 g/L肌苷+300 g/L焦磷酸钠时,反应7 h可得到肌苷酸质量浓度为153.7 g/L,收率为78%。李文峰等[37]使用磷酸转移酶工程菌菌体细胞催化肌苷5′-位磷酸化的工艺条件,研究结果表明:在整细胞PhoC酶活45 U,肌苷浓度100 mmol/L,焦磷酸浓度120 mmol/L时,反应6 h,肌苷转化率达到63.36%。在添加0.3%表面活性剂Trion-x-100时,肌苷转化率可提高到74.59%。Yuan等[38]用M.morganii酸性磷酸化酶突变株全细胞进行生物催化生产肌苷酸的研究,底物浓度为肌苷120 mmol/L和焦磷酸钠200 mmol/L时,反应7 h,肌苷酸产率为99.65%,此为目前报道最高指标。
4 总结与展望
酸性磷酸酶催化肌苷/鸟苷制备呈味核苷酸反应条件温和,不需要保护基团和提供ATP,而且磷酸酶具有专一性强的优点。日本味之素公司最早采用酸性磷酸酶转化工艺工业化生产呈味核苷酸,产量占日本呈味核苷酸总产量39%以上。酶转化法生产核苷酸尚未在国内工业化生产中应用。限制因素主要为生产成本高、酶活力不稳定、成品分离提纯难度大和收率低等诸多问题。针对上述瓶颈,近年来在酶法转化核苷酸过程中,不断有新工艺得到报道与应用,研究方向主要集中在酶的高效转化、磷酸盐的回收利用和鸟苷酶法磷酸化等工艺过程,工艺指标稳定提升的同时,一系列存在的生产难题也在不断得以解决和实现突破,相信在技术成熟后酸性磷酸酶转化法必将为核苷酸生产带来巨大变革。
