人工周期冻融胚胎移植中应用hCG对子宫内膜容受性的影响
2021-08-06郭帅帅
郭 郊 郭帅帅
辽宁省沈阳市妇婴医院生殖中心(110000)
人类冻融胚胎移植(FET)是体外受精-胚胎移植(IVF-ET)助孕技术中重要的组成部分,可以降低卵巢过度刺激的发生率,还可以避免部分促排卵方案新鲜周期胚胎移植与子宫内膜发育不同步的情况。胚胎质量和子宫内膜容受性是FET成功妊娠的关键,在胚胎质量无法改变情况下,提高子宫内膜容受性以提高胚胎种植率是临床医生关注的热点问题。人绒毛膜促性腺激素(hCG)在胚胎植入子宫内膜前就已开始分泌,有学者发现在FET前进行hCG宫腔灌注,可以提高IVF-ET的胚胎种植率[1],但FET前宫腔操作患者依从性较差。本研究采用肌注hCG的方式,探讨hCG对人工周期FET患者子宫内膜容受性的影响。
1 资料与方法
1.1 研究对象
选取2018年1月—2019年2月于本院生殖医学科行FET周期治疗的不孕女性为研究对象。纳入标准:①准备内膜方案为人工周期;②年龄<40岁;③卵巢储备功能正常;④至少有1枚优质冻存胚胎(D3卵裂期胚胎≥6CII级,D5囊胚期胚胎≥3BB);⑤近3个月未应用过可能影响血流参数的药物,如低分子肝素、阿司匹林等;⑥均为首次胚胎移植。排除宫腔粘连、子宫内膜息肉、子宫内膜结核、子宫腺肌病、子宫形态异常、生殖器官良恶性肿瘤等可能影响子宫内膜血流的疾病以及各种原因取消周期者。随机数字表法分为对照组与hCG组,按照移植胚胎时期进一步分为对照D3组、对照D5组与hCG D3组、hCG D5组。所有研究对象均知情同意,本研究经本院伦理委员会审核批准。
1.2 研究方法
采用激素替代人工周期方案准备子宫内膜,所有研究对象于月经周期或孕激素撤退性出血的第3日开始口服戊酸雌二醇片(补佳乐,德国拜耳医药,1mg/片)6mg/d共14d,B超监测子宫内膜形态及厚度,必要时调整雌激素剂量。当子宫内膜厚度≥8mm时hCG组肌注hCG(珠海丽珠,2000U/支)4000IU与生理盐水2ml混合液,对照组肌注2ml生理盐水,次日给予地屈孕酮片(达芙通,荷兰AbbottBiologicalsB.V.,10mg/片)40mg/d及阴道用黄体酮软胶囊(安琪坦,比利时贝比斯医药,200mg/粒)600mg/d转化内膜;应用孕激素第3天行D3卵裂期胚胎移植,第5天行D5囊胚期胚胎移植,胚胎移植后继续维持原用药方案。Voluson E8彩色多普勒超声诊断仪(GE公司),阴道容积探头RIC5-9-D,频率6.0~8.0 MHz,经阴道探头常规检查子宫及双附件有无异常病变,在矢状面测量子宫内膜厚度,开启CDFI,于子宫内膜交界处显示清晰的子宫螺旋动脉,检测子宫螺旋动脉血流动力学参数,包括收缩期峰值/舒张末期流速(S/D)、阻力指数(RI)、搏动指数(PI)。启动脉冲多普勒(PD)及3D功能键,利用VOCAL功能,多平面手动勾勒子宫内膜边缘,计算子宫内膜容积(V),开启Histogram功能自动计算子宫内膜血管指数(VI)、血流指数(FI)及血管血流指数(VFI),所有受检者均连续检测3次,取平均值。
1.3 观察指标及评价标准
记录并比较对照D3组与hCG D3组,对照D5组与hCG D5组hCG日(对照组为生理盐水日)及移植日子宫内膜厚度、子宫螺旋动脉血流动力学参数、子宫内膜血流指数及辅助生殖相关指标[3]。生化妊娠:移植术后14天血β-hCG高于正常范围,随后逐渐下降,超声未探及到孕囊回声。临床妊娠:移植术后14天血β-hCG高于正常范围,且移植后35天超声于宫内或宫外探及孕囊回声。生化妊娠率=生化妊娠例数/移植周期例数×100%。临床妊娠率=临床妊娠例数数/移植周期例数数×100%。早期流产率=孕12周内自然流产周期数/临床妊娠周期数×100%。着床率=孕囊数/总移植胚胎数×100%(单胚胎移植孕囊数仅计为1)[2]。
1.4 统计学方法
采用SPSS 20.0统计学软件。两个独立样本计量资料组间比较采用t检验,计数资料采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 一般资料
纳入研究对象共488例。对照组(D3)135例,年龄(30.4±4.3)岁,年龄≥35岁18例(13.3%),体质指数(BMI)(21.2±3.1)kg/m2,不孕(4.2±2.0)年,移植胚胎≥2枚110例(81.5%);hCG组(D3)129例,年龄(31.6±5.2)岁,年龄≥35岁12例(9.3%),BMI(21.1±4.1)kg/m2,不孕(4.6±2.0)年,移植胚胎≥2枚98例(76.0%)。囊胚期胚胎(D5)均为单胚胎移植,对照D5组105例,年龄(31.3±5.1)岁,年龄≥35岁11例(10.5%),BMI(21.0±5.5)kg/m2,不孕(4.2±1.9)年;hCG D5组115例,年龄(31.6±6.4)岁,年龄≥35岁12例(10.4%),BMI(21.8±5.7)kg/m2,不孕(4.4±2.1)年。各组年龄、年龄≥35岁比例、BMI、不孕年限等比较均无差异(P>0.05)。
2.2 卵裂期子宫内膜容受性
hCG日,对照D3组与hCG D3组子宫内膜各指标均无差异(P>0.05);移植日,对照D3组子宫内膜厚度、子宫内膜V、子宫内膜血流VI、FI、VFI均小于hCG D3组,子宫螺旋动脉S/D、RI大于hCG D3组(P均<0.05),子宫内膜分型、子宫螺旋动脉PI无差异(P>0.05)。见表1、表2。

表1 卵裂期两组hCG日子宫内膜容受性指标比较

表2 卵裂期两组移植日子宫内膜容受性指标比较
2.3 卵裂期移植指标
对照D3组胚胎着床率、临床妊娠率均小于hCG D3组(P<0.05),生化妊娠率、早期流产率、异位妊娠率两组无差异(P>0.05),见表3。

表3 卵裂期两组临床指标比较[%(例)]
2.4 囊胚期子宫内膜容受性
hCG日,对照D5组与hCG D5组子宫内膜容受性指标比较无差异(P>0.05);移植日,对照D5组子宫内膜厚度、子宫内膜V、子宫内膜血流FI、VFI均小于hCG D5组,子宫螺旋动脉RI大于hCG D5组(P均<0.05),子宫螺旋动脉S/D、PI、子宫内膜血流VI两组比较无差异(P>0.05),见表4、表5。
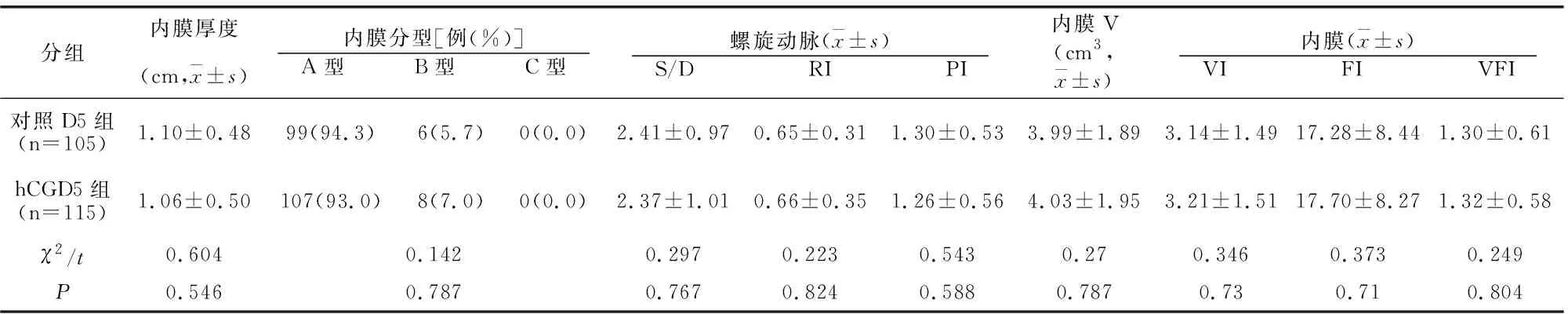
表4 囊胚期两组hCG日子宫内膜容受性指标比较
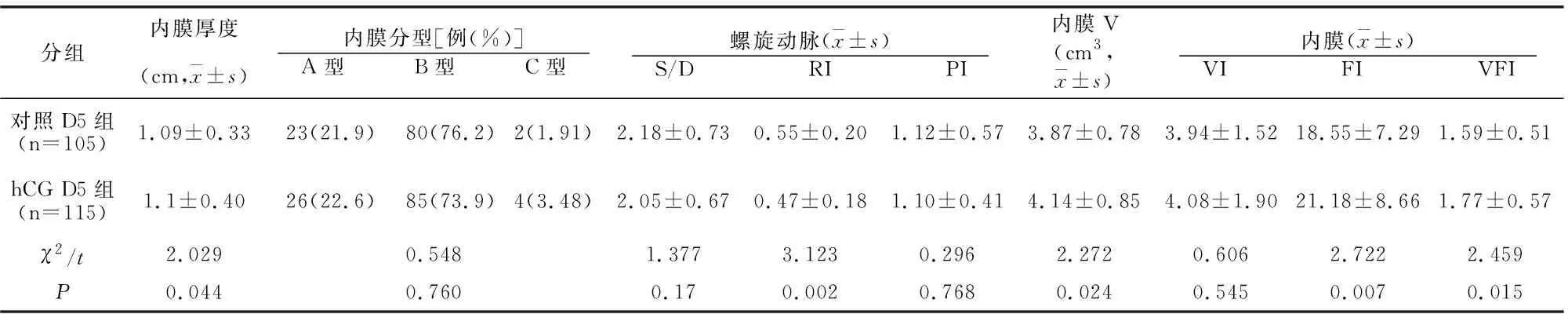
表5 囊胚期两组移植日子宫内膜容受性指标比较
2.5 囊胚期移植指标
对照D5组胚胎着床率、临床妊娠率均小于hCG D5组(P<0.05),生化妊娠率、早期流产率、异位妊娠率两组无差异(P>0.05)。见表6。

表6 囊胚期两组临床指标比较[%(例)]
3 讨论
目前认为,hCG在胚胎植入前就已经开始分泌,胚胎着床后开始大量释放。hCG与垂体分泌的黄体生成素(LH)的亚基结构相同,与LH拥有同一个受体,这类受体在子宫内膜组织表达,hCG的半衰期24h,远远长于LH的1h,且与受体的结合能力也优于LH,故在辅助生殖领域,hCG常被用来替代LH而发挥作用[3]。
胚胎着床率与妊娠率主要取决于子宫内膜容受性和胚胎质量,子宫内膜的容受能力与卵巢甾体激素、多种分子生物学因子及子宫内膜血流灌注有关[4]。有研究表明[5],hCG是与胚胎植入关系较为密切的胚胎源分子信号之一,hCG可以调控子宫内膜组织生物学因子的表达,如抑制子宫内膜组织中胰岛素样生长因子结合蛋白和巨噬细胞集落刺激因子的表达,增加白血病抑制因子、血管内皮生长因子、基质金属蛋白酶9的含量,进而促进子宫内膜的重塑化进程以及早期胚胎与子宫内膜上皮细胞的黏附过程,提高子宫内膜的容受性[6-7]。hCG还可以调节母-胎界面免疫功能,降低子宫内膜对胚胎的排斥反应,促进胚胎着床[8]。有学者[9]发现对于RIF患者,胚胎移植前进行r-hCG 500 IU宫腔灌注,移植日子宫内膜厚度大于未灌注组,胚胎着床率和临床妊娠率也随之升高。关于hCG对子宫内膜血流的影响,有研究发现在FET准备内膜期间肌肉注射小剂量hCG 会明显增加子宫内膜血流分支数目,降低子宫螺旋动脉放射状动脉RI、提高胚胎种植率及临床妊娠率[10-11]。
基于上述理论基础,本研究在人工周期FET的孕激素转化前给予肌肉注射hCG4000IU,拟模拟自然周期时的LH峰,通过观察子宫内膜血流灌注情况以及移植结局来分析hCG对子宫内膜容受性的影响。结果发现移植D3卵裂期胚胎移植日hCG组子宫内膜厚度、子宫内膜V、子宫内膜血流VI、FI、VFI值高于对照组,子宫螺旋动脉S/D、RI低于对照组,而移植D5囊胚期胚胎hCG组的病例子宫螺旋动脉S/D、PI、子宫内膜血流VI却未表现出差异,主要的差异在移植日子宫内膜厚度、子宫螺旋动脉RI、子宫内膜V、子宫内膜血流FI、VFI值方面。同时,不论移植D3卵裂期胚胎还是D5囊胚期胚胎,hCG均可以明显提高胚胎着床率和临床妊娠率,而这一作用是通过降低子宫螺旋动脉血流阻力、提高子宫内膜血流血管相关指数,增加血流灌注来实现的,hCG对子宫螺旋动脉血流及子宫内膜血流指数的作用可能与其提高子宫内膜血管内皮生长因子地表达有关,这尚需要进一步研究明确结论。此外,本研究中移植D5囊胚期胚胎的病例中,hCG对子宫内膜血流灌注的影响所体现的相关指标不如D3卵裂期胚胎明显,推测原因可能与hCG的半衰期有关。
总之,在人工周期FET转化内膜前给予hCG肌注可以改善子宫内膜血流灌注,以提高子宫内膜对胚胎的容受性,从而提高胚胎着床率和临床妊娠率。本研究中的病例均为首次移植周期,对于反复移植失败的病例 hCG的应用是否能改善移植结局是我们今后研究的方向。
