老年2型糖尿病患者并发骨质疏松的危险因素分析
2021-08-06郭玉珠黄爽
郭玉珠 黄爽
有研究数据显示[1],2型糖尿病(T2DM)患者发生骨折风险高出非糖尿病患者30%~50%,而我国2型糖尿病患病率超过10%,糖尿病患者数量居全球首位[2]。糖尿病除极易诱发各种血管疾病外,对骨骼系统损伤严重,据统计,2/3糖尿病患者存在骨密度(BMD)下降[3],而糖尿病与骨质疏松(OP)密切相关,OP是老年T2DM患者常见的慢性并发症[4]。此外,修双玲等Meta分析发现[5],T2DM合并OP是临床并发、易发骨折的全身性代谢性骨病,损害骨显微结构,增强骨脆性,降低骨量,是导致骨折率与致残率高发的重要原因[6]。但T2DM合并OP患者早期常无任何症状,易被忽视,直至病程发展至中后期,产生骨折、畸形、骨骼疼痛等症状[7],若不尽早治疗,待发生骨质疏松,会产生无法逆转的危害。鉴于此,本研究探讨老年T2DM患者并发OP的相关危险因素,进而为临床诊治提供参考依据。
1 对象与方法
1.1 研究对象
选取2018年6月—2019年12月在医院接受住院治疗的201例老年T2DM患者为研究对象,男129例,女72例;年龄62~82岁,平均71.52±5.07岁。纳入条件:符合《中国2型糖尿病防治指南》[8]内有关T2DM诊断标准;年龄≥60岁;患者与家属自愿参与本次调查,且积极配合疗护。排除条件:合并严重器质功能不全、肿瘤疾病;合并甲状腺、甲状旁腺、肾上腺等原发性疾病、骨代谢内分泌系统疾病;近6个月内服用皮质类固醇激素、维生素D或钙剂等;合并糖尿病酮症酸中毒等相关并发症;非T2DM所致OP。其中85例患者并发OP作为病例组,未并发OP患者116例作为对照组。
1.2 调查内容及方法
调查内容:①基本资料包括性别、年龄、BMI、吸烟史、是否贫血等;②病情资料包括糖尿病病程、低握力、是否有维生素D代谢异常等;③实验室指标包括糖化血红蛋白(HbA1C)、血肌酐(SCr)水平、血磷(P)、四肢骨骼肌质量指数(ASMI)。④指标检测与评估包括低握力诊断标准、实验室HbA1C、SCr、P以及ASMI测定。其中低握力诊断参考亚洲肌少症诊断标准[9],若女性<18 kg,男性<26 kg,则可判定为握力低;使用ADVIA2400全自动生化分析仪测定糖化血红蛋白(HbA1C)、血肌酐(SCr)水平、血磷(P);采用双能X线吸收仪测定患者骨密度与肌肉质量,首先计算四肢骨骼肌质量(ASM)=双上肢骨骼肌质量(kg)+双下肢骨骼肌质量(kg),接着计算四肢骨骼肌质量指数(ASMI)=ASM(kg)/身高(m)的平方[10],最终以肌肉含量减少诊断截值为ASMI男性<7.18 ,女性<5.73作为判定依据;是否贫血评判[11]:根据WHO贫血成人判定标准若女性Hb<120 g/L,男性Hb<130 g/L判定为贫血。
1.3 2型糖尿病诊断标准
根据美国糖尿病协会(ADA)制定的T2DM诊断标准[12]:存在以下任一状况可判定为T2DM:随机血糖水平≥11.1 mmol/L;FPG≥7.0 mmol/L;口服糖耐量试验(OGTT)2 h血糖水平≥11.1 mmol/L。
1.4 骨质疏松症诊断标准
参照WHO有关标准[13]:使用双能X线吸收法(DXA)测定T值,若>-1代表骨量正常,-1≤T值≤-2.5代表骨量减少,<-2.5判定为骨质疏松症。
1.5 统计学处理
采用SPSS 20.00统计学软件对数据进行统计分析,单因素分析时,计数资料组间构成比较采用χ2检验;计量数据采用“均数±标准差”表示,组间均数比较采用t检验。多因素采用Logistic回归模型。检验水准α=0.05,P<0.05为差异有统计学意义。
2 结果
2.1 影响老年T2DM患者并发骨质疏松的单因素分析
单因素分析结果显示,性别、年龄、BMI、握力水平、吸烟史、ASMI、血磷浓度、维生素D代谢异常、贫血是影响老年T2DM患者并发骨质疏松的因素(P<0.05),见表1。
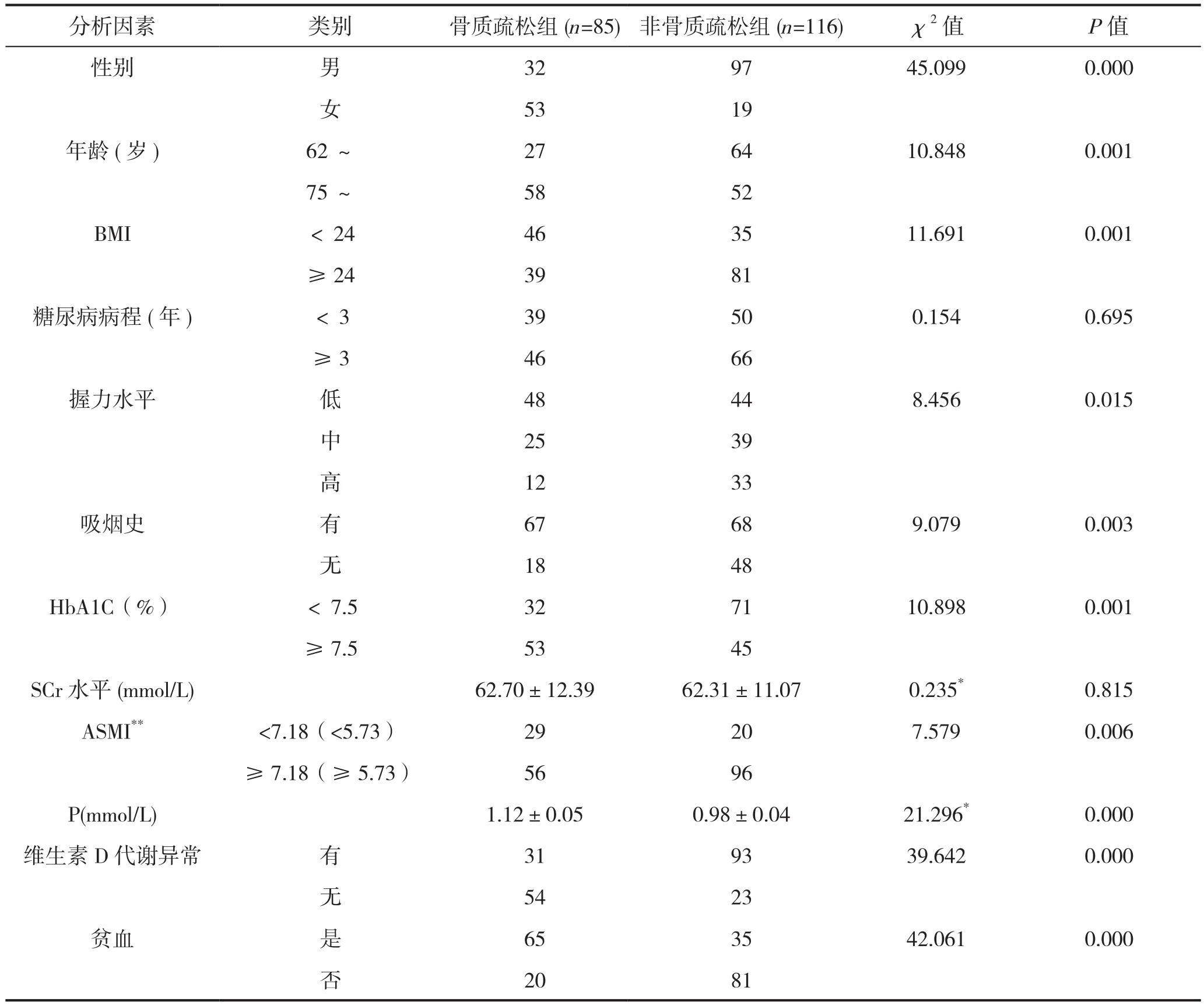
表1 影响老年2型糖尿病患者并发骨质疏松的单因素分析
2.2 影响老年2型糖尿病患者并发骨质疏松的多因素Logitic回归分析
多因素Logitic回归分析显示,年龄≥75岁、低握力、HbA1c≥7.5%、女性、ASMI、贫血是影响老年T2DM患者并发骨质疏松的因素(P<0.05),见表2。

表2 影响老年2型糖尿病患者并发骨质疏松的多因素Logitic回归分析
3 讨论
有研究表明[14],T2DM合并OP发病率超过60%,同时患多项慢性病会加速OP的发展进程,增加骨质疏松性骨折风险。概括多项指南与证据,总结并发OP机制,可归为如下4点[15]:①T2DM患者血糖控制欠佳,骨细胞活性与骨形成转化降低,骨密度减少;②长期偏高血糖致使维生素D代谢异常,影响骨代谢;③T2DM后期多饮食或体重异常、合并肾病等增加尿液排出钙质,易诱发低钙血症;④T2DM基因序列特定位点过度表达使低密度脂蛋白受体活性提升,代谢异常;⑤T2DM与OP复杂关系,骨形成与骨微环境受T2DM影响发生整体改变,老年T2DM患者骨密度降低50%~75%[15]。在此基础上,本研究纳入201例老年T2DM患者,探讨其并发OP独立影响因素为年龄≥75岁、低握力、HbA1c≥7.5%、女性、ASMI偏低、贫血等;BMI≥24为影响OP发生的独立保护因素。具体讨论如下:
(1)高龄:年龄≥75岁与T2DM并发OP高风险有关(OR=4.600),原因可能是老年患者随年龄增长,生理储备功能进行性降低,稳态维持及机体适应能力显著不足。
(2)女性:本调查发现,女性为老年T2DM患者OP发生的独立危险因素(OR=1.923),考虑原因在于女性经历绝经期,雌激素浓度迅猛降低,骨组织丧失雌激素保护,导致骨吸收多于骨形成,易发生OP。
(3)糖化血红蛋白(HbA1C):HbA1c是临床反映近3个月血糖调控有效指标。HbA1c≥7.5%是并发OP重要危险因素(OR=3.350),原因为HbA1c超过7.5%代表机体血糖调控水平低,体内长期高血糖会破坏破骨细胞,诱导骨吸收,进一步对肌肉骨骼系统,以及心血管、血液、内分泌系统产生负面影响[16]。
(4)低握力:本研究结果显示,低握力为老年T2DM患者并发OP的独立危险因素(OR=2.162),原因在于低握力反映低肌活动,会弱化骨骼负荷力,抑制骨吸收并促进成骨,降低肌力。这与有关报道提出[17]握力较高可延缓腰椎或股骨颈骨量流失一致。
(5)四肢骨骼肌质量指数(ASMI):老年T2DM患者低ASMI是OP独立危险因素(OR=2.555),究其原因,曹宗锐等研究证实[18]ASMI和骨密度呈正相关,骨密度会影响骨骼钙含量、胰岛素分泌等,ASMI数值越低,OP发生风险越高。
(6)贫血:贫血是影响T2DM合并OP的独立危险因素(OR=5.275),分析原因贫血预示低血红蛋白水平状况,血红蛋白作为运输氧气蛋白质,低氧血症会引发OP,增进氧化应激与细胞酸化,严重影响骨形成与重塑。
鉴于上述6项独立影响因素,对高龄、评估为低握力T2DM患者定期采用骨密度仪、定量CT等体检并监测骨密度,向患者及亲友提供疾病重要监测指标与相关知识辅助资料,提升自我保健知识;指导患者进食高铁、高维生素、高钙、低淀粉类膳食,监测维生素D或其他微量元素,预防贫血;鼓励患者适当户外活动,增加骨密度。
综上所述,老年T2DM患者并发OP风险偏高,其独立影响因素包括年龄、性别、握力水平、HbA1c含量、ASMI值、贫血等诸多因素,临床应尽早予以风险评估,并针对影响因素予以个体化干预,防护OP及相关并发症的发生。
