VATS联合肺大疱内OB胶固定治愈宽基底型巨大肺大疱并严重胸膜粘连1例及文献复习*
2021-08-04姜友军张培蓓郑梦凝叶贤伟1
姜友军,张培蓓,赵 丽,郑梦凝,许 川,叶贤伟1,△
(1.贵州医科大学附属人民医院呼吸与危重症医学科,贵阳 550002;2.贵州省人民医院呼吸与危重症医学科,贵阳 550002;3.贵州省人民医院胸外科,贵阳 550002)
肺大疱是直径大于1 cm且壁厚小于1 mm的肺泡腔扩张,是由不同病因导致肺泡壁破坏并相互融合所形成的含气囊腔。1937年由BURKE等提出巨型大疱性肺气肿,以描述因巨型肺大疱占据胸腔导致胸片上肺纹理大范围缺失的影像学表现,又名肺消失综合征;1987年ROBERTS等把占据单侧或双侧胸腔体积至少1/3且压缩周围肺实质的上叶肺大疱定义为巨大肺大疱(GPB),成为诊断GPB的影像学标准。GPB是慢性阻塞性肺疾病等细支气管炎性病变常见并发症[1],其国内发病率呈逐年升高趋势[2]。贵州省人民医院采用双孔VATS联合肺大疱内α-氰基丙烯酸酯快速医用胶(OB胶)固定,治愈1例宽基底型GPB并严重胸膜粘连患者,现报道如下。
1 资料与方法
1.1 一般资料
患者,男,55岁,主因“反复咳嗽、咳痰、胸闷10+年,加重1个月”于2019年10月12日入院。近20年来发生3次“左侧自发性气胸”,前2次均予对症治疗后好转,第3次予左侧胸腔闭式引流术并胸腔内药物注射行胸膜固定。曾每天吸烟30支,吸烟史20年,现已戒烟6年。既往有冠状动脉粥样硬化性心脏病、美国纽约心脏病协会(NYHA)心功能分级Ⅳ级、陈旧性肺结核。入院查体可见口唇轻度发绀,桶状胸,双侧语颤减弱,双肺叩诊呈过清音,左肺呼吸音减低,右肺呼吸音稍粗,双肺未闻及明显干湿啰音,余查体未见明显异常。查肺部HRCT示双肺散在炎性灶,多发肺大疱,左肺上叶较大者约136 mm×65 mm(图1)。血气分析示(FIO2:33%):pH 7.39,PaO2118 mm Hg,PaCO271 mm Hg,HCO3-43.0 mmol/L,BE 18.0 mmol/L,SO299%。心电图示窦性心动过速,心脏超声示心脏结构及功能正常,冠状动脉造影示左冠状动脉前降支近段少许非钙化斑块,管腔轻度狭窄(20%~30%)。因患者呼吸困难及存在自发性气胸可能,未能完善术前肺功能检查。诊断:(1)双肺多发巨大肺大疱并胸膜粘连;(2)慢性阻塞性肺疾病急性加重期并高二氧化碳血症;(3)冠状动脉粥样硬化性心脏病,不稳定型心绞痛,NYHA心功能分级Ⅳ级;(4)陈旧性肺结核。
1.2 治疗方法
入院后予氧疗,布地奈德、沙丁胺醇雾化吸入、多索茶碱静滴扩张支气管,洛贝林、尼可刹米兴奋呼吸中枢等对症治疗;患者胸闷、气促缓解不明显,考虑左肺上叶巨大肺大疱,正常肺组织被大面积压缩,肺功能下降。于2019年10月30日行手术治疗:静吸全身麻醉下双腔气管插管,取左侧腋中线第7肋间做2 cm切口作观察孔,腋前线偏前做3 cm切口作主操作孔,镜下见左侧胸膜腔广泛膜状粘连,予电凝钩分离部分粘连带暴露视野,左肺上叶肺大疱大小约10 cm×6 cm×12 cm,下叶见2个直径约4 cm肺大疱,基底广,难以行肺大泡切除。此3处肺大疱为靶肺大疱,定位并刺破肺大疱,并予萎陷的肺大疱内注入适量OB胶并轻压,使肺大疱内侧壁贴合,吸收性明胶海绵覆盖肺大疱创口,膨肺复张良好,检查创面未见明显漏气,同时胸腔内1次性灌注50%葡萄糖注射液200 mL行胸膜固定。术后持续左侧胸腔闭式引流,前3 d予甲泼尼龙琥珀酸钠20 mg/d静脉滴注,加强肺康复锻炼,氨酚双氢可待因对症止痛等治疗。术后第3天水封瓶内气泡明显减少,术后第7天未见气泡产生,予夹闭闭式引流管1 d后拔出胸腔引流管。
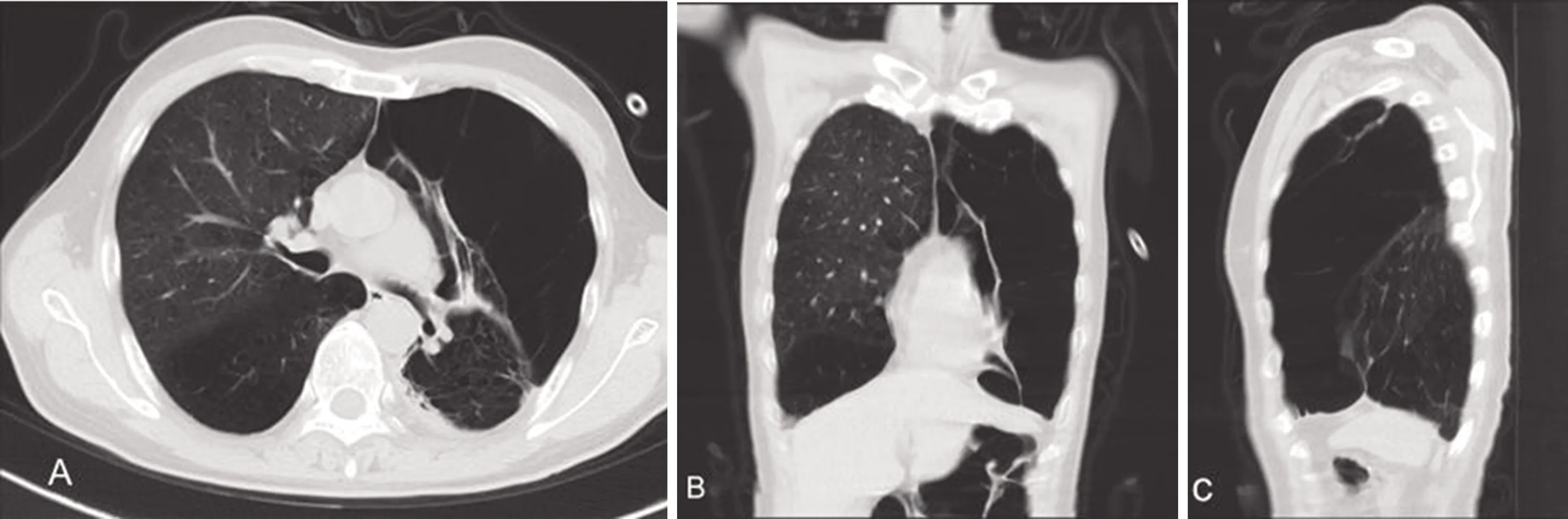
A:胸部CT横断面;B:胸部CT冠状面;C:胸部CT矢状面。
2 结 果
术后第5 天复查肺部HRCT示左侧健康肺组织复张良好,原肺大疱消失(图2)。6 min步行距离从术前的20 m提升到125 m,血气分析示PCO256 mm Hg,SO296%。于2019年11月10日治愈出院。
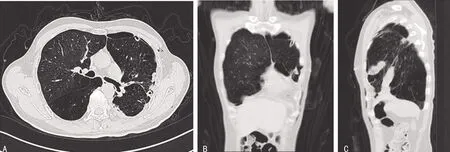
A:胸部CT横断面;B:胸部CT冠状面;C:胸部CT矢状面。
3 讨 论
GPB根据其影像学表现分为4型:Ⅰ型,狭颈肺大疱;Ⅱ型,宽基底部浅表肺大疱;Ⅲ型,宽基底部深位肺大疱;Ⅳ型,双侧GPB并气胸。GPB主要压迫周围肺实质、肺血管床及邻近器官,引起通气血流失衡、心肺功能下降等,导致呼吸困难、运动耐量及生活质量下降,以及自发性气胸[3-4]、急性呼吸衰竭[5]等。对于有呼吸困难、进行性呼吸功能不全或相关并发症的患者,应选择手术切除GPB[6-7],以缓解其对周围组织的压迫,从而改善肺心功能、提高生活质量[8]。目前,国内外治疗GPB的方法包括:经皮肺大疱穿刺引流术、内窥镜介入手术、外科手术,相比药物保守治疗,不同手术方式均能带给患者不同程度的获益[9]。
局部麻醉下经皮肺大疱穿刺置管引流术治疗GPB起源久远,其对手术器械、技术要求较低,操作简捷、经济微创,在GPB治疗中具有重要地位[10]。临床上常选择在CT引导下经皮肺大疱穿刺置管,并予肺大疱内注入生物胶+凝血酶+自体血[11]、生物胶[12]、抗菌药类[13]、滑石粉[14]等,联合肺大疱内持续负压吸引,利用肺大疱内无菌性炎性反应等,致使肺大疱粘连闭锁。术前应根据GPB分型选择合适的患者,完善肺部HRCT等评估肺大疱体积以指导每次注射粘连剂剂量,综合考量该手术给患者带来的风险及预期获益。该方法具有创伤小、操作简捷、费用较低、患者耐受性高等优势[11],也存在术中肺大疱内粘连剂注射过多溢出靶肺大疱引起周围健康肺组织或胸膜粘连、疼痛[13],术后肺大疱持续负压引流过程中,肺大疱萎陷后导管脱落导致治疗失败、气胸[10,14],以及发热、咯血、多次治疗等风险[11,13]。
随着呼吸介入病学的发展,采用内窥镜肺减容术(BLVR)日渐增多[15],主要包括经支气管镜放置支气管内单向活瓣、线圈、热蒸汽消融、肺泡内注射粘连剂等[6,9]。单向阀系统通过单向排除靶肺大疱内淤积的气体与分泌物,以萎陷过度膨胀的肺大疱[16-17];热蒸汽消融是经支气管镜予靶肺组织内释放热蒸汽,以诱发其无菌性炎性反应及纤维瘢痕修复等以闭锁肺大疱[18],最终达到肺减容目的。单向阀系统主要适用于不伴有旁路通气且叶间裂完整的重度非均质性肺气肿患者[19],应根据GPB所在肺叶及分型选择不同的手术方式[20],术前应完善Chartis系统检测以评估靶肺大疱旁路通气情况及肺部HRCT和心肺功能检测等[8,20];术中联合应用三维导航技术精准定位靶肺大疱,可能提高手术治疗成功概率[21]。既往研究发现,BLVR不仅能改善呼吸困难、肺功能、活动耐量、生活质量[19],且有效改善心脏前后负荷、降低肺动脉压力,以及避免肺血管床减少及肺脏弥散功能降低[8],同时也存在并发气胸、咯血、阻塞性肺炎、肉芽肿形成、活瓣移位等并发症[9]。
1950年报道外科肺减容术(LVRS)以来,得益于手术技术与并发症管理的改善,在1990年逐渐兴起[22]。2003年美国肺气肿治疗实验(NETT)纳入1 218例重度肺气肿患者,进行LVRS与药物治疗的随机对照研究,共有580例接受手术治疗,该组90 d病死率为7.9%(药物治疗组为1.3%),其高危亚组30 d病死率为16%(药物治疗组为0%),但截至第24个月时两组差异无统计学意义(P>0.05)[23]。虽然LVRS组较药物治疗组有更高的早期病死率,但术后短期和长期的随访研究表明,对重度肺气肿患者的呼吸困难、生活质量、活动耐量及肺功能、呼吸肌等指标有显著的改善,非均质性肺气肿比均质性肺气肿更加获益[24-26];从经济负担角度分析,LVRS组比药物治疗组具有优势[27]。LVRS包括传统开胸手术和VATS,开胸手术创伤大、患者耐受差等因素逐渐被较少应用,目前较多采用双孔VATS进行肺大疱切除术、肺叶切除术和肺减容术治疗GPB[8],或许达芬奇机器人手术更令人期待[28]。联合应用个体化麻醉通气策略[29-32]、胸腔闭式引流[33]、腔镜切割缝合器[34]等,能有效减少并发症和住院费用,缩短住院时间等。在NETT研究中LVRS组约90%的患者在术后30 d内发生肺泡漏气,而超过30 d的仅占12%;非高危亚组(511例)存在相应的肺脏(30%)和心脏(20%)并发症,以及肺部感染、缺氧等[22-23]。
综上所述,3种手术方式均能使患者获益。本研究中,肺大疱属于Ⅲ型,且合并严重胸膜粘连,不宜选择经皮肺大疱穿刺引流术或ELVR[14,20];因多发肺大疱,且基底广,手术切除困难,缝合肺大疱颈后漏气风险高,所需手术时间长,遂拟行双孔VATS[7,35]非切割方式去除肺大疱[36]。在排除手术绝对禁忌及在患者同意的前提下进行手术。通过术中观察得出,应用OB胶固定萎陷的肺大疱,比既往手术过程采用的切割缝合器、慕斯线结扎等方式[37],更能有效降低肺大疱发生严重漏气的概率,且缩短手术时间,术后未再气管插管及机械辅助通气。在围术期护理[38]及术后肺功能锻炼[39]等协同作用下,患者短时间内康复出院。本研究采取的VATS联合非切割方式去除GPB,具有手术时间短、患者易耐受、疗效确切、漏气概率小等优点,值得推广。
