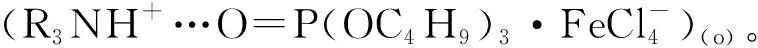用磷酸铵盐从N235中反萃取铁试验研究
2021-08-04何德文张雪凯赵堃祺周康根彭长宏
李 嘉,何德文,2,张雪凯,赵堃祺,周康根,2,彭长宏,2,陈 伟,2
(1.中南大学 冶金与环境学院,湖南 长沙 410083;2.中南大学 国家重金属污染防治工程技术中心,湖南 长沙 410083;3.中南大学 化学化工学院,湖南 长沙 410083)
氧化铝生产过程产生的赤泥中含有多种有价元素,如铁、铝、钙、钠、钛等,其中铁质量分数为5%~35%,且大多以赤铁矿形式存在,具有回收价值[1]。用盐酸浸出赤泥过程中,多种金属离子会同时溶解进入浸出液,使得铁的回收难度较大。采用溶剂萃取法可从溶液中有选择性萃取回收铁[2-5],但反萃取较为困难,需要较高浓度反萃取剂、较高反萃取级数和相比;另外,反萃取液中铁浓度较低,处理难度较大:因此,开发一种溶剂萃取回收铁工艺有重要意义。
常用的铁萃取剂中,碱性萃取剂如伯胺Aliquat336[6]、仲胺Amberlite LA-1、叔胺N235[7-8]萃取效果较好,萃取能力为伯胺>仲胺>叔胺,但叔胺的反萃取相对容易,且其可与中性磷类物质组成协萃体系,提高铁萃取率[9-10]。因此,以叔胺和中性磷类组成的萃取体系理论上可以实现对铁的高效萃取和反萃取。
从载铁有机相中反萃取铁通常采用盐酸、硫酸和硝酸等。但N235载Fe(Ⅲ)有机相,用低浓度盐酸反萃取,单级反萃取率仅75%左右[11];而用碱性溶液反萃取[10],经过3级逆流反萃取,铁反萃取率可达99.62%。碱性溶液在萃取达到平衡时pH较高,易引起Fe(Ⅲ)水解沉淀,有利于反萃取;但同时会造成油水夹杂,分相困难,有机相损失等问题。Fe(Ⅱ)相对Fe(Ⅲ)更易反萃取,所以可采用还原反萃取法,通过还原性物质,如锌粉[12]、H2[13]或SO2[14]将有机相中的Fe(Ⅲ)还原为Fe(Ⅱ),再进行反萃取,但此法操作难度较大、成本较高。目前,针对载铁N235的反萃取一般用稀盐酸、稀硫酸或纯水作反萃取剂,单级萃取率不够理想[11,15]。
试验研究了用N235+TBP+煤油萃取铁,然后用磷酸铵盐溶液反萃取铁,并研究了反萃取后有机相的萃取性能,进一步分析了萃取与反萃取机制,以期为酸性溶液中铁的回收提供一条思路。
1 试验部分
1.1 试验试剂与仪器
试验试剂:N235,三辛癸烷基叔胺,浅黄色透明液体,又名7301萃取剂,化学式R3N,R=C8或C8-10,三辛广东宏程生物科技有限公司,使用前无须纯化;TBP,磷酸三丁酯,化学式C12H27O4P,湖南汇虹试剂有限公司;煤油、磷酸,天津市恒兴化学试剂制造有限公司;FeCl3·6H2O、无水CaCl2、(NH4)2HPO4、NH4H2PO4、(NH4)3PO4,均为分析纯,国药集团化学试剂有限公司;盐酸,高级纯,国药集团化学试剂有限公司。
试验仪器:梨形分液漏斗;气浴恒温振荡器,ZD-85型,常州澳华仪器有限公司;电感耦合等离子光谱发射仪,ICP-AES,ICAP7400型赛默飞世尔科技公司;傅里叶红外光谱仪,FI-IR,NicoletiS50型;pH计,梅特勒-托利多仪器(上海)有限公司。
1.2 试验方法
赤泥模拟浸出液的配制:称取六水合氯化铁(FeCl3·6H2O)159.652 6 g,无水氯化钙(CaCl2)206.833 4 g,溶于一定量纯水中,再加入125 mL浓盐酸,待冷却至室温后加纯水定容至1 L。无水氯化钙溶解度大,用来充当氯源。模拟浸出液酸度为1.5 mol/L,化学成分见表1。

表1 赤泥模拟浸出液的化学成分
赤泥浸出液:取中国铝业股份有限公司广西分公司所产拜耳法赤泥,干燥、球磨后湿法浸出。浸出条件:盐酸浓度8 mol/L,浸出时间4 h,浸出温度80 ℃,液固体积质量比4/1,浸出后抽滤得到清液即为赤泥浸出液,其主要组成见表2。
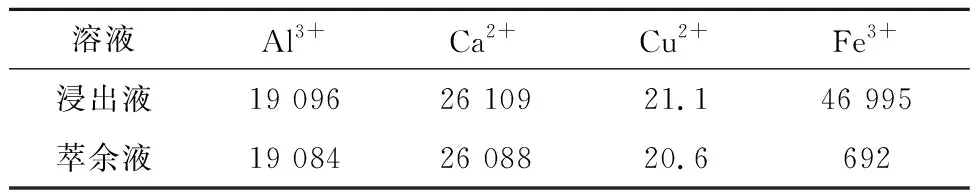
表2 赤泥浸出液及萃余液的主要化学组成 mg/L
有机相:按体积比2∶1∶3准确称取N235、TBP和煤油,混合均匀。
溶剂萃取铁:取一定体积有机相于分液漏斗中,按一定相比添加一定体积赤泥模拟浸出液,塞紧塞后将分液漏斗固定在气浴恒温振荡器上,待温度升至25 ℃后开启振荡,20 min后萃取过程达到平衡,关闭振荡器,取下分液漏斗自然分相。取萃余液分析其中铁离子质量浓度,萃余液主要组成见表2,通过差减法计算有机相中铁离子质量浓度及铁萃取率,计算公式为:
(2)
(3)
式中:η—铁萃取率,%;ρ—载铁有机相中铁离子质量浓度,g/L;ρ0、ρ1—萃取前、后水相中铁离子质量浓度,g/L;V—萃取后载铁有机相体积,L;V0、V1—萃取前、后水相体积,L。
反萃取:按一定相比向分液漏斗中加入反萃取剂和载铁有机相,塞紧塞后固定在气浴恒温振荡器上,温度升至设定值后开启振荡。反萃取结束后关闭振荡器,取下分液漏斗自然分相,取反萃取液分析其中铁质量浓度,计算铁反萃取率。计算公式为:
(4)
式中:ε—铁反萃取率,%;ρ—载铁有机相中铁离子质量浓度,g/L;V—载铁有机相体积,L;ρ2—反萃取液中铁离子质量浓度,V2—反萃取液体积,L。
1.3 分析方法
水相中各元素浓度用ICP-AES测定;水相pH用pH计测定;有机相萃取前后、反萃取前后官能团的变化采用FI-IR测定。
2 试验结果与讨论
2.1 反萃取剂种类及浓度对Fe(Ⅲ)反萃取率的影响
在有机相中Fe(Ⅲ)质量浓度为22.824 g/L、相比Vo/Va=1/1、反萃取时间20 min、反萃取温度25 ℃条件下,不同浓度的4种反萃取剂对Fe(Ⅲ) 反萃取率的影响试验结果如图1所示。

图1 不同浓度的反萃取剂对Fe(Ⅲ)反萃取率的影响
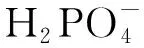
(5)
(6)
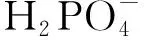
反萃取剂浓度为0.5 mol/L时,不同反萃取剂对Fe(Ⅲ)反萃取率的影响试验结果如图2所示。

图2 浓度0.5 mol/L条件下,不同反萃取剂对Fe(Ⅲ)的反萃取率
由图2看出,不同反萃取剂对Fe(Ⅲ)的反萃取能力为:(NH4)2HPO4>H3PO4>(NH4)3PO4>(NH4)H2PO4>H2O。综合考虑生产成本,试验确定选取(NH4)2HPO4作反萃取剂。
2.2 (NH4)2HPO4浓度对Fe(Ⅲ)反萃取率的影响
在有机相中Fe(Ⅲ)质量浓度为22.824 g/L、相比Vo/Va=1/1、反萃取时间20 min、反萃取温度25 ℃条件下,(NH4)2HPO4浓度对Fe(Ⅲ)反萃取率的影响试验结果如图3所示。

图3 (NH4)2HPO4浓度对Fe(Ⅲ)反萃取率的影响
由图3看出:随(NH4)2HPO4浓度升高,Fe(Ⅲ)反萃取率提高;(NH4)2HPO4浓度在0.5 mol/L时,Fe(Ⅲ)反萃取率达99.59%;(NH4)2HPO4浓度再升高,Fe(Ⅲ)反萃取率没有明显变化。综合考虑,确定(NH4)2HPO4浓度以0.5 mol/L为宜。
2.3 (NH4)2HPO4反萃取剂组成对Fe(Ⅲ)反萃取率的影响
由于(NH4)2HPO4溶液呈弱碱性(pH=7.8~8.2),反萃取时易引起Fe(Ⅲ)水解沉淀,进而引起油水夹杂、分相困难,造成有机相损失。试验通过加入H3PO4调节反萃取剂pH,同时控制总P浓度为0.5 mol/L来解决这个问题。
在有机相中Fe(Ⅲ)质量浓度为22.824 g/L、相比Vo/Va=1/1、反萃取时间20 min、反萃取温度25 ℃、总P浓度为0.5 mol/L条件下,6种不同反萃取剂组成对Fe(Ⅲ)反萃取率的影响试验结果如图4所示。
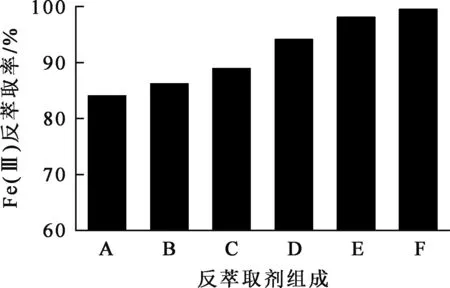
A—0.5 mol/L H3PO4;B—0.4 mol/L H3PO4+0.1 mol/L (NH4)2HPO4;C—0.3 mol/L H3PO4+0.2 mol/L (NH4)2HPO4;D—0.2 mol/L H3PO4+0.3 mol/L (NH4)2HPO4;E—0.1 mol/L H3PO4+0.4 mol/L (NH4)2HPO4;F—0.5 mol/L (NH4)2HPO4。图4 反萃取剂组成对Fe(Ⅲ)反萃取率的影响
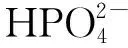
2.4 反萃取相比对Fe(Ⅲ)反萃取率的影响
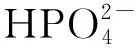

图5 Vo/Va对Fe(Ⅲ)反萃取率的影响
2.5 反萃取温度对Fe(Ⅲ)反萃取率的影响
在有机相中Fe(Ⅲ)质量浓度为22.675 g/L、反萃取剂组成为0.2 mol/L H3PO4+0.3 mol/L (NH4)2HPO4、相比Vo/Va=1/1、反萃取时间为20 min条件下,反萃取温度对Fe(Ⅲ)反萃取率的影响试验结果如图6所示。

图6 反萃取温度对Fe(Ⅲ)反萃取率的影响
由图6看出:温度对Fe(Ⅲ)反萃取效果影响不大,常温下,Fe(Ⅲ)反萃取率已在90%以上。考虑到温度越高,有机相分解损失越大,所以,确定反萃取在25 ℃下进行即可。
2.6 反萃取时间对Fe(Ⅲ)反萃取率的影响
在有机相中Fe(Ⅲ)质量浓度为22.321 g/L、反萃取剂组成为0.2 mol/L H3PO4+0.3 mol/L (NH4)2HPO4、相比Vo/Va=1/1、反萃取温度25 ℃条件下,反萃取时间对Fe(Ⅲ)反萃取率的影响试验结果如图7所示。可以看出:随反应进行,反萃取很快达到平衡,5 min时,Fe(Ⅲ)反萃取率达94.85%,之后趋于稳定。综合考虑,确定适宜的反萃取时间为5 min。

图7 反萃取时间对Fe(Ⅲ)反萃取率的影响
2.7 有机相循环
用N235+TBP+煤油萃取,用(NH4)2HPO4+H3PO4反萃取,得到再生有机相。再生有机相循环萃取7次所得反萃取液为最终反萃取液。有机相循环萃取试验结果如图8所示,最终反萃取液组成见表3。

表3 反萃取液的主要化学组成 mg/L

图8 再生有机相循环试验结果
萃取条件:有机相组成为35%N235+15%TBP+50%煤油,Vo/Va=2/1,温度25 ℃,时间20 min,分相时间20 min。
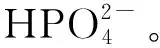
由图8看出:载铁有机相经(NH4)2HPO4+H3PO4溶液反萃取,Fe(Ⅲ)的萃取率和反萃取率均能维持较高水平;循环7次后,Fe(Ⅲ)的单级萃取率和反萃取率仍分别达98.76%和94.46%,循环效果较好。
由表3看出:赤泥浸出液经萃取和反萃取后,铁得到选择性分离;反萃取液中Ca2+、Mg2+、Na+、K+、Cu2+、Zn2+、Al3+等杂质离子含量很低,纯度较高,且磷铁质量比和pH指标合格,可用于下一步制备磷酸铁[16-18]。
2.8 萃取与反萃取机制
有机相的红外光谱分析结果如图9所示。

a—纯有机相;b—载铁有机相;c—再生有机相。图9 有机相的红外光谱分析结果
由图9看出:纯有机相、载铁有机相和再生有机相均在2 959、2 874 cm-1处出现C—H键伸缩振动吸收峰[19-21],在1 461、1 374 cm-1处出现C—H键对称和非对称振动吸收峰[22-23],在2 924、2 856 cm-1处出现(CH2)n中的碳链振动吸收峰[24-25],在1 025 cm-1处出现P—O—C特征峰[22]。TBP中P=O键在1 263 cm-1处出现的特征峰,萃取后偏移至1 243 cm-1处,为P=OHFeCl4吸收峰,表明铁被萃入到有机相中;再生后此特征峰又回到1 263 cm-1处,表明有机相成功再生,可循环使用[26-27]。N235萃取前出现在3 445 cm-1处的吸收峰为N—H键的吸收峰[28],萃取后偏移至3 377 cm-1处,表明铁被萃入到有机相中,再生后偏移至3 420 cm-1处,表明再生有机相经盐酸质子化产生的N—H+键相较于原来的N—H键吸收峰会有所偏移;同时由于H+带正电荷,再生后在循环中更容易与P=O键形成氢键,从而更有利于萃取。
综上所述:TBP不但可作为改性剂,也可与N235组成协萃体系共同萃取Fe(Ⅲ)。质子化的N235会与磷类萃取剂中的P=O键以氢键形式结合生成N—H+…O=P[28-29]。结合红外光谱分析结果推测,N235+TBP萃取Fe(Ⅲ)和(NH4)2HPO4反萃取铁的反应如下,其中,R3N代表N235,O=P(OC4H9)3代表TBP。
萃取:
Fe(Ⅲ)与Cl-配位,
(3)
N235与TBP结合,

(4)
有机相中,Cl-与FeCl4-交换实现萃取,
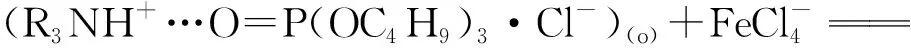
(5)
反萃取:
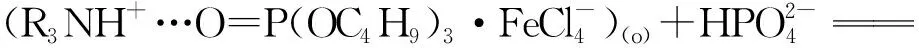
(6)
可知,N235与TBP在盐酸体系中会先结合,然后再与铁配位交换实现铁的萃取,同时也可以解释TBP的加入为何可消除第三相的产生。这与已有研究[4,30]结论具有一致性。
3 结论
以N235+TBP+煤油作有机相和磷酸铵盐溶液为反萃取剂可从赤泥酸浸液中回收铁。磷酸铵盐、水及纯磷酸反萃取铁的能力:(NH4)2HPO4>H3PO4>(NH4)3PO4>(NH4)H2PO4>H2O。以0.2 mol/L H3PO4+0.3 mol/L (NH4)2HPO4溶液为反萃取剂,在25 ℃下反应5 min, 控制Vo/Va=1/1,Fe(Ⅲ)单级反萃取率为95.2%。反萃取后的再生有机相有良好的循环性能。
赤泥盐酸浸出液经N235+TBP萃取和磷酸铵盐反萃取,实现了铁的选择性分离。反萃取液杂质含量低,磷铁比和pH指标合格,可用作制备电池级磷酸铁。