生物质不同部位制备炭基催化剂及其电催化氧还原性能
2021-07-29王可欣杨改秀孙永明李金平王春龙
王可欣 ,杨改秀 ,孙永明 ,李金平 ,王春龙,*
(1. 兰州理工大学 甘肃省生物质能与太阳能互补供能系统重点实验室,甘肃 兰州 730050;2. 中国科学院广州能源研究所 中国科学院可再生能源重点实验室,广东 广州 510640)
随着工业发展步伐与日俱增,能源和环境问题逐渐成为可持续发展的关键问题。燃料电池是一种绿色能源技术,有望成为未来的绿色能源转化装备[1]。但其阴极的氧还原反应(oxygen reduction reaction,ORR) 可逆性很低,交换电流密度较小(10-9-10-10A/cm2),需要催化剂加快反应进程,提高效率。而常用的铂基催化剂价格昂贵、储备稀少,明显阻碍了燃料电池的商业化进程。因此,新型高性能、低成本的代Pt催化剂的研发成为了近年的重点。
在众多的代Pt催化剂的研究中,生物质炭材料具有碳含量高、产量大、价格便宜、可再生等优点在被认为是催化氧还原领域最具应用潜力的催化剂之一,生物质自身富含多种分布均匀的杂原子(N、P、S等)这为原位合成掺杂型生物炭材料提供了必备条件,在热解炭化的过程中,这些杂原子能够掺杂到碳骨架中提高ORR的性能[2]。如Liu等[3]利用水葫芦制备N自掺多孔炭获得了较高的催化活性,起始电位约为0.98 V(vs. RHE),N掺杂到sp2杂化的碳骨架中能够诱导电荷再分配,形成石墨氮、吡啶氮、吡咯氮和氧化态氮,尤其是石墨氮和吡啶氮,促进O2分子的化学吸附和电子转移,以增强电催化性能。而P元素能改变各元素的电荷分布和前线轨道的能量特征[4],S元素影响炭材料的电子自旋密度以增大催化活性[5]。此外,杂原子共掺杂的协同效应使催化剂产生更多的活性位点,例如Zheng等[6]利用废虾壳制备N、P共掺杂炭材料,Song等[7]以海藻制备N、S双掺杂多孔炭,均获得良好的氧化原催化性能。此外,木质纤维素类生物质自身丰富的孔道结构也为生物炭材料的结构调控提供了原始条件,生物炭大都会保持木质纤维素类生物质的特有结构。如一维的柳絮[8]、蒲公英[9]、木棉纤维[10];二维的银杏叶[11]、大麻[12]、香蒲[13];三维的丝瓜海绵[14]、松木[15]等。由此可见,生物质原料自身特性对其热解产物影响很大。
目前,生物质热解制备炭材料常用的处理方法有直接热解法、水热法、化学活化法以及物理活化法等,其中,直接热解法操作简单,节能环保、对设备的腐蚀度低,是理想的热解方法,但是,直接热解法得到的生物质材料孔隙不发达,活性位点丰度不高,很难达到电催化过程的要求,大都需要物理或者化学活化剂的引入,以达到所得炭材料孔结构和活性位点的调控。为了获得高性能生物炭基氧还原催化剂的制备方法,研究生物质结构、组分对生物炭电极材料性能的影响具有重要意义。
苋菜是一年生草本植物,原产中国,其生长速度快、种植广泛,本身富含蛋白质、糖类、脂肪,以及多种维生素和矿物质[16],是很好的电极炭材料前驱体,苋菜叶里含有高浓度的氨基酸特别是赖氨酸,茎秆中纤维素含量较高[17],这为掺杂型生物炭基催化剂的合成提供了必备条件。苋菜叶中富含均匀分布的杂元素,苋菜茎具有天然的孔道结构,两者在组成和结构上具有较大差异。基于此,为了避免产地和种植方式等对生物质的影响,分别以同一苋菜的茎、叶为原料,通过一步直接热解法制备炭材料,探究其结构、组成对炭材料结构和性能的影响。并且分别探究了其在不同pH值条件下(酸性、中性、碱性)的ORR性能,获得生物质组成结构对炭材料ORR性能的影响机制。
1 实验部分
1.1 生物炭的制备
选取广州某菜市场购买的地苋菜为研究样本,取一定质量的苋菜原料,将茎(AS)、叶(AL)分离后放入80 ℃烘箱,烘干,研磨至粉末状备用。然后分别取等量原料放入坩埚后,在管式炉内进行热解反应,热解的升温速率为3 ℃/min,升温至800 ℃,恒温2 h,冷却至室温后,用HCl洗涤,用二次蒸馏水抽滤至中性。样品分别标记为ALC、ASC。
1.2 表征测试
通过X射线衍射仪(XRD, PANalytical)测试所得材料的晶体结构,采用CuKα靶,5°-100°扫描。拉曼光谱(Raman)通过激光共聚焦拉曼光谱仪(LabRAM HR800)测试,激发波长为532 nm,500-3500 cm-1扫描。材料表面的元素组成和化学组成分析通过X射线光电子能谱(XPS,ESCALAB250xi)和元素分析仪(Vario EL cube)完成。通过隧道扫描电子显微镜(SEM,Hitachi s-4800)和透射电子显微镜(TEM, Hitachi JEM-2100)观察生物炭的表面形貌和内部结构。应用全自动比表面积与孔径分布仪(ASIQMO002-2),并使用Brunnauer-Emmett-Teller(BET)方法和Barrett-Joynenr-Halenda(BJH)方法分别计算制备材料的比表面积和孔径分布。
1.3 电化学测试
电化学性能测试采用上海辰华CHI 660C电化学工作站连接三电极体系完成,玻碳电极为工作电极,饱和甘汞电极(SCE)为参比电极,铂电极为对电极。利用线性扫描伏安法(Linear Sweep Voltammetry,LSV)测试,测试的电解液分别为酸性:0.5 mol/L H2SO4溶液;中性:50 mmol/L 磷酸盐缓冲液(phosphate buffer solution PBS);碱性:0.1 mol/L KOH溶液,扫描速率为10 mV/s扫描范围分别为(-0.8)-0.4 V和(-0.8)-0.8 V。LSV测试的转速分别为400、625、900、1225、1600、2025、2500 r/min。电化学阻抗谱(electrochemical impedance spectroscopy,EIS)采用交流电压振幅为20 mV,频率范围为1 M-1 Hz,玻碳电极的测试面积为0.19625 cm2。通过Koutecky-Levich(K-L)方程计算ORR过程的相关动力学参数[18,19]:
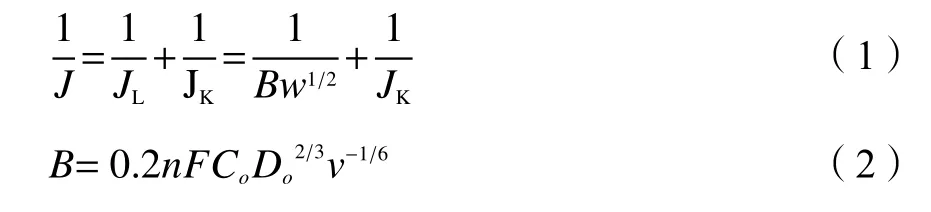
式中,J、JL和JK分别代表电流密度、扩散电流密度和动力学电流密度。 ω为盘电极的旋转速率,n为电子转移数,F为法拉第常数(F= 96485 C/mol)。Co为O2在电解质溶液中的浓度(在0.5 mol/L H2SO4溶液中,Co= 1.3 × 10-6mol/cm3;在50 mmol/L PBS溶液中Co= 1.26 × 10-6mol/cm3;在0.1 mol/L KOH溶 液 中,Co= 1.2 × 10-6mol/cm3),Do为O2在电解质溶液中的扩散系数(在0.5 mol/L H2SO4溶液中,Do= 1.8 × 10-5cm-2/s;在50 mmol/L PBS溶液中Do= 2.7 × 10-5cm-2/s;在0.1 mol/L KOH溶液中,Do= 1.9 × 10-5cm-2/s), ν为电解质溶液中的动力学黏度(在0.5 mol/L H2SO4、50 mmol/L PBS和 0.1 mol/L KOH溶液中,v= 0.01 cm-2/s)。0.2为旋转速率单位为r/min是所使用的常数。
2 结果与讨论
图1(a)是两种催化剂的XRD分析。从图中可以看到两种炭材料的峰位置基本相同,都在26°附近出现一个宽峰,对应于石墨碳(002)晶面的特征衍射峰。与ASC 相比,ALC(002)峰强度更高,说明其石墨化程度更高[20,21]。43°附近较宽的衍射峰是对应于石墨碳的(100)晶面,表现出很强的非晶态特征[22]。进一步通过Raman测试分析(图1(b))所制备炭材料的石墨化和表面缺陷度相关信息,由图可知,位于1340和1590 cm-1附近出现了两个特征峰,它们分别对应炭材料的的D峰和G峰。一般来说,D峰表示的是无序缺陷结构,G峰代表的是有序化石墨结构,D峰和G峰的强度比值(ID/IG)是炭材料的缺陷度的特征指数[8]。ALC的ID/IG为1.02低于ASC(1.06),这表明与ASC相比,ALC的石墨化程度较高,而ASC中缺陷更多[23]。该结果与XRD分析一致。
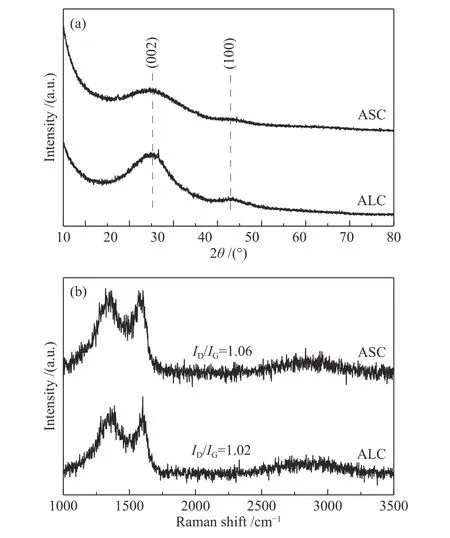
图1 两种生物炭XRD分析结果(a)、Raman分析结果(b)Figure 1 XRD patterns (a) and Raman spectrum (b) of two biomass based carbon materials
材料的元素和化学组成通过元素分析和XPS分析完成,如表1所示。XPS分析显示苋菜生物质含有丰富的氮元素,苋菜叶和茎原料的含氮量相近,原子百分比为5.43%-5.80%,通过高温热解以后,大部分氮元素保留在生物炭内。但元素分析和XPS分析共同显示,ASC的氮流失比ALC要更为严重,这可能是由于苋菜叶当中具有较高的氨基酸含量相关。
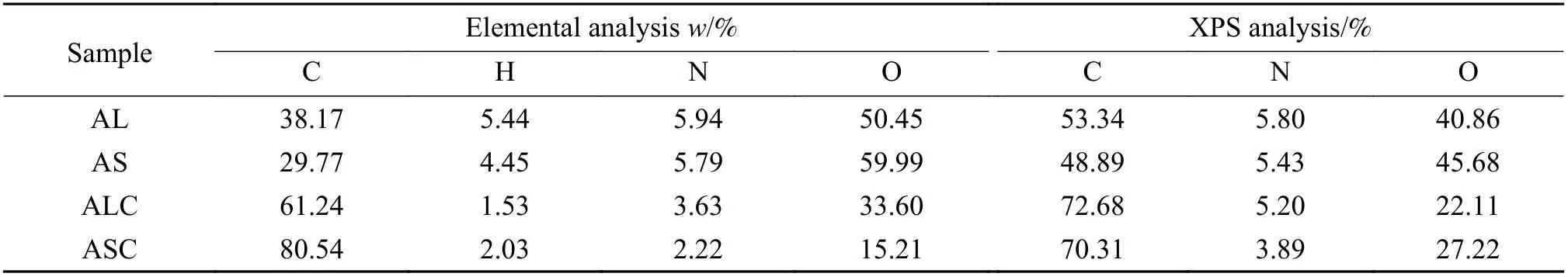
表1 元素分析和XPS分析Table 1 Elemental and XPS analysis of the samples
此外,氮的存在形式也会对炭材料的ORR性能产生影响,一般来说,其主要存在形式可分为吡啶氮(Pyridinic-N,~398.7 eV)、吡咯氮(Pyrrolic-N,~400.3 eV)、石墨氮(Quaternary N,~401.2 eV)和氧化态氮(N-oxides ~402.8 eV)。通过对N 1s进行分峰拟合(图2)可知,ALC和ASC氮形态分布相似,主要以吡咯氮为主,ALC的石墨氮和吡啶氮的总占比(46.3%)略高于ASC。因为吡啶氮和石墨氮有利于提供活性位点和降低传质阻力[24],并且石墨氮可以提高生物炭表面的电催化性能,所以它们的存在对ORR过程起着重要的作用[25]。结合XPS分析(表1),ALC的氮含量约为ASC的1.5倍,因此,ALC中石墨氮和吡啶氮的总含量(2.41%)显著高于ASC(1.64%),能够提供更多的活性位点。
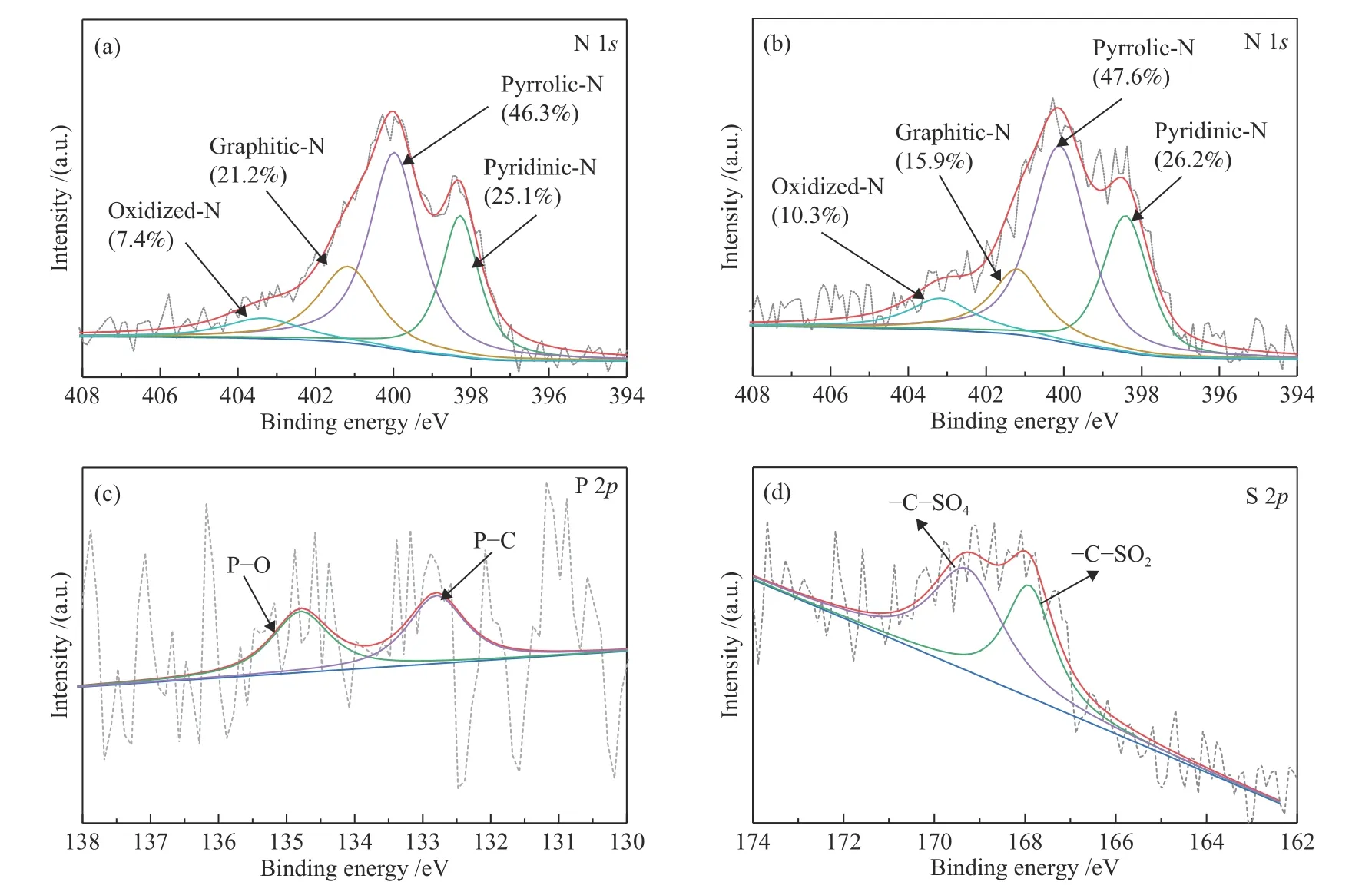
图2 ALC(a)和ASC(b)的XPS N 1s分峰图谱以及ALC的P 2p(c)和S 2p(d)分峰谱图Figure 2 XPS spectra and deconvolution of the N 1s of the ALC (a) and ASC (b), P 2p (c) and S 2p (d) spectra of the ALC
另外,P、S等元素的掺杂会对其性能产生影响,通过SEM/EDS对生物炭表面组成进行了测试,结果见图3,发现ALC表面的P含量为0.43%,S的含量为1.34%,而ASC的P含量几乎为零,硫含量仅为0.23%。通过ALC样品的P 2p和S 2p的XPS图谱(图2(c),(d))分析可知,电子结合能位于132.8和134.8 eV处的峰为P-C键和P-O键的特征峰[26],而电子结合能位于167.9和169.3 eV处的峰则相应于-C-SO2和-C-SO4的特征峰[27],这说明生物质自身杂原子的掺杂量不同,导致产物中杂原子的含量也不同。P、S的电负性不同于碳,会诱导产生更多的缺陷位和活性位点[28]。S原子的掺杂还可以引起相邻碳原子的不对称自旋,促进O2的吸附[29]。此外,P、S杂原子的共掺杂可以产生更强的协同效应,有助于提高炭材料的催化性能[26,30,31]。
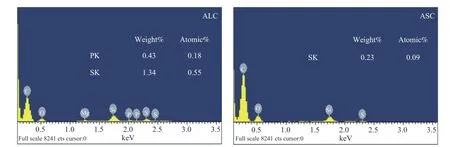
图3 ALC和ASC表面的SEM/EDS能谱谱图Figure 3 EDS spectra of ALC and ASC surfaces
通过傅里叶变换红外光谱(FT-IR)进一步对所得炭材料的表面组成进行表征。如图4所示,茎和叶子的原料及其对应的热解产物都出现了四个吸收峰,在ALC催化剂上,在3400 cm-1处的吸收峰可归因于羟基或羧基的O-H拉伸振动,和原料相比,热解产物的峰出现了偏移且强度加强,这可能是受到N-H(3500-3300 cm-1)伸缩振动的影响[32],说明热解产物中含有更高的氮含量。此外,1384和571 cm-1可归因于O-H弯曲振动[33],这表明热解产物表面富含含氧官能团。原料AL和AS中,2925和2854 cm-1左右的归属于-CHn[34],随着高温反应的进行,该键发生了断裂。位于2026、1600、1074和771 cm-1附近的峰分别对应于C≡C/C≡N、C=C/C=N/C=O、C-C/C-N、C-H[35]。相对于苋菜茎,苋菜叶的原料和热解产物的C=C/C=N/C=O的峰强度更明显,这说明苋菜叶热解产物的sp2杂化程度更强烈,石墨化程度更强;1074 cm-1附近的C-C/C-N键的峰,ALC明显强于ASC,表明ALC 的N掺杂更有效,与XPS结果一致。1270和680 cm-1处的峰分别对应的是为C-S和C-P键的红外吸收峰,且热解产物的峰强度比原料高,这说明,在热解过程中,有更多的C-S和C-P键形成,所制备的炭材料比生物质原料具有更高含量的P、S掺杂[36]。
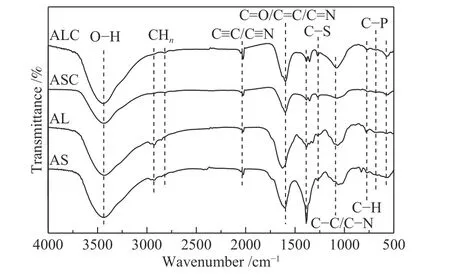
图4 AL、AS、ALC和ASC的红外光谱谱图Figure 4 FT-IR spectra of AL, AS, ALC and ASC
生物炭表面结构通过SEM进行分析,如图5所示。原料AL和AS的热解产物均呈现出多孔结构,ASC的纵向孔隙结构和孔道深度更明显,ALC表面的片层的微孔结构特征更为显著,这可能是由于运输营养物质的需要,茎的孔道结构更丰富,热解产物保留了原来的孔道结构,但是由于纤维素之间的作用比较紧密,因此,茎成分之间的作用键更强,导致热解炭产物结构更紧密。通过N2吸附-脱附等温测试可以看出,ALC和ASC均有H4型回滞环特征I/IV型曲线,这表明ALC和ASC有类似的孔径分布,存在微孔和介孔结构。显然ASC存在更多孔结构,使ASC比表面积为2749.3 m2/g,约为ALC的3.8倍(见表2)。这可能是因为植物的原料天然结构中茎比叶含有更多纤维状结构,使得高温热解后产生更多的孔隙。

图5 ALC(a)和ASC(b)的SEM照片Figure 5 SEM images of the ALC (a) and ASC (b)

表2 ALC和ASC的比表面积及孔容参数Table 2 Pore parameters of the ALC and ASC
通过旋转圆盘电极测试了所制备的炭材料在不同pH电解液中ORR性能。图6是ALC和ASC催化剂在不同pH溶液中,1600 r/min转速下的LSV曲线。由图可知,ALC在酸性、中性和碱性溶液中的起始电位分别是0.529、0.215 V 和-0.046 V(vs.SCE)均高于ASC的起始电位(0.197、0.102 V和-0.14 V)。这说明,ALC在较宽的pH范围内,对ORR表现出优异的电催化性能。这主要是因为生物炭材料的电催化性能受孔隙结构和杂原子掺杂所协同调控,所以尽管ASC表现出较高的比表面积,但是活性位点数量不充足,因此,其电催化活性低于ALC。为了进一步分析ORR性能差异的原因,对ALC和ASC进行了EIS测试,图7(d)显示了在PBS溶液中ALC和ASC的Nyquist曲线,在高频区的截距为材料在溶液中的欧姆阻抗Rs,主要包括溶液阻抗和生物炭自身的欧姆阻抗;半圆弧的直径为电荷传质阻抗Rct[37]。与ASC相比,ALC同时具有更低的欧姆内阻和电荷迁移阻力,说明ALC的导电性更好,这主要得益于其更高的石墨化程度和更多的催化活性位点[38]。
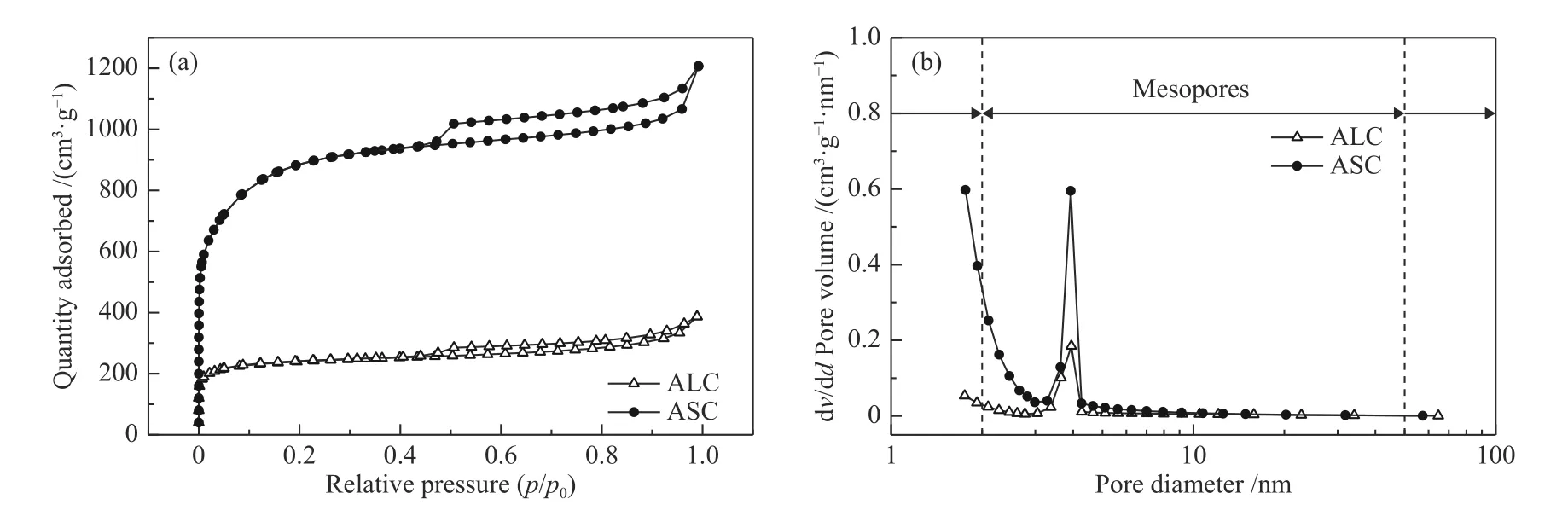
图6 ALC和ASC的N2等温吸附-附曲线(a)和孔径分布(b)Figure 6 N2 adsorption-desorption isotherms (a) and pore size distribution (b) of the ALC and ASC
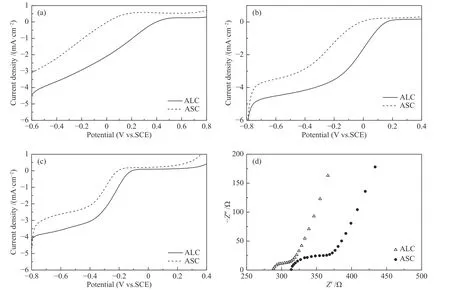
图7 ALC和ASC在O2饱和的0.5 mol/L H2SO4(a)、50 mmol/L PBS(b)和0.1 mol/L KOH(c)溶液中的1600 r/min LSV曲线以及在50 mmol/L PBS溶液中的EIS测试曲线Figure 7 1600 r/min LSV in O2-saturated 0.5 mol/L H2SO4 (a), 50 mmol/L PBS (b) and 0.1 mol/L KOH (c) and EIS curves in 50 mmol/L PBS(d) of the ALC and ASC
为了进一步比较苋菜叶、茎所制备的生物炭的ORR性能。Koutecky-Levich(K-L)方程计算了ORR过程中的电子转移数。一般来说,ORR反应主要分为两种途径,一种是理想的4e-反应,氧气直接还原为水(O2+ 4H++ 4 e-→2H2O)。另一种是2e-反应,先生成中间产物过氧化氢,再进一步还原成水。2e-途径会降低ORR反应效率,且生成H2会降低电流输出效率和催化剂催化活性,进而影响电池系统的效率[39]。图8为ALC和ASC在0.1 mol/L KOH电解质溶液中,于不同转速下的LSV图,以及K-L图。由电子转移数,图可知,ALC在0.4-0.7 V的电子转移数为3.36-3.67,而ASC为1.96-3.36,这表明氧气在ALC催化剂上的还原反应过程更接近4e-反应,且反应更为稳定。这一方面归因于ALC表面较高的石墨氮含量,有助于生物炭电子传导能力的提升,降低电荷转移阻力;另一方面,ALC生物炭中较高程度的N、P、S的掺杂,会改变碳原子周围的电荷密度和自旋密度,有助于产生更多的活性位点,有助于ORR过程中反应物和产物以及反应中间体的吸附和解离,从而促进反应过程动力学[40,41]。
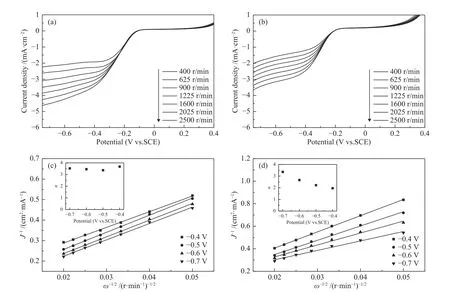
图8 ALC和ASC在O2饱和0.1 mol/L KOH溶液中不同转速的LSV图((a)、(b))及K-L图((c)、(d))Figure 8 LSV of the ALC and ASC in O2-saturated 0.1 mol/L KOH at different rotation rates ((a), (b) and their Koutecky-Levich plots ((c), (d))
3 结 论
本研究通过直接热解法分别制备了苋菜叶、茎生物炭,并考察了它们在不同pH溶液中的ORR性能。研究结果表明,与ASC相比,ALC生物炭材料的石墨化程度较高,表面具有更加丰富的杂原子共掺杂(N、P),特别是石墨氮和吡啶氮总含量较高,再加上合适的比表面积和孔分布,使得它不管在酸性、中性还是碱性溶液中都表现出更加优异的ORR性能。在中性溶液中,ALC起始点电位为0.215 V(vs.SCE);在酸性溶液中,两种生物炭的性能差异最为明显,ALC的ORR起始还原电位比ASC正移了0.332 V;特别是在碱性溶液中,ALC的电子转移数约为3.51,接近4e-反应。ALC及ASC的性能差异主要可归因于植株生长过程中元素组成分布和结构差异,叶子比茎含有更多种类的杂原子和氨基酸,在热解的过程中,可原位掺杂到碳骨架中,这为掺杂型高性能生物炭基ORR催化剂的原位合成提供了技术和方法。为燃料电池高性能、低成本代Pt催化剂的研发提供了新途径,说明生物炭基ORR催化剂是一种具有应用前景的燃料电池ORR 催化剂。
