原位同步辐射光电离质谱研究压力对3Mn10Fe/Ni催化剂上N2O形成途径的影响
2021-07-29许鸣皋朱宝忠杨玖重孙运兰
许鸣皋 ,文 武 ,朱宝忠,3 ,杨玖重 ,潘 洋,* ,孙运兰,3,*
(1. 安徽工业大学 冶金工程学院,安徽 马鞍山 243032;2. 中国科学技术大学 国家同步辐射实验室,安徽 合肥 230026;3. 常州大学 石油工程学院,江苏 常州 213164)
氮氧化物(NOx)是导致光化学烟雾、酸雨和臭氧损耗的主要空气污染物。目前,NOx主要来源于以化石燃料燃烧为主的火电厂、工业窑炉等固定源排放的烟气;其次来自船用重油柴油内燃机尾气、汽车尾气等移动源排放的尾气。当前,降低NOx最为有效的技术为选择性催化还原NOx(SCR)技术[1,2]。一氧化二氮(N2O)作为氨选择性催化还原反应中主要副产物之一,已被列入受管制的温室气体(GHG)污染物名单,其全球变暖潜力是CO2的298倍,对满足基于CO2的燃料经济和GHG标准的能力产生负面影响[3,4]。
催化剂是氨选择性催化还原(NH3-SCR)技术的关键,其活性对NOx和N2O的减排有着巨大的影响。文献中报道了各种各样的SCR催化剂,包括贵金属(如Pt、Pd、Rh、Au、Ag)[5-8]和过渡金属(如V、W、M、Cu、Fe、Mn、Ce)[9]。贵金属催化剂活性高,但价格昂贵,过渡金属催化剂成本低,抗中毒能力强。Fe基催化剂有很好的应用前景,Mn的添加可以有效提升Fe基催化剂的低温脱硝活性,Ni具有肉眼可见的网状结构,价格低廉,是承载催化剂的重要载体之一。铁和锰(Fe-Mn)基催化剂因其良好的低温SCR活性(350 ℃以下),近年来获得了广泛的关注和研究[10-13]。然而,Fe-Mn基催化剂在应用中受到了极大地限制,主要集中在以下两个方面[14,15]:第一,催化剂容易中毒而失去活性(例如:碱金属中毒、SO2中毒和H2O中毒等);第二,反应中伴随一定量N2O的形成。
到目前为止,针对Fe-Mn基催化剂SCR反应中N2O形成途径仅在常压下进行了随温度变化规律的研究[16,17]。同位素标记实验表明[18],在SCR条件下,N2O中的两个N原子一个来自NH3,另一个来自NO。Yang等[10,18]研究表明,Fe-Mn基催化剂上低温SCR反应中N2O的形成主要遵循两种机制,类似于NH3-SCR过程中N2的形成,即Eley-Rideal机制(后简称E-R机制,即气态NO与过活化NH3的反应);另一种是Langmuir-Hinshelwood机制(后简称L-H机制,即吸附NO3-与相邻位点吸附态NH3的反应)。
反应体系的复杂性造成了N2O生成途径的多样性[19],与温度[20]、环境[21]和制备方法[22]对反应途径的影响力相同,压力作为外在因素也同样对反应体系起到不可忽视的作用,特别注意到的是,轮船燃动系统中低压SCR系统已经得到研究和应用[23,24],大型船舶正是通过采用在重油柴油内燃机涡轮增压器下游低温段(≤ 250 ℃)增设低压SCR系统达到脱除尾气中NOx的目的,且NOx的脱除率可以达到90%[25]。然而,关于低压对NH3-SCR反应中N2O生成途径的影响机制报道极少。
基于研究组通过对网状泡沫镍负载不同量铁锰催化剂SCR催化活性的研究结果[26-28],发现3Mn10Fe/Ni具有良好催化剂催化活性(NOx转化率 ≥ 98%),具备了良好的应用前景,然而N2O在3Mn10Fe/Ni催化剂上的形成机理研究报道极少,因此,针对3Mn10Fe/Ni催化剂SCR反应体系中如何抑制N2O的生成,进一步研究该催化剂的催化机制具有重要的研究意义。同步辐射光电离质谱技术作为一种软电离的原位探测方法,具有无极性歧视、原位探测和分析快速等优点[29,30],在催化、燃烧和氧化热解等反应体系中得到了广泛的应用[29,31,32],本工作拟利用同步辐射光电离质谱装置(SR-PI-MS)结合常压和低压原位反应器,对3Mn10Fe/Ni催化剂SCR反应过程中N2O的形成过程进行了原位探测和动态追踪,探究了不同反应压力对N2O生成途径的影响规律,为生产生活中N2O的减排与防治提供一定的理论指导,为低温脱硝Fe-Mn基催化剂的应用奠定理论基础。
1 实验部分
1.1 仪器与装置
本次实验全部在合肥国家同步辐射实验室的燃烧光束线(BL03U)完成。来自于波荡器的同步辐射真空紫外光(VUV)由一块200 lines/mm的平面光栅(Horiba Jobin Yvon,法国)进行单色化,该光栅覆盖的光子能量为7.5-22 eV,能量分辨为3000(E/ΔE@ 10 eV)。高次谐波通过在气体滤波池中通入氩气(Ar)来进行滤除,经滤波后到达实验站的平均光子通量可以达到1013光子/s。
催化实验装置本组之前已有报道[29,30]。简言之,该装置主要由原位催化反应器和光电离质谱系统组成,结构示意图如图1所示。原位催化反应器分为低压反应器和常/高压反应器。
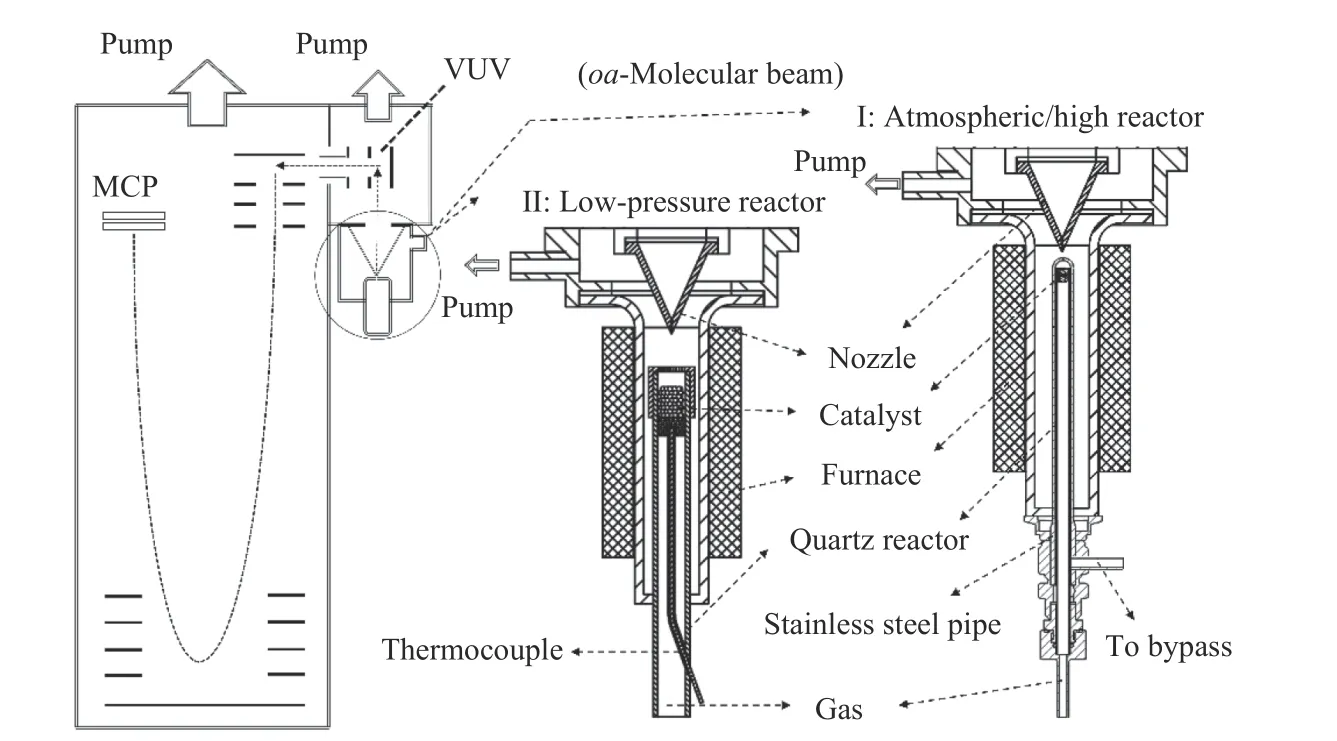
图1 原位光电离质谱示意图Figure 1 Schematic diagram of in-situ synchrotron radiation photoionization mass spectrometry
1.1.1 常/高压反应器
该反应器由反应腔、管式炉(工作范围为25-750 ℃)和高压不锈钢反应管组成。高压反应器置于反应腔中,由不锈钢高压外管、内衬石英管和石英喷嘴组成。内衬石英管用于盛装催化剂样品,从催化剂表面脱附的气相产物从不锈钢高压管末端小孔(60 μm)喷出,进入真空腔,再经石英喷嘴(450 μm)进行取样进入电离室。喷嘴距离高压管微孔出口为1-2 mm。反应腔压力由压力传感器、蝶阀(型号61232-KEGG-0002, VAT,瑞士)和真空泵组成。本文中该反应器工作压力为101.325 kPa[30]。
1.1.2 低压反应器
该反应器由反应腔、管式炉(工作范围为25-750 ℃)和石英反应管组成。石英管(外径8 mm,内径6 mm,长度150 mm)置于反应腔中,前端10 mm处放置一块石英砂板,用于固定催化剂。在石英砂板的另一端插入热电偶(K型)与催化剂相邻,用于实时反馈反应温度。从催化剂表面脱附的气相产物经石英喷嘴(450 μm)进行取样进入电离室。反应腔压力由压力传感器、蝶阀(型号61232-KEGG-0002, VAT,瑞士)和真空泵组成。该反应器工作压力一般 ≤ 0.665 kPa[29]。
1.1.3 质谱系统
该系统主要由一台自制正交反射式飞行时间质谱仪(oa-RTOF-MS)、电离室等组成。经石英喷嘴取样形成分子束进入电离室,与同步辐射真空紫外光(VUV光)交叉后被电离,离子由oa-RTOFMS进行质量分析,电信号由VT120C前置放大器(EG & G, ORTEC, Oak Ridge, TN)放大,由P7888-2采集卡(FAST Comtec, Germany)记录。
1.2 主要材料与试剂
硝酸铁Fe(NO3)3·9H2O、硝酸锰Mn(NO3)2(质量分数50%)均为分析纯,购于国药集团化学试剂公司。氩气(99.999%)、氧气(99.999%)、氪气(99.99%)、一氧化氮(混合气,摩尔分数2.5% NO、97.5% Ar)和氨气(混合气、摩尔分数2.5% NH3、97.5% Ar)均购置于南京特种气体有限公司。
催化剂采用浸渍法制备。分别称取一定量的Fe(NO3)3·9H2O和Mn(NO3)2,加入适量去离子水配置成所需要浓度的溶液后,将一定量的碎片状泡沫镍与上述配制好的溶液混合,磁力搅拌1 h,然后在干燥箱中105 ℃下干燥12 h,再将干燥后的催化剂样品放入马弗炉中500 ℃焙烧5 h,得到3Mn10Fe/Ni(后文简称fresh)催化剂。
1.3 实验条件
实验设置气体总流量为100 SCCM,体积空速比(GHSV)为30000 h-1,催化剂(80 ± 1) mg,载气为氩气,实验中通入5%氪气(Kr)矫正光强和仪器所造成的误差。实验气体配比以及其他条件如
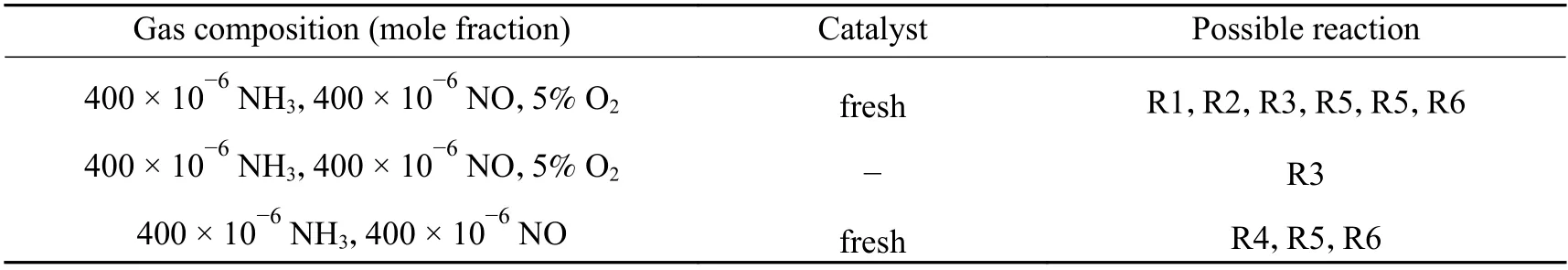
表1所示。
1.4 实验方法
实验分别在高压反应器(101.325 kPa)和低压反应器(0.266 kPa)中进行。在100-500 ℃进行定温催化实验,温度间隔为50 ℃,共计9个温度点。每次以100 s/point采集质谱信号,获取各组分随温度变化的质谱图。光电离效率光谱(PIE)实验是在恒温(400 ℃)、恒压(101.325 kPa)下完成,光子强度为12.6-13.2 eV,单步为0.03 eV/20 s。
由式(1)-(3)计算催化剂的N2O选择性以及NOx和NH3的转化率:

式中, [N2O]out为N2O在线监测的气体含量,[NOx]in、 [NOx]out分别为NOx进口和在线监测的气体含 量, [NOx]=[NO]+[NO2]; [NH3]in、 [NH3]out分 别 是NH3进口和在线监测的气体含量。
2 结果与讨论
2.1 催化剂的选择
Cao等[33]和Zhang等[34]文献中报道,在120-240 ℃下Fe-Mn催化剂NOx转化率分别为65%-90%和30%-85%。基于前期的研究基础[26-28],通过对网状泡沫镍负载不同量铁锰催化剂SCR催化活性的研究结果进行对比,发现fresh催化剂具有良好的低温(120-240 ℃)SCR催化活性(NOx转化率 ≥ 98%),具备了良好的应用前景,然而对N2O的形成机理研究暂未涉及,因此,针对fresh催化剂SCR反应体系中如何抑制N2O的生成具有重要的研究意义。
由于催化剂的比表面积大小有限,活性位数量存在最大值,所以随着空速的提升,NOx的转化率呈现下降趋势[26]。为了克服扩散限制,在开展N2O实验时,选择了较高的GHSV (30000 h-1)来获得较低的NOx转化率(< 70%),从而充分测试催化剂催化活性极限。
2.2 不同压力对N2O选择性的影响
为了研究压力对fresh催化剂上N2O生成途径所造成的影响,实验设置了三种工况(见表1)以及两种压力条件(101.325、0.266 kPa)。图2显示了压力为101.325 kPa,温度为400 ℃,体积空速为30000 h-1时,NH3-SCR反应体系中气相物种的光电离质谱图,其中,反应物为NH3、NO和O2,反应产物为N2O、H2O和NO2。图2中的附图为质荷比 =44质谱峰的光电离效率曲线(PIE图,其拐点12.88 eV对应于N2O的电离能)。通过在线光电离质谱技术结合原位反应器可以实现fresh催化剂上NH3-SCR反应体系中各组分变化的原位监测,光电离截面定量方法可参考文献[35]。
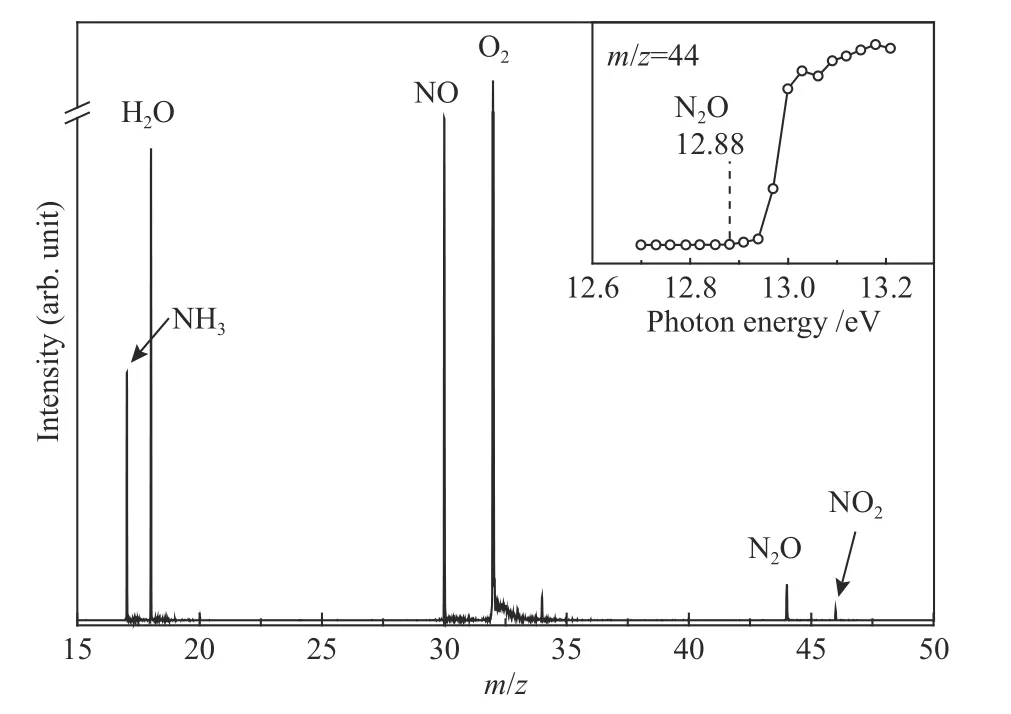
图2 光子能量为13 eV时fresh催化剂上SCR反应气相物种的光电离质谱图;插图为N2O的PIE图[36]Figure 2 Mass spectrum of the gas phase species in SCR reaction on fresh catalyst at the photon energy of 13 eV Inset is the PIE spectrum of the m/z = 44 species reaction conditions:101.325 kPa; 400 ℃; NH3+NO+O2+fresh;GHSV: 30000 h-1
图3展示了三种工况以及不同压力下N2O选择性随温度的变化,下文基于三种工况分别讨论了两种压力条件下N2O选择性的变化规律。
2.2.1 在NH3+NO+O2+fresh工况下
在NH3+NO+O2+fresh(标况)工况下,由图3(a)、(b)可知,不同压力条件下N2O的选择性随着温度的升高均呈现先升后降的趋势,在300 ℃时N2O的选择性增幅呈现放缓趋势,400 ℃时选择性到达峰值,101.325和0.266 kPa条件下N2O的选择性峰值分别为18.19%和23.69%,后逐渐下降,证明N2O的生成量逐渐减少。对比图3(a)和(b)发现低压(0.266 kPa)条件促进N2O的生成,提高了选择性。
2.2.2 在NH3+NO+O2工况下
为了研究fresh催化剂在N2O生成途径中的作用机制,设置空管对照组为NH3+NO+O2(无催化剂)工况,通过图3(a)可知,101.325 kPa条件下,N2O的选择性呈现随温度逐渐增强的规律,在500 ℃时达到9.2%,并且并未到达峰值。然而由图3(b)可以发现,对比101.325、0.266 kPa条件下N2O的选择性变化规律截然不同,在250-400 ℃呈现先增后减的变化规律,而且选择性偏低,具体原因在下文中分析。
2.2.3 在NH3+NO+fresh工况下
为了研究O2在N2O生成途径中的作用规律,实验对比标准工况,设置NH3+NO+fresh(无氧条件)工况作为第二对照组。通过图3(a)可知,101.325 kPa压力下N2O的选择性较低,在100-400 ℃,随温度提高呈现先增后减的变化规律,在250 ℃时到达峰值7.24%,而在0.266 kPa压力条件下,N2O的选择性保持较低水平,说明低压明显抑制了无氧工况下N2O的生成途径。
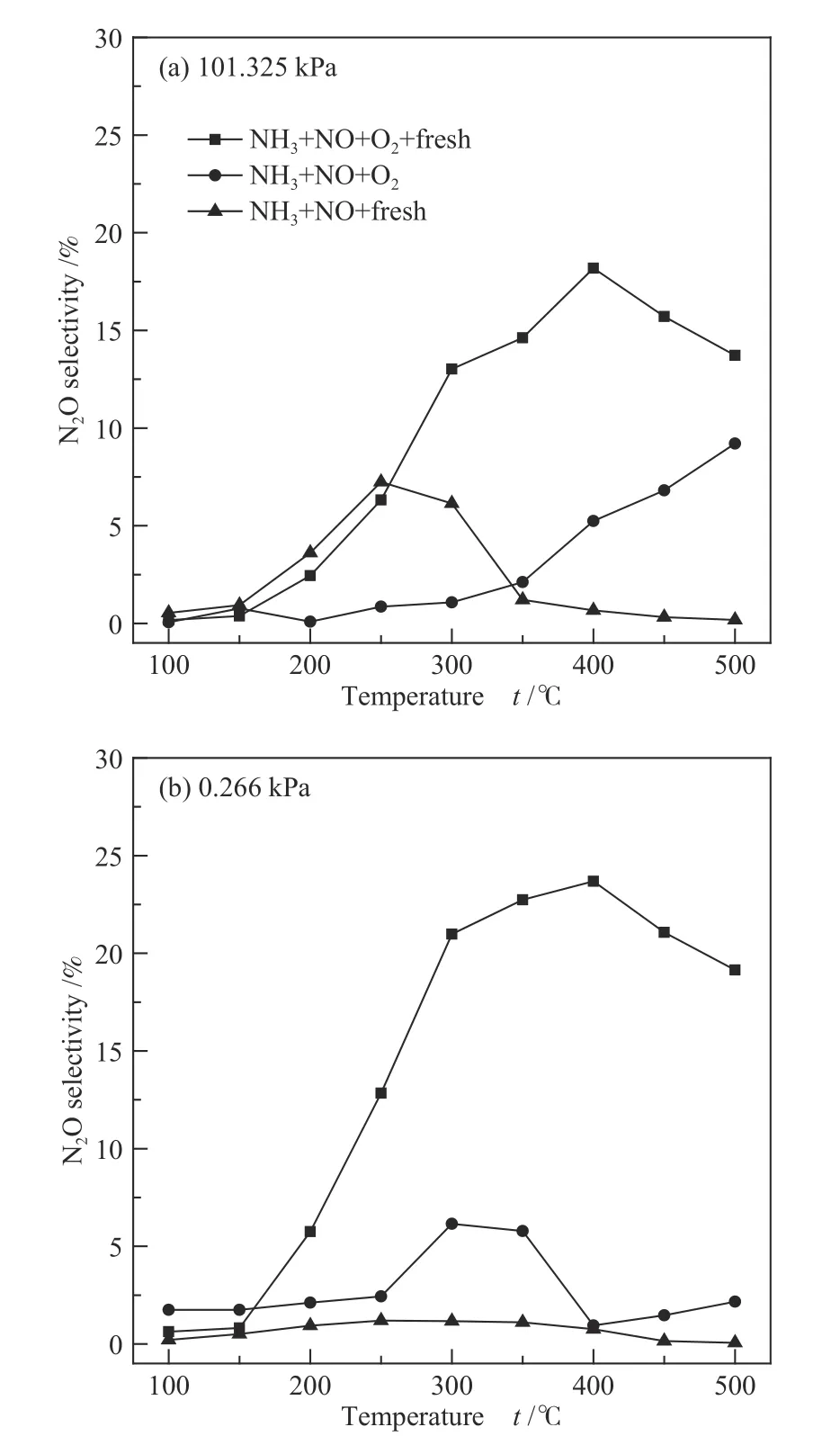
图3 不同压力下N2O选择性随温度的变化Figure 3 Trend diagram of N2O selectivity with temperature under different pressures
基于以上分析,fresh催化剂和氧气同时存在以及低压条件下N2O的选择性明显高于其他两种工况,其峰值在20%-25%,而且低压促进了N2O的生成。由此可见,fresh催化剂与氧气均是N2O在高温段(250-500 ℃)大量形成的必要条件。
2.3 不同压力对N2O生成途径影响
图4和图5分别展示了三种工况以及不同压力下NOx和NH3转换率随温度的变化。根据前人文献[9,19,37,38],N2O主要来源可分为非选择性氧化还原(NSCR)以及NH3在O2中的氧化(NSNO)等途径,其中,涉及的生成路径如下反应(R1)-(R6):
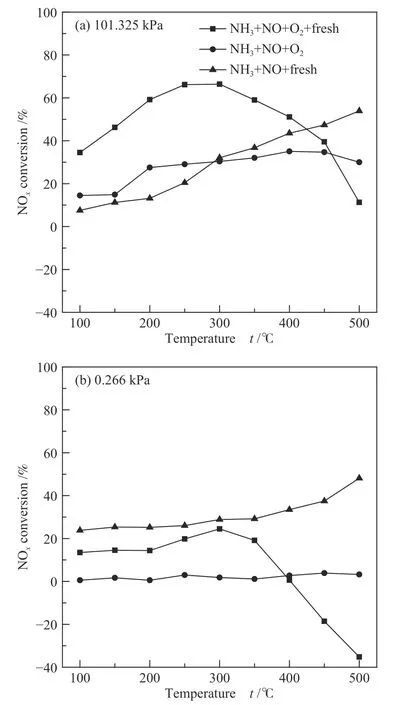
图4 不同压力下NOx转换率随温度的变化Figure 4 Trend diagram of NOx conversion rates with temperature under different pressures
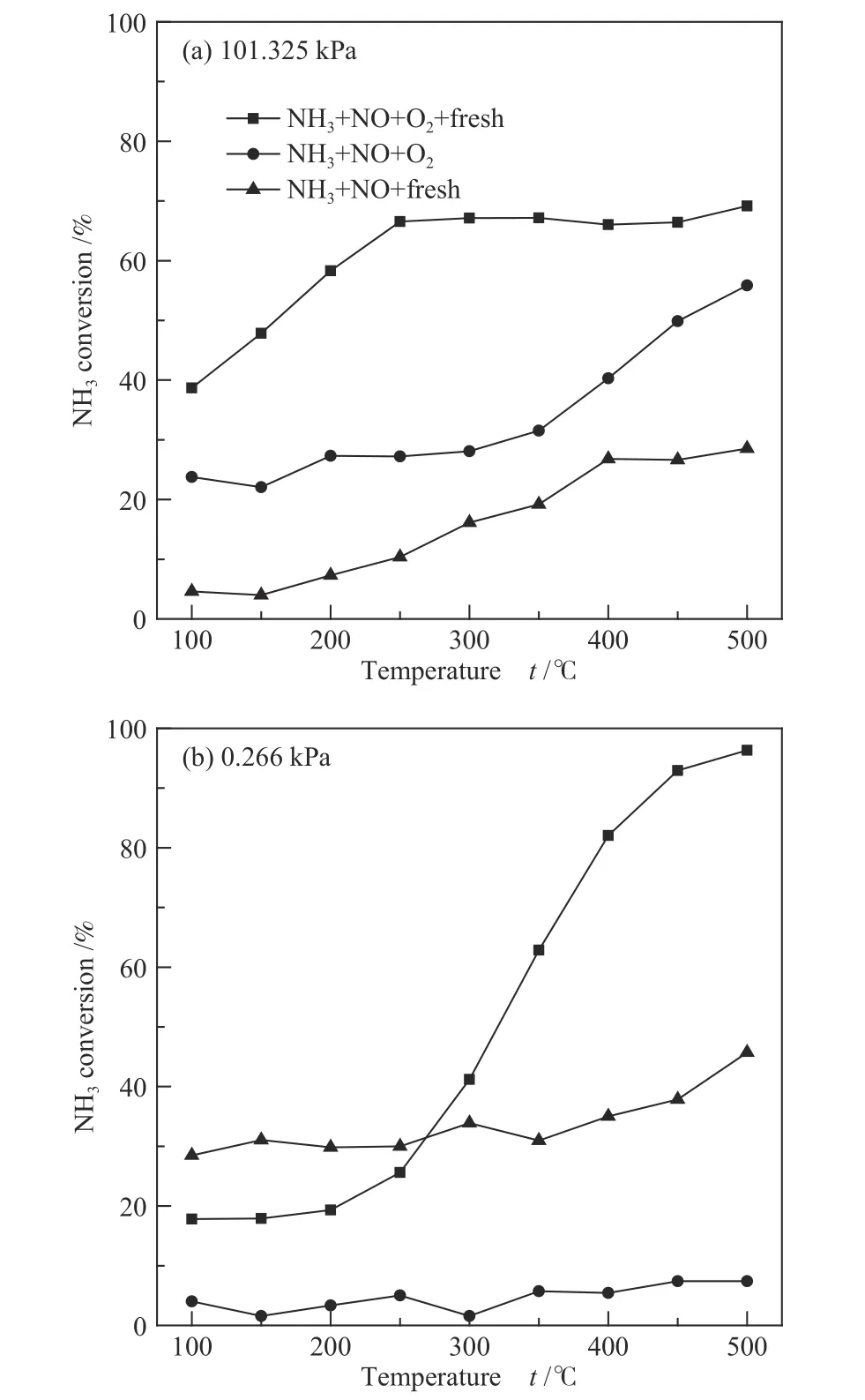
图5 不同压力下NH3转换率随温度的变化Figure 5 The trend diagram of NH3 conversion rates with temperature under different pressures

本工作在三种工况条件下进行了N2O生成途径分析,气体组成对应的可能的反应列于表1。针对不同工况条件下所涉及N2O生成路径不同,从三个方面分析压力对生成路径的影响规律。
前人普遍认为[39,40],标况下NSCR(R1)反应和NSNO(R2)反应是导致N2O大量生成的主要途径,而N2O中O的来源则与O2和催化剂密切相关。研究表明[19],N2O在低温和高温阶段形成的机制不同,根据温度的不同可以将N2O的生成途径分为低温机制和高温机制:第一,低温机制:主要是通过E-R和L-H机制的非选择性催化反应生成N2O,这与N2的生成机制相似,并与之竞争;第二,高温机制:主要是通过吸附态NH3的氧化反应,此时催化剂表面吸附态NH3相较于气相分子更容易被氧化而生成N2O。Suarez等[41]研究表明,在氨氧化条件下,过渡金属氧化物上存在的中间物质NH和NHO可以相互反应形成N2O。
根据图4(a)和图5(a)可知,100-250 ℃,NOx和NH3两者转换率持续升高,且曲线上升斜率保持高度一致性,说明NOx和NH3同比例被消耗,基于前人对SCR和NSCR机制[39,40]的阐述,结合图3(a)标准工况下N2O曲线规律分析可知,在100-250 ℃,R1占据N2O生成量的主导地位,在催化剂表面NSCR产物N2O以及SCR产物N2的生成反应同时进行。250-400 ℃,NOx转换率保持下降趋势,而NH3先保持平稳后略有上升,但是N2O的转化率随温度不断升高并达到最大值,证明此过程中N2O主要来R2;400-500 ℃,N2O的转换率呈现下降趋势,而NH3转化率升高,NOx转换率降低,说明吸附态NH3在高温下被氧化为NOx产物,NOx与N2O生成途径产生竞争关系。由图4(b)和图5(b)可以发现,0.266 kPa压力条件下N2O的选择性以及NOx和NH3转换率与101.325 kPa呈现相似的规律。相比常压条件,低压促进了R2路径生成更多的N2O,同时降低了SCR反应的程度。在400-500 ℃,低压加剧吸附态NH3氧化生成NOx反应,甚至NOx转换率呈现为负增长。
在无催化剂工况下,对比图3(a)和图5(a)发现,N2O的选择性与NH3转化率在350 ℃时发生明显提升,并且斜率保持一致,表明在此过程中N2O主要来源于反应R3,而且随着温度的升高,反应R3占据N2O生成途径的主导地位。同时NOx的转化率保持缓慢增长的趋势,NOx的消耗路径主要与NH3发生氧化还原反应。在0.266 kPa压力下,NH3和NOx的转化率均降至极低水平,此时N2O的生成量极少,证明低压减弱了反应R3,N2O的选择性明显低于101.325 kPa。
在无氧条件下,由图4(a)和图5(b)可知,NOx和NH3转化率保持了高度一致性,此时R4是N2O的主要来源,而NOx歧化反应R5和NOx分解反应R6生成途径对于N2O生成量的贡献较弱,随着温度的升高,N2O的竞争性产物N2的生成途径逐渐占据消耗NOx和NH3的主要因素。对比常压条件,低压提高了NOx和NH3的转换率,相反,N2O的选择性较低,这可能由于低压降低了R4反应。
3 结 论
非选择性催化反应(NSCR)和吸附态NH3氧化(NSNO)是3Mn10Fe/Ni催化剂上N2O形成的主要途径。
占据生成N2O主导地位的形成机制在低温和高温下有所不同。在100-250 ℃,N2O的主要生成来源于E-R和L-H机制的NSCR途径,且与N2生成处于竞争关系;在250-400 ℃,N2O的生成主要来源于NSCR和NSNO途径的共同作用,随温度的升高,后者逐渐占据主导地位;400-500 ℃,N2O主要来源于NSNO途径,并与NH3氧化产物NOx处于竞争关系,随温度上升前者所占分支比逐渐下降。
低压(0.266 kPa)降低了NOx和NH3转化率,同时降低了fresh催化脱硝性能。但却促进了通过NSNO反应在高温区生成N2O的反应途径,使得N2O选择性增幅达到5.5%。此外,低压提高了fresh催化剂表面NO歧化和分解反应在N2O生成途径体系中的比重,但降低了高温段气相NH3氧化生成N2O的选择性。
