三七药酒对大鼠佐剂性类风湿关节炎的药效评价
2021-07-21陈玲芳邵敬宝印晓红沈炜普俊勇姚建标陈烨张利竣石楠石森林
陈玲芳 邵敬宝 印晓红 沈炜 普俊勇 姚建标 陈烨 张利竣 石楠 石森林
三七药酒是云南希陶绿色药业股份有限公司生产(国药准字Z53021182),由三七、红花、大血藤、乳香、没药、醋延胡索、醋香附、四块瓦和苏木等药物组成,具有舒筋活络、散瘀镇痛、祛风除湿、强筋壮骨等功效,临床用于治疗跌打损伤,风湿骨痛,四肢麻木等症。本研究选择佐剂性类风湿关节炎大鼠模型综合评价三七药酒治疗类风湿性关节炎的药效作用,为三七药酒治疗类风湿性关节炎(RA)的临床研究提供药效学实验基础。
1 材料与方法
1.1 实验动物 Wistar雄性大鼠60只,体质量(180±20)g,浙江中医药大学动物实验中心代购,动物生产许可证号:SYXK(浙)2013-0184。饲养环境:12 h光照,12 h黑暗,温度20~22℃,湿度45%~65%。
1.2 药物与试剂 基酒(批号20170305)由浙江康恩贝制药股份有限公司提供,三七药酒(批号171018)由云南希陶绿色药业股份有限公司提供,雷公藤多苷片(批号1607102B)购自浙江得恩德制药有限公司,完全弗氏佐剂(10 mg/ml BCG)购自sigma公司。
1.3 仪器 足趾容积测量仪(山东医学科学院设备站),自动染色机(Leica),RM2245切片机(Leica)。
1.4 造模与给药 60只大鼠适应性喂养3 d后,称重,剔除体质量>220 g或<160 g的大鼠,剩余的按照随机数字法分为七组,即空白组、模型组、基酒组、雷公藤多苷组、三七药酒低剂量组、三七药酒中剂量组、三七药酒高剂量组,每组各8只。空白组大鼠右后足底皮内注射0.1 ml氯化钠注射液,其余大鼠右后足底皮内注射0.1 ml完全弗氏佐剂,注射后用手指按压针孔20 s[1]。于造模当天开始,分组灌胃给药,记录为D1,给药期间正常饮食。空白组、模型组灌胃纯化水,基酒组灌胃基酒,雷公藤多苷组灌胃雷公藤多苷混悬液(1.5 mg/kg),三七药酒低剂量组灌胃基酒稀释的三七药酒(3 ml/kg),三七药酒中剂量组灌胃基酒稀释的三七药酒(6 ml/kg),三七药酒高剂量组灌胃三七药酒原液(9 ml/kg)。灌胃剂量按大鼠体重0.4 ml/100 g,1次/d。
1.5 观察指标 (1)大鼠体重:分别于造模前1天(D0)、造模后每2天的给药前、末次给药后(D21)以及禁食不禁水>12 h后的D22进行称重。(2)大鼠足跖容积测定:采用大鼠足跖容积测量仪,测量深度以踝关节毛际线处为标准,分别于造模D1的造模前、之后每两天的给药前进行,D21末次给药前为最后一次测定。(3)大鼠痛阈测定:分别于造模D1、以后每2天的给药前,D21末次给药前为最后一次,取大鼠右后足趾中部,采用大鼠电子压痛测量仪进行足趾压痛值测定。(4)大鼠足踝周长测定:于造模第13 d开始,之后每两天给药前,D21末次给药前为最后一次,用软尺测定大鼠右后足踝最肿部位的周长。(5)大鼠踝关节HE染色:大鼠处死后,截取患侧踝关节,除去足部皮肤,以及多余筋膜和肌肉,浸泡于10% EDTA液中脱钙,行HE染色,电镜下观察踝关节的病理变化。
1.6 统计学方法 采用SPASS 17.2统计软件。各个检测指标的样本均数以()表示,采用多个样本均数的方差分析,进行q检验。以P<0.05为差异有统计学意义。
2 结果
2.1 各组大鼠体质量比较 见表1。
表1 各组大鼠体质量比较[g,()]
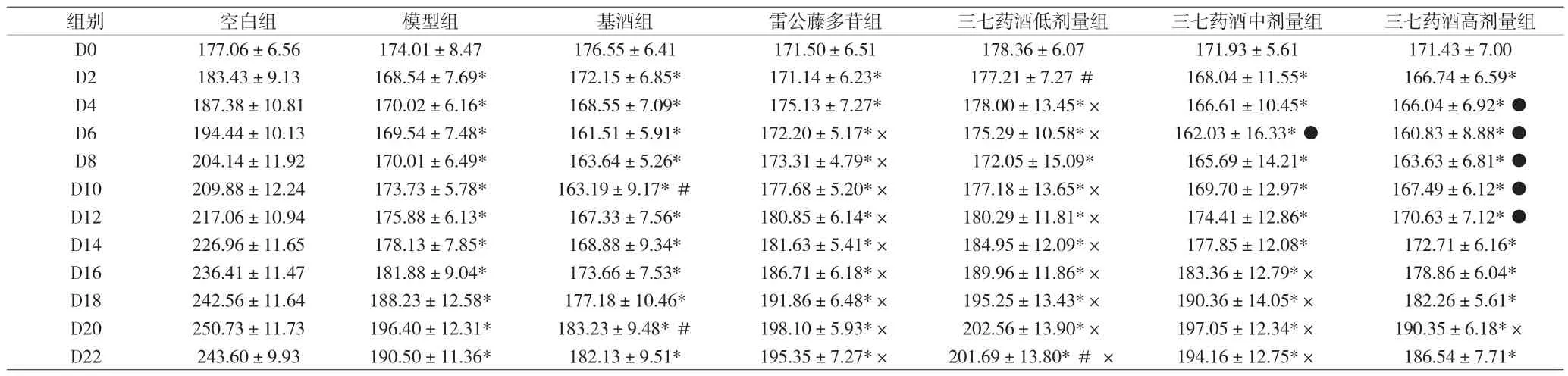
表1 各组大鼠体质量比较[g,()]
注:与空白组比较,*P<0.05;与模型组比较,#P<0.05;与基酒组比较,×P<0.05;与雷公藤多苷组比较,●P<0.05
组别 空白组 模型组 基酒组 雷公藤多苷组 三七药酒低剂量组 三七药酒中剂量组 三七药酒高剂量组D0 177.06±6.56 174.01±8.47 176.55±6.41 171.50±6.51 178.36±6.07 171.93±5.61 171.43±7.00 D2 183.43±9.13 168.54±7.69* 172.15±6.85* 171.14±6.23* 177.21±7.27 # 168.04±11.55* 166.74±6.59*D4 187.38±10.81 170.02±6.16* 168.55±7.09* 175.13±7.27* 178.00±13.45*× 166.61±10.45* 166.04±6.92* ●D6 194.44±10.13 169.54±7.48* 161.51±5.91* 172.20±5.17*× 175.29±10.58*× 162.03±16.33*● 160.83±8.88*●D8 204.14±11.92 170.01±6.49* 163.64±5.26* 173.31±4.79*× 172.05±15.09* 165.69±14.21* 163.63±6.81* ●D10 209.88±12.24 173.73±5.78* 163.19±9.17*# 177.68±5.20*× 177.18±13.65*× 169.70±12.97* 167.49±6.12*●D12 217.06±10.94 175.88±6.13* 167.33±7.56* 180.85±6.14*× 180.29±11.81*× 174.41±12.86* 170.63±7.12*●D14 226.96±11.65 178.13±7.85* 168.88±9.34* 181.63±5.41*× 184.95±12.09*× 177.85±12.08* 172.71±6.16*D16 236.41±11.47 181.88±9.04* 173.66±7.53* 186.71±6.18*× 189.96±11.86*× 183.36±12.79*× 178.86±6.04*D18 242.56±11.64 188.23±12.58* 177.18±10.46* 191.86±6.48*× 195.25±13.43*× 190.36±14.05*× 182.26±5.61*D20 250.73±11.73 196.40±12.31* 183.23±9.48*# 198.10±5.93*× 202.56±13.90*× 197.05±12.34*× 190.35±6.18*×D22 243.60±9.93 190.50±11.36* 182.13±9.51* 195.35±7.27*× 201.69±13.80*# × 194.16±12.75*× 186.54±7.71*
2.2 各组大鼠足跖容积比较 见表2。
表2 各组大鼠足跖容积比较[ml,()]
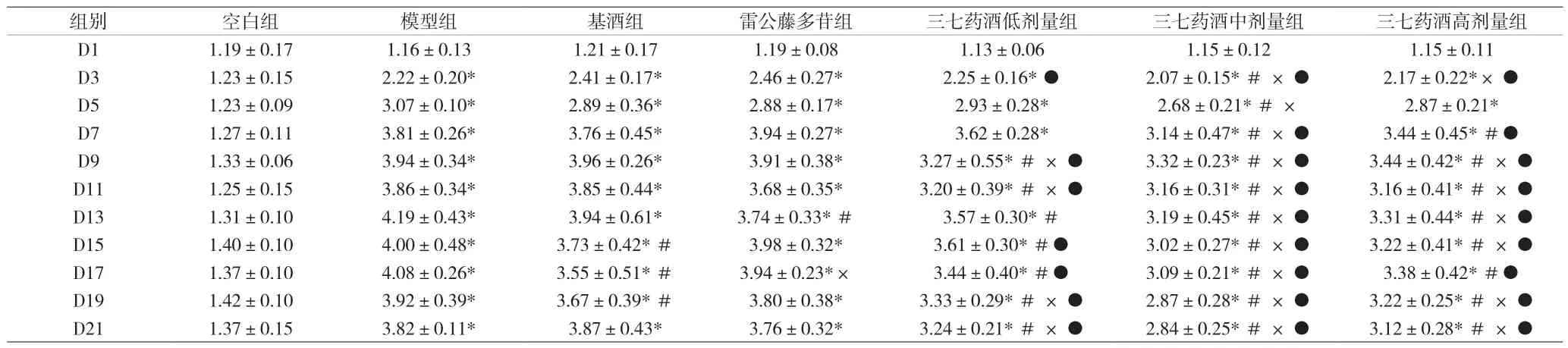
表2 各组大鼠足跖容积比较[ml,()]
注:与空白组比较,*P<0.05;与模型组比较,#P<0.05;与基酒组比较,×P<0.05;与雷公藤多苷组比较,●P<0.05
组别 空白组 模型组 基酒组 雷公藤多苷组 三七药酒低剂量组 三七药酒中剂量组 三七药酒高剂量组D1 1.19±0.17 1.16±0.13 1.21±0.17 1.19±0.08 1.13±0.06 1.15±0.12 1.15±0.11 D3 1.23±0.15 2.22±0.20* 2.41±0.17* 2.46±0.27* 2.25±0.16*● 2.07±0.15*# × ● 2.17±0.22*× ●D5 1.23±0.09 3.07±0.10* 2.89±0.36* 2.88±0.17* 2.93±0.28* 2.68±0.21* # × 2.87±0.21*D7 1.27±0.11 3.81±0.26* 3.76±0.45* 3.94±0.27* 3.62±0.28* 3.14±0.47* # × ● 3.44±0.45* #●D9 1.33±0.06 3.94±0.34* 3.96±0.26* 3.91±0.38* 3.27±0.55*#×● 3.32±0.23*#×● 3.44±0.42*#×●D11 1.25±0.15 3.86±0.34* 3.85±0.44* 3.68±0.35* 3.20±0.39*#×● 3.16±0.31*#×● 3.16±0.41*#×●D13 1.31±0.10 4.19±0.43* 3.94±0.61* 3.74±0.33*# 3.57±0.30*# 3.19±0.45*#×● 3.31±0.44*#×●D15 1.40±0.10 4.00±0.48* 3.73±0.42*# 3.98±0.32* 3.61±0.30*#● 3.02±0.27*#×● 3.22±0.41*#×●D17 1.37±0.10 4.08±0.26* 3.55±0.51*# 3.94±0.23*× 3.44±0.40*#● 3.09±0.21*# × ● 3.38±0.42*#●D19 1.42±0.10 3.92±0.39* 3.67±0.39*# 3.80±0.38* 3.33±0.29*#×● 2.87±0.28*#×● 3.22±0.25*#×●D21 1.37±0.15 3.82±0.11* 3.87±0.43* 3.76±0.32* 3.24±0.21*#×● 2.84±0.25*#×● 3.12±0.28*#×●
2.3 各组大鼠痛阈值变化情况比较 见表3。
表3 各组大鼠痛阈值变化情况比较[g,()]
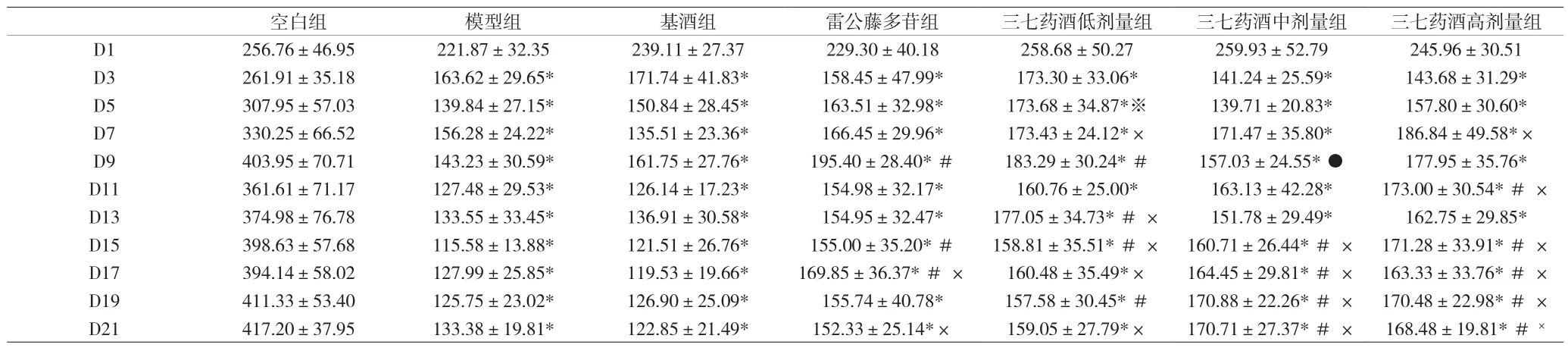
表3 各组大鼠痛阈值变化情况比较[g,()]
注:表示与空白组比较,差异有统计学意义 *P<0.05;表示与模型组比较,差异有统计学意义#P<0.05;表示与基酒组比较,差异有统计学意义 ×P<0.05;与雷公藤多苷组比较差异有统计学意义 ● P<0.05
空白组 模型组 基酒组 雷公藤多苷组 三七药酒低剂量组 三七药酒中剂量组 三七药酒高剂量组D1 256.76±46.95 221.87±32.35 239.11±27.37 229.30±40.18 258.68±50.27 259.93±52.79 245.96±30.51 D3 261.91±35.18 163.62±29.65* 171.74±41.83* 158.45±47.99* 173.30±33.06* 141.24±25.59* 143.68±31.29*D5 307.95±57.03 139.84±27.15* 150.84±28.45* 163.51±32.98* 173.68±34.87*※ 139.71±20.83* 157.80±30.60*D7 330.25±66.52 156.28±24.22* 135.51±23.36* 166.45±29.96* 173.43±24.12*× 171.47±35.80* 186.84±49.58*×D9 403.95±70.71 143.23±30.59* 161.75±27.76* 195.40±28.40*# 183.29±30.24*# 157.03±24.55*● 177.95±35.76*D11 361.61±71.17 127.48±29.53* 126.14±17.23* 154.98±32.17* 160.76±25.00* 163.13±42.28* 173.00±30.54* # ×D13 374.98±76.78 133.55±33.45* 136.91±30.58* 154.95±32.47* 177.05±34.73* # × 151.78±29.49* 162.75±29.85*D15 398.63±57.68 115.58±13.88* 121.51±26.76* 155.00±35.20*# 158.81±35.51*#× 160.71±26.44*#× 171.28±33.91*#×D17 394.14±58.02 127.99±25.85* 119.53±19.66* 169.85±36.37*# × 160.48±35.49*× 164.45±29.81*# × 163.33±33.76*# ×D19 411.33±53.40 125.75±23.02* 126.90±25.09* 155.74±40.78* 157.58±30.45*# 170.88±22.26*# × 170.48±22.98*# ×D21 417.20±37.95 133.38±19.81* 122.85±21.49* 152.33±25.14*× 159.05±27.79*× 170.71±27.37*# × 168.48±19.81*# ×
2.4 各组大鼠裸关节周长比较 见表4。
表4 各组大鼠裸关节周长比较[cm,()]
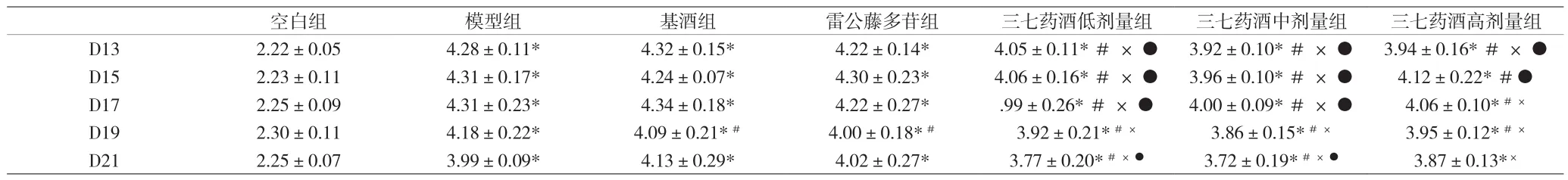
表4 各组大鼠裸关节周长比较[cm,()]
注:与空白组比较,*P<0.05;与模型组比较,#P<0.05;与基酒组比较,×P<0.05;与雷公藤多苷组比较差异有统计学意义 ●P<0.05
空白组 模型组 基酒组 雷公藤多苷组 三七药酒低剂量组 三七药酒中剂量组 三七药酒高剂量组D13 2.22±0.05 4.28±0.11* 4.32±0.15* 4.22±0.14* 4.05±0.11*#×● 3.92±0.10*#×● 3.94±0.16*#×●D15 2.23±0.11 4.31±0.17* 4.24±0.07* 4.30±0.23* 4.06±0.16*#×● 3.96±0.10*#×● 4.12±0.22*#●D17 2.25±0.09 4.31±0.23* 4.34±0.18* 4.22±0.27* .99±0.26*#×● 4.00±0.09*#×● 4.06±0.10*#×D19 2.30±0.11 4.18±0.22* 4.09±0.21*# 4.00±0.18*# 3.92±0.21*#× 3.86±0.15*#× 3.95±0.12*#×D21 2.25±0.07 3.99±0.09* 4.13±0.29* 4.02±0.27* 3.77±0.20*#×● 3.72±0.19*#×● 3.87±0.13*×
2.5 各组大鼠踝关节病理变化 空白组大鼠踝关节组织学结构正常,胞浆红染,细胞形态正常;模型组大鼠关节滑模增生,有大量炎性细胞侵润,胞浆嗜酸性增强;基酒组大鼠关节滑模增生,有大量炎性细胞侵润,胞浆嗜酸性增强,可见较多免疫沉淀物;雷公藤多苷组关节滑模增生较模型组减轻,可见炎性细胞侵润;三七药酒低剂量组滑膜增生与雷公藤多苷组相当,偶见炎症细胞侵润;三七药酒中剂量组滑膜增生与雷公藤多苷组相当,偶见炎症细胞侵润;三七药酒高剂量组滑膜增生较三七药酒中剂量组严重,炎症细胞侵润较三七药酒中剂量和低剂量组严重。病理改变见图1。
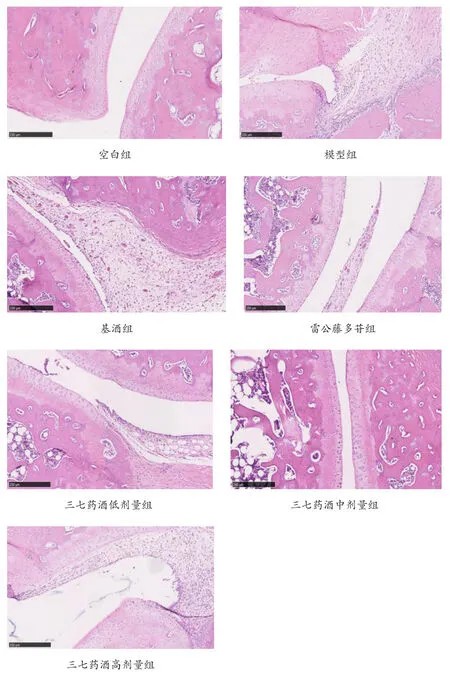
图1 各组大鼠踝关节HE染色(×100)
3 讨论
类风湿性关节炎(RA)是一种自身免疫性疾病,其发病原因及机制十分复杂。一般认为,RA是遗传易感者在某种特殊环境因素的激发下,启动由自身反应性T 细胞介导的自身免疫反应,进而引起一系列炎症、免疫反应和关节滑膜的增生,最终导致滑膜炎、关节破坏和全身器官受损[2-4]。
AA模型是由Pearson在20世纪50年代创立的一种免疫性关节炎动物模型。AA模型的发病特点、关节疼痛、肿胀和病理改变、骨质破坏和滑膜增生等与临床上患者RA病理学改变相似,经过多次改良,已成为目前筛选研究治疗RA药物较为理想的动物模型之一[5]。AA模型的发病原理主要是分子模拟理论。AA免疫是T细胞介导的慢性全身性炎症反应,其中辅助性T细胞(Th)中T细胞亚群之间的平衡紊乱是AA大鼠免疫功能异常的重要特征之一。
三七总皂苷具有活血化淤的作用。姜辉等[6]研究发现,三七总皂苷对AA大鼠具有一定的保护作用,其机制可能与调节细胞因子的产生有关。顾超兰等[7]研究发现,红花的有效成分红花黄色素能显著缓解佐剂型关节炎大鼠的关节炎症,其机制与下调炎症因子IL-1β及TNF-α的表达有关。付钰等[8]研究发现,中药大血藤可抑制AA大鼠滑膜细胞分泌MMP-2、MMP-9,减轻其参与或介导的对滑膜组织造成的损害,控制滑膜炎症的发生。李小敏等[9]研究苏木醇提取物对类风湿性关节炎(RA)的治疗作用,发现苏木醇提取物可以减轻佐剂关节炎大鼠的足趾肿胀。本研究进一步证实,三七药酒具有良好的消肿、减痛和促进踝关节黏膜修复的药效作用,其作用机制可能是通过抑制炎症细胞的分泌、减少炎性细胞浸润而发挥镇痛、抗炎作用,通过抑制关节滑膜增生来保护关节滑膜组织,但三七药酒高剂量组的病理结果尚不理想,故需进一步研究探讨。
