输尿管软镜联合吸引鞘钬激光碎石术治疗6例直径2 cm以上肾结石报告
2021-05-07施靖宇谢国海张东旭刘万樟
施靖宇,方 立,谢国海,张东旭,刘万樟,黄 挺,程 跃
(1.宁波大学医学院外科学,浙江宁波 315211;2.宁波市第一医院泌尿外科,浙江宁波 315010)
目前,直径2 cm以上肾结石的治疗仍首选经皮肾镜取石术(percutaneous nephrolithotomy,PCNL)[1]。与PCNL相比,输尿管软镜碎石术(flexible ureteroscopy lithotripsy,FURL)虽然有肾脏损伤小、出血风险低、住院时间短等优点,但清石效率低[2-3],有学者尝试使用输尿管软镜治疗>2 cm的肾结石取得了一定疗效,但存在手术时间长、二次手术率高的缺点[4-5]。我们自行设计的带有负压吸引通道的一次性输尿管导引鞘Ⅱ型(吸引型鞘,专利号:ZL201420605063.5,海盐康源医疗器械有限公司)理论上可以增加灌注液流速,平衡肾盂内压,同时将碎石直接吸出体外,提高碎石效率。2019年1~3月,我们通过输尿管软镜联合吸引鞘“摩西”钬激光碎石术治疗>2 cm的肾结石患者,现将结果报告如下。
1 资料与方法
1.1 一般资料本研究经宁波市第一医院医学伦理委员会审核批准。本组共纳入具有完整随访资料的6例患者,其中男性4例,女性2例;年龄32~75岁,平均(50.8±14.0)岁。经腹平片(kidney ureter bladder,KUB)及计算机断层扫描(computed tomography,CT)等影像学检查明确诊断,本研究中结石位于左侧2例、右侧4例,均未发现明显肾积水;结石最大直径3.0~8.2 cm,平均(4.4±1.8)cm,平均CT值(790±173)Hu。其中合并糖尿病2例,高血压3例,术前均维持血糖和血压平稳。所有患者术前均未留置双J管。
1.2 治疗方法本研究使用一次性输尿管导引鞘Ⅱ型(简称“吸引鞘”)进行输尿管软镜下钬激光碎石术。吸引鞘结构(图1A)主要包括:鞘管、密封塞、工作通道和负压吸引通道,密封塞连接工作通道可形成密封环境(图1B);工作通道侧壁设置负压调节孔(图1C),可手动调节负压吸引压力。

A:导引鞘全貌(①鞘管;②工作通道;③负压吸引通道;④密封塞);B:密封塞的使用(⑤密封塞连接工作通道);C:负压调节孔(⑥工作通道侧壁开孔)。
手术按常规进行,通常选用F12/14吸引鞘(女性使用长度为35.5 cm的吸引鞘,男性使用长度为45 cm的吸引鞘),连接密封塞与工作通道,置入F8柏立可拆卸式输尿管软镜和200 μm“摩西”钬激光光纤,依结石CT值及结石的大小,调节碎石单发能量0.5~1.0 J,碎石频率50~70 Hz,吸引压力0.04 MP,采用“雾霾化”碎石,将结石击碎至小于1 mm的碎片(图2),以利于随冲洗液吸出体外。

图2 通过吸引鞘吸引出的碎石粉末
术中密切关注灌注液回流情况,通过持握手指控制负压调节孔的大小手动调节吸引压力,也可辅助使用智能灌注泵:若灌注液回流好,术中视野清晰,可持续吸引;若肾盂黏膜塌陷,表明吸引力过大,可降低吸引压力;若灌注液回流不佳,肾盂扩张,则退出输尿管软镜以排出堵塞的碎石块或血块。
术后留置双J管1~2根。术后第1天复查KUB及CT,以后每2周复查KUB,直至KUB所见无结石残留或残留结石碎片<4 mm且无临床症状时,再次复查CT并拔除双J管,若仍有较大结石残留行二期输尿管软镜联合吸引鞘手术治疗。手术均由1名资深医师主刀。
2 结 果
本组6例患者均成功置鞘,4例一次性顺利清除结石,一期清石率为66.7%(4/6);2例术后复查提示>4 mm的阳性结石残留,行二期手术后,1例顺利清除残余结石(图3A~C),1例肾下盏结石因软镜无法触及而残留(图3D~F),二期清石率为83.3%(5/6)。手术时间(从进镜开始至双J管留置完成)为66~170 min,平均(129.9±30.9)min。术后出现Clavien Ⅱ并发症1例(表现为出现发热>38 ℃,升级抗生素治疗后好转),无Clavien Ⅲ及以上并发症。完成2个月随访后,1例肾下盏结石残留,余无结石残留,具体见表1。
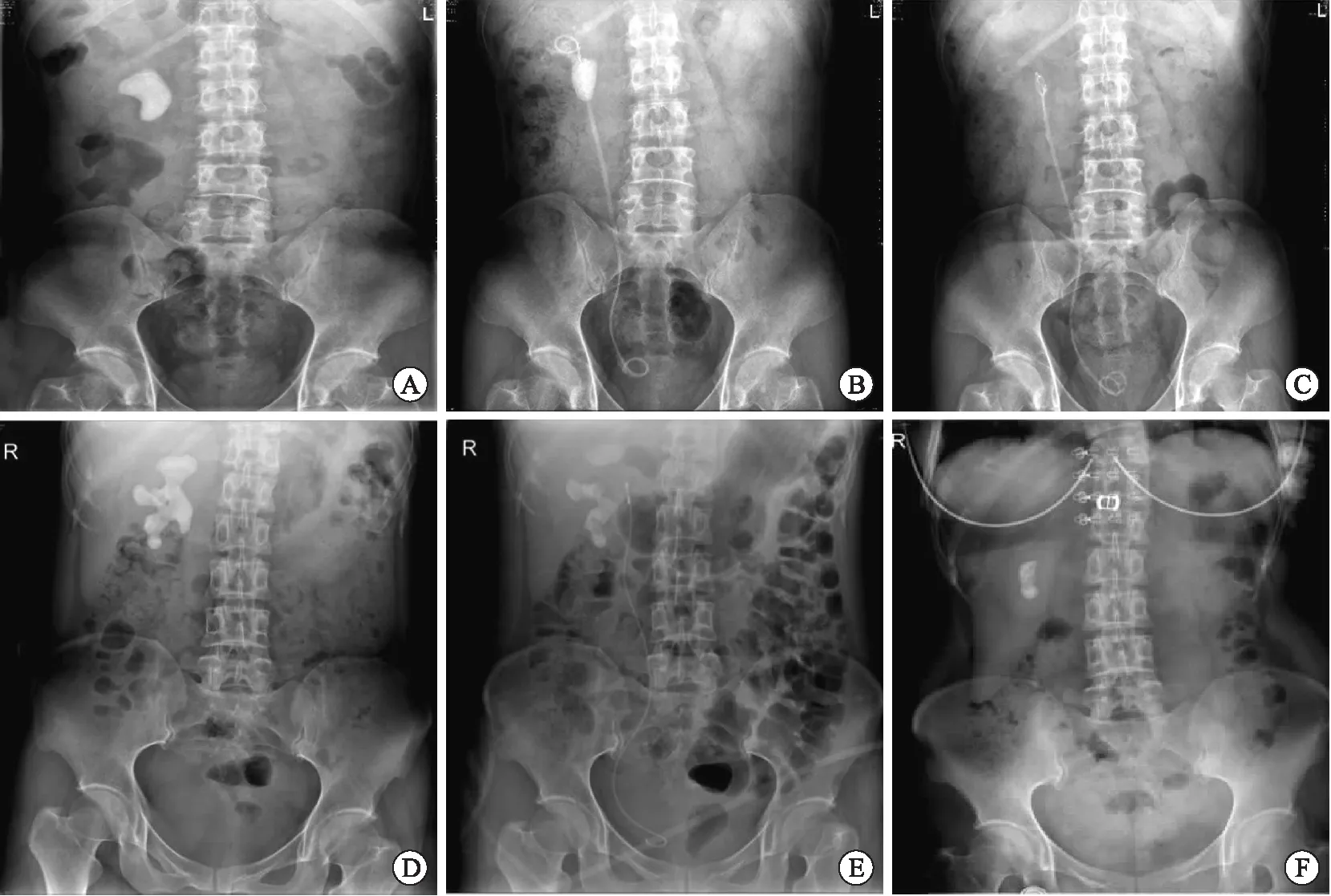
A:术前;B:1期碎石术后;C:2期碎石术后。A~C为患者3,D~F为患者5。
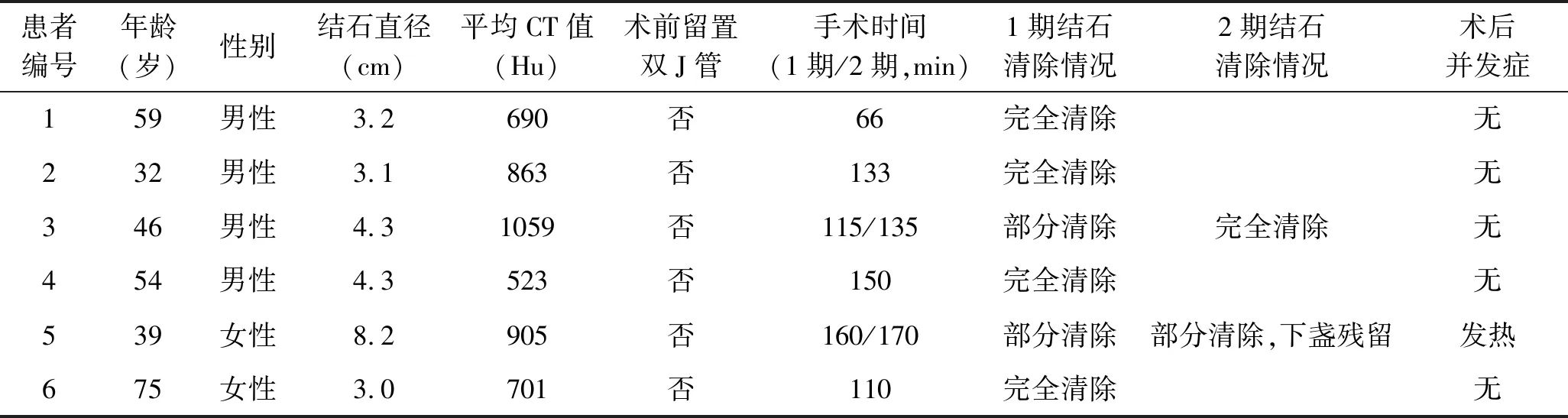
表1 6例患者临床资料
3 讨 论
输尿管软镜自20世纪60年代首次报道使用以来,经过设备的不断改进,FURL已经成为了治疗2 cm以下肾结石的主要方法[6]。最近有报道显示运用FURL治疗2~3 cm肾结石时尚能达到较理想的疗效[7],但在处理更大肾结石的过程中,需要多次手术才可以达到理想的结石清除率[4-5]。目前,FURL处理2 cm以上肾结石的主要缺陷为清石效率低,而在实际手术过程中则体现出以下问题:软镜的工作通道细小且狭长,自然状态下通道内流量有限,极易造成肾盂内压失衡;如果肾盂内压高,则可以直接引起肾裂伤出血,另外肾内高压将肾盂内碎石释放出的细菌和毒素压入血液中,会引起感染;如果肾盂内压低,较小的灌流就不能有效地将”雾霾化”碎石冲出体外,造成碎石堆积,导致手术视野模糊,增加手术时间,且钬激光产生的热量蓄积在狭小空间内,会造成局部热损伤。同样受限于工作通道的大小,FURL使用的光纤较细,钬激光碎石效率有限,在处理大结石时就需要花费更多的时间。本研究尝试运用“摩西”技术和自主研发的吸引鞘来解决上述问题。
在“粉末化碎石”理论的基础上[8],分析“摩西”钬激光碎石后的结石,我们定义了“雾霾化”碎石,即在术中将结石粉碎成<1 mm的碎片(粉碎程度较粉末化缩小1倍)。钬激光“摩西”技术能够更好地“雾霾化”碎石[9-10],在软镜碎石过程中采用“摩西”技术可加快“雾霾化”进程,甚至达到完全“雾霾化”碎石,更小的结石碎片将更易悬浮在灌注液中,利于碎石随灌注液排出。
泌尿系结石手术中,肾盂内压的控制尤为重要,我们认为PCNL术中传统的镜-鞘组合模式下,肾盂内压不仅与灌注压有关,还与镜鞘比密切相关[11]。FURL术中,肾盂内压也仅可通过软镜和鞘之间的间隙来控制。通过对现有输尿管镜和导引鞘组合的体外实验,我们发现软镜镜体的远近端粗细一致,区别于输尿管镜远端细近端粗的结构,使灌注液能够更顺畅地通过输尿管软镜和输尿管导引鞘之间的间隙回流,可以获得较小的肾盂内压[12]。由此我们提出了软镜手术镜鞘比(ratio of endoscope-sheath dia-meter,RESD)的概念,定义为输尿管软镜外径与输尿管导引鞘内径之比,并通过研究得出镜鞘比小于0.75的输尿管软镜和导引鞘组合在理论上是安全的[13]。而实际的手术操作中,受到液体性质、碎石等因素的影响,灌流情况并不能达到体外实验时那么理想,受限于器械的构造,通过镜鞘比所能降低肾盂内压的程度是有限的。在流出通道大小一定的情况下,增加吸引力可明显加快流速,提高灌流率。我们在2014年提出输尿管负压吸引鞘的概念并申请专利,吸引鞘与普通输尿管鞘相比,增加了负压吸引通道,在手术中体现出以下几点优势:①将被动灌流转变为主动吸引,可以平衡输尿管肾盂腔内压力,减少肾破裂、感染等并发症的发生;②悬浮在灌注液中的“雾霾化”碎片可减少流出阻力,与堆积的碎石一同吸引出体外,既提高手术视野清晰度又加快了碎石排出;③碎石所释放出的细菌及毒素和激光所产生的热量随灌流液快速吸引出体外,降低了感染风险,减少了黏膜热损伤的可能性;④负压可以吸附结石,避免钬激光在碎石过程中出现结石逃逸。本研究初步结果证明:“摩西”钬激光“雾霾化”碎石联合吸引鞘,能平衡肾盂内压,提高术中灌流效率,使手术视野清晰,提高了碎石效率,加快了结石排出的速度,缩短了手术时间,减少了并发症的发生。
有学者使用的自制输尿管软镜工作鞘带有肾盂内压实时监测功能[14]。本研究中采用的吸引鞘未配置测压设备,考虑原因如下:①增加测压组件将会占用本就不宽裕的清石空间;②测压受到的影响因素复杂,如置鞘的位置、灌流通道堵塞等,另外肾内解剖结构不同,各肾盏内局部压力都可能存在差异,因此局部测压意义并不大,而且过分依赖数字化控制的测压,若出现测压不准的情况,后果严重。本研究术中使用的吸引鞘可以手动控制吸引压力,平衡肾盂内压,根据我们的经验,术中肾盂内压的评估可以采用一种简单易行的观察法:若肾盂黏膜下血管纹理清晰,黏膜壁微塌陷或无明显扩张,则肾盂内压在安全范围内;反之,若血管纹理消失或肾盂扩张呈顶棚状,则要调整灌注及吸引的参数以控制肾盂内压。
结石负荷的增加对碎石时间影响很大,理论上结石直径增加1倍,体积增加约7倍,碎石时间也成3次方增加。指南中首选FURL治疗肾结石的上限是2 cm,本研究中结石平均直径达4.4 cm,直径增加了1倍多,而得益于“摩西”钬激光和吸引鞘的运用,平均手术时间仍能控制在2 h左右。虽然碎石和排石效率明显提高,但在处理4 cm以上和CT值>1 000 Hu的结石时,尚不能达到一期完全清石。
综上所述,输尿管软镜碎石术中结合“摩西”钬激光“雾霾化”碎石,可提高碎石效率,配合吸引鞘,可增加灌流率,平衡肾盂内压,有效改善术中视野清晰度,加快碎石主动排出速度,减少因肾内压增高而可能带来的并发症。因此,输尿管软镜联合吸引鞘“摩西”钬激光碎石术治疗2 cm以上单发为主的肾结石可行。而软镜弯曲度易造成肾下盏结石残留;因钬激光和吸引效率欠佳,4 cm以上和CT值>1 000 Hu的结石二次手术几率大,期望未来能出现更高效“雾霾化”的钬激光、灵活度更好的软镜设备和吸引效率更高的鞘。本研究为初步使用经验报告,不足之处在于为回顾性研究且样本量较小,该技术的疗效尚需大规模样本随访及随机对照研究结果进一步验证。
