微球状Bi3 O4 Cl/BiOI复合光催化剂的制备及性能
2021-04-10程良良肖逸帆丁婷婷肖新颜
程良良,肖逸帆,王 奕,丁婷婷,肖新颜
(华南理工大学 化学与化工学院,广东 广州510641)
随着科学技术和工业的迅猛发展,人类正面临着日益严重的环境污染和能源短缺问题。光催化技术可以利用丰富的太阳能,产生活性自由基来降解对环境有害的物质,实现能量的转化,引起了人们广泛的关注[1]。在各种光催化剂中,由于BiOX(X=Cl,Br和I)具有复杂的能带结构和独特的Sillén层状结构,引起众多研究者的兴趣[2]。Bi3O4Cl属于Sillén家族中的一员,[Bi3O4]穿插在两个Cl离子中间交替排列形成独特的晶体结构,这种结构可以提供足够的空间极化相关的原子和轨道,形成内建电场。形成的电场可以促进光生载流子的分离效率,提高光催化活性[3]。虽然Bi3O4Cl具有合适的能带结构(2.76 e V),可以被可见光激发,但它的可见光响应范围小、载流子的迁移速度慢,导致其应用受到极大的限制[4]。与其他具有合适能带结构的半导体光催化剂复合,构建复合光催化剂是一种能有效解决上述问题的方法之一。HUANG等[5]在水热条件下通过离子交换法制备了AgCl/Bi3O4Cl复合光催化剂,发现AgCl的引入可以增加比表面积,提高光生载流子的分离效率和光吸收能力。光催化活性评价结果表明,复合光催化剂对罗丹明B(Rh B)的降解率分别比单纯AgCl和Bi3O4Cl高2.2和2.4倍。MA等[6]通过一种简单的混合与煅烧法制备了Bi3O4Cl/g-C3N4复合光催化剂,发现Bi3O4Cl与g-C3N4复合可以增加催化剂的比表面积,发挥二者的协同效应,促进光生载流子的分离。
BiOI的禁带宽度较窄、可见光响应强,可以作为光敏剂改性其他带隙较宽的半导体(如,Zn-和BiOCl[9])。CHEN等[10]为了提高Bi2MoO6在可见光区域的光催化性能,以BiOI为光敏剂,制备了BiOI/Bi2MoO6复合光催化剂。CHAI等[11]为提高BiOCOOH可见光光催化能力,制备了BiOI/BiOCOOH复合物。利用BiOX电子和结构的相似性,选择两种Bi系半导体构建异质结光催化剂,是一种提高光催化性能的有效方法。CHEN等[12]利用BiOI和Bi2O2CO3结构的相似性,在常温下制备了BiOI/Bi2O2CO3复合光催化剂,该复合物降解RhB、甲基蓝(MB)以及它们的混合物,均表现出显著高于单纯BiOI和Bi2O2CO3的光催化性能。目前,很少有研究者利用Bi3O4Cl调控BiOI的结构,并对Bi3O4Cl/BiOI复合光催化剂降解有机污染物的机理进行研究。为此,本工作采用Bi3O4Cl调控BiOI的结构,构建Bi3O4Cl/BiOI复合光催化剂,对其结构性能进行系列表征。
1 实验部分
1.1 试剂与仪器
五水合硝酸铋,天津市科密欧化学试剂有限公司;乙二醇,江苏强盛功能化学股份有限公司;氯化铵,广州市贺隆贸易有限公司;无水乙醇,南京化学试剂股份有限公司;碘化钾,陕西圣瑞医药科技有限公司;甲基橙,天津市致远化学试剂有限公司。
分析天平,BS 110 S型,北京赛多利斯科学仪器有限公司;超声波清洗机,JP-040S型,深圳洁盟清洗设备有限公司;集热式恒温加热磁力搅拌器,DF-101S型,河南予华仪器有限公司;电热鼓风干燥箱,DHG-9070A型,上海一恒科学仪器有限公司;高速台式离心机,TGL-16G型,上海安亭科学仪器厂;箱式电阻炉控制箱,SX-2.5-10型,天津市泰斯特仪器有限公司;冷场发射扫描电子显微镜,SU8220型,日本日立高新技术公司;X射线衍射仪,D8 ADVANCE型,德国布鲁克公司;多功能光化学反应仪,SGY-1型,南京斯东柯电气设备有限公司;管型长弧氙灯,XG2100型,北京天脉恒辉光源电器有限公司;可见分光光度计,WFJ 2100型,上海尤尼柯仪器有限公司;紫外-可见漫反射光谱仪,U-3010型,日本日立高新技术公司;荧光分光光度计,F-4500型,日本日立高新技术公司。
1.2 实验方法
1.2.1 Bi3O4Cl纳米片的制备
将五水硝酸铋超声溶于装有20 m L乙二醇的烧杯1中,氯化铵超声溶于装有50 m L去离子水的烧杯2中。然后将烧杯1中的溶液逐滴加入烧杯2中。混合溶液继续搅拌10 min。随后混合溶液转入水热釜中,将水热釜置于鼓风干燥箱中,升温至160℃反应12 h,自然冷却至室温,离心分离后,分别用去离子水和无水乙醇各洗涤3次,再置于烘箱中干燥12 h,得到Bi3O4Cl的前驱体。再称取上述得到的0.5 g前驱体加入至不带盖的坩埚中,坩埚置于马弗炉中以5℃·min-1的升温速率升至500℃,维持该温度3 h,自然冷却至室温,得到Bi3O4Cl纳米片[6]。
1.2.2 Bi3O4Cl/BiOI复合光催化剂的制备
将五水硝酸铋超声溶于装有20 m L乙二醇的烧杯中形成均匀溶液,向其中加入0.02 g制备好的Bi3O4Cl,将混合溶液超声30 min并继续搅拌1 h,得到均一溶液A。将碘化钾溶于装有20 m L去离子水的烧杯中,形成溶液B。将B液逐滴加入至A液中,继续搅拌10 min,得到均匀的混合溶液。将混合溶液转移至水热釜中,置于鼓风干燥箱中,升温至120℃反应6 h,自然冷却至室温,离心分离后,分别用去离子水洗和无水乙醇各洗涤3次,置于烘箱中干燥12 h,得到Bi3O4Cl/BiOI复合物,记为10%Bi3O4Cl/BiOI(10%为Bi3O4Cl与BiOI的质量比)。以同样的方法制备Bi3O4Cl/BiOI质量分数5%、30%和50%,分别记为5%、30%和50%Bi3O4Cl/BiOI。
1.3 光催化性能评价
选取MO为目标降解物,对制备的催化剂的光催化性能进行评价。具体操作步骤:在带冷阱的圆柱形石英玻璃反应器中,将0.1 g催化剂超声分散于300 m L 10 mg·L-1的MO溶液中。在光照之前,磁力搅拌60 min进行暗处理,确保达到吸附平衡。然后,打开500 W氙灯进行光照,每隔15 min取4 m L反应液于离心管中,光照时间设定为90 min。整个降解过程中,通循环冷却水,以保持温度在20℃左右。取样后,用分光光度计测量MO溶液的吸光度,然后计算MO的降解率(η):
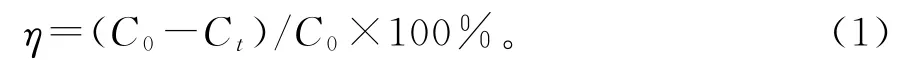
式中,C0和Ct分别为MO的初始浓度(t=0 min时)及照射时间t时的浓度。
2 结果与讨论
2.1 XRD分析
BiOI,Bi3O4Cl和Bi3O4Cl/BiOI复合物的XRD谱图见图1。如图1所示,制备的单纯Bi3O4Cl在24.05°,29.19°,29.70°,31.44°,31.70°,46.56°和51.50°可观察到衍射峰,分别对应于(411),(002),(020),(222)和晶面(PDF#36-0760)[13]。而BiOI符合四方晶相的峰型特征,其在29.65°,31.67°,45.37°,51.35°和55.15°可检测在衍射峰,分别对应于(102),(110),(200),(114)和(212)晶面(PDF#10-0445)[14]。对于复合光催化剂,10%Bi3O4Cl/BiOI的XRD谱图上未出现Bi3O4Cl的衍射峰,这可能是因为Bi3O4Cl的含量低,在复合催化剂分散性好。增加Bi3O4Cl的含量,当Bi3O4Cl与BiOI质量比增加到30%时,可以观察到在21.28°和22.18°处出现2个衍射峰,分别对应于Bi3O4Cl的(310)和(011)晶面。继续增加Bi3O4Cl的含量,上述的两个峰峰强度变得更强,此外在54.85°处出现一个新的衍射峰,对应于Bi3O4Cl的晶面。综上所述,XRD的结果表明Bi3O4Cl与BiOI成功复合。
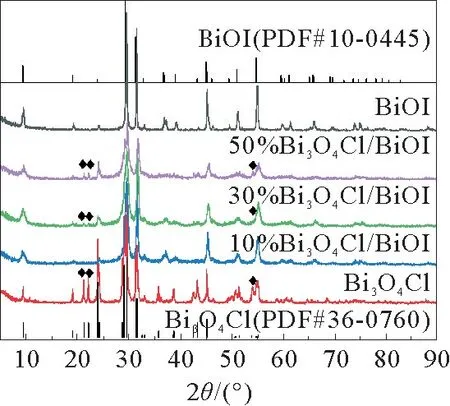
图1 BiOI,Bi3 O4 Cl和Bi3 O4 Cl/BiOI复合物的XRD谱图Fig.1 XRD patterns of BiOI,Bi3 O4 Cl and Bi3 O4 Cl/BiOI composites
2.2 形貌分析
图2为光催化剂的SEM照片。

图2 BiOI、Bi3 O4 Cl、10%Bi3 O4 Cl/BiOI复合物的SEM照片Fig.2 SEM images of pure BiOI,Bi3 O4 Cl,10%Bi3 O4 Cl/BiOI composite
从图2(a)和2(b)可看出,BiOI是由多个无序的微米片(宽度约1.2μm,长度约1.6μm)堆叠成不规则的块状。图2(c)表明Bi3O4Cl呈片状且带有细小颗粒。由图2(d)可观察到,10%Bi3O4Cl/BiOI由有序生长的片组装成微球(直径约3μm)。
图3和图4为光催化剂的形貌和晶格结构。

图3 10%Bi3 O4 Cl/BiOI复合物的TEM照片Fig.3 TEM images of 10%Bi3 O4 Cl/BiOI composite

图4 10%Bi3 O4 Cl/BiOI复合物的HRTEM照片Fig.4 HRTEM image of 10%Bi3 O4 Cl/BiOI composite
从图3(a)可观察到,10%Bi3O4Cl/BiOI呈微球状,这与SEM观察结果一致。从图4的10%Bi3O4Cl/BiOI HRTEM计算得到,宽度分别为0.194和0.308 nm的两条晶格条纹,分别对应于Bi3O4Cl的(222)晶面和BiOI的(102)晶面。TEM和HRTEM结果表明,成功制备了Bi3O4Cl/BiOI复合光催化剂。
2.3 UV-Vis DRS分析
图5是Bi3O4Cl,BiOI,5%Bi3O4Cl/BiOI,10%Bi3O4Cl/BiOI和30%Bi3O4Cl/BiOI样品的UVVis DRS分析。
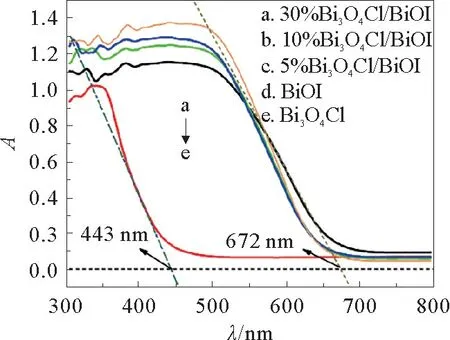
图5 BiOI,Bi3 O4 Cl和Bi3 O4 Cl/BiOI的紫外-可见漫反射光谱Fig.5 UV-Vis diffuse reflectance spectra of BiOI,Bi3 O4 Cl and Bi3 O4 Cl/BiOI
如图5所示,Bi3O4Cl吸收边界位于443 nm处,表现出较强的紫外吸收能力,BiOI的光吸收范围最宽,其吸收边界位于672 nm处,而Bi3O4Cl/BiOI复合物的吸收边界相对于BiOI有轻微的偏移。继续增加Bi3O4Cl的含量,光的吸收强度在400~500 nm之间有显著增强,表明Bi3O4Cl的引入促进了复合物的可见光吸收。由于Bi3O4Cl与BiOI都是直接半导体,可采用如下Kubelka-Munk(KM)公式[15]计算禁带宽度:
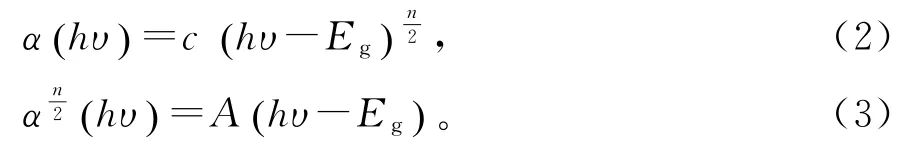
式(2)和式(3)中,A,α,υ,h和Eg分别表示比例常数、吸收因子、光频率、普朗克常数和禁带宽度。通过(αhυ)1/2对hυ作图,采用线性外插法进行估算,得到Bi3O4Cl和BiOI的禁带宽度分别为1.70和2.60 e V(如图6所示)。
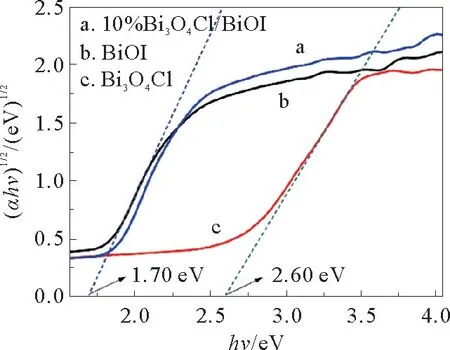
图6 BiOI与Bi3 O4 Cl的禁带宽度Fig.6 Band gaps of BiOI and Bi3 O4 Cl
2.4 光催化性能评价
光催化剂的光催化性能测试在模拟太阳光辐照下进行,结果见图7。
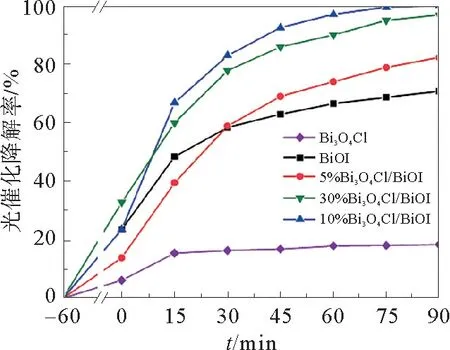
图7 BiOI,Bi3 O4 Cl和Bi3 O4 Cl/BiOI对MO的光催化降解率Fig.7 Photocatalytic degradation rate of MO solution(10 mg·L-1)with different photocatalysts
如图7所示,单纯Bi3O4Cl对目标污染物MO的降解率只达到13%,这可能是Bi3O4Cl较弱的可见光响应能力限制了其光催化性能。而单纯BiOI、5%Bi3O4Cl/BiOI,10%Bi3O4Cl/BiOI和30%Bi3O4Cl/BiOI对MO的降解率分别达到71%、82%、99.8%和97%。因此,在Bi3O4Cl/BiOI复合物中,合适的Bi3O4Cl含量为10%,此时,Bi3O4Cl能在复合物中较好分散,且Bi3O4Cl与BiOI能形成较大的接触面。
2.5 PL分析
光致发光光谱(PL)可用于研究催化剂的载流子分离效率。图8为不同样品的光致发光光谱图,激发波长为350 nm。
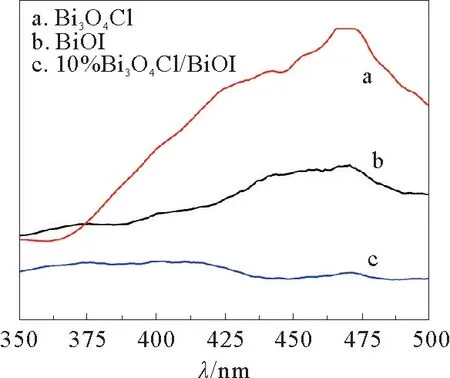
图8 BiOI,Bi3 O4 Cl和10%Bi3 O4 Cl/BiOI复合物的光致发光光谱图Fig.8 PL spectra of bare BiOI,Bi3 O4 Cl and 10%Bi3 O4 Cl/BiOI composite
与纯Bi3O4Cl和BiOI相比,10%Bi3O4Cl/BiOI复合物的发射峰强度显著降低,这表明Bi3O4Cl与BiOI的复合可以抑制光生载流子的复合,提高光生载流子的分离效率。
2.6 光催化机理分析
为了确定MO降解过程中发生作用的主要活性物种,进行了捕获试验。在含有10%Bi3O4Cl/BiOI样品的MO溶液中,加入对苯醌(BQ)、叔丁醇(TBA)和草酸(OA)捕获剂,分别捕获超氧基自由基(·)、羟基自由基(·OH)和空穴(h+)。加入捕获剂后的MO的降解效率如图9。
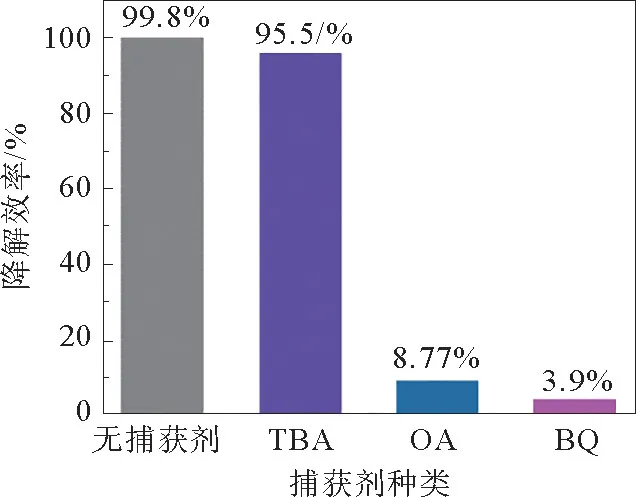
图9 10%Bi3 O4 Cl/BiOI降解MO活性自由基捕获实验Fig.9 Active radical capture experiments for MO degradation over 10%Bi3 O4 Cl/BiOI composite
由图9可以看到,BQ和OA的加入会显著降低催化剂的光催化性能,表明在模拟太阳光照下,10%Bi3O4Cl/BiOI样品降解MO的主要活性物质是·和h+。
除了活性自由基的种类,半导体的能带位置对光催化机理分析也非常重要。为此,对样品进行了莫特-肖特基测试,见图10。
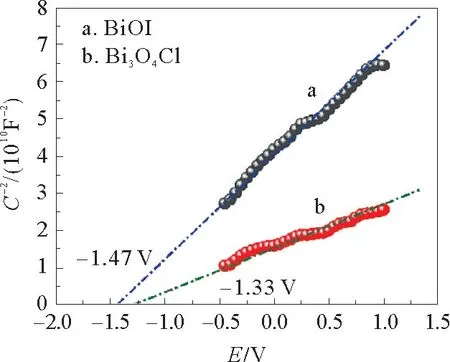
图10 Bi3 O4 Cl和BiOI莫特-肖特基测试Fig.10 M-S curves of Bi3 O4 Cl and BiOI samples
由图10可见,Bi3O4Cl和BiOI图线的斜率都为正,表明它们都为n型半导体。通过做切线并将切线外延至与X轴相交,可分别得到BiOI与Bi3O4Cl的平带电势为-1.47 V和-1.33 Vvs.Ag/AgCl(-1.27 V和-1.13 Vvs.NHE)。一般地,n型半导体的导带比平带电势更负0.10 V。因此,通过计算可得到BiOI与Bi3O4Cl的导带电势为-1.17 V和-1.03 Vvs.NHE。再根据前面得到的催化剂的禁带宽度,可利用公式(4)计算出半导体的价带电势:

BiOI与Bi3O4Cl的价带电势分别为0.53和1.57 V。
基于以上讨论提出了10%Bi3O4Cl/BiOI复合物降解MO的机理。莫特-肖特基实验结果见图11。由图11可见,BiOI的平带电势比Bi3O4Cl低,热力学上电子更容易从BiOI转移至Bi3O4Cl。如图11(a)所示,当Bi3O4Cl与BiOI接触时,为了实现费米能级的平衡,BiOI上的电子倾向于穿过界面向Bi3O4Cl转移,导致BiOI的费米能级向下移动,Bi3O4Cl的费米能级向上移动[16]。当费米能级达到平衡时,在费米能级附近,BiOI表面形成带正电,而在Bi3O4Cl表面形成带负电的电子层。最终在界面处形成一个内部电场,电场方向由BiOI指向Bi3O4Cl。在上述形成的空间电荷区,BiOI上的电子会受到带负电的Bi3O4Cl表面的排斥,造成BiOI上的电子电势能增加和BiOI能带边缘向上弯曲。同样地,Bi3O4Cl上的电子会受到带正电的BiOI表面的吸引,造成Bi3O4Cl上的电子电势能的减小和Bi3O4Cl能带边缘向下弯曲[17]。图11(c)和11(d)为两种可能的载流子迁移路径,Bi3O4Cl和BiOI都可以在模拟太阳光下被激发并产生光生载流子。通常情况下,II型和Z型异质结的构建都有利于光生载流子的分离和光催化性能的提高。如果Bi3O4Cl与BiOI电子转移方式与II型异质结机理相符(如图11(c)),电子就会从BiOI的导带流动到Bi3O4Cl的导带。但是,根据内电场的方向,电子不能按照这种方式流动,因为BiOI导带上的电子会受到带负电的Bi3O4Cl表面的电荷排斥,Bi3O4Cl价带上的空穴会受到带正电的BiOI表面的排斥。因此,Bi3O4Cl与BiOI更有可能形成Z型异质结机理(如图11),Bi3O4Cl导带上的电子流动到BiOI的价带并与这里的空穴复合,最终BiOI导带上会集聚还原能力更强的电子,Bi3O4Cl价带上集聚氧化性更强的空穴。在发生光反应时,BiOI导带上的光生电子(-1.17 Vvs.NHE)可以与催化剂表面吸附的氧气分子反应生成·,-0.33 Vvs.NHE)。同时,Bi3O4Cl价带上的空穴(1.57 Vvs.NHE)可以直接氧化MO,而不能与水分子发生反应生成·OH(OH-/·OH,2.38 Vvs.NHE),上述分析与自由基捕获实验的结果相符。
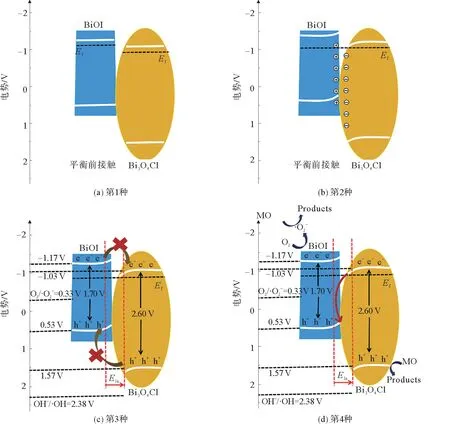
图11 10%Bi3 O4 Cl/BiOI复合物降解MO可能的Z型光催化机理Fig.11 Plausible Z-scheme photocatalytic mechanism of 10%Bi3 O4 Cl/BiOI composite for degrading MO
3 结 论
采用煅烧-水热法成功制备了不同比例的微球状Bi3O4Cl/BiOI复合光催化剂。选取MO为目标降解物,对光催化剂的光催化活性进行评价。结果表明:Bi3O4Cl/BiOI复合光催化剂的光催化性能明显优于单纯的Bi3O4Cl和BiOI,且10%Bi3O4Cl/BiOI对MO的降解率最高。Bi3O4Cl与BiOI复合后,显著提高了Bi3O4Cl在可见光区的响应能力,抑制了Bi3O4Cl和BiOI光生载流子的复合,使复合后光催化性能的大幅提高。
