川芎嗪联合mTOR抑制剂调控卵巢癌SKOV-3细胞增殖、侵袭迁移的实验研究
2021-03-18程春来吕晓君
程春来,车 元*,丁 雯,吕晓君
0 引言
卵巢癌是女性生殖器官常见的恶性肿瘤之一,严重威胁女性的健康,目前临床上对于卵巢癌的治疗主要为手术治疗、紫杉醇或多柔比星联合铂类药物化疗、靶向治疗及免疫治疗、放射治疗等[1-3]。雷帕霉素靶蛋白(mTOR)是一种丝氨酸/苏氨酸激酶,mTOR信号通路促进物质代谢,参与细胞凋亡、自噬,在多种疾病中发挥重要作用。近年来,研究表明,mTOR抑制剂能够有效抑制胃癌、肺癌、卵巢癌等肿瘤细胞的增殖分化及转移,发挥抗肿瘤作用[4-6],其中,雷帕霉素是目前已明确的第一代mTOR抑制剂。川芎嗪是从传统中药材川芎中提取得到的单体化合物,具有心脑血管保护作用、抗血小板聚集、改善微循环、增强机体免疫力及抗肿瘤作用[7-12]。本文主要通过研究川芎嗪联合mTOR抑制剂对卵巢癌SKOV-3细胞增殖、侵袭迁移的作用,为卵巢癌的治疗提供参考和依据。
1 材料
1.1 主要仪器 酶标仪购自北京岛津公司,双垂直电泳仪、转印电泳仪、凝胶成像仪、流式细胞仪均购自伯乐生命医学产品有限公司。
1.2 药品与试剂 川芎嗪购自Sigma公司,雷帕霉素购自北京索莱宝科技有限公司,RNA提取试剂盒、PI3K、AKT、mTOR和GAPDH抗体均购自Proteintech公司,细胞周期与细胞凋亡检测试剂盒、RIPA蛋白裂解液购自上海碧云天公司,ECL显色液购自Thermo公司。RPMI1640培养基、胰蛋白酶、MTT、Transwell小室、Matrigel基质胶均购自北京索莱宝科技有限公司。
1.3 细胞 人卵巢腺癌细胞SKOV-3购自中国科学院上海生命科学研究院细胞资源中心。
2 方法
2.1 细胞培养与传代 从-80 ℃冰箱中取出SKOV-3细胞冻存管,于37 ℃恒温溶解后移至超净工作台,加入适量的 RPMI1640 培养基(含 10%胎牛血清),1 000 r/min 条件下离心 8 min。弃去上清,加入适量培养基使细胞重悬,并小心接种于培养皿中,于 37 ℃、5%CO2恒温培养箱培养,定期更换新鲜培养液并传代。
2.2 MTT法检测川芎嗪联合雷帕霉素对SKOV-3细胞增殖的影响 根据文献方法确定川芎嗪及雷帕霉素给药浓度[13-16],在96孔板上分别设置给药组(分别为40 μmol/L川芎嗪组、5 μmol/L雷帕霉素组、40 μmol/L川芎嗪联合5 μmol/L雷帕霉素组)、对照组及调零组,每组设置5个复孔,调零组只加入等量培养液,不加入细胞悬液,其余各组加入对数生长期的SKOV-3细胞,并使其密度为1×104个/ml。各组在37 ℃、5%CO2培养箱中培养24 h,对照组及调零组更换新鲜培养液,给药组川芎嗪组加入终浓度为40 μmol/L的川芎嗪,雷帕霉素组加入终浓度为5 μmol/L的雷帕霉素、川芎嗪联合雷帕霉素组加入终浓度为40 μmol/L的川芎嗪及终浓度为5 μmol/L的雷帕霉素,并继续于培养箱中培养48 h。培养结束后,在避光的环境下每孔加入20 μl MTT溶液(5 mg/ml),于培养箱中避光孵育4 h,然后吸去上清液,每孔加入150 μl DMSO,置于振荡器上震荡5 min至蓝紫色结晶完全溶解后于酶标仪490 nm处测定OD值。按照如下公式计算细胞抑制率:
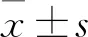
细胞抑制率(%)=
2.3 Transwell实验检测SKOV-3细胞侵袭能力 Matrigel基质胶融化后进行稀释,将稀释过的Matrigel胶包被Transwell小室底部,风干待用。取对数生长期的SKOV-3细胞,使用不含胎牛血清的RPMI1640培养基继续培养24 h,然后收集细胞,并调整细胞密度为1×105个/ml。将Matrigel胶包被的Transwell小室置于24孔细胞培养板中,小室加入200 μl细胞悬液,下室加入600 μl含20%胎牛血清的培养基,川芎嗪组及雷帕霉素组分别加入川芎嗪(40 μmol/L)及雷帕霉素(5 μmol/L),川芎嗪联合雷帕霉素组同时加入川芎嗪(40 μmol/L)及雷帕霉素(5 μmol/L),对照组不加药物处理,每组重复5个样本。置培养箱中常规培养48 h,取出小室,弃去培养液,使用PBS洗2遍,然后用70%甲醇固定30 min,台盼蓝染色,使用PBS洗3遍,用棉球轻轻拭去表面残留细胞和凝胶,倒置显微镜观察穿膜细胞数。统计各组细胞侵袭抑制率,细胞侵袭抑制率(%)=(1-给药组穿膜细胞数/对照组穿膜细胞数)× 100%。
2.4 划痕实验检测SKOV-3细胞迁移能力 取对数生长期的SKOV-3细胞,培养24 h后,对照组加入新鲜培养基,川芎嗪组及雷帕霉素组分别加入川芎嗪(40 μmol/L)及雷帕霉素(5 μmol/L),川芎嗪联合雷帕霉素组同时加入川芎嗪(40 μmol/L)及雷帕霉素(5 μmol/L),继续培养48 h后,将各组细胞接种于Matrigel基质胶包被的 96 孔板上,常规培养至形成单层细胞,沿培养板底部做划痕,在显微镜下记录划痕相对距离,继续培养24 h,再次记录划痕相对距离,统计细胞迁移距离,迁移距离=0 h划痕相对距离-24 h划痕相对距离。
2.5 实时定量PCR检测SKOV-3细胞中Bax、Bcl-2的mRNA水平 采用RNA提取试剂盒分别提取分别经40 μmol/L川芎嗪、5 μmol/L雷帕霉素、40 μmol/L川芎嗪联合5 μmol/L雷帕霉素作用48 h后的SKOV-3细胞的总RNA。将提取的总RNA逆转录成cDNA后,实时定量PCR检测各组SKOV-3细胞中GAPDH、Bax、Bcl-2的mRNA水平。各检测基因的实时定量PCR引物见表1,实时定量PCR结果采用2-△△Ct法计算相对表达量。

表1 用于实时定量PCR检测的基因引物序列
2.6 Western blot检测 将对数生长期的SKOV-3细胞于6孔板中培养至贴壁后,川芎嗪组及雷帕霉素组分别加入川芎嗪(40 μmol/L)及雷帕霉素(5 μmol/L),川芎嗪联合雷帕霉素组同时加入川芎嗪(40 μmol/L)及雷帕霉素(5 μmol/L),各组继续培养48 h后,分别加入裂解液提取总蛋白,采用BCA法测定蛋白浓度,处理好待测样品后,取50 μg蛋白进行SDS-PAGE电泳分离,转膜,将分离的蛋白电转移至PVDF膜上。封闭液室温封闭1 h后,经PI3K、Akt、mTOR抗体(1∶1 000)孵育,4 ℃过夜。PBST充分洗膜后,加入二抗(1∶2 000)室温孵育1 h,PBST清洗后显色液显影,利用凝胶成像仪成像后,应用Image J软件进行免疫印迹灰度值检测。
2.7 细胞周期检测 分别取经40 μmol/L川芎嗪、5 μmol/L雷帕霉素、40 μmol/L川芎嗪联合5 μmol/L雷帕霉素作用48 h后的SKOV-3细胞,用PBS洗2遍后,加入预冷的70%乙醇固定,过夜。次日取出,离心(2 500 r/min,5 min,4 ℃),用移液枪吸除上清液,涡旋震荡使SKOV-3细胞松散。用PBS洗涤SKOV-3细胞2次,然后加入已配好的碘化丙啶染色液,37 °C染色30 min后,利用流式细胞仪,进行细胞周期检测。
3 结果
3.1 川芎嗪联合雷帕霉素对SKOV-3细胞增殖的影响 川芎嗪联合雷帕霉素对SKOV-3细胞的增殖抑制率见图1。结果表明,与对照组相比,川芎嗪组、雷帕霉素组及川芎嗪联合雷帕霉素组OD值均显著降低(P<0.05),表明单独或联合使用川芎嗪和雷帕霉素均能明显抑制SKOV-3细胞的增殖;与川芎嗪组或雷帕霉素组相比,川芎嗪联合雷帕霉素组能够使SKOV-3细胞的增殖抑制率显著提高(P<0.05),提示川芎嗪联合雷帕霉素能够显著抑制卵巢癌细胞的增殖,且作用效果优于单独使用川芎嗪或雷帕霉素。

图1 川芎嗪联合雷帕霉素对SKOV-3细胞的增殖抑制率
3.2 川芎嗪联合雷帕霉素对SKOV-3细胞侵袭力的影响 各组SKOV-3细胞侵袭力见图2。结果表明,与对照组相比,川芎嗪组、雷帕霉素组及川芎嗪联合雷帕霉素组SKOV-3细胞穿膜细胞数均显著减少(P<0.05),同时,与川芎嗪组或雷帕霉素组相比,川芎嗪联合雷帕霉素组SKOV-3细胞侵袭抑制率显著升高,差异有统计学意义(P<0.05),提示川芎嗪联合雷帕霉素能够有效抑制卵巢癌细胞的侵袭力,且侵袭抑制率优于单独使用川芎嗪或雷帕霉素。
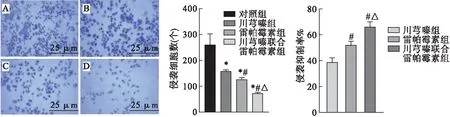
图2 各组SKOV-3细胞Transwell实验结果(40)
3.3 川芎嗪联合雷帕霉素对SKOV-3细胞迁移力的影响 各组SKOV-3细胞迁移距离见图3。结果表明,与对照组相比,川芎嗪组、雷帕霉素组及川芎嗪联合雷帕霉素组SKOV-3细胞迁移距离显著缩短(P<0.05),提示单独使用川芎嗪或雷帕霉素,或川芎嗪与雷帕霉素联合使用均能明显抑制卵巢癌细胞的迁移力;与川芎嗪组或雷帕霉素组相比,川芎嗪联合雷帕霉素组SKOV-3细胞迁移距离显著缩短,差异有统计学意义(P<0.05),提示川芎嗪联合雷帕霉素能够明显抑制卵巢癌细胞的迁移力,其作用效果优于单独使用川芎嗪或雷帕霉素。
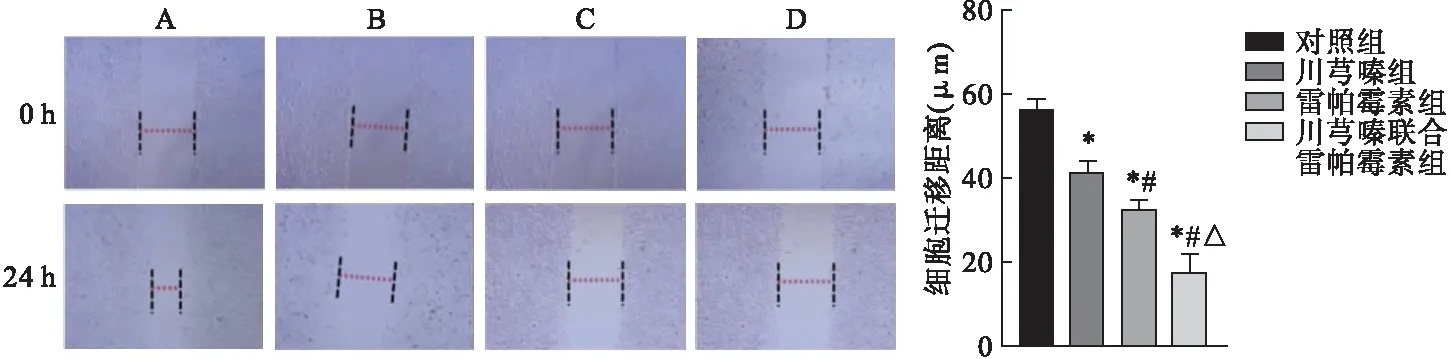
图3 各组SKOV-3细胞划痕实验结果(40×)
3.4 川芎嗪联合雷帕霉素对SKOV-3细胞Bax、Bcl-2的mRNA水平的影响 各组SKOV-3细胞Bax、Bcl-2的mRNA水平见图4。结果表明,与对照组相比,川芎嗪组、雷帕霉素组及川芎嗪联合雷帕霉素组SKOV-3细胞Bax mRNA水平显著升高(P<0.05),Bcl-2水平显著降低(P<0.05);同时,与川芎嗪组或雷帕霉素组相比,川芎嗪联合雷帕霉素组SKOV-3细胞Bax mRNA水平显著升高(P<0.05),Bcl-2 mRNA水平显著降低(P<0.05),提示川芎嗪联合雷帕霉素能够显著提高卵巢癌细胞内Bax水平,降低Bcl-2水平,这可能与川芎嗪联合雷帕霉素促进卵巢癌细胞凋亡机制有关。
3.5 川芎嗪联合雷帕霉素对SKOV-3细胞PI3K、Akt、mTOR水平的影响 各组SKOV-3细胞PI3K、Akt、mTOR水平见图5。结果表明,与对照组相比,川芎嗪组、雷帕霉素组及川芎嗪联合雷帕霉素组SKOV-3细胞PI3K、Akt、mTOR水平均显著降低(P<0.05),同时,与川芎嗪组或雷帕霉素组相比,川芎嗪联合雷帕霉素组SKOV-3细胞PI3K、Akt、mTOR水平显著降低(P<0.05),提示川芎嗪联合mTOR抑制剂可能通过调节卵巢癌细胞中PI3K/Akt/mTOR信号通路相关蛋白水平,从而起到对卵巢癌细胞的抑制作用。
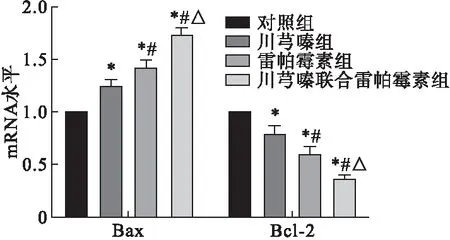
图4 各组SKOV-3细胞Bax、Bcl-2的mRNA水平
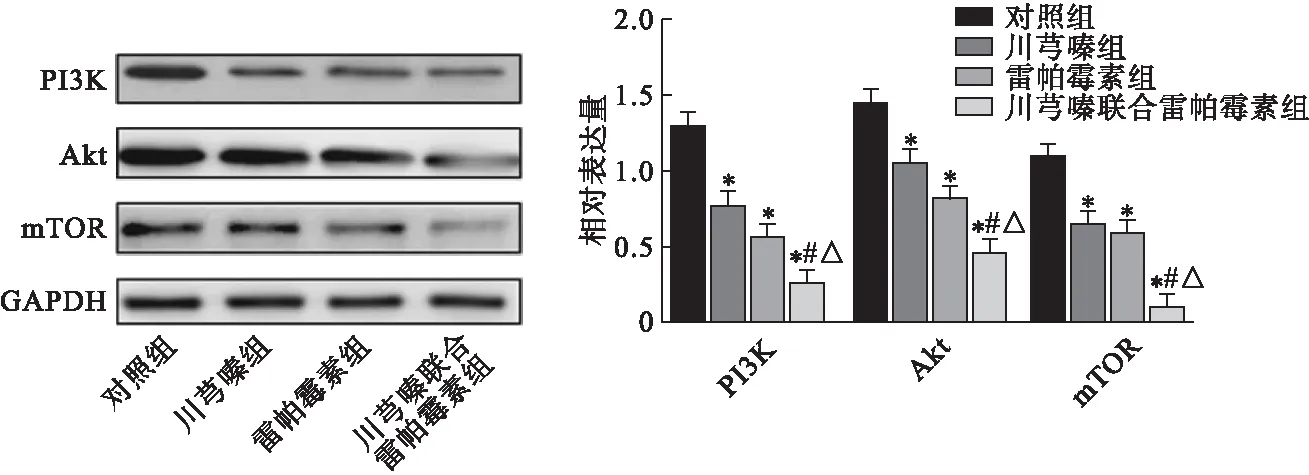
图5 各组SKOV-3细胞PI3K、Akt、mTOR水平
3.6 川芎嗪联合雷帕霉素对SKOV-3细胞周期的影响 见图6。结果表明,与对照组相比,川芎嗪组、雷帕霉素组及川芎嗪联合雷帕霉素组G1期SKOV-3细胞显著增加(P<0.05);与川芎嗪组或雷帕霉素组相比,川芎嗪联合雷帕霉素组G1期SKOV-3细胞显著增加(P<0.05),提示川芎嗪联合mTOR抑制剂能够显著影响卵巢癌细胞周期,改变卵巢癌细胞分裂过程,引起卵巢癌细胞G1/S期阻滞,从而抑制卵巢癌细胞的增殖,起到肿瘤抑制作用。
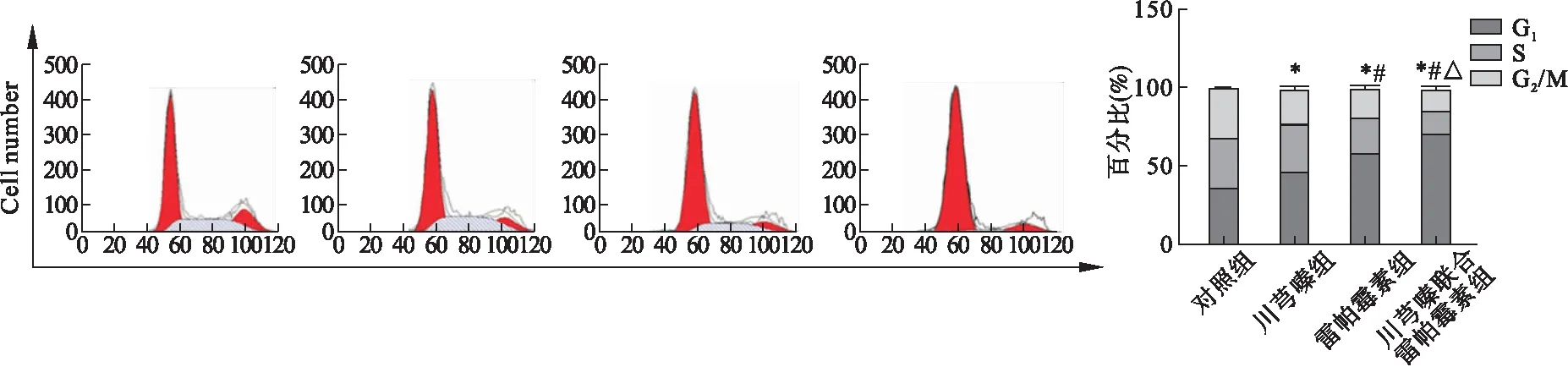
图6 川芎嗪联合雷帕霉素对SKOV-3细胞周期的影响
4 讨论
近年来,随着众多学者对于川芎嗪的深入研究,川芎嗪对多种肿瘤的药理活性逐渐被发现。Chen等[17]研究表明,川芎嗪能够通过抑制血管内皮生长因子诱导的血管生成,进而抑制黑色素瘤转移;黄芬等[18]研究证实,川芎嗪联合CIK细胞能通过下调细胞基质金属蛋白酶-2,上调基质金属蛋白酶抑制剂-2蛋白表达,抑制骨架微丝重排,进而抑制肝癌HepG2细胞的迁移及侵袭;杨劭劼等[19]发现,川芎嗪可以通过影响PTEN/AKT/cyclinD1信号通路,进而诱导外阴鳞癌细胞SW962的凋亡,并抑制其转移和侵袭;李高兵等[20]则证实了川芎嗪能够抑制Wnt信号通路的激活,进而抑制人肺癌细胞A549细胞的增殖、侵袭和迁移;来岳标等[21]发现,对于耐药肺癌细胞,川芎嗪也表现出显著的促凋亡作用,并参与调节丝裂原活化蛋白激酶信号通路;同时,殷娟等[22]发现,川芎嗪可以通过调节基质金属蛋白酶-9的表达,抑制IL-8诱导的SKOV3细胞迁移。而川芎嗪联合mTOR抑制剂雷帕霉素对于卵巢癌细胞的抗肿瘤活性,目前尚未见报道。本文研究川芎嗪联合mTOR抑制剂雷帕霉素对于卵巢癌SKOV-3细胞的作用,结果表明,川芎嗪联合雷帕霉素能够显著抑制卵巢癌SKOV-3细胞的增殖,抑制SKOV-3细胞侵袭、迁移,同时促进SKOV-3细胞促凋亡基因的表达,抑制抗凋亡基因的表达,抑制PI3K/Akt/mTOR信号通路的异常激活,其作用效果显著优于单独使用川芎嗪或单独使用雷帕霉素,这为后期深入研究川芎嗪联合mTOR抑制剂对细胞内信号转导通路及基因的靶向调节作用提供了基础。此外,本研究结果表明,川芎嗪联合mTOR抑制剂能够显著影响卵巢癌细胞周期,引起卵巢癌细胞G1/S期阻滞,这提示川芎嗪联合mTOR抑制剂可能对其他影响细胞周期相关通路存在潜在或反馈调节作用,值得进一步研究。由于时间及仪器等条件的限制,本研究未能进一步探讨川芎嗪联合mTOR抑制剂对细胞内基因的靶向调节作用,同时,川芎嗪与mTOR抑制剂的联合使用比例对细胞周期、相关信号通路是否具有不同的作用强度,在今后的研究中将进一步探讨。
综上所述,川芎嗪联合mTOR抑制剂能够显著抑制卵巢癌SKOV-3细胞增殖、侵袭和迁移,其机制可能与调节PI3K/Akt/mTOR信号通路有关。
