腹腔镜抗反流手术治疗胃部分切除术后胃食管反流的疗效观察
2021-03-18翁晓晖朱晓燕谢志杰王知非
翁晓晖,朱晓燕,贺 强,陶 亮,谢志杰,王知非,陈 浩
(1.海宁市中心医院普通外科,浙江 海宁,314408;2.浙江省人民医院肝胆胰外科;3.浙江中医药大学第二临床医学院)
近年,近端胃癌发病率逐步上升。对于近端胃癌患者,全胃切除或近端胃切除术均破坏了胃的连续性、完整性,并导致严重的胃食管反流症状,其中近端胃术后严重反流发生率在50%以上。而远端胃大部切除术后常发生胆汁反流。针对术后出现的胃食管反流情况,我们采取了多种措施预防,如胃空肠Roux-en-Y吻合、空肠间置术,术后辅以质子泵抑制剂、促胃肠动力药物等治疗。2018年2月至2019年10月浙江省人民医院与浙江省海宁市中心医院收治了5例胃切除术后反流性食管炎合并食管裂孔疝患者,并施行腹腔镜下食管裂孔疝修补及Nissen胃底折叠术,疗效显著,现将体会报道如下。
1 资料与方法
1.1 临床资料 5例患者中近端胃癌根治术1例,远端胃癌根治毕Ⅰ吻合术1例,胃大部切除术3例。首次手术距今5~8年。男3例,女2例,42~80岁,平均(62.24±14.37)岁,其中2例合并高血压病。患者主诉:均反酸、烧心、胸前区疼痛,且平躺后加重。术前胃食管反流病发病风险评分10~13分。5例患者均口服艾斯奥美拉唑片,40 mg每天,一次,时间13个月~4年。术前均行胃镜检查、食管钡餐造影,并证实胃食管反流合并食管裂孔疝,术前1 d晚口服聚乙二醇电解质散2盒行肠道准备,术前禁食6 h以上。患者及家属均签署知情同意书。
1.2 手术方法 采用气管插管全麻,患者取平卧分腿位,主刀立于患者右侧,助手分别立于两腿之间及左侧。建立气腹,分离腹腔粘连,避开手术疤痕,于脐左上方3 cm处做1 cm切口,直视下逐层入腹,确定无肠管粘连后穿刺10 mm Trocar,气腹压力维持在10 mmHg,其余切口围绕上腹部呈扇形分布,进腹后分离腹腔粘连(图1)。由小弯侧开始游离至右侧膈肌角(图2),再游离左侧残胃与膈肌粘连,避免损伤胃壁(图3),暴露食管裂孔,用导尿管牵拉食管下段及残胃近端牵拉,以充分暴露(图4)。超声刀游离食管下段至膈胸膜返折处。由下至上关闭食管裂孔,并用补片修补(图5)。将游离的胃后壁由后方绕过食管下端,在其前方与胃前壁间断缝合浆肌层,包绕食管下段(图6)。胃底两侧与膈肌裂孔周围固定3~4针。
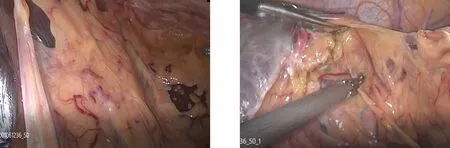
图1 进腹后腹腔内广泛粘连 图2 由小弯侧分离粘连
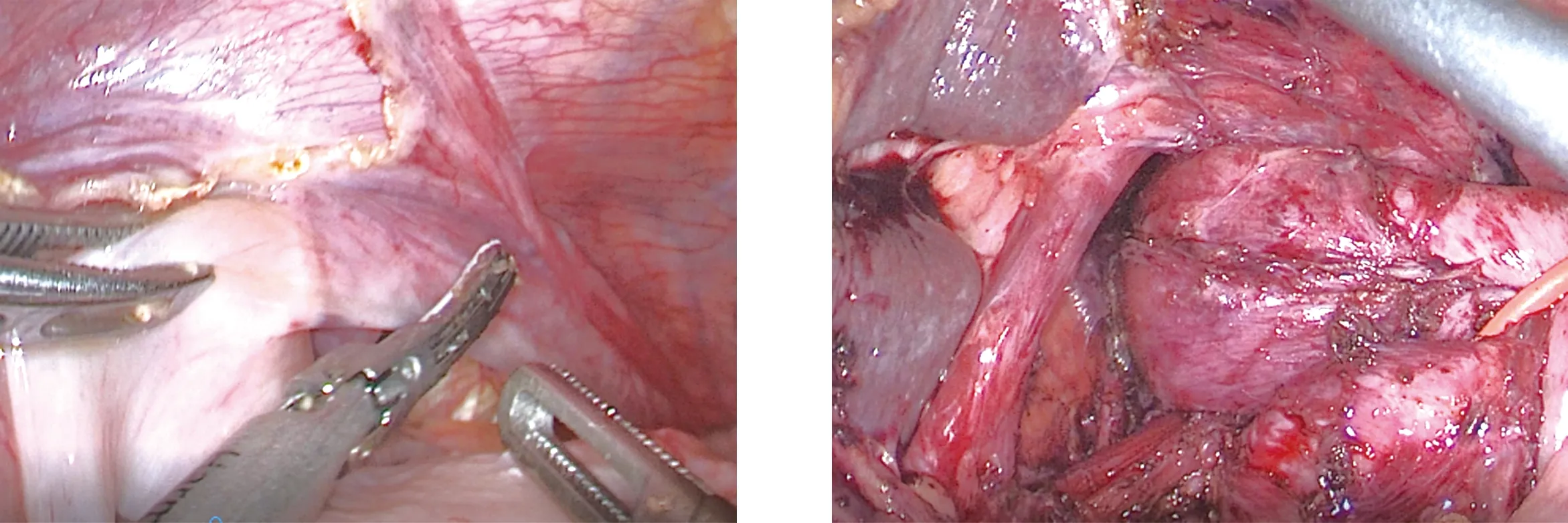
图3 游离左侧残胃与膈肌粘连 图4 暴露食管裂孔

图5 修补裂孔,放置补片 图6 放置支撑管胃折叠
2 结 果
5例患者均在腹腔镜下完成手术,均采用Nissen胃底折叠术及食管裂孔疝修补术,无一例中转开腹,手术时间70~120 min,出血量50~80 mL,术后24 h后开始进食流质饮食,术后住院3~10 d。1例患者术后出现短期吞咽困难,嘱延长进食流质时间约10 d后渐缓解,未做特殊处理,考虑术后折叠瓣处食管下段水肿可能,并下床活动。术后随访6个月,均无吞咽困难情况,反酸、恶心、胸前区烧灼感等症状明显改善,且均不再服用质子泵抑制剂。
3 讨 论
一般认为,近端胃切除术中虽然保留了残胃的储袋消化及内分泌功能,保留了正常消化道结构,但切除了食管下端及胃食管结合部,导致术后胃食管反流发生率相当高。而远端胃切除术后残胃容量、排空能力减低及远端幽门抗反流结构丧失,常出现胃内容物向食管反流,胆汁残胃反流[1]。用于肥胖症袖状胃部分切除术后治疗胃食管反流已成为重要的问题[2]。胃部分切除术后消化道重建方式与反流密切相关,食管空肠Roux-en-Y吻合最为常见,需充分游离食管下段,缺点在于需做多个吻合口,术后发生吻合口漏的可能性较大。而有学者认为,空肠间置术相较Roux-en-Y吻合抗反流效果更强。
目前,保守治疗尤其质子泵抑制剂治疗近端胃大部切除术后反流性食管炎获得了主导地位,在质子泵抑制剂的基础上加用促胃肠道动力药物或胃黏膜保护剂取得一定疗效,可缓解患者的临床症状[3]。但质子泵抑制剂不能改变胃食管反流的发生机制,也不能减少反流次数[4]。微量射频技术也被应用于临床治疗胃食管反流病。2007年汪忠镐等报道微射频治疗可起到立竿见影的效果,而且方法简捷、安全、价廉。2013年美国胃肠内镜外科医师学会也推荐微射频治疗。但对于合并食管裂孔疝等贲门处解剖结构变异的患者,尤其食管裂孔>2 cm的病例,射频治疗的效果较差。
自1956年Nissen胃底折叠术问世,因其抗反流病的疗效确切,使其理念深入人心[5]。但治疗胃部分切除术后胃食管反流则鲜有报道,主要是行近端胃癌术后残胃容积有限,行胃折叠术有一定困难,术后服用质子泵抑制剂及H2受体拮抗剂能获得部分改善。而长期以来,部分患者药物治疗效果越来越差。本组5例手术我们体会:(1)术前需行消化道造影,以了解胃的容积,残胃容积足够大才能有效折叠,单纯胃折叠术虽然操作简单,但有腹部手术史的患者,从建立气腹开始就容易造成二次损伤,因此我们建议开放建立气腹,在腔镜监视下选择合适位置穿刺其余Trocar,避免损伤,进腹后需仔细耐心分离粘连。由小弯侧无血管区进入,辨认右侧膈肌角,并向后方游离显露左右膈肌角交界部位,从而确定左侧膈肌角位置,左右贯通后,用导尿管将食管下段向右侧牵引,分离左侧粘连,切除多余的脂肪组织,最后游离出食管后通道。(2)虽然部分贲门周围癌手术患者的食管较短,仍需尽量向上游离至膈胸膜,一定仔细辨认胸膜,尽量靠近食管侧,但应避免损伤迷走神经。由疏松组织处分离,避免损伤胸膜,同时与麻醉师紧密配合,避免突发胸膜损伤造成医源性气胸的发生。如遇残余腹段食管较短,应尽可能向近端游离出5 cm左右,如仍达不到要求,只能放弃折叠,仅行单纯修补食管裂孔。(3)需充分分离粘连,尤其脾胃韧带处的胃短血管及前一次手术形成的侧支循环,也应避免残胃血供影响,确保足够胃折叠即可,游离大弯侧时尤其避免损伤脾脏,一旦损伤出血,可严重影响手术进程,必要时不得不中转开放手术。(4)既往研究确立了抗反流术后迷走神经损伤与胃动力受损之间的关系[6],术中应辨认迷走神经后干支以避免损伤,通常迷走神经后干位于食管后方,因而游离食管裂孔时可将食管向前上方牵引,于两侧膈肌脚汇合处前方疏松结缔组织内寻找白色条索状的后干,将其同食管一起拉向前方,防止游离食管后壁时损伤,然而胃部分切除术后的患者,往往此处粘连明显,情况并不完全明朗,更需要耐心解剖。(5)缝合食管裂孔后建议使用轻量补片修补,避免复发,补片边缘应至少超过疝边缘2 cm以上。固定补片后方时需注意避免缝合到胸主动脉,以免造成难以控制的大出血。(6)行胃折叠时,需在保证残胃血供的前提下,充分游离胃底组织,以确保胃无张力包绕食管;而行360°折叠会造成折叠瓣处食管水肿,引起术后梗阻。行折叠前经口放入支撑管到达预折叠瓣远端,再行折叠,会获得比较合适的松紧度。(7)因患者存在消化道手术史,因此术后饮食宣教尤为重要,需嘱咐患者严格执行少量多餐,细嚼慢咽,从流质到半流质慢慢过渡,避免进食过多造成吞咽困难。
综上,传统腹腔镜下抗反流手术治疗胃部分切除术后胃食管反流合并食管裂孔疝近期疗效显著,本组5例均取得满意疗效。但胃食管反流是胃部分切除术后常见并发症,也与患者的预后息息相关,因此对于绝大多数需行胃部分切除术的患者而言,第一次手术时即应考虑到术后胃食管反流问题,需要设计消化道重建方案,以最大程度减少胃食管反流的发生,如对于近端胃癌,全胃切除术后Roux-en-Y吻合术后反流发生率低于近端胃大部切除术;而双通道空肠间置消化道重建术后食管反流发生率显著低于Roux-en-Y吻合[7],也明显低于单通道空肠间置术[8]。Shinoto等发现,Roux-en-Y吻合组食管下段酸性、碱性反流率均低于毕Ⅰ、毕Ⅱ式吻合组。我们知道毕Ⅱ式联合Braun吻合也能降低远端胃大部切除术后胆汁反流发生率。Cui等[9]通过随访发现,毕Ⅱ式联合Braun吻合组残胃胆汁反流发生率高于Roux-en-Y吻合组,但差异无统计学意义。
对于合并食管裂孔疝的胃大部切除术后反流患者,常需大剂量质子泵抑制剂才能取得效果,研究表明,20 mg每日两次的雷贝拉唑较20 mg每日一次更能有效改善胃食管反流病典型症状与咳嗽[10]。但长期服用加倍剂量质子泵抑制剂并不能解决根本问题,反而带来消化系统肿瘤发生的风险[11]。不论消化内科医生抑或胃肠外科医生均需考虑患者可能从传统腹腔镜下抗反流手术中受益。
