碳酸镧联合西那卡塞、骨化三醇对血液透析伴继发性甲状旁腺功能亢进症的疗效
2021-01-27徐骏王笑薇刘旻齐向明
徐骏 王笑薇 刘旻 齐向明
安徽医科大学第一附属医院1血液净化中心,2肾脏内科(合肥230022)
血液透析技术的迅速发展有效提高了终末期肾病患者生存率,然而由于血液透析产生的各种并发症也困扰着临床医生与患者,其中甲状旁腺功能亢进是血液透析最为常见的并发症类型之一[1]。继发性甲状旁腺功能亢进症(secondary hyperparathyroidism,SHPT)以甲状旁腺增生和甲状旁腺激素(parathyroid hormone,PTH)持续升高为主要特点,可进一步造成患者钙磷代谢紊乱,增加患者不良预后风险[2]。骨化三醇抑制患者甲状旁腺腺体分泌,促进患者肠道对钙的吸收,但长期使用易导致高钙、高磷血症,加速血管和软组织钙化,增加心脑血管风险[3]。西那卡塞是美国食品与药物管理局唯一批准的用于人体的拟钙剂药物,广泛应用于SHPT 的治疗。然而过高的PTH 需增加西那卡塞使用量,加大患者经济负担,影响依从性,同时也增加了继发性低钙血症发生风险。高磷血症是引起维持性血液透析患者发生SHPT 的始动因素[4]。碳酸镧是不含钙和铝的磷酸盐结合剂,对磷具有较高的亲和力,可与食物中的磷结合生成磷酸镧,除极少被人体吸收外,大部分可随着粪便排出体外[5]。本研究回顾性分析碳酸镧联合西那卡塞、骨化三醇对维持性血液透析伴SHPT 患者的疗效,并与西那卡塞、骨化三醇进行对比,阐述联合用药的价值。
1 资料与方法
1.1 一般资料回顾性分析本院门诊2017年1月至2020年4月90 例维持性血液透析伴甲状旁腺功能亢进患者临床资料,依照给药方式,将采用单纯骨化三醇治疗的患者16 例纳入C 组,采用西那卡塞联合骨化三醇治疗的患者36 例纳入B 组,采用碳酸镧联合骨化三醇、西那卡塞的患者38 例纳入A 组。C 组包括男9 例,女7 例;年龄36~78 岁,平均(64.49 ± 13.25)岁;透析时间15~110 个月,平均(64.93 ± 20.83)个月;原发疾病:糖尿病肾脏疾病5 例,慢性肾小球肾炎6 例,高血压肾病3 例,慢性肾盂肾炎1 例,其他1 例。B 组包括男20 例,女16 例;年龄35~79 岁,平均(64.51± 13.40)岁;透析时间17~113 个月,平均(65.25 ± 19.93)个月;原发疾病:糖尿病肾脏疾病11 例,慢性肾小球肾炎14 例,高血压肾病7 例,慢性肾盂肾炎3 例,其他1 例。A 组包括男21 例,女17 例;年龄36~79 岁,平均(64.42 ± 13.50)岁;透析时间16~112 个月,平均(65.41 ± 19.77)个月;原发疾病:糖尿病肾脏疾病12 例,慢性肾小球肾炎15 例,高血压肾病8例,慢性肾盂肾炎2 例,其他1 例。三组患者一般资料比较差异无统计学意义(P>0.05)。
1.2 纳入标准(1)确诊为肾脏疾病,于本院行维持性血液透析,透析龄>1年;(2)合并SHPT,血清全段甲状旁腺激素(immunoreactive parathyroid hormone,iPHT)水平>300 ng/L;(3)3 个月内未接受过磷结合剂和维生素D 类似物的治疗;(4)经医院伦理委员会批准通过;(5)临床资料完整。
1.3 排除标准(1)甲状腺腺瘤患者;(2)原发性甲状旁腺功能亢进,特发性高血钙、肾小管性酸中毒等;(3)多发性骨髓瘤;(4)合并恶性肿瘤或严重心血管疾病;(5)合并严重感染;(6)过敏体质,对本研究所用药物过敏者;(7)合并肝功能异常;(8)合并胃肠道疾病,如消化性溃疡、吞咽困难、肠梗阻等。
1.4 治疗方法所有患者均通过金宝公司生产的血液透析仪透析治疗,低分子肝素钠抗凝,超滤量设置为:1 500~4 800 mL,血流量设置为200~250 mL/min。治疗过程中注意低磷饮食,透析液使用标准碳酸盐,透析钙浓度:1.25 mmol/L。在此基础上C组患者给予口服骨化三醇胶囊(厂家:上海罗氏制药有限公司,批准文号:国药准字H20140597),起始给药剂量为0.25 μg/d,睡前口服,每4 周调整剂量,若可耐受则可调整至最大剂量0.5 μg/d。B 组在C 组患者的基础上给予口服盐酸西那卡塞(厂家:协和发酵麒麟(中国)制药有限公司,批准文号:国药准字J20140122),给药剂量25 mg/次,1 次/d,晚餐后口服,每4 周依照iPHT、血钙、血磷检查结果调整剂量,最大剂量不超过75 mg/d。A组给予碳酸镧联合西那卡塞、骨化三醇,西那卡塞、骨化三醇给药方式与给药剂量同B 组与C 组,在此基础上加用碳酸镧咀嚼片(厂家:英国Hamol Limited,批准文号:国药准字H20171351),给药剂量依照患者血磷水平进行调整,≥2.26 mmol/L 者给药剂量为500 mg/次,<2.26 mmol/L 者为250 mg/次,3 次/d,餐中嚼服,治疗后第4 周调整剂量,血磷水平>1.78 mmol/L 者,剂量:250 mg/次;1.13~1.78 mmol/L 者维持原剂量;<1.13 mmol/L 者减少至250 mg/次或停药处理,三组患者均持续治疗6 个月。
1.5 观察指标(1)临床症状:比较三组患者治疗前与治疗后6个月皮肤瘙痒、骨关节疼痛、不宁腿综合征症状改善情况。(2)甲状旁腺体积:治疗前与治疗后6 个月患者均接受颈部超声检查,测量治疗前后甲状旁腺的长、宽和厚度。(3)血液指标:分别与治疗前、治疗后1、3、6个月透析前空腹采血,测定血钙、血磷、血清iPTH 含量。血钙通过离子选择电极法检测,矫正钙浓度为标准,矫正钙[40-血白蛋白(g/L)]×0.02+血清总钙(mmol/L);血磷通过离子选择电极法检测;血iPTH 通过化学发光法测得。(4)比较三组患者治疗期间不良反应发生情况。
1.6 统计学方法采用SPSS 22.0 统计学软件,计量资料多组间比较采用单因素方差分析,组间两两比较采用独立样本t检验,组间计数资料比较通过χ2检验,P<0.05 代表差异有统计学意义。
2 结果
2.1 三组iPTH 水平和达标率比较三组患者治疗前iPTH 水平比较(P>0.05);3 组患者治疗后1、3、6 个月iPTH 水平均较治疗前降低,且A 组低于B 组,B 组低于C 组(P<0.05);A 组治疗后3 个月iPTH 达标率84.21%高于C 组50.00%(P<0.05);三组患者血清iPTH 水平变化见图1。A 组、B 组治疗后6 个月iPTH 达标率分别为94.74%、83.33%高于C 组56.25%(P<0.05)。见表1。
2.2 三组患者临床症状改善情况比较三组患者治疗后皮肤瘙痒、骨关节疼痛症状均较治疗前改善(P<0.05);三组患者治疗后皮肤瘙痒、骨关节疼痛、不宁腿综合征比例比较差异无统计学意义(P>0.05)。见表2。

表1 三组iPTH 达标率比较Tab.1 Comparison on controls rates of iPTH among the three groups 例(%)

图1 三组患者治疗前后血清iPTH 含量变化Fig.1 Changes of serum iPTH levels before and after treatment in the three groups
2.3 三组甲状旁腺大小比较三组治疗前甲状旁腺大小比较差异无统计学意义(P>0.05);三组患者治疗后甲状旁腺长、宽、厚均较治疗前减少,且A 组与B 组小于C 组(P<0.05),见表3。
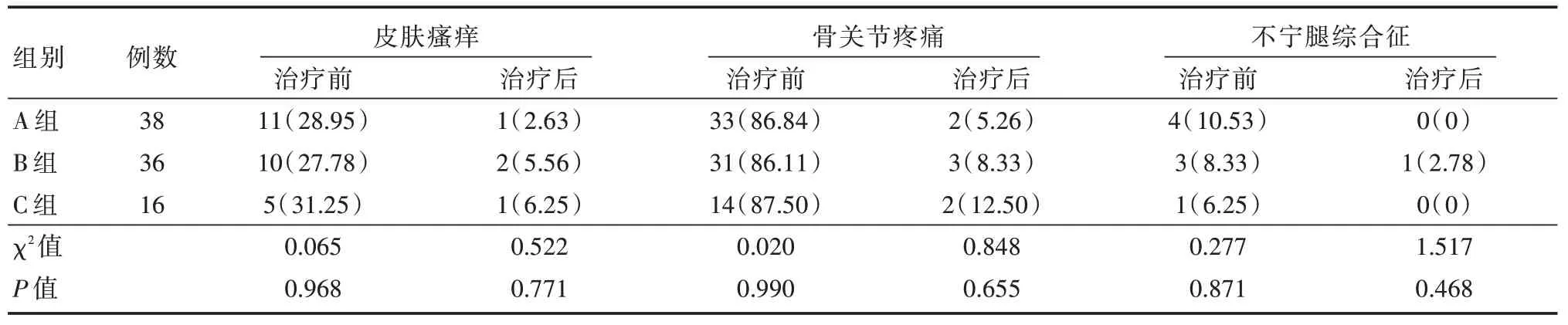
表2 三组患者临床症状改善情况比较Tab.2 Comparison on the improvement of clinical symptoms among the three groups 例(%)
表3 三组甲状旁腺大小比较Tab.3 Comparison on the size of parathyroid glands among the three groups ± s,cm

表3 三组甲状旁腺大小比较Tab.3 Comparison on the size of parathyroid glands among the three groups ± s,cm
注:与C 组比较,*P <0.05
组别A 组B 组C 组F 值P 值例数38 36 16长治疗前0.90 ± 0.05 0.89 ± 0.04 0.91 ± 0.05 1.112 0.333治疗后0.64 ± 0.06*0.65 ± 0.07*0.83 ± 0.05 57.554<0.001宽治疗前0.55 ± 0.03 0.54 ± 0.02 0.55 ± 0.02 1.763 0.178治疗后0.37 ± 0.06*0.39 ± 0.05*0.47 ± 0.05 19.306<0.001厚治疗前0.42 ± 0.02 0.43 ± 0.03 0.42 ± 0.03 1.571 0.214治疗后0.26 ± 0.02*0.27 ± 0.03*0.34 ± 0.02 63.308<0.001
2.4 三组钙磷代谢水平比较三组患者治疗前钙磷代谢水平比较(P>0.05);C 组患者治疗后1、3、6 个月血钙、血磷以及钙磷乘积均较治疗前升高(P<0.05);A 组、B 组患者治疗后1、3、6 个月血钙、血磷以及钙磷乘积均较治疗前降低(P<0.05);A 组、B 组治疗后血钙、血钙、钙磷乘积低于C 组,A 组血磷、钙磷乘积低于B 组(P<0.05)。见图2。
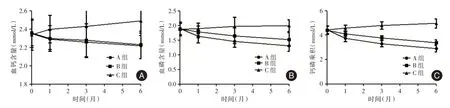
图2 三组钙磷代谢水平比较Fig.2 The levels of calcium metabolism were compared among the three groups
2.5 三组不良反应发生率比较治疗过程中,C 组患者出现腹泻1 例,肌肉痛1 例;B 组患者出现恶心3 例,腹泻1 例,肌肉痛2 例,头痛1 例;A 组患者出现恶心2 例,腹泻2 例,肌肉痛1 例,头痛2 例。三组患者治疗期间不良反应发生率比较差异无统计学意义(P>0.05)。见表4。
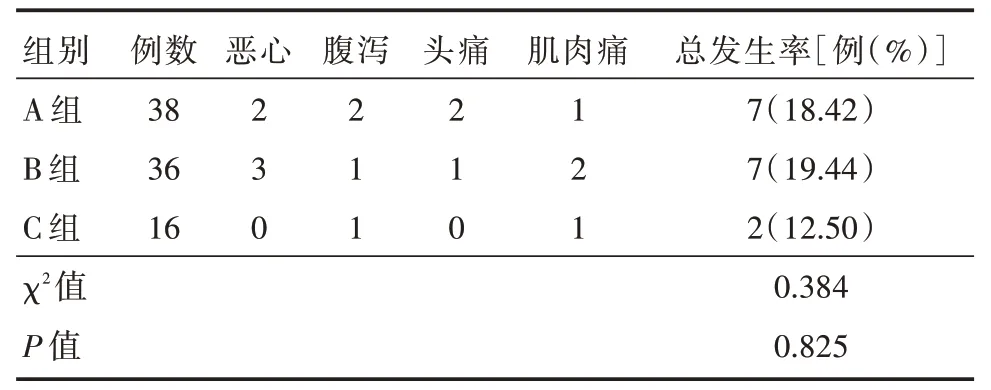
表4 三组不良反应发生率比较Tab.4 Comparison on the incidence of adverse reactions among the three groups 例
3 讨论
超过50%的血液透析患者出现SHPT 症状,SHPT 是肾性骨病发病重要环节,可使机体出现异位钙化和钙化防御,导致骨骼系统遭到破坏,患者神经和心脑血管系统疾病的发生,严重影响患者生活质量[6]。研究表明[7]接受长期透析治疗的患者当其体内iPTH 含量超过600 pg/mL 时,死亡风险相应明显增加。近年来,SHPT 的治疗方式多样,临床比较常见的治疗方式主要包括新型磷结合剂、活性维生素D 及其类似物、钙敏感受体激动剂、透析方案调整、手术治疗[8-9]。
骨化三醇作为一种高选择性的维生素D 受体激活剂,是治疗SHPT 的主要药物之一,口服后经小肠吸收,在肝脏25-羟化酶作用下转化为1,25-(OH)3D3发挥作用,抑制PTH 的合成及分泌、促进小肠对钙的吸收,增加甲状旁腺细胞中维生素D受体的表达[10-11]。西那卡塞是新型血液透析致甲状旁腺亢进症治疗药物,是一种钙敏感受体激动药物,可直接作用于甲状旁腺细胞表面钙敏感受体,刺激其对钙的吸收,从根本上达到抑制PTH 合成和分泌钙的作用[12]。长期接受血液透析治疗状态下,大部分患者会出现高磷血症,虽可通过延长透析时间,增加透析频率等方式来加强血磷清除能力,但这一操作成本较高,且由于各个透析中心技术存在差一定的差异,透析清除血磷受限[13-14]。因此本研究在西那卡塞、骨化三醇治疗的基础上联合使用碳酸镧,碳酸镧为新型磷酸盐结合剂,不含钙、铝,和磷的结合能力极强,且大部分可以胆汁形式排出体内,安全性较高,对患者大脑、肝脏、骨骼无害,在降低血磷含量的同时不会对iPTH 生成造成过度抑制和增加钙含量[15-16]。
本研究结果显示在西那卡塞、骨化三醇的基础上联合使用碳酸镧可更有效的控制患者病情,此时iPTH 达标率高达94.74%,效果显著。对比不同时间点患者血清iPTH 含量差异,A 组治疗后1、3、6 个月血清iPTH 含量均低于B 组和C 组,进一步说明联合三者联合用药在控制血清iPTH 含量方面的作用效果显著,HUTCHISON 等[17]研究结果支持本结论。SHPT 可引起骨骼系统破坏,导致骨痛、皮肤瘙痒、关节炎、肌病、神经和心血管等多系统损害。吴丽英等[18]研究结果表明西那卡塞治疗后,患者体内反映成骨细胞功能的碱性磷酸酶,骨钙素和反映破骨细胞功能的β胶原特殊序列等骨代谢指标均明显下降,说明西那卡塞联合骨化三醇可改善高转运骨病患者的骨代谢状态。本研究中A 组与B 组治疗后临床症状改善情况优于C 组,与其研究结果一致。本研究中A 组与B 组患者治疗后甲状腺体积小于C 组,但A 组与B 组比较无明显差异,肾衰竭状态下,甲状旁腺增生是SHPT 的重要组成部分,拟钙剂的使用可阻碍甲状旁腺增生,钙敏感受体的激活减少激素分泌的同时也可以减少甲状旁腺细胞增殖。
骨化三醇促进肠道对钙磷的吸收以及肾小管对钙磷的重吸收,加重异位钙化风险[19]。本研究中C 组患者治疗后血钙与血磷含量明显升高,A 组与B 组治疗后后血钙与血磷含量含量下降,且低于C 组,西那卡塞在降低血iPTH 含量的同时可降低血钙,西那卡塞的使用削弱了骨化三醇血钙升高作用,避免了继发性高血钙的发生,降低了转移性钙化风险。高磷血症可独立于低钙血症以及低维生素D 活性之外直接刺激患者合成甲状旁腺素,控制血磷有利于降低血iPTH。本实验中A 组患者在西那卡塞、骨化三醇的基础上加用碳酸镧降磷治疗,治疗后患者血磷水平下降,患者血磷含量低于B 组与C 组,这与XIPELL 等[20]的研究结果一致。李长红等[21]研究指出在骨化三醇冲击治疗过程中,未服用碳酸镧的患者血磷含量升高可导致不得不减少骨化三醇给药剂量或治疗方案终止。钙磷乘积是异位钙化风险预示的可靠指标,本研究中A 组钙磷乘积低于B 组与C 组,血磷控制效果较优。本研究中三组患者不良反应发生率比较差异无统计学意义,联合用药具有较高的安全性。
综上所述,碳酸镧联合西那卡塞、骨化三醇可改善维持性血液透析伴SHPT 患者临床症状,在有效降低患者血清iPHT 激素含量的同时,可控制钙磷代谢水平,用药安全性较高。
