2-(4-羟基)苯基酞菁钴的合成及对去除噻吩的催化活性研究*
2021-01-08薛科创杨艳丽
薛科创,杨艳丽,成 琳
(1.陕西国防工业职业技术学院 化学工程学院,陕西 西安710300;2.西安国祯环保工程有限公司,陕西 西安710016)
1 课题研究的背景及意义
随着石油资源的开发及二次加工技术的发展,石油资源的用量越来越大,但随之而来的是石油中的含硫化合物沿着石油的产品链进入到下游产品中,含硫化合物中的噻吩,是一种杂环化合物,具有芳香性,是石油最简单的噻吩类化合物,石油中其他噻吩类化合物都是不同碳原子数不同取代基的噻吩[1-3],随着这些产品的使用,含硫化合物进入到空气中,不但污染了环境,还影响了产品的稳定性,甚至破坏了化工生产过程的催化剂[4,5],因此,除去石油中的噻吩类化合物成为环境保护者及化学工作者研究的重点问题[6,7]。
人们在20 世纪初就发现了酞菁,发现它是一个具有 18 个 π 电子的 π,π 共轭及 p,π-共轭体系的配合物,这样非常庞大的共轭体系,应该是非常稳定的。人们根据推测不断探索,发现它的确具有良好的热稳定性和化学稳定性。而且共轭体系有利于电子的传递,很适合用于催化。薛科创[8-11]等人合成了四羧基酞菁铝、四硝基酞菁铝、四氨基酞菁铝及双核六硝基酞菁铝、双核六氨基酞菁铝、双核六羧基酞菁铝,通过这些物质的催化活性研究表明,取代基及共轭体系对酞菁的催化活性有一定的影响,具有吸电子能力的硝基降低了催化活性,而具有供电子能力的氨基、羟基增大了酞菁的催化活性,而且供电子基团越多,其催化活性越好。
前期的研究都是酞菁对乙硫醇的催化活性研究,乙硫醇结构简单,相对容易去除,而噻吩是一个杂环共轭分子,去除需要更高活性的催化剂,基于此,本文欲合成共轭体系更大的酞菁体系,以研究其对噻吩的去除能力。
2 实验部分
2.1 试剂及仪器
4-(4-羟基)苯基邻苯二甲酸酐、邻苯二甲酸酐及CoCl2(AR 阿拉丁试剂公司)是合成2-(4-羟基)苯基酞菁钴的主要原料,硝基苯和其他试剂为分析纯,科密欧化学试剂公司。
2-(4-羟基)苯基酞菁钴的表征采用德国Bruker 红外光谱仪测定,美国紫外-可见光谱仪以及德国elementar 元素分析仪。油品中噻吩含量的测定采用安捷伦气相色谱仪。
2.2 2-(4-羟基)苯基酞菁钴的合成
参考文献[12-13]报道的方法进行2-(4-羟基)苯基酞菁钴的合成,其具体反应原理见图1。取1 支250mL 三口烧瓶,加入80mL 溶剂硝基苯并强力搅拌,然后加入5mmol 的4-(4-羟基)苯基邻苯二甲酸酐,邻苯二甲酸酐5.18g、CoCl21.3g,等搅拌均匀后再加入0.2g 的钼酸酐作为催化剂以及4.0g 尿素,于180℃反应5h 后将其冷却到室温。
将硝基苯过滤后得到的反应混合物球磨均匀,烘干,然后用依次在30mL 去离子水、30mL 丙酮、30mL 甲苯中各回流 3h,滤饼烘干后用 30mL 1.0mol·L-1NaOH 进行水解,过滤后,滤液与30mL 1.0mol·L-1的HCl 反应,结束后用去离子水冲洗滤饼直到滤液pH 值为7,最后110℃烘干滤饼即为产物。
产物经干燥后为深绿色,质量为:0.76g,经计算产率为:22.91%,熔点测定,结果超过了300℃(与其他酞菁类似),采用德国elementar 元素分析仪测定此物质中碳、氢、氮含量分别为:C,68.53;H,3.17;N,16.64,与按照 2-(4-羟基)苯基酞菁钴分子式(分子式 C38H20CoN8O,其中:C,68.78;H,3.04;N,16.89)基本一致,说明此物质与2-(4-羟基)苯基酞菁钴具有相同的分子式。利用德国Bruker 红外光谱仪收集2-(4-羟基) 苯基酞菁钴的数据为(单位:cm-1):3404,2926,1712,1389,1104,950,730,1611,1463,792。用DMF 作为溶剂,2-(4-羟基)苯基酞菁钴的紫外-可见光谱数据为:257,313,655,680nm。
2.3 去除噻吩的催化活性测定
在92#汽油中加入一定量的噻吩,配制成浓度为5ml·L-1的噻吩溶液,用移液管取25mL 噻吩溶液,在通入 O2下不断搅拌,O2的流速控制在 5mL·min-1,加入催化剂2-(4-羟基)苯基酞菁钴0.3g,30min 测定一次汽油中噻吩的含量,直到噻吩含量不再下降为止。
3 结果与讨论
3.1 2-(4-羟基)苯基酞菁钴的结构表征
将2-(4-羟基)苯基酞菁钴与KBr 混合研磨压片,采用德国Bruker 红外光谱仪收集的2-(4-羟基)苯基酞菁钴的红外光谱数据并绘图,其红外光谱图见图2。
由图2 可以看出,出现的比较明显的特征吸收峰是由于2-(4-羟基)苯基酞菁钴和水分子中都含有羟基,因此,3402cm-1处出现了宽度很大而且吸收强度很大的峰,但不能确定2-(4-羟基)苯基酞菁钴中羟基的存在,由于2-(4-羟基)苯基酞菁钴中的O-H 产生了摇摆振动,因此,在1712cm-1处出现了的特征吸收峰[13],在 1389,1104,950 以及 792cm-1处产生了4 个明显的吸收峰,这4 个吸收峰归因于酞菁环的振动吸收,在1611 和1463cm-1处为苯环的吸收峰,这可能是酞菁环上4 个苯环的吸收锋,也可能是与酞菁环相连的苯环的吸收峰;在1227cm-1处出现的吸收峰可能是由于酞菁环中有C-N 键的伸缩振动引起的;由于2-(4-羟基)苯基酞菁钴中C-H 的面外弯曲振动[10],在902cm-1处产生的吸收峰归因于C-H 键的面外弯曲振动[14]。
2-(4-羟基)苯基酞菁钴的紫外-可见吸收峰也出现在 B 带和 Q 带,B 带为 257,313nm,Q 带为 655,680nm。和2-羟基酞菁铝的紫外-可见光谱比较,波长变短,向紫外区域移动,能量增加,这可能是由于苯环与酞菁环的共轭,使得酞菁能量增加的原因[15]。
3.2 2-(4-羟基)苯基酞菁钴对去除噻吩的催化活性讨论
测定在催化剂2-(4-羟基)苯基酞菁钴及2-羟基酞菁钴作用下,汽油中噻吩的含量,然后换算成去除率绘图,见图3。
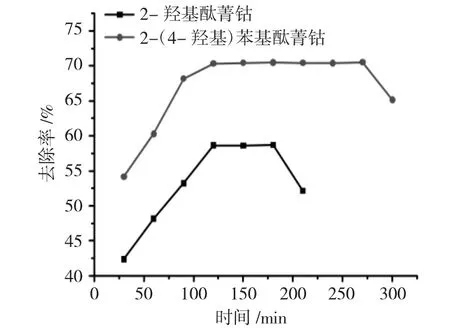
图3 噻吩的去除率Fig.3 Catalytic activity for the removal of thiophene
由图3 可以看出,2-(4-羟基)苯基酞菁钴及2-羟基酞菁钴对噻吩的去除率明显不如乙硫醇的去除率[15],这可能是由于噻吩是环状化合物,并且具有芳香性,比较稳定,硫原子难以从体系中去除的原因。
此外,2-羟基酞菁钴的最大去除率只有58%,而且催化剂的活性持续到180min 就开始下降,而2-(4-羟基)苯基酞菁钴从反应开始到结束,催化活性一直比2-羟基酞菁钴高,最大去除率达到了70%,并且一直持续到270min 才开始下降。究其原因,两种催化剂的区别在于,2-(4-羟基)苯基酞菁钴的结构中,羟基和酞菁环之间多了一个苯环,羟基、苯环、酞菁环三者构成了一个更为庞大的共轭体系,对反应中电子的传递更有利,促使了反应的进行。
4 结论
本文合成了2-(4-羟基)苯基酞菁钴,采用德国Bruker 红外光谱仪测定,美国紫外-可见光谱仪以及德国elementar 元素分析仪对所合成的2-(4-羟基)苯基酞菁钴进行了证明,然后以2-(4-羟基)苯基酞菁钴作为催化剂,研究了其去除汽油中噻吩的催化活性。结果表明,2-(4-羟基)苯基酞菁钴由于其具有庞大的共轭体系,有利于电子的转移,使得噻吩的去除率达到了70%。
