骨水泥强化骨折与非骨折脱钙羊椎骨的生物力学比较*
2020-12-23王志坤冯庆裕张贤森李再学谢文伟
王志坤,冯庆裕,张贤森,李再学,谢文伟
东莞市松山湖中心医院骨科(广东东莞 523326)
目前全球人口老龄化趋势日益明显,骨质疏松性椎体压缩骨折(OVCF)已逐渐成为老年人常见的骨折类型[1],约占骨质疏松性骨折的45%。经皮椎体强化术,包括经皮椎体成形术和球囊后凸成形术,已成为治疗OVCF的常规手术方法,并取得了广泛满意的疗效[2]。随着手术患者的增多,有大量文献报道术后再发椎体骨折的发生率较高。因此,有学者认为骨水泥椎体强化术可能会增加再发椎体骨折的风险,特别是邻近椎体,但是目前并没有确切的证据[3-6]。我们于2020年1—3月对骨水泥强化骨折椎体及邻近非骨折椎体力学改变作一研究,现报告如下。
1 材料与方法
1.1 实验材料 X 光机(北京航天中兴医疗系统有限公司生产,中国), C 型臂X光机(通用医疗器械厂生产,美国),骨密度仪XR-36 型双能X 线(Lunar 公司,美国),SW10 电子式万能试验机(济南恒瑞金试验机厂制造,中国),普通冰箱(青岛海尔公司,中国),椎体成形术器械(山东龙冠医疗器械用品有限公司,中国),注射器(5 mL、10 mL、20 mL),(江苏公司,中国),PMMA 骨水泥、PMMA 液相(天津市合成材料工业研究所,中国),牙托粉(广州市石膏制品厂,中国),成年新鲜山羊腰椎15具,于附近屠宰场购买。
1.2 实验方法
1.2.1 标本处理及分组 成年新鲜山羊腰椎15具,剥离并切除周围肌肉、韧带和骨膜,椎间盘组织、软骨终板,保留骨性终板的完整,分离成单椎体,注意保留椎体后部。经过肉眼与 DR 观察,无明显骨缺损,无病变与畸形,产生75个椎体。修剪部分横突和棘突的尖端,以便于测试。根据配对设计,将连续的3个椎体标本配成对子(L1~L3,L4~L6),交叉分配到A、B、C组,每组25个,A组不脱钙,B组脱钙后骨水泥强化骨折椎体组,C组脱钙骨水泥强化非骨折椎体组,使3组间标本均衡可比。分别将3组椎体放入恒温干燥箱,105℃干燥1 h后秤干重。以阿基米德定律用酸式滴定管精确测量每个椎体的体积。用双能X射线吸收仪(DEXA)测量骨密度(BMD)。
1.2.2 脱钙方法 用锥子在椎骨横突和小关节中线的交界处钻入椎弓根。用钝尖椎弓根探针将此孔伸入椎体40 mm深。直径约为4 mm,相当于钝型椎弓根探针的直径。然后A组用盐泡纱布包裹,密封在塑料袋中,冷冻保存在-20℃直到测试日。B组与C组参考Atilla Akbay的脱钙方法[7],将每个椎骨单独放置在装有500 mL盐酸脱钙溶液的玻璃量杯中,溶液的温度是20~22℃。将一个塑料锥形接头插入椎弓根上的孔,连接一根60 cm长的塑料管,先推注50 mL脱钙剂溶液。然后,用控制注射器式输液泵将480~500 mL脱钙剂溶液通过同一个孔注入椎骨,该泵的输液速度为40 mL/h。另一个椎弓根采用相同的步骤再脱钙12 h,共脱钙时间为24 h。然后用自来水冲洗椎骨,用500 mL盐水冲洗椎弓根孔,将脱钙液从标本中完全冲洗干净。再次测量椎体重量及骨密度。所有的样品都解冻达到室温,并在整个注射和测试期间保持湿润。见图1。
1.2.3 骨水泥强化骨折及非骨折椎体模型的生物力学测试 将B组脱钙后的羊椎骨,用牙托粉固定两个终板,安放于力学实验仪平行金属板上,调整试验机的高度,使得单元椎的上下两个面与模具贴合,并用 1 mm/min 的加载速度预压,力量达到100 N 时停止,目的为消除蠕变运动,并且使椎体充分固定于模具之中,不至于滑脱掉落影响数值的测定,充分固定完毕后试验力调零;采用5 mm/min的加载速度垂直轴向压缩,试验力精确度为 0.01 N,位移精确度为 0.01 mm,试验中严密观察各个椎体变化,加载至椎体强度失效停止。将骨折后的B组椎体和C组脱钙后的羊椎骨,采用椎体成形穿刺针,通过两个椎弓根的输液孔,经双侧椎弓根穿刺椎体中央处,C臂透视确认,配备PMMA骨水泥,常温下等待8 min后,在C型臂X线机监控下,经双侧穿刺针向每椎体注入3 mL骨水泥(图2)。等待骨水泥完全凝固。按上述测试方法分别加载三组椎体至椎体强度失效,通过对荷载-位移关系图的分析,确定了失效强度及失效位移。根据图表计算刚度(N/mm),整个过程保持室温恒定并使用注射器向椎体上喷洒生理盐水以保持湿润,减少误差。
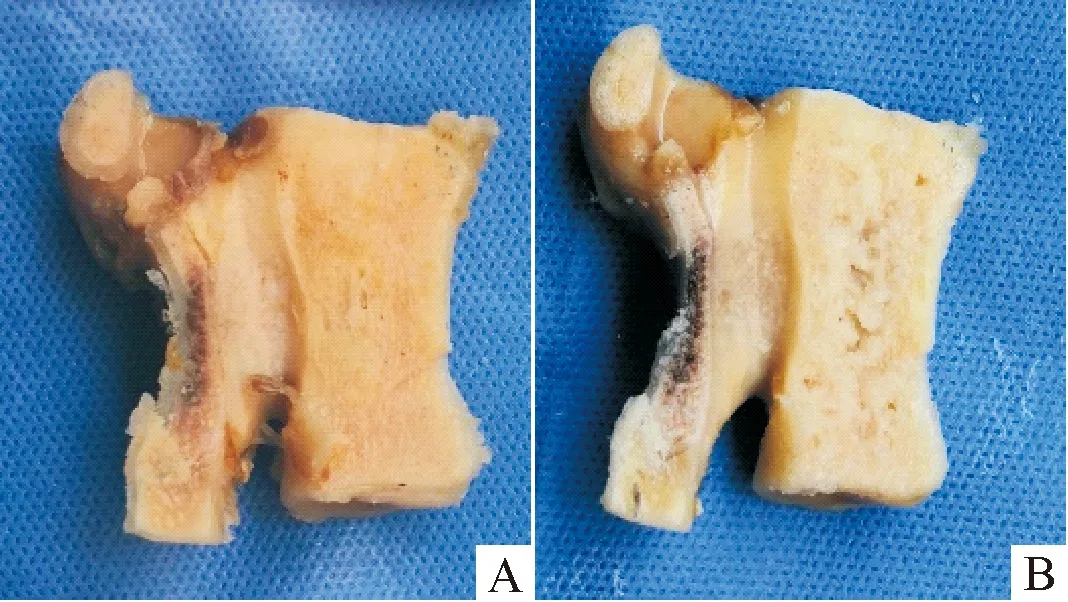
注:A:羊椎骨脱钙前矢状位切面图;B:羊椎骨脱钙后矢状位切面图,观察到脱钙后椎体皮质变薄和终板下可见的致密的软骨下骨松动
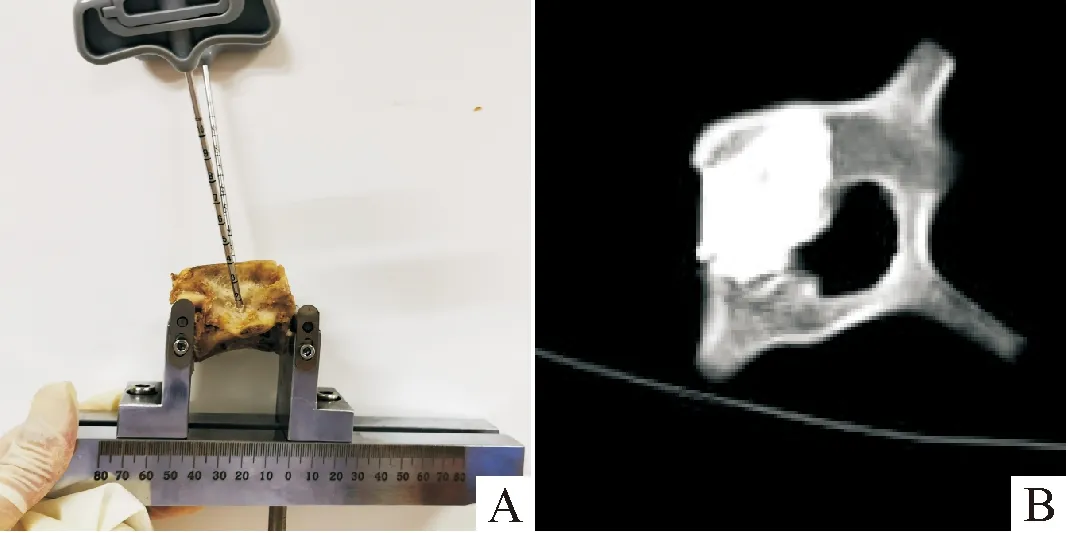
注:A:脱钙羊椎骨模型经双侧椎弓根插入穿刺针;B:脱钙羊椎骨模型经椎体强化术后CT横截面
2 结果
2.1 骨质疏松羊椎骨模型建模结果 A、B、C三组椎体脱钙前的重量、骨密度、体积差异无统计学意义(P>0.05),B组脱钙前后的骨密度下降比达32.6%,差异有统计学意义(P<0.01)。C组脱钙前后的骨密度下降达31.9%,差异有统计学意义(P<0.01),B、C两组脱钙后骨密度差异无统计学意义(P>0.05)。见表1。
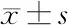
表1 3组椎骨骨密度、重量、体积的比较
2.2 生物力学测试结果 B组失效强度比A组下降123%,差异有统计学意义(P<0.01),B组刚度比A组下降102.6%,差异有统计学意义(P<0.01)。B组骨水泥强化后的失效强度及刚度分别是强化前的2.5倍和5倍,是C组失效强度的1.7倍,刚度的4.8倍,C组失效强度比骨水泥强化前的B组增加48.6%,差异有统计学意义(P<0.01),刚度稍增加3.3%,但差异无统计学意义(P>0.05)。失效位移差异无统计学意义(P>0.05)。见表2。
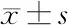
表2 3组椎骨失效强度、失效位移、刚度的比较
3 讨论
由于目前供研究的人体尸体标本有限,关于骨质疏松的研究,有学者建议利用羊椎骨建立骨质疏松模型模拟人体骨质疏松椎体进行生物力学研究[8-9]。而利用脱钙的方法建立骨质疏松模型是得到国内外学者所认可的[7,10]。该方法快速、简便、可控、而且费用低。至于如何判断是否成功建立骨质疏松动物模型的标准取决于骨密度下降比。由于动物不能参考人类的数据进行标准差判断,故一般以造模前后骨密度值下降25%为骨质疏松的诊断标准[7]。在我们的模型中,脱钙前和脱钙后的骨密度平均下降32.3%。根据骨密度低于0.75 g/cm2被认为是骨质疏松症[11]。本研究脱钙后椎体骨密度平均为0.74 g/cm2。因此,有理由说我们的脱钙方案能够成功地降低羊椎骨的骨密度。如图1所示,脱钙过程导致椎骨皮质变薄和骨小梁成分脱钙。椎骨的力学性质(刚度、应变、极限载荷等)与骨基质的矿化程度有关[12-13]。Turner[14]观察到抗扭强度与矿物含量成正比,且大部分取决于矿物含量。本研究对羊椎骨进行24 h酸的脱钙处理,羊椎骨骨矿质逐渐减少,骨密度随之下降,而椎体的失效强度和刚度均随之下降。本研究结果表明,脱钙方案也能模拟骨质疏松症患者脊柱椎体力学性能的退化。这是一个制作骨质疏松椎骨容易获得的方法,它具有晚期骨质疏松症的生物力学性质。用该方法制作的羊椎体可用于椎体最大强度及刚度测量的研究。
刘祥飞等[15]报道单侧入路椎体成形术生物力学效果与双侧入路接近,但本研究采用临床较常用的双侧入路,双侧共注射3 mL PMMA骨水泥。通过我们建立的模型,对比B组椎体骨折前及骨折后椎体强化术后力学变化,结果显示可增加椎体强度约2.5倍和刚度约5倍,与Seei等[16]的研究结果一致。Seei等[16]的生物力学研究表明骨水泥会增加伤椎的刚度和强度,骨水泥填充后的伤椎会导致相邻椎体负荷增加,从而引起随后的骨折。Fahim等[17]和Bedemann等[18]的研究也指出椎体成形术会改变脊柱的载荷传递,导致邻近椎体负荷增加,从而增加未治疗相邻椎体骨小梁隐匿性骨折或邻近椎体骨折的风险。椎体的强度和刚度与骨密度密切相关,与骨密度远低于正常水平的人相比,那些骨密度正常或接近正常的椎体可能表现出较少的椎体成形效果。李家琼等[19]报道椎体的骨疏松越重,椎体成形后受到的应力越高。临床行椎体成形的患者均是骨质疏松的患者,故椎体成形术后明显增加椎体的强度及刚度。
恢复椎体刚度和增加椎体强度可能是椎体强化的理想的结果。但从本研究结果显示椎体强化术导致椎体刚度值明显大于初始值,导致邻近椎体 “应力集中”效应明显,从而增加骨折风险,故有必要增加邻近椎体的抗压强度。所以临床上在椎体发生骨质疏松性压缩骨折后,骨折椎体强化同时,对邻近未骨折椎体进行预防性强化,符合生物力学需要,尤其骨质疏松明显的患者。Alkalay等[20]报道经椎体成形术后的骨折椎骨强度增加。Furtado等[21]通过骨折后与正常人椎体成形的生物力学比较,得出结论:预防性椎体成形增加了破坏强度,同时保持了刚度。与本研究C组中骨水泥强化非骨折椎体的力学改变一致。
关于为何骨水泥强化骨折椎体比强化非骨折椎体的强度和刚度均增加明显。分析原因,骨水泥比松质骨坚硬得多。根据大量的生物力学数据,向椎体腔内注射水泥可显著增加椎体的刚度和极限强度。这些变化使邻近椎体的压力大幅度增加。本研究认为当椎体发生骨折,椎体表面密质骨受到破坏,椎体形态发现改变,终板塌陷,抗压能力及刚度随之下降,此时靠椎体内松质骨支撑,此时向椎体注射骨水泥后,骨水泥比松质骨坚硬得多,骨水泥沿骨折线间隙分布为主,通过在终板之间建立水泥桥,完成替代松质骨支撑,此时椎体的强度与刚度相当于骨水泥的强度与刚度,得到大大的提高。而骨水泥强化非骨折椎体,椎体表面的密质骨完整性仍存在,即使注射骨水泥,骨水泥通过小梁间隙流动,导致弥漫性骨水泥云层在增强和非增强骨区域之间有连续的过渡。这使得界面处的应力集中越小,力传递越平滑,椎体的强度及刚度仍主要靠表面的密质骨维持,故其最大强度及刚度没有骨折椎体改变明显。
本研究的不足之处,第一,本研究所建立的羊椎骨模型中的骨小梁的结构在脱钙后仍然存在,从组织学和形态学更符合骨软化症,而不是骨质疏松症,为了真实模拟骨质疏松症,胶原含量和骨小梁本身的结构需要去除,但是在本研究的模型中没有去除。但是这种组织学和形态学的变化不应否认该模型的实验意义。从生物力学的角度来看,结构特性是最重要的。因此,本研究所作的羊椎骨模型具有生物力学观察和相关实验研究的价值。第二,本研究只检查了单椎体垂直轴向压缩负荷,而没有检查脊柱功能单位,没有研究椎间盘在椎体强化术后生物力学中的作用及人体脊柱活动时的多方向的负载。第三,根据Kurutz等[22]研究,预防性椎体强化的力学性能与骨水泥面和椎体终板距离及和终板接触次数等因素有关,本研究没有作具体分析,故仍需进一步研究。
利用脱钙方法建立的羊椎骨模型具有骨质疏松力学性能,在轴向的加载条件下,经骨水泥强化的骨折与非骨折羊椎骨的失效强度及刚度均有增高,而且骨折椎体增加明显,表明骨水泥强化能恢复骨折椎体的力学性能,但导致椎体刚度明显升高,对邻近非骨折椎体预防性强化有助于提高椎体抗压强度,维持椎体刚度,可能对预防邻近椎体骨折有作用。
