酸促进2-乙烯基苯胺与重氮的[5+1]环化合成2-芳基喹啉
2020-11-13马养民
南 江,陈 璞,马养民
(陕西科技大学化学与化工学院,中国轻工业轻化工助剂重点实验室,西安710021)
喹啉衍生物是一类重要的杂环化合物,广泛存在于天然产物和合成化学品中[1~5].其中,2-芳基喹啉衍生物不仅具有多种生物活性,而且表现出特殊的光电性质及配位能力,现已被广泛应用于医药[6]、发光材料[7]、电池[8]、生物探针[9]和催化反应[10]等领域. 辛可芬,其结构为2-苯基取代的喹啉羧酸,是一种已上市的止痛药,被用于治疗痛风[6];金属铱配位的2-芳基喹啉络合物被用作有机发光半导体材料的核心骨架[7];[11C]THK-951是一种11C标记的2-芳基羟基喹啉衍生物,其作为生物探针在阿尔兹海默症的早期诊断方面具有潜在的应用价值[9].因此,发展有效合成2-芳基喹啉的方法受到关注,目前已报道的合成方法主要分为4类[11].前2类为苯胺或邻位取代苯胺参与的[3+3]或[4+2]环化反应,包括传统的Combes[12],Doebner-miller[13],Friedlander[14],Pritzinger[15]反应及其改进方法等,尽管这2 类方法已有很大的发展,但仍存在条件苛刻、选择性差或底物价格昂贵等问题.第3类为分子内环化反应,如2-氨基苯乙烯酮在光[16]、四丁基碘化铵[17]或苄胺[18]催化下发生分子内环化合成2-芳基喹啉,但此方法底物难以制备的缺陷限制了其发展.第4类为[5+1]环化反应,此方法在合成喹啉的同时可对产物2号位进行特定功能化,具有高度的选择性,是近年来合成2-取代喹啉的常用方法,但此方法通常需要金属催化剂参与反应[19~21].因此,从廉价易得的原料出发,发展无金属且有效的[5+1]环化合成2-芳基喹啉的方法具有重要意义.
重氮化合物作为强大的合成子在过渡金属催化下被广泛用于构筑多种环状化合物,在该研究领域,重氮作为C2源已有大量的研究[22~30],相比之下其为C1源的发展较为受限,在构建六元杂环方面成功的例子更是屈指可数[19,31,32].2017年,Cheng等[19]在过渡金属钯催化下,以重氮化合物作为C1源,与2-乙烯基苯胺在150℃下反应合成了一系列2-芳基取代喹啉.但该方法需要加入贵金属催化剂钯,反应条件苛刻,成本较高.因此,发展一种以重氮作为C1源、无金属参与且条件温和的方法合成2-芳基喹啉化合物具有重要的价值.
基于前文[33,34]对2-乙烯基苯胺合成喹啉衍生物的研究,本文以2-乙烯基苯胺与重氮化合物在三氟乙酸催化下发生[5+1]环化反应,合成了24个2-芳基喹啉(Scheme 1).该方法无需过渡金属参与,反应成本低,操作简便,官能团容忍度高,能以中等至良好的产率得到一系列2-芳基喹啉,同时丰富了重氮化合物作为C1源参与的新型有机反应.

Scheme 1 Synthetic routes of 2⁃arylquinolines
1 实验部分
1.1 试剂与仪器
石油醚和乙酸乙酯,分析纯,购于广东光华科技股份有限公司;三氟乙酸,分析纯,购于百灵威科技有限公司;柱层析硅胶(200~300目)购自天津科密欧试剂有限公司;其它试剂均购于萨恩化学技术有限公司或阿拉丁试剂有限公司.
Bruker AVANCEⅢ400型核磁共振波谱(NMR)仪和Maxis UHR-TOF型高分辨质谱(HRMS)仪,德国Bruker公司.
1.2 实验过程
参照文献方法分别制备化合物 1a~1f[35],1g[19],1h[34],1i~1j[35],1k[34],1l[20],1m[35],1n[20],1o[34],1p[36],1q[34],2a~2e[37],2f[38]和2g~2h[39]. 各化合物的质谱数据及理论值列于表1,核磁共振表征结果见图S1~S50(见本文支持信息).

Table 1 HRMS data of compounds 1a—1q and 2a—2h
向15 mL的耐压瓶中依次加入0.2 mmol 2-乙烯基苯胺(1a)、0.3 mmol重氮化合物(2a)和1.6 mL三氟乙酸,在氩气条件下,于120℃搅拌反应10 h;冷却,用饱和碳酸氢钠溶液和乙酸乙酯进行萃取,合并、干燥有机相,过滤,经旋转蒸发除去溶剂,得到粗产品,经硅胶柱色谱(石油醚/乙酸乙酯体积比为100~30∶1)纯化得到相应的目标化合物3a.采用相同方法合成化合物3b~3x.所有化合物的理化性质数据列于表2,核磁共振表征数据列于表3,所得谱图见图S51~S98(见本文支持信息).

Table 2 Appearance,yields,melting points(m.p.)and HRMS data of compounds 3a—3x

Table 3 1H NMR and13C NMR data of compounds 3a—3x

Continued
2 结果与讨论
2.1 反应条件的筛选
以2-乙烯基苯胺(1a)与重氮化合物(2a)为反应底物,0.4 mmol三氟乙酸作为添加剂,于120℃和氩气条件下分别以N,N-二甲基甲酰胺(DMF)、乙二醇二甲醚(DME)、四氢呋喃(THF)、1,4-二氧六环、甲苯、乙腈和乙酸为溶剂,均未明显检测到目标产物3a(表4中Entries 1~7).当三氟乙酸的量增加到2.0 mmol,产物的产率仍未明显提高(表4中Entries 8~14).当以六氟异丙醇为溶剂时,反应产率提高至47%(表4中Entry 15).以六氟异丙醇作为溶剂,对添加的乙酸、对甲苯磺酸和特戊酸进行筛选,反应产率均有不同程度的降低(表4中Entries 16~18).当反应溶剂为三氟乙酸时,反应的产率显著提高,达到78%(表4中Entry 19).以三氟乙酸作为溶剂,继续考察反应条件的影响,当反应在空气或氧气条件下进行时,产率均有所下降(表4中Entries 20~21).最后,对反应的温度进行考察,当温度为100℃时,产率为69%(表4中Entry 22),140℃时产率下降为56%(表4中Entry 23).因此,确定了反应最优条件:三氟乙酸作为溶剂,氩气条件下于120℃反应10 h.

Table 4 Optimization of reaction conditionsa
2.2 底物的拓展
在最佳反应条件下,对底物的适用性范围进行了考察,结果表明,该方法具有良好的底物适用性(见表2).首先,对苯胺类底物进行了研究,利用含有不同取代基的2-乙烯基苯胺类底物1a~1q与重氮化合物2a进行反应.当R2为苯基、取代苯基、萘基、杂环或烷基,均能以中等至良好的产率得到产物3a~3f;当乙烯基被苯基和甲基取代或环庚基取代时,分别以63%和54%的产率得到产物3g和3h;同时考察了苯胺环上不同电子效应的取代基对反应的影响,当取代基为给电子或吸电子取代基时,均能得到相应的产物3i~3p,且吸电子取代基相对有利于反应进行;考察了苯胺环氨基邻位的取代基,也得到了预期产物3q.然后,对重氮化合物的适用范围进行了研究,利用2-乙烯基苯胺1a与重氮化合物2b~2h进行反应.当R4为取代苯基,噻吩,呋喃或萘环时,均能以良好的产率得到产物3r~3v;且当R4为甲基取代或氢时,也能以59%和63%的产率得到产物3w和3x.
2.3 反应机理探究
根据上述实验结果,提出了可能的反应机理(Scheme 2).以底物1a和2a为例,首先,1a和2a在三氟乙酸催化下发生亲核加成反应,再脱去一分子水和一分子氮气形成亚胺中间体A′[44,45],A′质子化形成中间体B′,B′再发生分子内的亲电加成得到六元环状中间体C′,再去质子得到中间体D′,最后芳构化得到产物 3a[46,47].
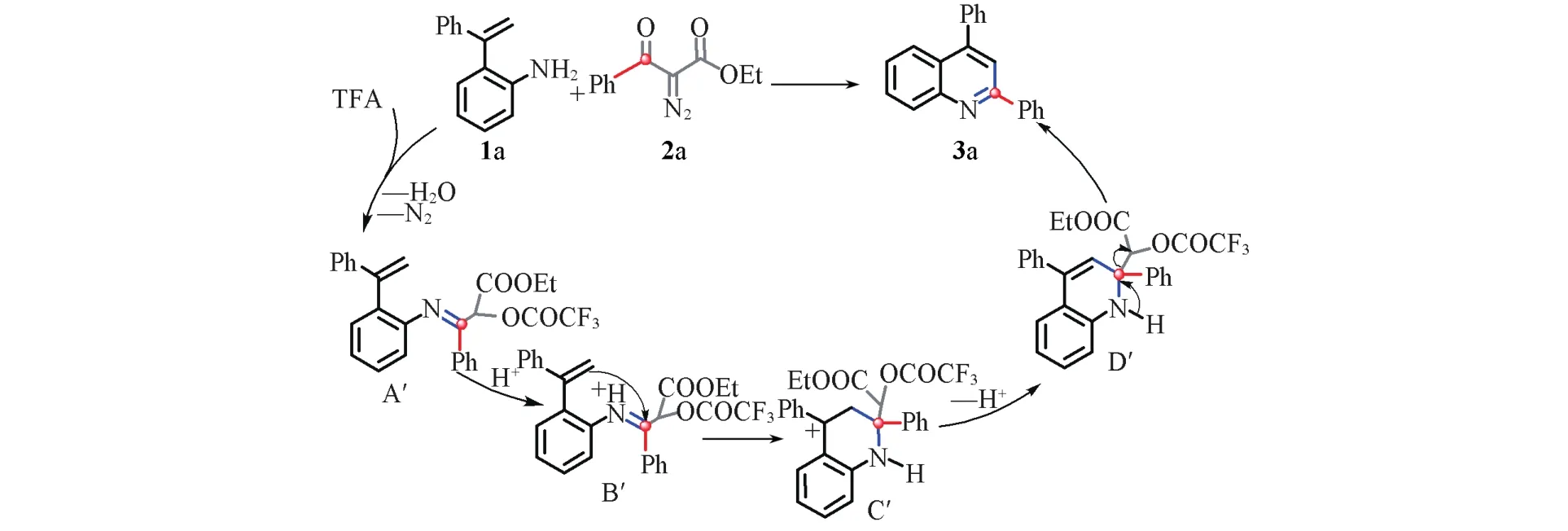
Scheme 2 Proposed mechanism of reaction
3 结 论
以2-乙烯基苯胺类化合物和重氮化合物作为原料,三氟乙酸作为溶剂,经[5+1]环化反应合成了多种2-芳基取代喹啉.该方法底物廉价易得,反应无需金属催化剂,且具有良好的官能团容忍性,丰富了重氮化合物参与的反应,为2-芳基喹啉的合成提供了新方法.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/cjcu20200340.
