先天性房间隔缺损相关TBX5基因新突变研究
2020-10-27王珊珊王天明刘兴元
王珊珊 王天明 刘兴元
先天性心脏病是人类最常见的发育畸形,其中又以心房间隔缺损(ASD)、心室间隔缺损的发生率最高[1]。严重的心脏间隔缺损可导致脑损伤或中枢神经发育延迟、肺动脉高压、血栓栓塞、感染性肺炎或心内膜炎、充血性心力衰竭、心律失常,甚至心源性猝死[1-3]。越来越多的研究表明遗传缺陷是先天性心脏缺损的主要病因,已经发现了60多个致病基因,其中大部分编码的是心脏核心转录因子[4-5]。作为一个重要转录因子,国外的研究发现TBX5基因突变可导致多种类型的先天性心脏病,但以ASD最为多见[6-7]。因此,有必要研究TBX5基因在中国汉族ASD患者中的突变率并揭示其致病机制。
1 对象与方法
1.1 研究对象
在2017年3月至2019年7月间从中国汉族人群收集了62例无血缘关系的新生儿ASD患儿和108名无血缘关系且年龄、性别相匹配的健康对照者。全部入选研究对象均详细了解病史及家族史,进行全面体格检查、超声心动图检查和常规化验检查。所有ASD患者均有超声心动图检查证据,所有健康对照者的超声心动图检查结果正常且无先天性心脏病家族史。在62例ASD患儿中,男37例,女25例,年龄为0~28 d,平均年龄10 d,有阳性家族史者4例;在108名健康对照者中,男65名,女43名,年龄为0~28 d,平均年龄10 d。本研究遵循医学伦理规范,经法定监护人知情同意后收集其外周静脉全血约0.2 mL,使用血液基因组DNA纯化试剂盒(德国Qiagen公司)提取基因组DNA。
1.2 方法
1.2.1 TBX5基因体外扩增 通过聚合酶链反应(PCR)体外特异性扩增TBX5基因整个编码区,剪接位点所用的引物见参考文献[8]。应用热启动高保真 DNA聚合酶(德国Qiagen公司)和TBX5基因扩增引物等试剂,以基因组DNA为模板,在C100 Touch型PCR仪(美国Bio-Rad公司)上扩增TBX5基因片段。每一个PCR的总体积是50 μL,包括双蒸水26 μL、5×PCR缓冲液10 μL(含有dNTP)、5×Q液10 μL、正向引物(20 μmol/L)1 μL 、逆向引物(20 μmol/L)1 μL、基因组DNA(100 ng/μL)1μL、Taq DNA 聚合酶(2.5 units/μL) 1 μL。PCR条件:首先95 ℃ 热激活5 min,随后35个循环,每一循环95 ℃变性30 s、62 ℃退火30 s、72 ℃延长1 min,最后72 ℃延长8 min。所扩增的产物经过1.5%琼脂糖凝胶电泳分离后,用凝胶回收试剂盒(德国Qiagen公司)纯化。
1.2.2 TBX5基因测序分析 使用正向或反向TBX5基因扩增引物,以纯化的基因片段为模板,应用DNA循环测序试剂盒(美国Applied Biosystems公司)在ProFlex型PCR仪(美国Thermo Fisher公司)上进行测序PCR反应。每一测序PCR的总体积为20 μL,其中包括双蒸水9 μL、纯化的DNA片段(50 ng/μL)2 μL、上游或下游引物(2 μmol/L) 1 μL、预混合液8 μL。测序PCR的条件见参考文献[9]。测序PCR产物经纯化后在3730型DNA测序仪(美国Applied Biosystems公司)上进行测序。将所测的NTBX5序列与Nucleotide数据库(https://www.ncbi.nlm.nih.gov/Nucleotide)中的TBX5序列(登陆号:NM_000192.3)进行对比分析以识别TBX5基因突变。如果发现TBX5基因突变,检索SNP (https://www.ncbi.nlm.nih.gov/SNP)、genomAD (http://gnomad.broadinstitute.org)、PubMed (https://www.ncbi.nlm.nih.gov/PubMed)和万方(http://librarian.wanfangdata.com.cn)数据库,以明确所发现的基因突变是否有报道。
1.2.3 真核表达质粒构建及定位诱变 野生型TBX5-pcDNA3.1真核表达质粒构建如前所述[8]。以野生型TBX5-pcDNA3.1为模板,使用一对以突变点为中心、长31个碱基的互补引物和QuikChange定位诱变试剂盒(美国Strategene公司)通过PCR引入所发现的点突变,经DpnI酶切、凝胶电泳分离后纯化可得突变型TBX5-pcDNA3.1质粒,然后经测序证实。表达萤火虫荧光素酶的报告质粒心房利钠因子-荧光素酶(ANF-luc)及表达海肾荧光素酶的内对照质粒pGL4.75如前所述[8]。
1.2.4 细胞培养、转染及报告基因分析 COS-7细胞的培养、借助脂质体进行的细胞质粒转染如前所述[8]。转染后48 h 收集、裂解细胞,应用双荧光素酶报告基因分析试剂盒(美国Promega公司)依次检测萤火虫、海肾荧光素酶的活性,并以二者的比值表示ANF基因启动子的转录活性。每种质粒转染实验均1式3份平行进行,以3次实验结果的平均值作为最终的结果。
1.3 统计学分析
连续变量以均数±标准差表示。两组组间连续变量的比较使用非配对Student′st检验;分类变量的比较使用Fisher′s精确概率检验或Pearson′s卡方检验。以双侧检验值P<0.05表示有统计学差异。
2 结果
2.1 发现TBX5基因新突变
通过对62例无血缘关系的ASD患儿的TBX5基因进行测序分析,结果在1例家族史阴性的ASD患儿中发现了1个杂合性突变,其TBX5基因编码核苷酸序列第318位的胞嘧啶(C)变成了鸟嘌呤(G),即c.318C>G突变,相应地氨基酸编码序列第106位的酪氨酸密码子变成了终止密码子,即p.Y106X突变,突变率约为1.6%。该无义突变不存在于108名健康对照新生儿,在SNP、genomAD、PubMed和万方数据库中也未见报道。该携带TBX5基因突变的ASD患儿的超声心动图见图1。TBX5基因c.318C>G杂合突变及其纯合野生型对照碱基序列见图2。
2.2 突变型TBX5的转录活性丧失
如图3所示,等量(0.6 μg)的野生型和Y106X突变型TBX5对靶基因心房利钠肽(ANP)启动子的转录激活作用分别约为12倍和1倍(纯合突变型TBX5与纯合野生型TBX5比较:t=13.89,P<0.01);而等量(各0.3 μg)的野生型和Y106X突变型TBX5共转染时,对ANP启动子的转录激活作用约为5倍(杂合突变型TBX5与纯合野生型TBX5比较:t=7.4,P<0.01)。
图 1 携带TBX5基因突变的ASD患儿的超声心动图
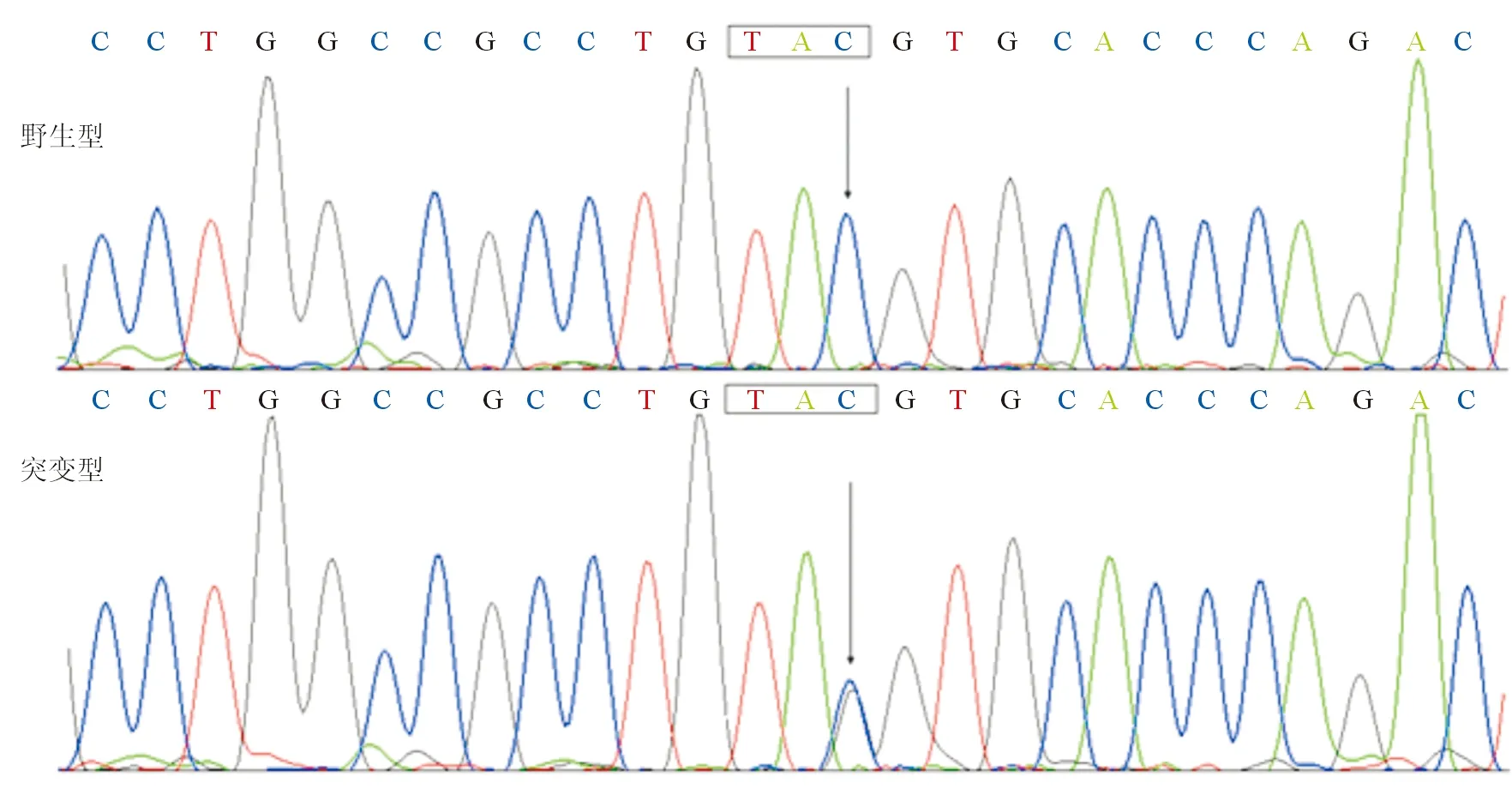
注:箭头分别指向TBX5基因c.318C>G杂合突变型C/G和纯合野生型C/C序列

注:与纯合野生型TBX5相比,P均<0.01
3 讨论
本研究在1例先天性ASD新生患儿中检测出了1个新的TBX5基因杂合突变c.318C>G(p.Y106X),该无义突变不存在于108名健康对照者。生化分析表明该突变导致TBX5对靶基因的转录激活功能障碍。因此,TBX5基因c.318C>G(p.Y106X)突变很可能是导致该新生儿患者ASD的分子病因。
人类TBX5基因位于染色体12q24.1,编码蛋白质由518个氨基酸组成。TBX5蛋白含有一个功能上非常重要的结构域,被称为T盒(氨基酸53-241),主要作用是与特定的靶基因启动子DNA结合以激活或增加其表达以及与其他转录合作伙伴相互作用协同调节靶基因的表达[6-8]。先前的实验研究表明,TBX5可单独激活或与转录合作伙伴GATA4、GATA6、NKX2-5和TBX20等协同激活在心脏发育过程中表达的多个重要靶基因,包括ANP、肌球蛋白重链6(MYH6)、血清反应因子(SRF)和缝隙连接蛋白 40(CX40)等,而且GATA4、GATA6、NKX2-5和TBX20等功能缺失性突变均可导致ASD[5-7]。在本研究中,在ASD患者发现的TBX5突变位于T盒,导致TBX5蛋白截短,失去了大部分T盒结构,预测可导致TBX5的转录功能障碍。报告基因分析表明,突变型TBX5对靶基因ANF的转录激活作用消失。这些研究结果表明,基因突变所致的 TBX5单倍性不足可能是ASD的分子机制之一。
TBX5基因功能异常导致胚胎心脏发育畸形如ASD等已在动物模型得到证实。在小鼠胚胎发育过程中,TBX5大量表达于心脏新月体和线性心脏管、左心室、室间隔、小梁、心房以及心脏传导系统[10-11]。TBX5基因敲除纯合子小鼠胚胎期死亡,主要原因在于心脏环化障碍以及左心室和窦房结发育不全;而TBX5基因敲除杂合子小鼠则可表现为ASD、室间隔缺损、心内膜垫缺损、左心室发育不良以及传导系统功能异常,包括房室和束支传导阻滞等[10-12]。这些动物实验研究表明TBX5在胚胎心脏正常发育方面发挥着关键作用。
人类TBX5大量表达于胚胎及出生后心脏[13],TBX5基因突变可导致Holt-Oram 综合征即手心综合征,表现为手、前肢及心脏畸形以及传导阻滞,而且心脏畸形可单独出现,其中以ASD最为常见[6]。研究发现,TBX5基因功能丧失性突变还可导致扩张型心肌病[8,14]、心房颤动[15]、急性心肌梗死[16]。本研究在ASD患儿发现TBX5基因功能丧失性突变,提示其将来可能易于发生扩张型心肌病、心房颤动或急性心肌梗死。
总之,本研究发现TBX5基因新突变可导致ASD,并初步揭示了其致病机制,对ASD的个体化防治具有一定的临床意义。
