离子色谱法同时测定白茅根中的及Cl-含量
2020-10-19王月莎
王月莎,张 蕊,刘 凡,吴 亮,张 颖
(乐山师范学院 化学与资源环境学院,四川 乐山 614000)
0 引言

常见的无机阴离子的测定方法有分光光度法和离子色谱法:分光光度法具有耗时较长,所用试剂往往有一定毒性,在测定色素较多的样品时容易产生误差等缺点[8],离子色谱法前处理比分光光度法简便,测定快速,可同时检测多种阴离子,适合批量样品的检测。
实验拟采用超声辅助提取白茅根中的阴离子,然后通过离子色谱法测定白茅根中的硫酸根、亚硝酸根、氯离子含量。该方法可用于快速、批量分析中药材白茅根中的无机阴离子含量。
1 材料和仪器
1.1 仪器
离子色谱仪(ICS-900,赛默飞世尔科技(中国)有限公司)、高速万能粉碎机(ZN-400A中国吉首中诚制药机械厂)、超声仪(KQ3200型,昆山市超声仪器有限公司)、万分之一电子天平(AL104梅特勒-托利多仪器(上海)有限责任公司)、离心机(TDL-40B)、注射器(5 mL一次性使用无菌注射器带针,四川普瑞斯生物科技有限公司)、IC-RP小柱(HP Pre宁波鸿谱仪器科技有限公司)、0.45 μm微孔滤膜(PES,津腾)。
1.2 主要试剂
实验用水为高纯水,亚硝酸钠、硫酸钾以及氯化钾等试剂均为分析纯,N2(>99.99%)。
2 方法
2.1 对照品溶液的配制

2.2 RP小柱活化
用注射器抽取5 mL色谱纯甲醇溶液,以2~4 mL/min推入RP小柱,弃滤液;抽取10 mL去离子水,以2~4 mL/min推入RP小柱,弃滤液,将注射器平放20 min。
2.3 样品阴离子含量测定
精确称取粉碎后的样品2 g,置于100 mL烧杯中,准确加入去离子水50 mL,超声处理后,转移提取液于离心管中,设置转速及时间,取上清液以2~4 mL/min推入经活化后的RP小柱,弃去前3 mL,收集流出液,再用0.45 μm微孔滤膜过滤,滤液可直接进样。在选择出的最佳流速和淋洗液浓度条件下测定样品中硫酸根、亚硝酸根、氯离子三种阴离子的含量。
2.4 色谱仪器参数
色谱条件:AS11-HC,4 mm×250 mm离子交换柱、AG11-HC,4 mm×50 mm保护柱、AERS-500,4 mm抑制器、电导检测器、RFC-30淋洗液在线发生器、柱温室温、进样量为10 μL。以氢氧化钾为淋洗液(10~30 mmol/L),洗脱时间10 min。
3 实验结果及讨论
3.1 超声时间对提取白茅根中阴离子的影响
准确称取白茅根样品20 g于1 000 mL圆底烧瓶中,再向烧瓶中加入500 mL超纯水,在室温下进行超声处理,分别于3 min、5 min、10 min、15 min、20 min、25 min后采样进行测定,将采集的提取液转移至干净、干燥的离心管中离心20 min(转速3 000 r/min)。取上清液过活化后的IC-Rp小柱,收集流出液,再用0.45 μm微孔滤膜过滤,滤液直接进样。结果显示15 min时,样品峰基本保持不变。故实验采用超声时间为15 min。
3.2 淋洗液种类的选择
实验比较了将Na2CO3/NaHCO3溶液及KOH溶液作为淋洗液的区别,结果显示,KOH对样品的分离能力较Na2CO3/NaHCO3更好,系统背景信号更低,干扰更小,因而实验选择KOH作为淋洗液。
3.3 淋洗液流速对阴离子分离情况的影响
准确称取白茅根样品20 g于1 000 mL圆底烧瓶中,再向烧瓶中加入500 mL超纯水,在室温下进行超声处理15 min,将采集的提取液转移至干净、干燥的离心管中离心20 min(转速3 000 r/min)。取上清液过活化后的IC-Rp小柱,收集流出液,再用0.45 μm微孔滤膜过滤,在流速分别为0.5 mL/min、0.6 mL/min、0.7 mL/min、0.8 mL/min、0.9 mL/min、1.0 mL/min下进行测定,实验结果见表1、表2、表3。
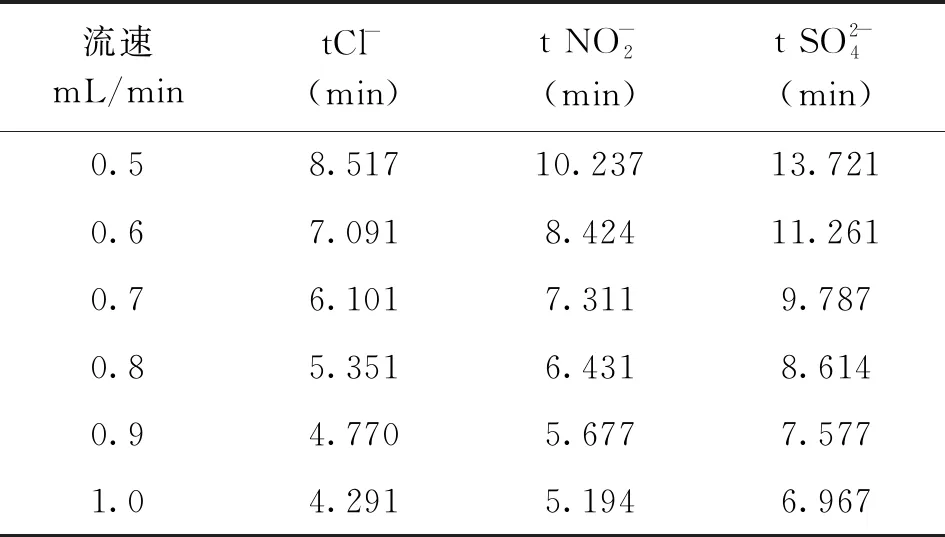
表1 流速对保留时间的影响

表2 流速对分离度的影响

表3 流速对半峰宽的影响

续表3
从表中数据可知,氯离子、亚硝酸根和硫酸根三种阴离子的保留时间随着流速的增大而变小,流速增大会加快白茅根中的三种阴离子的洗脱速度。但其分离度随着流速的增大变化不大,说明流速的变化对分离度的影响不大。其半峰宽随着流速的增大而逐渐减小,峰宽越来越窄,峰型也越来越好看。所以,在能把氯离子、亚硝酸根、硫酸根三种阴离子都分离开的情况下,可以选择较快的流速。本实验的离子色谱仪在超过1.0 mL/min时,泵压力不是很稳定,故本实验的最佳流速为0.9 mL/min。
3.4 阴离子分离情况随梯度浓度的变化
改变淋洗液浓度梯度,在不同的保留时间、分离度、峰高、峰宽和峰形图中找到白茅根中阴离子最佳的淋洗液浓度和流速。实验结果见表4、表5、表6。

表4 淋洗液对保留时间的影响

表5 淋洗液对分离度的影响

续表5

表6 淋洗液对半峰宽的影响
KOH溶液作为淋洗液使用时,其浓度选择相对较“挑剔”,当其浓度较高时,分离效果将会变差,浓度较低时,分析时间将会较长。本着绿色环保的思想,节约淋洗液成本,并使得阴离子峰得以较好的分离,淋洗液应尽量选择较小浓度,故拟定最高浓度为30 mmol/L。改变初始浓度梯度,从以上数据可知,氯离子、亚硝酸根、硫酸根的保留时间随着淋洗液浓度的增大而变小,淋洗液浓度增大会加快白茅根中阴离子的洗脱速度。氯离子、亚硝酸根、硫酸根的分离度随着淋洗液浓度的增大而变小,淋洗液浓度增大会降低白茅根中的阴离子的分离效果,当淋洗液初始浓度为19 mmol/L时,氯离子与亚硝酸根不能完全分离。氯离子、亚硝酸根、硫酸根和硝酸根四种阴离子的半峰宽随着淋洗液浓度的增大而逐渐减小,峰宽越来越窄,峰型也越来越好看。因此,综合时间和分离度,本实验的离子色谱仪在当淋洗液初始浓度为18 mmol/L,最终浓度为30 mmol/L,分析时间为10 min时,分离效果最佳。
3.5 仪器最佳参数色谱图
确保氯离子、亚硝酸根和硫酸根三种阴离子都能完全分离的情况下,为了提高工作效率,节约时间及实验药品,仪器的最佳流速为0.9 mL/min,最佳初始淋洗液浓度为18 mmol/L,最终浓度为30 mmol/L。最佳仪器条件色谱图见图1。由图可知,亚硝酸根离子与硫酸根离子、氯离子分离度良好。样品出峰时间:氯离子<亚硝酸根离子<硫酸根离子。

图1 最佳仪器条件的色谱
3.6 白茅根中无机阴离子含量的测定
按设定的色谱条件,待基线稳定后,依次取相同体积的标准工作溶液和待测样品溶液,装入离子色谱进样器的进样小管中,开始测定,根据保留时间定性,标准曲线法定量。
3.6.1 线性关系
分别将稀释了2倍、5倍、10倍、25倍的混合标准使用液以及混合标准使用液原液装入离子色谱仪进样器的进样小管中,按照上述设置的色谱条件分离、测定。以峰面积为纵坐标,标准溶液的浓度为横坐标,分别绘制三种离子的标准曲线,得出其回归方程、相关系数、线性范围,实验结果见表7。

表的线性方程
3.6.2 样品测定及精密度、重复性实验
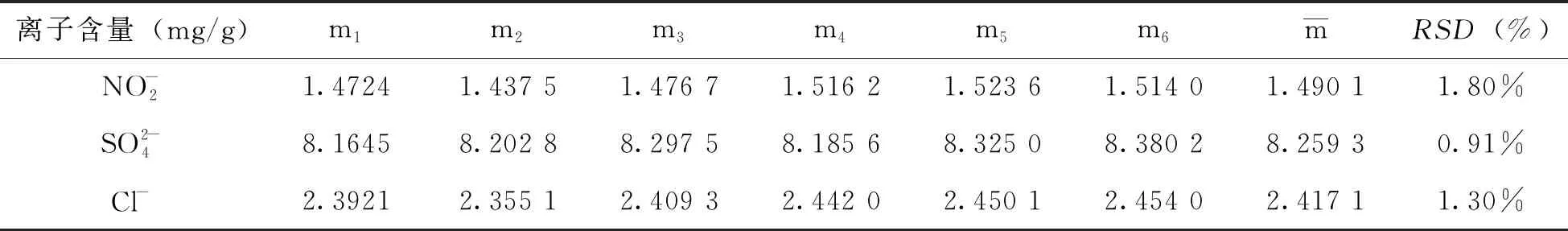
表8 样品测定及精密度试验
3.6.3 稳定性

3.6.4 加标回收率
精确称取6份已知含量的白茅根粉末2 g(精确至0.000 1),其中3份加入相当于样品含量120%的阴离子对照液,另外三份加入相当于样品含量80%的阴离子対照液,测定结果见表9。三种阴离子的平均回收率在95.2%~104.5%,表明该方法能满足测定需求。
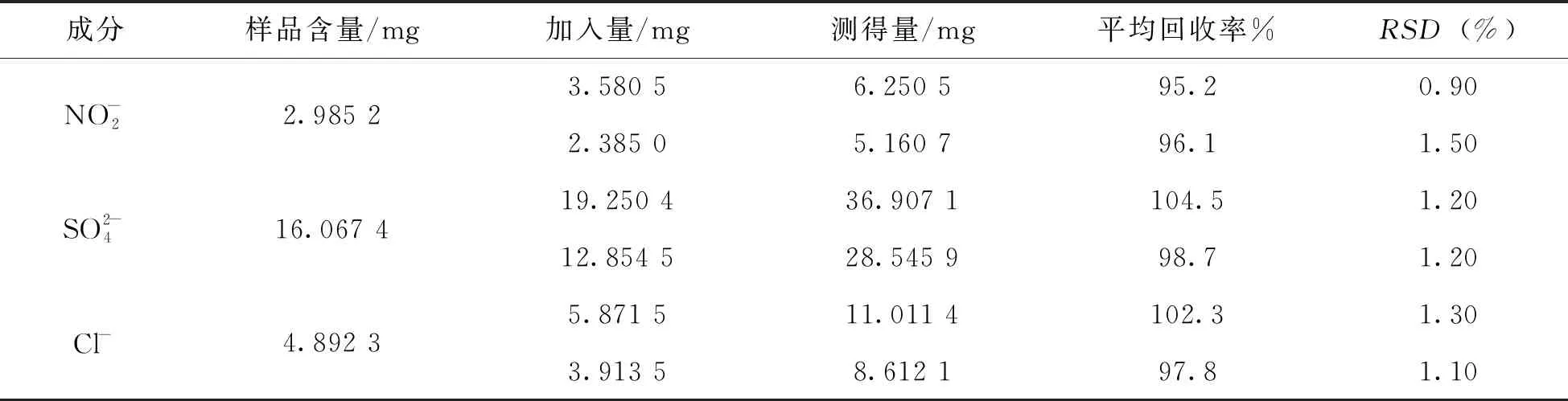
表9 白茅根样品中阴离子加标回收率实验(n=2)
4 结论

