穿破石对人肝微粒体CYP450酶的抑制活性研究
2020-10-12陈诗卉梁现蕊
陈诗卉,梁现蕊
(浙江工业大学 药学院,浙江 杭州 310014)
穿破石即桑科柘属植物构棘Cudraniacochinchinensis或柘树Cudraniatricuspidata的根。穿破石无味、稍苦、性凉,具有祛风、清热利湿、解毒消肿等功效,主治风湿疼痛、瘀伤、黄疸、腮腺炎、肺结核、胃和十二指肠溃疡等症状[1]。一方面,穿破石的药理活性较丰富,据已有文献报道:穿破石的抗炎镇痛作用显著[2],其水提取物对肝损伤具有良好的治疗作用,有一定的保肝效果[3];另一方面,穿破石具有较高的抑菌活性,而且抑菌谱广[4]。穿破石在临床上主要用于治疗输卵管阻塞性不孕、尿结石和肝胆湿热型黄疸等症状[5],临床应用前景广阔,但目前关于其联合用药时对体内CYP酶是否有影响的研究还较少。
中药有其独特的纯天然性和相对较小的毒副作用,临床上常与西药联合用于疾病的治疗,但由于许多中药会对CYP酶产生不同程度的影响,随着中药处方使用的增多及其与药物之间的联用,在药物-药物之间可能会产生许多相互作用[6],如银杏叶提取物和桑叶提取物均会对体内的代谢酶和转运蛋白产生一定的抑制作用[7-8]。中药是多种化合物组成的混合物,成分较为复杂,通常以单味或复方入药,因此研究提取物比研究单一的活性成分更加准确[9]。CYP450酶是最重要的药物代谢酶系统之一,在药物代谢中起到非常重要的作用,是人体异源生物转化中重要的I相酶[10],参与人体内大量化合物的生物转化,是药物代谢的主力军,参与了人体药物代谢的90%以上,来自CYP1,CYP2和CYP3家族的亚型酶与临床上大多数药物的代谢有关[11]。临床研究表明:对P450酶的诱导或抑制效应是引起人类不良药物反应(ADR)的重要原因之一,而抑制效果被认为是CYP450酶涉及的药物相互作用机制中比例最大的[12]。中药化学成分较为复杂,其中可能含有一种或多种CYP450亚型酶的有效抑制剂,从而导致不同程度的药物-药物相互作用[13]。因此,研究中药化学成分对CYP酶的作用,对于有效避免不良药物反应具有重要的意义[14]。穿破石作为传统中药,广泛运用于中药处方中[15-16],与其他中药或者西药结合共同治疗疾病。为了评估穿破石的用药安全性,笔者以超高效液相色谱为检测手段,通过混合探针底物法,在体外建立了人肝微粒体孵育体系,研究其对CYP450酶的抑制活性,为临床提供安全、有效、合理的联合用药参考。
1 材 料
1.1 仪 器
Waters Acquity超高效液相色谱仪,美国Waters公司;HHT-5恒温水浴锅,常州国华电器有限公司;KQ 5200DE数控超声波清洗器,昆山市仪器有限公司;Barnstead TII超纯水系统,美国Thermo Fisher Scientific公司;XS 205 DualRange分析天平,瑞士Mettler Toledo公司;Miulab MIX-28涡旋振荡器,杭州MIULAB仪器有限公司;Heraeus Biofuge Stratos离心机,美国Thermo Fisher Scientific公司。
1.2 药品和试剂
混合人肝微粒体,蛋白质量浓度20 mg/L,瑞德肝脏疾病研究上海有限公司AKT;六水氯化镁MgCl2·6H2O,质量分数≥98%,上海Solarbio科技有限公司;氧化型辅酶Ⅱ二钠NADP+,质量分数≥98%,上海Solarbio科技有限公司;6-磷酸葡萄糖脱氢酶1 000 U,上海Solarbio科技有限公司;6-磷酸葡萄糖二钠G-6-P,质量分数≥98%,上海Solarbio科技有限公司;磷酸盐缓冲液PBS 100 mmol/L,pH 7.4,上海Solarbio科技有限公司;非那西丁、氯唑沙宗、甲苯磺丁脲,北京天威泰达科技有限公司;睾酮、酮康唑,质量分数≥98%,上海Solarbio科技有限公司;α-萘黄酮、磺胺苯吡唑,质量分数≥98%,上海凛恩科技发展有限公司;氯美噻唑,上海毕得医药科技有限公司。
2 方法与结果
2.1 试剂配制

表1 试剂配制
阳性抑制剂的制备:分别称取适量阳性抑制剂磺胺苯吡唑、α-萘黄酮、氯美噻唑、酮康唑,加入如表1所示的相应溶剂配制成一定浓度的储备溶液,置于-20 ℃冰箱中保存备用。
NADPH再生系统溶液的制备:分别称取适量的MgCl2·6H2O,NADP+,G-6-P和6-磷酸葡萄糖脱氢酶对照品,加入一定量的PBS溶液溶解稀释,MgCl2·6H2O,NADP+和G-6-P的最终浓度分别为50,10,50 mmol/L,6-磷酸葡萄糖脱氢酶为40 U/mL,现配现用。
穿破石提取液的制备:准确称取一定量的穿破石粉末,置于干燥洁净的具塞锥形瓶中,按照m(穿破石)∶V(体积分数为60%的甲醇)=1 g∶50 mL的料液比向锥形瓶中加入体积分数为60%的甲醇溶液,于100 HZ,35 ℃下超声45 min,提取液冷却后抽滤得到滤液,经旋转蒸发浓缩后,于冷冻干燥机中干燥24 h,得到淡黄色穿破石提取物。精密称取38.89 mg穿破石提取物,用1 mL体积分数为40%的甲醇溶液溶解配制成38.89 mg/mL的穿破石提取液,置于-20 ℃冰箱中保存备用[17]。
混合探针底物的配制:分别取适量底物对照品非那西丁、甲苯磺丁脲、氯唑沙宗、睾酮储备溶液,加入一定量的PBS溶液溶解稀释,非那西丁、甲苯磺丁脲、氯唑沙宗和睾酮在溶液中的终浓度分别为200,200,200,225 μmol/L。
2.2 体外抑制实验
穿破石提取液对人肝微粒体的抑制实验分为实验组和对照组,对照组又包括阳性对照、阴性对照和空白对照,所有体外抑制实验均一式3份,取平均值进行分析。孵育体系的体积为200 μL,其组成:pH 7.4的100 mmol/L磷酸钾缓冲液、NADPH再生系统溶液(包括1 mmol/L NADP+,5 mmol/L G-6-P,4 U/mL 6-磷酸葡萄糖脱氢酶和5 mmol/L MgCl2)、1 mg/mL(即53.1 pmol/mg)的人肝微粒体蛋白和混合探针底物组成,有机溶剂的体积分数<1%[18]。
实验组由孵育体系和穿破石提取液组成,穿破石提取液的质量浓度分别为0.005,0.010,0.10,0.50,1.00,2.00,4.00 mg/mL。阳性对照组由孵育体系和单独的阳性抑制剂组成,阳性抑制剂分别为磺胺苯吡唑0.50,2.00,4.00,16.00,20.00 μmol/L;睾酮0.10,0.50,10.00,20.00,60.00 μmol/L;α-萘黄酮0.10,0.50,1.00,10.00,20.00 μmol/L;氯美噻唑0.50,1.00,2.00,4.00,20.00 μmol/L。阴性对照组由孵育体系和与抑制剂等体积的PBS组成。空白对照组除体系中使用灭活人肝微粒体,于95 ℃水浴中加热5 min外,其余均与阴性对照组相同。
将上述孵育体系分别在37 ℃水浴条件下孵育5 min后,加入混合探针底物启动反应,于37 ℃水浴条件下再共同孵育60 min;孵育结束,加入冰乙腈200 μL,超声5 min混匀后,于离心机中在13 000 r/min下离心15 min;取60 μL上清液,与80 μL超纯水混匀即得检测样品,取该样品10 μL,按表2中所示条件进行超高效液相色谱分析。分析所用色谱柱为Acquity UPLC BEH C18柱,2.1 mm×100 mm,1.7 μm;流动相由水和乙腈组成,V(水)∶V(乙腈)=S∶Y,柱温保持在30 ℃,由于探针底物的最大吸收波长不同,分别在245 nm和230 nm下检测[19-20]。
在第十届江苏科技期刊“金马奖”的评选中,《实用心电学杂志》荣获“十佳创新团队奖”。11月21日,在苏州召开的2018江苏省科技期刊学会学术年会上,江苏省科技期刊学会向本刊颁发了获奖证书。

表2 超高效液相色谱洗脱条件
2.3 数据处理及分析
以底物作为参考,根据剩余底物的相对峰面积,得到抑制率公式为
(1)
式中:K为抑制率;A0,A1和A2分别为空白组、实验组和阴性组剩余底物的相对峰面积。将穿破石提取液、标准抑制剂的浓度转换成对数值,然后用GraphPad Prism 8.0.1软件绘制抑制率-浓度对数值的曲线,计算对CYP450酶活性抑制一半时所需的药物或者抑制剂的浓度IC50。
2.4 方法学验证
2.4.1 专 属 性
为探究抑制实验的专属性,将实验分为A,B,C 3组进行研究。A组为空白肝微粒体,以PBS替代,不加混合探针底物与抑制剂,其余操作按2.2节进行;B组向于95 ℃水浴中加热5 min灭活的人肝微粒体中加入一定浓度的混合探针底物标准溶液,不加抑制剂,其余操作按2.2节进行;C组将一定浓度的混合探针底物标准溶液加入空白人肝微粒体中,不加抑制剂,其余操作按2.2节正常孵育。将所得样品进行UPLC检测后,专属性结果如图1色谱图所示。由图1(a)可知:在底物的出峰时间段里,空白肝微粒体中并没有干扰性杂质出现。图1(b,c)中1号峰为非那西丁,2号峰为氯唑沙宗,3号峰为甲苯磺丁脲,4号峰为睾酮,对比可知:底物的出峰时间没有太大的变化,说明肝微粒体并不会对底物的出峰时间产生干扰,专属性良好。

图1 专属性实验的UPLC谱图
2.4.2 标准曲线、检测限和定量限
将人肝微粒体进行灭活处理后,向其中加入不同浓度的混合探针底物标准溶液,按2.2节条件操作,并以底物的相对峰面积和浓度为坐标,制成标准曲线,回归计算后得到4种底物的线性回归方程,以信噪比S/N=10为定量限,S/N=3为检测限,通过线性相关系数R2可以发现4种底物的线性关系良好,结果如表3所示。
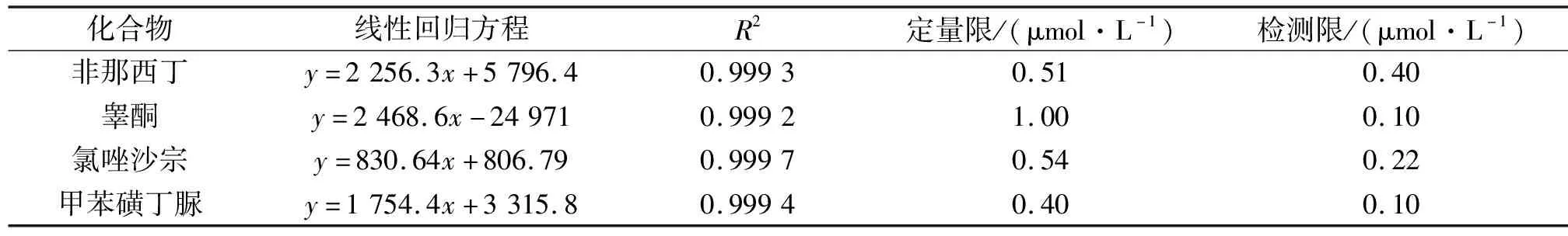
表3 线性回归方程
2.4.3 提取回收率和基质效应
提取回收率的测定:按照标准曲线中的浓度范围,选择高、中、低3个浓度配制混合底物探针样品,每个浓度平行3份,加入到于95 ℃水浴中加热5 min灭活后的人肝微粒体中,按2.2节条件进行孵育后得到T1样品,即正常孵育样品;灭活处理人肝微粒体按2.2节条件孵育后,加入同样配制的高、中、低3个浓度样品,每个浓度平行3份,得到T2样品,即不经孵育样品,将T1样品与T2样品浓度相除即可得到提取回收率。
基质效应的测定:按照标准曲线中的浓度范围,选择高、中、低3个浓度配制混合底物探针样品,每个浓度平行3份,加入到灭活后的人肝微粒体中,按2.2节样品前处理条件操作后得到J1样品,即基质样品;同样配制高、中、低3个浓度的样品,每个浓度平行3份,不加人肝微粒体,按2.2节样品前处理条件操作后,得到J2样品,即无基质样品,将J1样品与J2样品浓度相除即可得到基质效应。
各底物的提取回收率良好,没有明显的基质效应,且相对标准偏差值RSD均较低,结果如表4所示。

表4 回收率和基质效应
2.4.4 日内精密度和日间精密度
按照标准曲线中的浓度范围,选择高、中、低3个浓度配制混合底物探针样品,每个浓度平行6份,加入到灭活后的人肝微粒体中,按2.2节条件操作后进样,根据结果得到日内精密度;连续测定3 d后,根据结果计算得到日间精密度。各底物的日内精密度和日间精密度相对标准偏差值RSD均较低,结合相对准确度RE,说明该实验方法可靠准确,重现性较好,结果如表5所示。

表5 精密度和准确度
2.4.5 稳定性考察
按照标准曲线中的浓度范围,选择高、中、低3个浓度配制混合底物探针样品,每个浓度平行操作6份,加入到灭活处理后的人肝微粒体中,分别置于自动进样器中24 h,-4 ℃条件下冷藏24 h,冻融循环3次等条件下,均能保持稳定[21]。采用UPLC对4种探针底物药物进行检测的方法稳定、可靠,并具有较好的重现性,可用于评价本研究中的穿破石提取液质量浓度对CYP450酶的影响,对临床前的用药状况进行预测,确保用药的安全性。
2.5 穿破石对人肝微粒体CYP450酶的抑制作用
根据抑制效果,可将化合物分为有效抑制化合物,即IC50≤10 μmol/L或≤20 μg/mL;中等抑制化合物,即10 μmol/L≤IC50≤50 μmol/L或20 μg/mL≤IC50≤100 μg/mL;弱抑制化合物,即IC50≥50 μmol/L或≥100 μg/mL[22-23]。根据统计学软件GraphPad Prism 8.0.1对剩余底物峰面积的拟合计算结果,可以得到穿破石提取液质量浓度对CYP450各亚型酶的抑制效果,如图2所示。穿破石提取液对CYP1A2的IC50值为0.356 1 mg/mL,对CYP3A4的IC50值为0.332 4 mg/mL,对CYP2C9的IC50值为0.404 9 mg/mL,对CYP2E1的IC50值为0.861 5 mg/mL。

图2 穿破石提取液对人肝微粒体细胞色素P450酶4种亚型的抑制曲线
通过拟合计算,可得阳性抑制剂对4种CYP亚型酶的抑制曲线,如图3所示。α-萘黄酮对CYP1A2的IC50值为2.57×10-4mg/mL,酮康唑对CYP3A4的IC50值为9.21×10-3mg/mL,磺胺苯吡唑对CYP2C9的IC50值为1.95×10-3mg/mL,氯美噻唑对CYP2E1的IC50值为4.30×10-4mg/mL。4种阳性抑制剂的IC50均为参考值的正常范围内,该孵育体系符合肝微粒体抑制活性实验的要求。与阳性抑制剂对比,对4种人肝微粒体CYP450亚型酶来说,穿破石提取液均具有弱抑制性。

图3 阳性抑制剂对4种CYP亚型酶的抑制效果
以穿破石在处方中一天的总用量为30 g,以一天两次为例[16],则每次穿破石用量为15 g,按穿破石提取液制备时的提取率计算,水煎后最多能得到988.58 mg穿破石粗提物,按人体中的血液为5 L进行估算,可得血液中穿破石的质量浓度为0.197 7 mg/mL,与计算得到的IC50值相比,其质量浓度低于4种亚型酶的IC50值。从体外实验的数据来看,一方面,说明穿破石提取液并不会对CYP450酶产生较大的抑制效果;另一方面,说明当其与这4种亚型酶的底物药物联用时,不会对底物药物在肝中的代谢产生影响,底物药物用药治疗时,同时服用穿破石,仍然可以正常地清除底物药物,不会由于穿破石对CYP450酶的抑制活性而使底物药物在体内积累引起细胞毒性。
3 结 论
选择CYP1A2,CYP3A4,CYP2C9,CYP2E1 4种亚型酶为研究对象,研究穿破石提取液对CYP450酶的酶活性抑制效果。通过混合底物探针法,建立人肝微粒体体外孵育体系,采用超高效液相色谱作为检测手段,以剩余底物峰面积为指标进行计算,得到穿破石提取液对CYP450酶的抑制IC50值,并对含量测定方法进行方法学验证,证明该方法灵敏度较高,稳定性良好。与阳性抑制剂对比,可以看出:对这4种亚型酶来说,穿破石提取液均属于弱抑制化合物。当穿破石与4种亚型酶的底物药物进行联用时,不会因为影响到底物药物在体内的代谢,导致药物在体内积累产生毒性,而产生明显的药物-药物相互作用。本研究为穿破石在临床上的用药及药物联用安全提供了参考依据,同时,研究所采用的方法,也可用于其他药物临床前用药的评估,对于预测潜在的药物相互作用,规避用药风险,具有重要的意义。
