Box-Behnken响应面法优化盆炎灵颗粒的醇沉工艺研究
2020-10-09蔡霈郑艺王哲明
蔡霈 郑艺 王哲明

[摘要] 目的 优化盆炎灵颗粒的醇沉工艺。 方法 在单因素试验的基础上,以醇沉前液相对密度、乙醇终浓度与静置时间为考察因素,以绿原酸、芍药苷、阿魏酸、丹酚酸B、去甲异波尔定、甘草苷、延胡索乙素、落新妇苷的转移率与固体去除率的综合评分值为考察指标,采用基于Box-Behnken设计的响应面法优化盆炎灵颗粒的醇沉工艺。色谱条件:色谱柱为Agilent TC-C18(250 mm×4.6 mm,5 μm),流速1.0 mL/min,流动相A为乙腈,流动相B为0.2%磷酸水溶液,梯度洗脱(0~10 min,2% A;10~40 min,2%~12% A;40~80 min,12%~18% A;80~110 min,18%~25% A;110~120 min,25%~50% A),柱温30℃,检测波长200~400 nm。 结果 最佳醇沉工艺条件为醇沉前液相对密度1.13,乙醇终浓度60%,静置时间21 h。验证试验结果显示,综合评分的预测值与实测值相对偏差为0.7%。 结论 优化的醇沉工艺方法简单、操作简便且结果准确稳定,可为盆炎灵颗粒的制剂生产提供可靠的理论依据。
[关键词] Box-Behnken;响应面法;醇沉工艺;转移率;固体去除率
[中图分类号] R284.2 [文献标识码] A [文章編号] 1673-7210(2020)08(a)-0032-06
[Abstract] Objective To optimize the ethanol precipitation process for Penyanling Granules. Methods Based on the single factor test, the relative density of the liquid before ethanol precipitation, the final ethanol concentration and the ethanol precipitation time were used as factors. The transfer rates of chlorogenic acid, paeoniflorin, ferulic acid, salvianolic acid B, norisoboldine, liquiritin, tetrahydropalmatine, astilbin and the composite score of solid removal rate were selected as evaluation indexes. The ethanol precipitation process of Penyanling Granules was optimized by Box-Behnken response surface method. Chromatographic conditions: the column was Agilent TC-C18 (250 mm×4.6 mm, 5 μm), the flow rate was 1.0 mL/min. The mobile phase A was acetonitrile and the mobile phase B was 0.2% phosphoric acid solution with gradient elution (0-10 min, 2% A; 10-40 min, 2%-12% A; 40-80 min, 12%-18% A; 80-110 min, 18%-25% A; 110-120 min, 25%-50% A). The column temperature was 30℃ and the detection wavelength was 200-400 nm. Results The optimal ethanol precipitation process was as followed: the relative density of the extract was 1.13, and ethanol was added to allow the content of ethanol to reach 60%, and then been placed for 21 h. The test results indicated that the relative difference of comprehensive scoring value between predicated value and measured value was 0.7%. Conclusion The optimal ethanol precipitation process is simple, easy to operate and the results are accurate and stable, which can provide a reliable theoretical basis for the preparation production of Penyanling Granules.
[Key words] Box-Behnken; Response surface methodology; Ethanol precipitation process; Transfer rate; Solide removal rate
盆炎灵颗粒是已在湖南省妇幼保健院临床使用20年的中药复方制剂,由醋延胡索、香附、败酱草、丹参、茯苓等多味中药材组成,具有通畅血脉、消散瘀滞、消炎镇痛等功效,主要用于妇科盆腔炎性疾病的治疗[1]。中药制剂的醇沉工艺是在制剂过程中应用不同浓度乙醇将其除杂、精制有效成分的关键步骤,具有工艺成熟、操作简便、设备简单等优点,能够减少患者日服用剂量,增加患者顺应性,同时减少颗粒的吸湿性,使其成型性更好,增加制剂的稳定性,延长储存时间[2-5]。由于中药成分复杂,对于中药复方的醇沉工艺研究需要在处理过程中同时考虑多味药材的有效成分含量以及固体去除率的变化。本试验采用基于Box-Behnken的星点设计-结合响应面法[6-9],以醇沉后样品中绿原酸、芍药苷、阿魏酸、丹酚酸B、去甲异波尔定、甘草苷、延胡索乙素、落新妇苷的转移率和固体去除率的综合评分值为考察指标,优化盆炎灵颗粒的醇沉工艺,为规范盆炎灵颗粒的生产工艺以及后续的研究提供理论依据。
1 仪器与试药
1.1 仪器
LC-10AT高效液相色谱系统(日本岛津公司),SPD-M20A检测器(日本岛津公司),SB25-12DTN超声波清洗机(宁波新芝生物科技股份有限公司),DZF-6050型真空干燥箱(上海三發科学仪器有限公司),TDZ4-WS低速台式离心机(长沙湘仪离心机仪器有限公司),Mettler Toledo XS205型电子分析天平(德国梅特勒-托利多公司,精度万分之一),0.22 μm微孔滤膜(美国密理博公司)。
1.2 药材、药品与试剂
盆炎灵颗粒处方中各味药材从湖南衡东县中药饮片厂购买,当归(20170316,甘肃)、丹参(20170626,河北)、大血藤(20170317,湖南)、乌药(20170318,安徽)、败酱草(20170316,湖南)、赤芍(20170316,四川)、三棱(20170317,广西)、醋延胡索(20170316,浙江)、醋香附(20170319,安徽)、甘草(20170316,内蒙古)、土茯苓(20170316,广东)经湖南省中医院王竹鑫主任药师鉴定,均符合《中华人民共和国药典》[10]中各项规定。
8种标准物质为绿原酸、去甲异波尔定、芍药苷、阿魏酸、甘草苷、落新妇苷、延胡索乙素、丹酚酸B(中国食品药品检定研究院,批号分别为110753-201411、111825-201402、110736-201604、110773-201614、111610-201106、111798-201504、110726-201617、111562-201212,纯度≥98%,用于含量测定);乙腈(色谱纯)、甲醇(色谱纯)为蒸馏水自制,其余试剂均为国产分析纯。
2 方法与结果
2.1 绿原酸、去甲异波尔定、芍药苷、阿魏酸、甘草苷、落新妇苷、延胡索乙素、丹酚酸B的含量测定
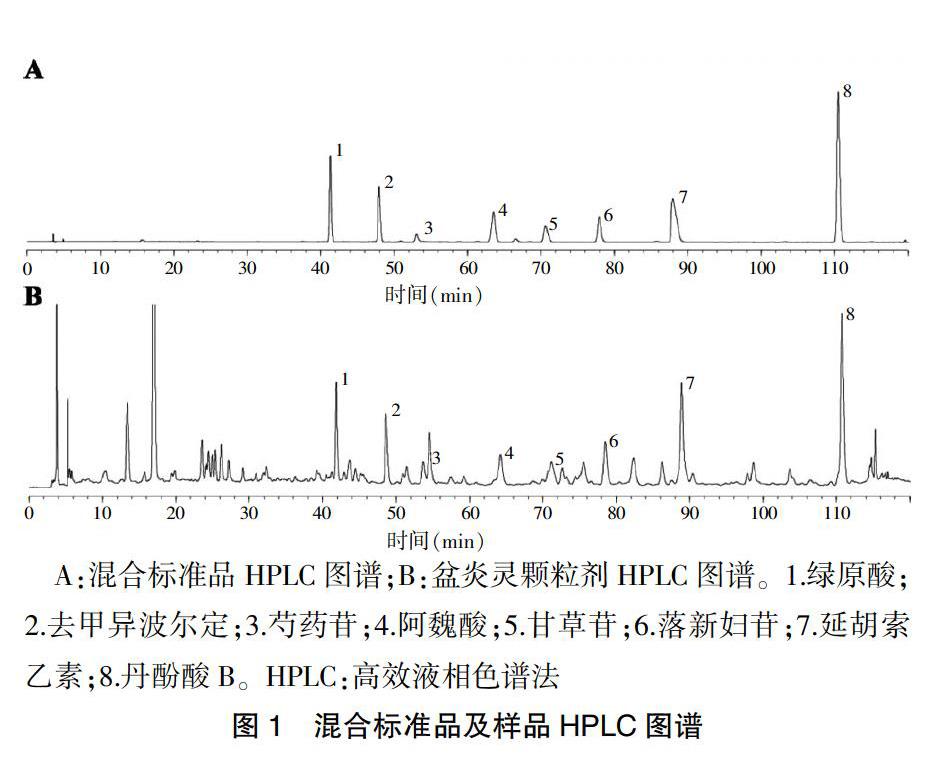
2.1.1 色谱条件 色谱柱:Agilent TC-C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.2%磷酸水溶液(B);梯度洗脱:0~10 min,2% A;10~40 min,2%~12% A;40~80 min,12~18% A;80~110 min,18~25% A;110~120 min,25~50% A;流速:1.0 mL/min;柱温:30℃;检测波长:200~400 nm(绿原酸:327 nm;阿魏酸:316 nm;甘草苷:237 nm;芍药苷:230 nm;延胡索乙素:280 nm;去甲异波尔定:280 nm;丹酚酸B:286 nm;落新妇苷:291 nm);进样量:10 μL[11]。混合标准品及样品的HPLC图谱见图1。
A:混合标准品HPLC图谱;B:盆炎灵颗粒剂HPLC图谱。1.绿原酸;2.去甲异波尔定;3.芍药苷;4.阿魏酸;5.甘草苷;6.落新妇苷;7.延胡索乙素;8.丹酚酸B。HPLC:高效液相色谱法
2.1.2 对照品溶液配制 精密称取绿原酸、芍药苷、去甲异波尔定、甘草苷、落新妇苷、延胡索乙素、丹酚酸B、阿魏酸标准物质适量,加甲醇分别配制成浓度为1.721、3.111、0.415、0.239、0.345、0.694、2.686、0.168 mg/mL标准对照品溶液,用0.22 μm微孔滤膜滤过即为对照品溶液。取上述8种对照品置于同一容量瓶中,以甲醇定容,混合液中各对照品浓度与上述标准对照品溶液相同,即得混合对照品溶液。各标准曲线制作、精密度、重复性、稳定性以及加样回收率试验已在相关研究[12]中完成,均符合要求。
2.1.3 供试品溶液的制备 量取盆炎灵提取液或醇沉上清液适量,相当于生药材25 g,置于25 mL的锥形瓶中,加入甲醇定容,摇匀,转速5000 r/min,离心半径为10 cm,离心10 min,上清液用0.22 μm微孔滤膜滤过,即为供试品溶液。
2.2 物质转移率的测定
取“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件测定绿原酸、芍药苷、去甲异波尔定、甘草苷、落新妇苷、延胡索乙素、丹酚酸B、阿魏酸的物质量,并按下式计算各物质的转移率。转移率=醇沉上清液中物质量/盆炎灵提取液中物质量×100%。
2.3 固体去除率的测定
精密吸取盆炎灵提取液或醇沉上清液适量(相当于生药材25 g),置于已干燥至恒定质量的蒸发皿中,水浴蒸干后于105℃干燥3 h,置于干燥器中冷却30 min,恒重后精密称定质量,计算固体去除率。固体去除率=(盆炎灵提取液干膏质量-醇沉上清液干膏质量)/盆炎灵提取液干膏质量×100%。
2.4 单因素考察
单纯以各有效物质转移率或固体去除率来评价醇沉工艺的优劣,可能会出现有效物质与杂质同时保留或去除的情况,难以得到合理的结果。因此在本研究中,采用多指标综合评价法对盆炎灵提取液醇沉工艺进行综合评价。中药水提液醇沉工艺权重系数的设计应当在优先保留有效成分的前提下,尽可能多地去除杂质,故设置固体去除率权重系数为40[13-14]。绿原酸、芍药苷、去甲异波尔定、甘草苷、落新妇苷、延胡索乙素、丹酚酸B、阿魏酸的转移率权重系数均为7.5(各标准物质权重系数相等),在此基础上进行综合评分。
利用综合评分值(P)对试验结果进行分析:以Y表示试验中指标成分的测定值(绿原酸、芍药苷、去甲异波尔定、甘草苷、落新妇苷、延胡索乙素、丹酚酸B、阿魏酸的转移率及固体去除率的测定值分别为Y1、Y2、Y3、Y4、Y5、Y6、Y7、Y8、Y9),Z表示指标成分的测定值的标准化数据(Z=Y/Ymax)[9],综合评分值P=(Z绿原酸+Z芍药苷+Z去甲异波尔定+Z甘草苷+Z落新妇苷+Z延胡索乙素+Z丹酚酸B+Z阿魏酸)×7.5+Z固体去除率×40。
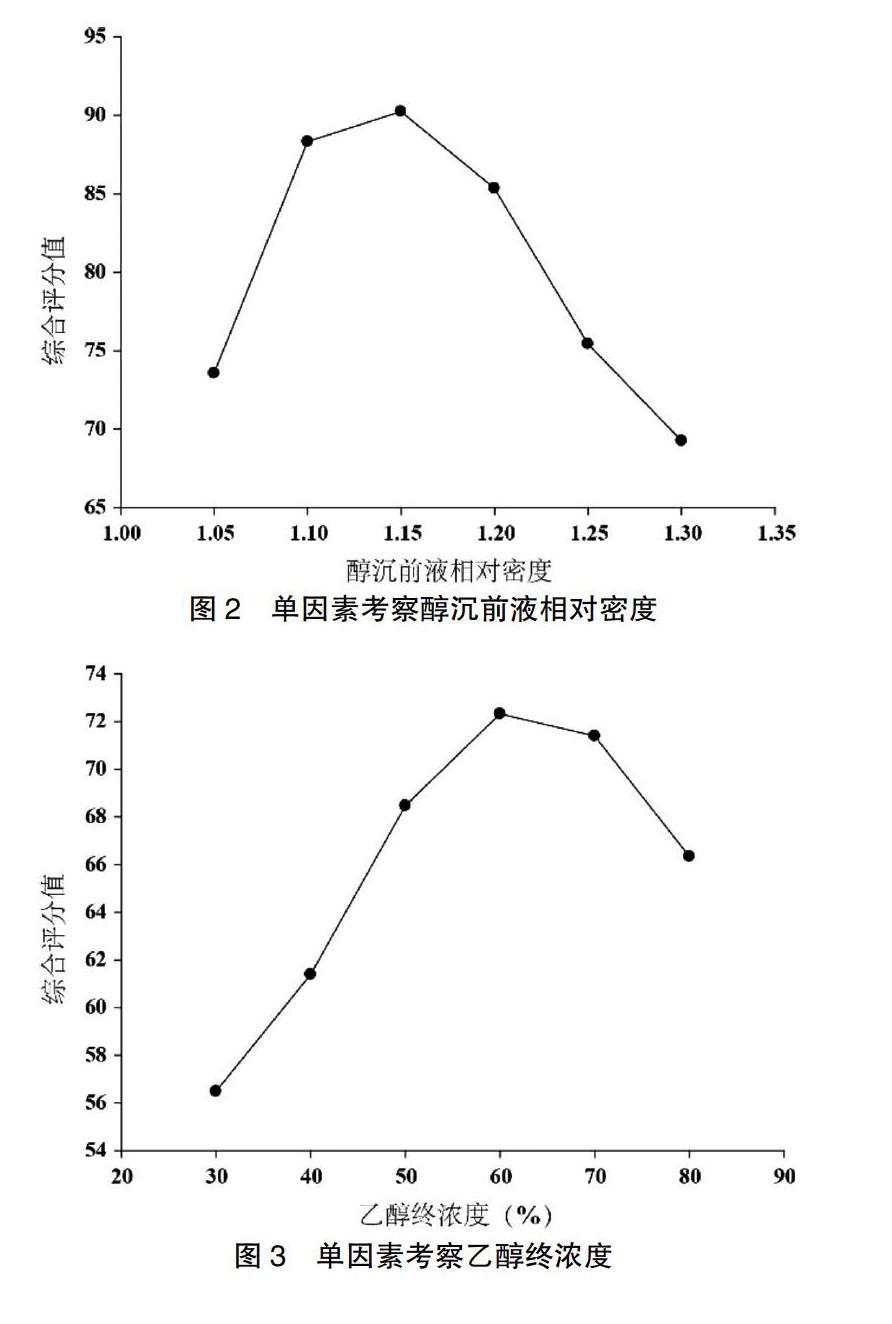
2.4.1 醇沉前液相对密度 在乙醇终浓度为60%、静置时间为24 h的情况下,考察醇沉前液相对密度分别为1.05、1.10、1.15、1.20、1.25、1.30。将醇沉上清液按照“2.1.3”项下方法制备成供试品溶液后进行分析,按“2.2”項下方法测定绿原酸、芍药苷、去甲异波尔定、甘草苷、落新妇苷、延胡索乙素、丹酚酸B、阿魏酸的转移率,按“2.3”项下方法测定固体去除率,并按综合评分法进行计算。以醇沉前液相对密度1.15时,综合评分最高。见图2。
2.4.2 乙醇终浓度 在醇沉前液相对密度为1.15、静置时间为24 h的情况下,考察乙醇终浓度分别为30%、40%、50%、60%、70%、80%。将醇沉上清液按照“2.1.3”项下方法制备成供试品溶液后进行分析,按“2.2”项下方法测定绿原酸、芍药苷、去甲异波尔定、甘草苷、落新妇苷、延胡索乙素、丹酚酸B、阿魏酸的转移率,按“2.3”项下方法测定固体去除率,并按综合评分法进行计算。以乙醇终浓度为60%时,综合评分最高。见图3。
2.4.3 静置时间 在醇沉前液相对密度为1.15、乙醇终浓度为60%的情况下,考察静置时间分别为4、8、16、24、32、40 h。将醇沉上清液按照“2.1.3”项下方法制备成供试品溶液后进行分析,按“2.2”项下方法测定绿原酸、芍药苷、去甲异波尔定、甘草苷、落新妇苷、延胡索乙素、丹酚酸B、阿魏酸的转移率,按“2.3”项下方法测定固体去除率,并按综合评分法进行计算。当静置时间达到16 h时后,随着时间延长,综合评分值无明显变化。见图4。
2.5 Box-Behnken响应面法优化提取条件
2.5.1 Box-Behnken响应面法试验设计与试验结果 经上述单因素试验确定考察因素分别为A(醇沉前液相对密度)、B(乙醇终浓度,%)、C(静置时间,h)。采用3因素3水平的Box-Behnken响应面分析法进行试验设计,考察因素与考察水平见表1。
按照前述评分方法,利用P对试验结果进行评分。Box-Behnken响应面法试验设计与试验结果见表2。
应用Design-Expert 10.0软件对各试验的综合评分值进行回归分析,得到回归方程为:P=89.84-0.077A+5.64B+2.34C+5.90AB-2.32AC-4.36BC-2.90A2-20.24B2-1.45C2(R2 = 0.9986)。方程中一次项的系数绝对值表明各因素对综合评分值的影响程度。由上述回归方程可知,各考察因素对盆炎灵醇沉工艺的影响程度为B>C>A。对回归方程进行回归统计方差分析,见表3。
用F检验来判定回归方程中各考察因素对综合评分值的影响,概率P < 0.01时为高度显著影响,概率P < 0.05时为显著影响。由表3可知,模型概率P < 0.01,提示该模型具有高度显著性,R2 = 0.9986,提示模型拟合程度好。应用Design-Expert 10.0软件考察醇沉前液相对密度、乙醇终浓度和静置时间的两两相互作用对醇沉工艺的影响,绘制了该实验条件的响应面图,得到3个开口向下的凸形曲面。考察的3个因素与盆炎灵颗粒醇沉工艺综合评分值呈抛物线关系,并且在考察的实验条件范围内,存在着响应值的极大值。见图5。
经过中心组合设计优化醇沉条件,最优工艺条件:醇沉前液相对密度1.125、乙醇终浓度60.83%、静置时间21.10 h。
2.5.2 验证试验 参照上述最优醇沉工艺,并结合试验条件的可操作性,调整为醇沉前液相对密度1.13,乙醇终浓度60%,静置时间21 h,综合评分值为90.8773。按照该优化工艺进行3批次醇沉验证试验,结果综合评分值为90.2759,与预测值比较,相对偏差为0.7%(<5%)。见表4。
3 讨论
本研究首先通过单因素试验初步筛选使各因素水平能够在星点设计范围之内,以提高试验设计的精确性;之后采用Box-Behnken响应曲面分析法,建立盆炎灵颗粒纯化工艺的二次回归数学模型,并分析了各因素对响应值的影响。中药醇沉工艺的探索中,常用正交试验来进行研究,但正交试验仅能给出最佳因素水平组合,不能优化出更好的条件[15-17],而Box-Behnken响应曲面分析法能够通过对试验结果进行数据拟合,构建影响因素与响应值之间的拟合模型,从而推算出最佳工艺条件。对于多因素试验研究,Box-Behnken响应面法是最佳的分析方法[18-21]。从上述试验结果可知,本研究中所建立的数学模型拟合程度高,试验误差小。最佳的盆炎灵颗粒醇沉纯化工艺条件:醇沉前液相对密度1.13、乙醇终浓度60%、静置时间21 h。在此醇沉条件下盆炎灵颗粒中各主要有效物质的转移率均>70%,且与预测值相差较小。由响应面法优化得到的盆炎灵颗粒醇沉工艺参数准确、可靠,说明该数学模型具有指导工业生产的意义。对所选取指标进行了合理的权重系数分配,使得有效物质转移率结合固体去除率的综合评分更加合理,为盆炎灵颗粒制剂生产的工艺优化提供参考依据。
[参考文献]
[1] 欧阳波,潘涛,王秀梅,等.盆炎灵颗粒的提取工艺研究[J].中国医药指南,2013,11(10):3-6.
[2] 施晓虹,杨日昭,赵立杰,等.醇沉处理前后中药水提液理化性质的变化及其与喷雾干燥黏壁的关系[J].中国中药杂志,2020,45(3):328-335.
[3] 陈路,吴无畏,唐炳兰,等.板山岗颗粒药材提取工艺优化研究[J].中国药业,2020,29(1):20-22.
[4] 朱智德,罗宇东,肖明,等.十味鹅黄颗粒的醇沉及干燥工艺研究[J].中国当代医药,2018,25(25):11-15.
[5] 晏晨,丁丽馨,张卫青,等.枳茵益子安母颗粒醇沉工艺的优化[J].中成药,2018,40(7):1630-1632.
[6] 王永香,米慧娟,张传力,等.Box-Behnken响应面法优化热毒宁注射液金银花和青蒿(金青)的醇沉工艺研究[J].中草药,2015,46(5):671-678.
[7] 邵晶,孙政华,郭玫,等.Box-Behnken设计-响应面法优化参芪复方总多糖醇沉工艺[J].中国医药工业杂志,2016, 47(8):1012-1015.
[8] 肖兰英,刘洋,吴东,等.多指标综合评分法优选黄芪通便颗粒水提醇沉工艺[J].江西中医药,2019,50(435):57-61.
[9] 王连红,张建梅,都玲玲,等.Box-Behnken设计优化蔓荆子总黄酮DES提取工艺研究[J].山东林业科技,2019, 49(6):13-15.
[10] 国家药典委员会.中华人民共和国药典[S].一部.北京:中国医药科技出版社,2015.
[11] 蔡霈,肖作奇,潘涛,等.HPLC法检测不同干燥方式与温度对盆炎灵颗粒主要有效成分的影响[J].中医药导报,2018,24(22):57-61.
[12] 肖作奇,潘濤,欧阳波,等.盆炎灵颗粒HPLC指纹图谱研究[J].中国新药杂志,2015,24(16):1897-1901.
[13] 林传权,莫全毅,刘佳,等.胃乃安新制剂的醇沉工艺优化[J].中国新药与临床药理,2013,24(5):514-518.
[14] 袁佳,李页瑞,陈勇,等.多指标正交设计优选丹参水提液醇沉工艺[J].中国医药工业杂志,2010,40(11):826-829.
[15] 王文平,倪健,冷新,等.多指标正交试验优化芪蛭益肺颗粒水提醇沉工艺[J].中国中医药信息杂志,2018,25(9):71-75.
[16] 潘艳琳,韩莹,李劭,等.藿砂颗粒剂的澄清工艺研究[J].海峡药学,2019,31(12):6-9.
[17] 何艳春,莫秋瑜,黄瑞松,等.正交试验优化十味参归灌肠液的水提醇沉工艺研究[J].广西医科大学学报,2019, 36(11):1843-1846.
[18] 万丹娜,饶倩如,俞梦莹,等.Box-Behnken设计-响应面法优化山楂的醇沉工艺[J].中国药房,2018,29(15):2078-2081.
[19] 李永祝,文远大,余俊,等.Box-Behnken设计-效应面法优选清咽爽喉颗粒醇沉工艺研究[J].湖南中医杂志,2017,33(6):165-167.
[20] 马馨桐,肖凤琴,邱明阳,等.多指标综合评分法优选复方降脂缓释片的水提醇沉工艺及活性研究[J].中国医院药学杂志,2019,39(17):1759-1765.
[21] Box-Behnken响应面法结合多指标综合加权法优选升麻中酚酸类成分的提取工艺[J].中国药房,2016,27(13):1835-1838.
(收稿日期:2019-12-13)
