血氧水平依赖功能磁共振成像联合扩散张量成像技术在脑肿瘤外科治疗中的价值
2020-09-02赵凌倩
王 乐,赵凌倩
手术切除是目前脑肿瘤的首选治疗方法,对于发生在脑功能区附近或直接侵犯到脑功能区的肿瘤,外科治疗目标是最大限度地切除肿瘤并保护神经功能,以提高病人术后的生存质量[1]。因此,术前能准确地判断脑肿瘤与重要功能区的关系在脑肿瘤的外科治疗中至关重要。磁共振成像(magnetic resonance imaging,MRI)具有高空间分辨率和高组织分辨率特点,已经成为脑肿瘤的主要诊断手段,其中血氧水平依赖功能磁共振成像(blood oxygenation level dependent-functional magnetic resonance imaging,BOLD-fMRI) 通过血氧饱和度的对比变化来反映脑神经功能活动情况,因此,可无创地对脑功能区进行定位,除准确定位大脑皮层脑功能区外,皮层下纤维束保护对神经功能保存也同样起着非常重要的作用。扩散张量成像(diffusion tensor imaging,DTI)是目前唯一能活体显示脑白质纤维束(corticospinal tract,CST)的方法,可以清晰显示纤维束的形态、走行及方向。Pillai等[1]应用BOLD- fMRI、DTI技术及术中超声辅助神经导航结合神经电生理监测帮助术前正确评估肿瘤、锥体束和皮层激活区之间关系,从而制订合理手术方案,并在术中直观指导。本研究分析2018年1月—2020年3月山西医科大学第一医院神经外科收治的病灶累及M1区的脑肿瘤病人25例临床资料,旨在探索BOLD-fMRI与DTI技术在脑肿瘤外科治疗中的联合应用价值。
1 资料与方法
1.1 临床资料 收集2018年1月—2020年3月在山西医科大学第一医院神经外科收治的脑肿瘤病人25例(脑肿瘤组),其中男11例,女14例;年龄40~73岁,平均61岁。按照肿瘤种类分为3组,星形细胞瘤组(11例),转移瘤组(6例),脑膜瘤组(8例)。入组标准:常规MRI检查证实肿瘤位于幕上中央沟附近,并累及相邻手运动皮层功能区;所有病人均经手术病理证实;病人意识清醒,有一定自控能力和交流能力,能配合MRI扫描;患肢肌力为Ⅱ级以上,能进行双手简单运动;无持续性癫痫发作史;为了排除利手因素的影响,所有病人均为右利手。
选取与病人年龄、性别相匹配的10名正常人作为对照组,其中男5名,女5名,年龄25~70岁,平均52岁。正常对照组选择标准:意识清楚,无任何脑部疾病和手术史,无四肢运动障碍史,均为右利手。
1.2 仪器与方法
1.2.1 BOLD-fMRI任务模式 采用组块(BLOCK)设计,以拇指与其余四指的对指运动为刺激任务,刺激和休息的呈现时间为30 s,运动频率均为2 Hz,各重复3次,呈现顺序为ARARARARARAR (rest,R;active,A)。详见图1。健侧手的运动作为对照,采用任务模式与患侧手相一致。
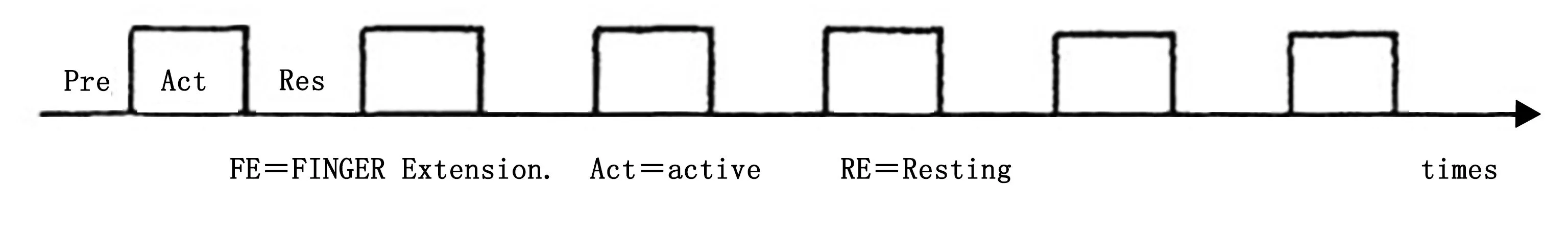
图1 Block运动模式图
检查前对病人及健康者进行充分交流及适应性训练,争取受检者最大程度配合。在检查前,告知病人及健康者对指运动的节奏、频率及周期,进行训练以确保观察者熟悉任务;并告知其在检查过程中需集中注意力,尽可能排除其余杂念;同时,注意保持头部的绝对静止,尽量减少吞咽运动,除了手的运动外,躯体其余部位尽可能放松保持不动。检查过程中,用海绵衬垫填塞受检者头部与线圈间隙,并用绷带固定头部,身下垫泡沫软垫。
1.2.2 成像设备及参数 使用美国GE公司HDxt 3.0T超导磁共振扫描仪,头颈联合线圈(8通道),病人仰卧位,所有BOLD及DTI扫描均在增强扫描前进行。常规T1WI扫描参数:扫描基线与前后联合的连线平行,范围从颅底至颅顶,共20层。层厚 3 mm,FOV 240 mm,TR/TE=3 000/40 ms。BOLD-fMRI扫描参数:采用梯度回波-回波平面成像(GRE-EPI)序列,基线及层厚与T1WI参数相同,翻转角90°,矩阵96 cm×96 cm, FOV=240 mm,NEX=1。总扫描时间384 s,其中,预扫描24 s;运动、静止交替6次,共360 s。DTI扫描参数:使用扩散敏感单次激发平面回波序列行轴位扫描,覆盖整个大脑半球和脑干,TR/TE=12 000/ Minimum ms,FOV=240 mm 扫描层数36层,层厚3 mm,无间隔,b值分别取0、1 000 mm2/s,在15个方向施加梯度脉冲,得到原始图像后传至工作站进行处理。高分辨率全脑结构图像:采用FSPGR序列, TE: Minimum?翻转角:25 层厚2.0 mm,矩阵256×256,NEX=1.0,FOV=240 mm。扫描范围从延髓下部到大脑半球顶部颅板下全脑范围。
1.2.3 数据处理
1.2.3.1 BOLD-fMRI图像后处理及分析 将BOLD-fMRI原始图像数据传输到离线工作站,使用基于Matlab平台的SPM软件进行预处理。预处理过程包括:①头动校正(realign),目的是检测受试者头部在三维平移和三维旋转上的空间变化,并对其进行校正,本研究剔除超出运动校正标准(头部三维平移<1.5 mm和三维旋转<1.5°)的数据,以克服头部运动对实验结果的影响(见图2);②配准(coregister),将BOLD图像与高分辨T1WI全脑结构图进行配准,保证功能像与解剖像的准确吻合(见图3);③平滑(smooth),采用统一的三维高斯过滤对图像进行空间平滑处理,平滑核的半高宽设为6 mm,以降低空间噪声。
经过处理获得激活图,在激活图内测量感兴趣区的总激活像素数,并将激活图与解剖图相叠加。数据测量指标包括脑瘤侧和非脑瘤侧M1区BOLD信号范围、强度。首先,为了避免由于个体差异导致的M1区(也称初级运动区,the primary motor cortex,PMA)的
BOLD信号激活强度(T值)和范围(V值)的差距较大,将测定的每个人左右两侧大脑半球Ml区BOLD信号的T值和V值进行标准化处理,得出相对激活强度值(relative activation T value,rT)和相对激活范围值(relative activation V value,rV)。之后,分别对正常组和脑肿瘤组进行处理。对于正常组,采用左右两侧大脑半球M1区BOLD信号T值和V值比值的均值,得出正常人的rT值和rV值;对于脑肿瘤病人,假设由于脑肿瘤对手运动区的影响,肿瘤侧的激活强度和范围同非肿瘤侧存在差异,因此,采用肿瘤侧M1区BOLD信号的T值和V值和非肿瘤侧相比,得出rT值和rV值。即rT=肿瘤侧T值/非肿瘤侧T值;rV=肿瘤侧V值/非肿瘤侧V值。最后,当脑区活动水平在体素水平满足阈限P<0.1且k>5个体素时,不同组间该区域的激活值比较有统计学意义。
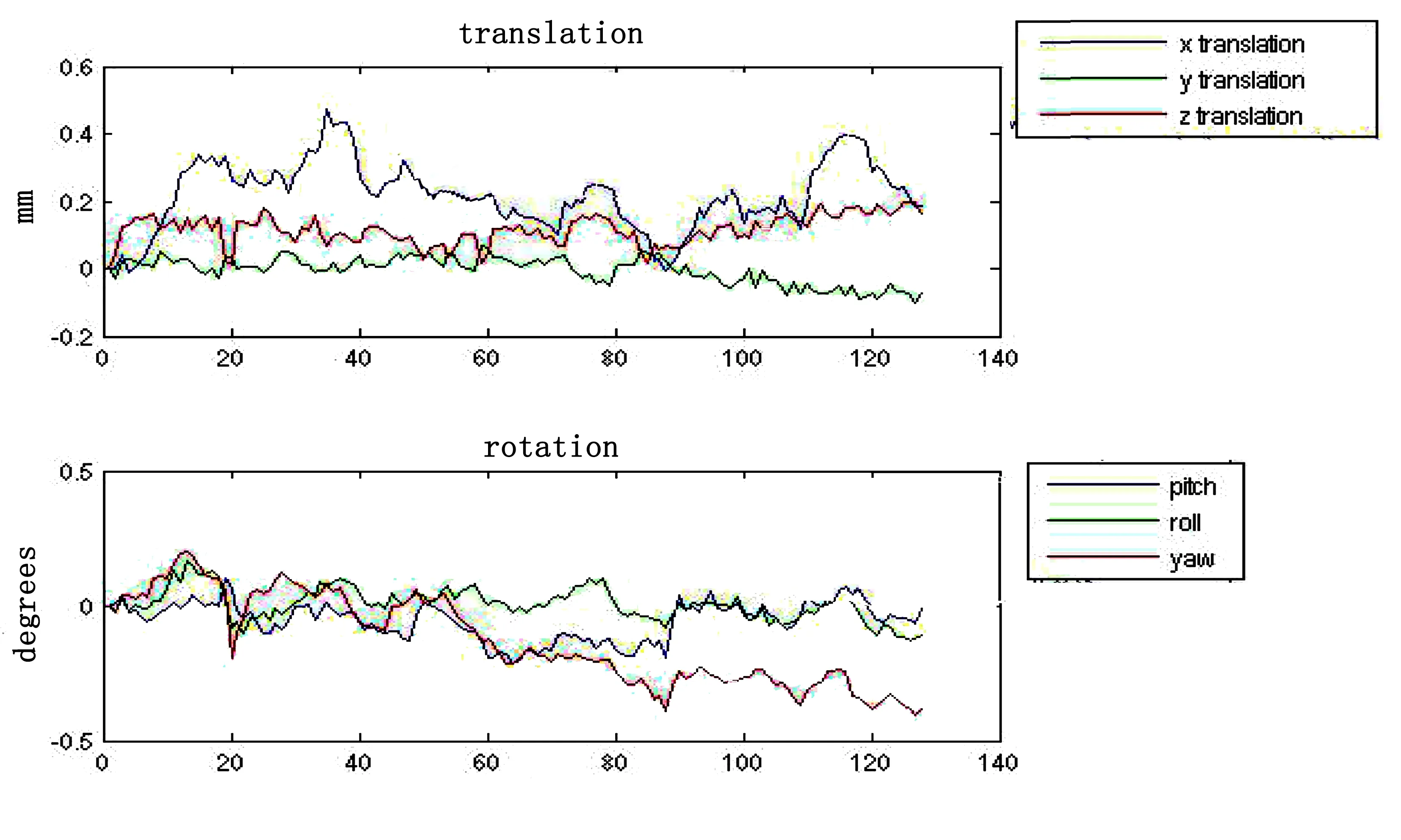
图2 运动校正
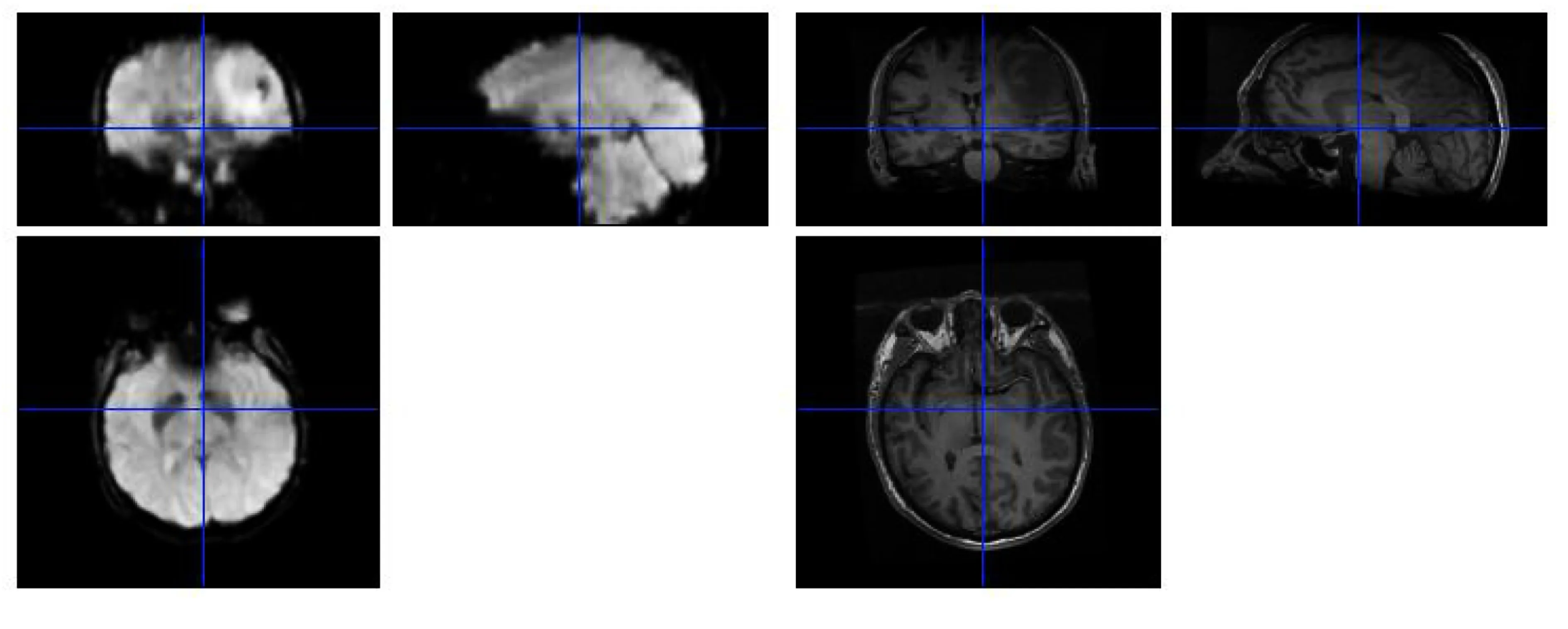
图3 图像配准
1.2.3.2 DTI数据处理及分析 将DTI原始图像数据传输至PC机,应用GE ADW4.4工作站及配套DTI处理软件,显示FA图及彩色编码方向(directionally encoded color map, DEC)图。并由两位医生在DEC图或FA图的基础上进行CST的3D纤维束成像。在脑桥基底部设置ROI,重建双侧CST。根据FA图、DEC图及3D纤维束图综合评价观察CST的移位及破坏情况。皮质脊髓束(CST)改变分为4种基本形式,破坏:CST纤维中断消失,失去其方向性及完整性;浸润:与健侧对照,纤维部分中断,位置和形态异常,FA信号降低,但DEC图方向可以辨认;移位:与健侧对照,纤维位置和形态发生改变,但FA信号正常;完整:CST保持其方向性及完整性。
1.3 统计学处理 采用SPSS 16.0 统计软件进行检验。多组间采用单因素方差分析,分析不同类型的脑肿瘤组与正常组间M1区BOLD信号rT和rV差异。当组间存在差异时,两两比较采用LSD-t检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 正常人手运动功能区(hand representation area, HRA)位置和形态 中央沟呈延长的斜行S状,分为内侧部、膝部和外侧部,膝部又分为3个曲度,两个凸向前,1个凸向后,在轴位上呈倒Ω形,其前方与之对应的即是HRA,HRA位于中央前回呈一柄形或钩状结构,在轴位上呈ω或倒Ω形。详见图4。
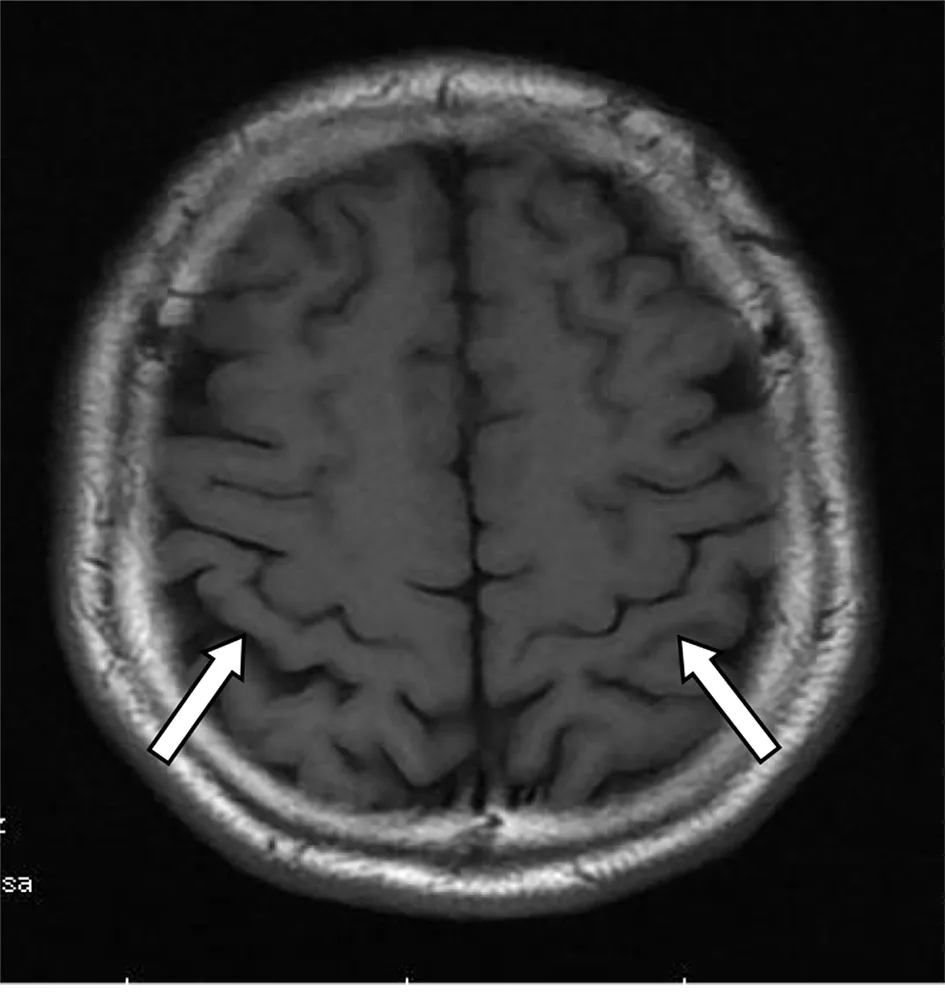
图4 HRA在轴位上呈ω或倒Ω形(箭头)
2.2 BOLD-fMRI结果分析脑肿瘤对邻近手运动功能区的影响 所有病人患侧和健侧的M1区均有激活,健侧M1区呈曲柄状、条状及不规则形等表现,位于中央沟附近,与脑回走行大体一致。患侧M1区形态变化较大,主要表现为:呈散在的斑点状;体积稍缩小或无明显改变,或被推挤移位;形态位置正常呈曲柄状、线条状。
2.2.1 不同肿瘤组间rV比较(见表1) 各组间rV比较差异有统计学意义。两两比较结果显示:正常组与星形细胞瘤组、正常组与转移瘤组、星形细胞瘤组和转移瘤组、脑膜瘤组与转移瘤组之间比较差异有统计学意义。
表1 各组间rV比较(±s)
P<0.05;与转移瘤组比较,③P<0.05。
2.2.2 不同肿瘤组间rT比较(见表2) 各组之间rT比较差异无统计学意义,不同肿瘤激活强度一样。
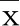
表2 各组间rT比较(±s)
2.3 DTI结果分析脑肿瘤对邻近皮质脊髓束的影响 皮质脊髓束受压、移位,在各组脑肿瘤中表现一致,部分病例皮质脊髓束受到破坏,失去正常形态。详见表3。
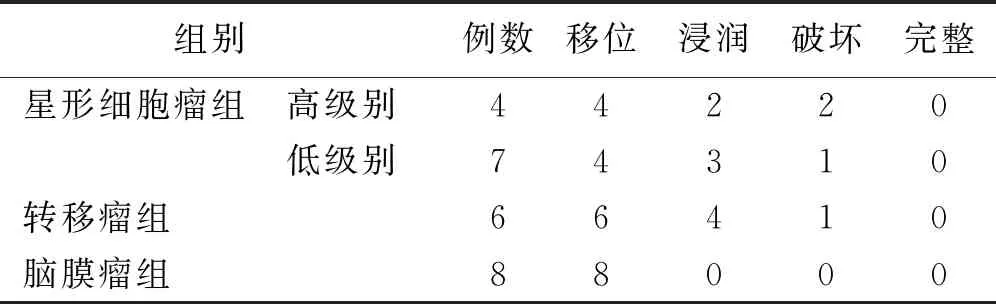
表3 各组脑肿瘤对邻近皮质脊髓束的影响 单位:例
2.4 典型病例影像资料分析 病例[1],男,46岁,左侧肢体活动不利6个月,右顶部镰旁脑膜瘤。详见图5、图6。病例[2],男,左上肢麻木半月,右颞叶星形细胞瘤Ⅲ级。详见图7、图8。
图5 病例[1]手运动脑皮层激活图
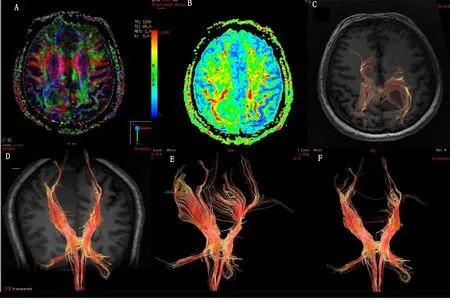
图6 病例[1]皮质脊髓束显示图
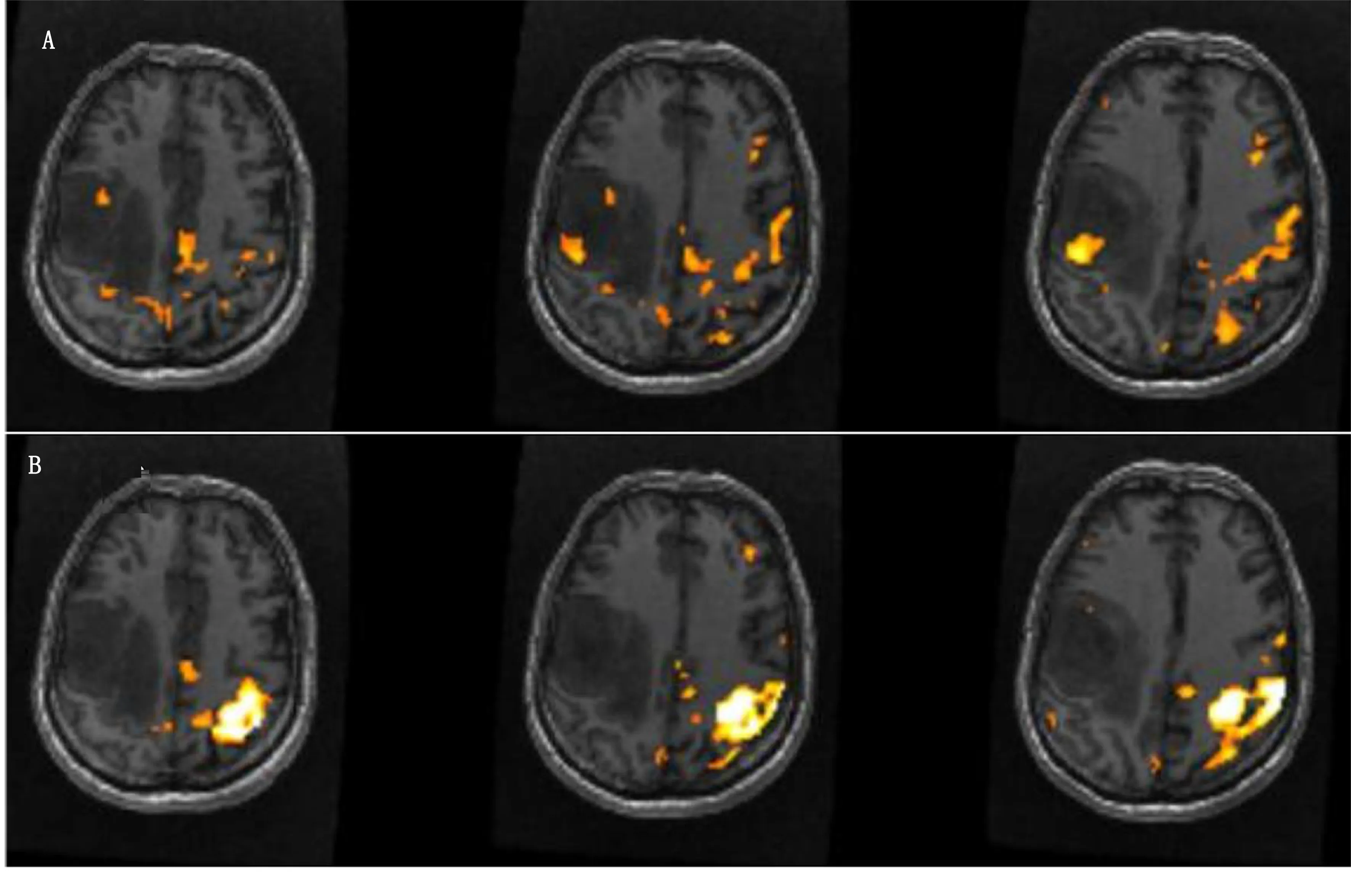
图7 病例[2]手运动脑皮层激活图
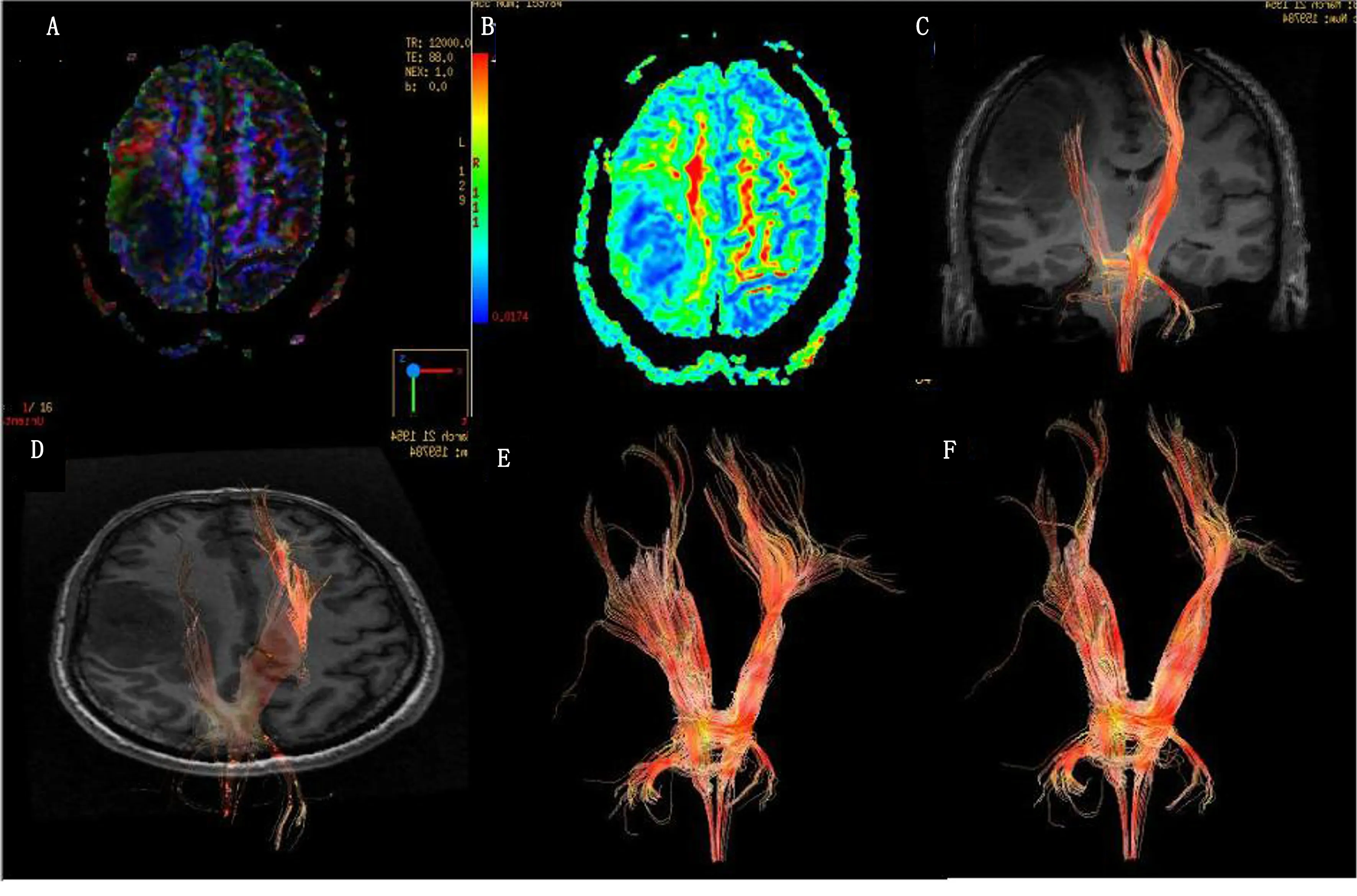
图8 病例[2]皮质脊髓束显示图
2.5 手术切除情况及术后致残率比较 肿瘤组25例中,肿瘤全切23例,次全切2例,完整切除率为92.00%。术中均成功避开手运动皮层激活区及周围皮质脊髓束进行手术入路设计及肿瘤切除。术后手运动障碍1例,其余24例病人手肌力仍为Ⅱ级以上,致残率为4.00%。
3 讨 论
为了避免生长在脑功能区附近或直接侵犯到脑功能区的肿瘤病人术后发生偏瘫的风险,术前一方面需要识别病人的大脑皮层运动区,并判断与肿瘤的位置关系,从而辅助确定开颅的位置;另一方面需要了解病人的皮质脊髓束走行和形态,明确冠辐射的哪一部分实际上携带着运动束及其与肿瘤的关系,进一步规划肿瘤切除范围[2]。这些脑重要功能区以及白质纤维束的术前准确识别可有效指导手术方案的制定,辅助实现肿瘤最大风范围安全切除。
目前,术中皮层电刺激(electrical cortexes stimulation,ECS)被认为是对于脑功能区定位的金标准[3],但这种方法具有创伤性,且手术时间长,对麻醉的要求较高,大大限制了其在临床中的应用;大部分情况下依靠外科医生术中根据解剖学标志来判断,但由于个体间存在差异及病变可导致邻近脑功能区移位、变形或显示不清,使得传统依赖解剖学经验定位大脑皮层功能区方法不可靠[4]。
BOLD-fMRI作为一种新的技术手段,可以通过脑功能区血氧饱和度的对比变化来反映脑神经功能活动情况,可无创地定位脑功能区,这也引起了研究者的关注,进行了大量研究比较了术前 BOLD-fMRI和ECS在定位脑功能区方面的效果,结果提示两者间有着较高的一致性,认为 BOLD-fMRI可以替代ECS对皮层功能区进行准确定位[5-10]。本研究主要关注病人的手运动功能,通过任务态fMRI进行显示,结果所有病人手运动皮层区(M1区)显示良好,并且呈不同激活形态和范围:高级别胶质瘤病人患侧激活区呈弥散分布,可能与肿瘤的占位效应使大脑皮层功能发生重组有关[11],而脑膜瘤病人的运动皮层内激活区呈明显受压缩小改变。本研究结果与前人的研究结果一致:Roux等[12]对17例肿瘤位于运动皮层区的病人进行BOLD-fMRI检查,发现病人肿瘤呈浸润性生长,运动皮层激活区明显移位,其移位程度与肿瘤浸润程度有关;金晓等[13]对发生于额顶叶的胶质瘤病人进行术前BOLD-fMRI评价,发现胶质瘤可引起中央沟及附近功能区面积及位置的变化,并认为这种因胶质瘤引起的功能区面积减小及移位,是主要运动功能区损伤后的适应性反应。至于激活程度,本研究结果显示,病人与正常者比较差异无统计学意义,而高万军等[14]研究结果则认为脑肿瘤的级别是影响M1区激活强度的主要因素,因此,后续将扩大样本量进行进一步的研究。
对于皮质脊髓束的显示,DTI是目前唯一可以无创性地显示活体白质纤维束的检查技术,能够直观地显示白质纤维束的形态和位置,对术前评估纤维束的受累情况起着至关重要的作用[15]。本研究中,表现为单纯受压、移位者8例,患侧纤维束发生浸润、破坏者17例;低级别胶质瘤和脑膜瘤主要是直接推移、分离相邻皮质脊髓束,而高级别胶质瘤主要通过直接浸润、破坏相邻皮质脊髓束。分析其原因可能是低级别星形细胞瘤由于生长速度缓慢且浸润程度较低,对相邻脑组织主要为推挤作用,很少破坏相邻功能区和白质纤维束;而相对于WHO分级均在Ⅲ级以上的高级别星形细胞瘤及转移瘤,生长较快且具有高度侵袭性,从而直接造成相邻功能区及白质纤维束的破坏。皮质脊髓束的完整性与肿瘤的生长方式及侵袭程度直接相关,因此,DTI对脑肿瘤良性恶性诊断提供了有价值的参考,同时可以预测病人术后手运动功能恢复情况等。
BOLD-fMRI与DTI具有互补性,单独使用其中一种技术都无法满足神经外科手术的需求,只有两者联合应用才能将其应用价值最大化[16]。Berntsen等[17]认为术前联合应用BOLD-fMRI和DTI检查有助于手术方式的合理化。在脑肿瘤手术中联合应用BOLD-fMRI和DTI技术进行指导,明显降低了术后并发症[18]。因此,BOLD-fMRI和DTI技术显示脑皮层功能区以及皮质脊髓束的可行性后,也进一步将术前获得的功能区激活图以及纤维束示踪图加入术中神经导航系统,辅助神经外科医生切除肿瘤,结果术后除1例高级别胶质瘤外,其余脑肿瘤均实现完全切除,并且仅有该病人术后手肌力被评为1级,其余均在2级以上,充分显示了依据BOLD-fMRI和DTI技术制定手术计划具有重要临床价值。
尽管BOLD-fMRI 联合DTI对于脑肿瘤最大范围安全切除优势明显,但是在实际应用过程中仍面临一些问题,如:①激活图像阈值的选择受人为主观因素的影响;②有时简单的任务很难一次性地获取全面、准确的功能区定位信息等[19-20]。
综上所述,BOLD-fMRI及DTI的联合应用在脑肿瘤形态学成像及功能成像之间架起了一座桥梁,为进一步阐明功能皮层激活特点与神经通路结构特征性的关系开拓了广阔的空间,为临床研究脑肿瘤与邻近功能区的关系提供了技术上的支持,且术中配合导航系统实现了最大程度切除肿瘤的同时也保护了运动功能,充分彰显了其临床应用价值,有助于实现延长病人生存期及提高病人生存质量的目标。
